2019届中考化学专题总复习:工业流程题含答案
- 格式:doc
- 大小:177.55 KB
- 文档页数:13

2019年安徽省中考化学题型针对性练习19工业“流程题”1.某工厂废液中含有氯化铜和氯化亚铁。
某课外小组要将废液进行处理并得到铜和氧化铁两种产品。
过程如图所示。
(1)加入A物质发生的化学反应方程式为:;(2)操作Ⅰ和Ⅱ的名称是,其中除用到烧杯、漏斗和铁架台外,还需要的玻璃仪器是;(3)检验C过量的方法是;(4)经过处理后,氧化铁中铁元素(填“等于”、“小于”、“大于”)原废液中氯化亚铁中铁元素质量。
2.某化学兴趣小组设计利用稀硫酸浸取某废弃的氧化铜锌矿制取活性氧化锌的方案(氧化铜锌矿主要成分为CuO 和ZnO,其余成分既不与酸反应,也不溶解于水),部分实验流程如下:(1)将氧化铜锌矿粉碎的目的是,操作1的名称是。
所用到的玻璃仪器有玻璃棒、烧杯、。
(2)在氧化铜锌矿中加入稀硫酸要过量,其目的是,主要成分发生反应的化学方程为(写出一个即可)。
(3)得到滤渣1含有的金属是。
3.工业上炼铁炼钢和轧制钢材的主要流程如图。
已知生铁的含量含碳量为2%﹣4.3%钢的含碳量为0.03%﹣2%。
(1)反应:①Fe2O3+3CO2Fe+3CO2,②Fe2O3+3C2Fe+3CO.属于置换反应的是,用于高炉炼铁的原理是(填序号)(2)炼铁的固体原料需经过粉碎,其目的是。
(3)热空气和高炉气体的主要成分有一种相同,这种气体的化学式是。
炉渣中含有硅酸钙(CaSiO3),其中硅元素的化合价是。
(4)炼钢炉中,通入纯氧的目的是。
将钢锭轧成钢板,体现了金属的性。
(5)钢铁制品可能会生锈,写出用稀硫酸除锈反应的化学方程式。
4.硫酸在工业上有着重要的用途。
以黄铁矿(主要成分为FeS2)为原料生产硫酸的原理及SO2H2SO4工艺流程可简示如下:FeS(1)工业生产过程中将矿石粉碎以及在吸收装置中液体由上而下形成喷雾状的目的是。
(2)在实验室模拟制硫酸时用如图装置吸收三氧化硫,除了达到与工业上相同的目的外,还可能考虑的因素是。
(3)工业上常用熟石灰来吸收尾气中的二氧化硫,请写出反应的化学方程式。

专题四工艺流程图题类型1 与碳酸钙有关的流程(10年3考:2015.13,2012.13,2011.13)1.(2011安徽13题)医用氯化钙常用于合成药物。
以工业碳酸钙(含少量Fe3+等杂质)为原料生产二水合氯化钙(CaCl2·2H2O)的流程如图所示。
第1题图(1)写出第①步中碳酸钙与盐酸反应的化学方程式:________________________。
(2)第②步中是否发生化学变化?________(填“是”或“否”)。
(3)操作a的名称是________,实验室进行该操作时玻璃棒的作用是__________________。
(4)青少年正处于生长发育阶段,需要摄入足够的钙,写出一种合理的补钙方法:______________________________________________。
2.醋酸钙[(CH3COO)2Ca]是一种常用的药物,以蛋壳(主要成分为碳酸钙)为原料回收膜并制备醋酸钙的一种工艺流程如下。
第2题图(1)加入盐酸使壳膜分离的过程属于________(填“物理”或“化学”)变化;实验室进行过滤操作后,若滤液仍有浑浊,原因可能是____________。
(2)煅烧过程中发生反应的基本反应类型为__________________。
(3)在反应I中制备石灰乳,而不是制备澄清石灰水的原因是____________________,写出熟石灰在农业上的一种用途______________________。
(4)反应II为中和反应,写出其反应的化学方程式:____________________________。
3.乙炔(C2H2)又称电石气,是一种重要的化工原料和燃料。
工业上生产乙炔的流程如图所示:第3题图(1)步骤②中先将固体和焦炭粉碎的目的是__________________,该反应的化学方程式________________________。
(2)步骤③中加入X的化学式是__________,进行操作I时,漏斗内液面应低于__________。

(完整版)初三化学工艺流程题题一、中考化学流程题1.工业上用闪锌矿(主要成分是ZnS、FeS)冶炼锌,主要流程如下:(1)焙烧炉中,ZnS转化为ZnO。
补全该反应的化学方程式。
___________ZnS+___________高温___________ZnO+___________SO2(2)酸浸槽中,硫酸与锌焙砂反应得到用于电解的酸浸液。
反应过程中需不断搅拌,其目的是___________。
(3)酸浸渣的主要成分是铁酸锌(ZnFe2O4,其中Fe为+3价)。
底吹炉中,主要发生如下反应:①3ZnFe2O4+C 高温2Fe3O4+3ZnO+CO↑②ZnFe2O4+CO 高温2FeO+ZnO+CO2③ZnO+CO 高温Zn(蒸气)+CO2反应①~③中,化合价发生改变的元素有___________。
(4)最终可以获得锌的设备有___________。
2.Li2CO3是生产锂电池的重要原料,电解铝废渣(主要含AlF3、LiF、NaF、CaO等物质)可用于制备Li2CO3。
已知:Li2CO3的溶解度:0 ℃ 1.54 g;20 ℃ 1.33 g;80 ℃ 0.85 g。
(1)在加热条件下酸浸,反应生成能腐蚀玻璃的氟化氢(HF )气体,写出AlF 3发生反应的化学方程式:_________,该化学反应属于____________反应(填写基本反应类型)。
(2)滤渣B 的主要成分是____________。
(3)“转化”后所得LiHCO 3溶液中含有的Ca 2+需要加入Li 3PO 4除去。
除钙步骤中其他条件不变,反应相同时间,温度对除钙率和Li 2CO 3产率的影响如图所示。
随着温度升高最终Li 2CO 3的产率逐渐减小的原因是_____________________。
(4)热分解后,获得Li 2CO 3需趁热过滤的原因是____________。
进行过滤操作需要的玻璃仪器有玻璃棒、______________、_______________,玻璃棒的作用是______________。

全国2019年中考化学试题分单元汇编工艺流程题16.(2019年·东营)碳酸钡是工业上一种重要的化工产品,以下是某工厂用含二氧化硅杂质的碳酸钡原料来生产碳酸钡的工艺流程,请你根据流程回答下列问题(说明:操作B为洗涤,干燥)(1)生产流程中为节约成本,生成的气体B直接应用于流程中,其气体B是二氧化碳。
(2)操作A的名称为过滤。
(3)流程中溶液A中含有的溶质有BaCl2和HCl (写化学式)。
(4)写出反应室中有关反应的化学方程式(任意一个即可)Na2CO3+BaCl2═BaCO3↓+2NaCl或者NaOH+HCl=NaCl+H2O或者2NaOH+CO2=Na2CO3+H2O 。
(5)写出电解氯化钠溶液的化学方程式2NaCl+2H2O通电2NaOH+H2↑+Cl2↑。
解析(1)生产流程中为节约成本,生成的气体B直接应用于流程中,气体B是含二氧化硅杂质的碳酸钡和盐酸反应得到的气体,而二氧化硅和盐酸不反应,所以气体B是碳酸钡和盐酸反应生成的二氧化碳。
(2)操作A分离得到固体和液体,所以为过滤。
(3)流程中溶液A是二氧化硅杂质的碳酸钡和过量的盐酸反应得到的溶液,所以含有的溶质有生成的氯化钡以及剩余的盐酸,对应的化学式为 BaCl2和HCl。
(4)写出反应室中有关反应的化学方程式(任意一个即可) Na2CO3+BaCl2═BaCO3↓+2NaCl 或者NaOH+HCl=NaCl+H2O或者2NaOH+CO2=Na2CO3+H2O。
(5)根据图可知电解氯化钠溶液生成氢氧化钠以及氢气和氯气(根据质量守恒定律推得),则对应的化学方程式为2NaCl+2H2O通电2NaOH+H2↑+Cl2↑。
答案:(1)二氧化碳(2)过滤(3)BaCl2和HCl(4)Na2CO3+BaCl2═BaCO3↓+2NaCl或者NaOH+HCl=NaCl+H2O或者2NaOH+CO2=Na2CO3+H2O (5)2NaCl+2H2O通电2NaOH+H2↑+Cl2↑27.(2019年·临沂)以空气等为原料可合成氨、尿素[CO(NH2)2],以下是简易生产流程的一部分。
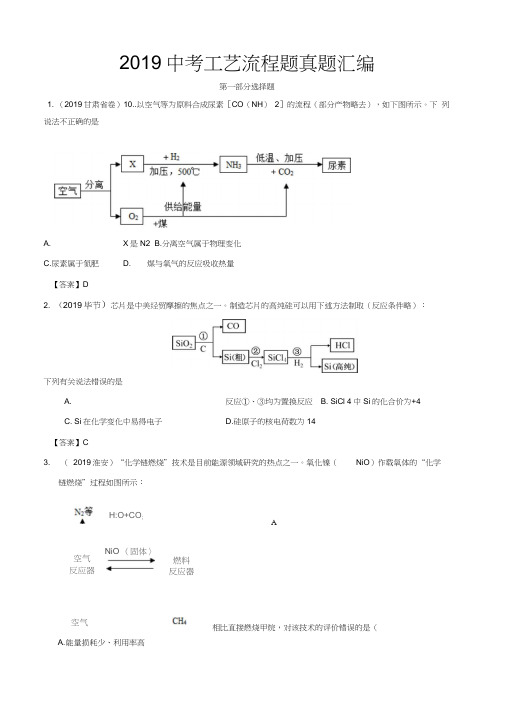
2019中考工艺流程题真题汇编第一部分选择题1. (2019甘肃省卷)10..以空气等为原料合成尿素[CO (NH ) 2]的流程(部分产物略去),如下图所示。
下 列说法不正确的是A.X 是N2 B.分离空气属于物理变化 C.尿素属于氮肥 D.煤与氧气的反应吸收热量【答案】D2. (2019毕节)芯片是中美经贸摩擦的焦点之一。
制造芯片的高纯硅可以用下述方法制取(反应条件略):下列有关说法错误的是A.反应①、③均为置换反应 B. SiCl 4中Si 的化合价为+4 C. Si 在化学变化中易得电子 D.硅原子的核电荷数为14【答案】C 3.( 2019淮安)“化学链燃烧”技术是目前能源领域研究的热点之一。
氧化镍( NiO )作载氧体的“化学链燃烧”过程如图所示:H:O+CO ;AA. 能量损耗少、利用率高空气 反应器NiO (固体〉燃料 反应器空气相比直接燃烧甲烷,对该技术的评价错误的是(B. 较安全,减少爆炸风险C. 消耗等质量甲烷,参加反应氧气较少D. 有利于分离和回收较纯净的二氧化碳【答案】C4. (2019扬州)工业上,利用溶液X (溶质为CuCl2和HCI)在50C时与Cu反应制作电路。
CuCb消耗后,HCuC b经处理又能转化为CuCl2,流程如图。
下列说法错误的是()双氧水Cu反应I反应II* CuCk已知:①反应I CuCI 2+C U+2HC I= 2HCuCb②反应n 2HCuC1+fQ= 2CUCI2+2H2OA.反应I和n涉及的元素中仅Cu O元素的化合价发生了变化B. 反应n中生成的CuCl2质量与溶液X中CuCl2质量一定相同C. 工业上,每溶解6.4kg Cu时,外界只需提供34kg 10%勺双氧水就能使生成的HCuCb全部转化为CuCbD.若由Cu、CuCI、CuCl2中的若干种组成的10.66g混合物中,铜元素为 6.4g,则该混合物中一定含CuCL【答案】B5. (2019攀枝花)为了从含有FeSQ、CuSQ的工业废水中回收Cu和硫酸亚铁晶体,某学习小组设计并完成了以下实验。
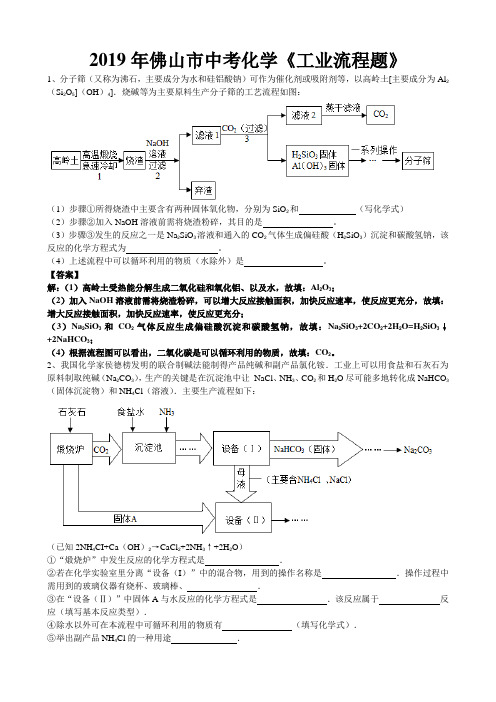
2019年佛山市中考化学《工业流程题》1、分子筛(又称为沸石,主要成分为水和硅铝酸钠)可作为催化剂或吸附剂等,以高岭土[主要成分为Al2(Si2O5](OH)4].烧碱等为主要原料生产分子筛的工艺流程如图:(1)步骤①所得烧渣中主要含有两种固体氧化物,分别为SiO2和(写化学式)(2)步骤②加入NaOH溶液前需将烧渣粉碎,其目的是。
(3)步骤③发生的反应之一是Na2SiO3溶液和通入的CO2气体生成偏硅酸(H2SiO3)沉淀和碳酸氢钠,该反应的化学方程式为。
(4)上述流程中可以循环利用的物质(水除外)是。
【答案】解:(1)高岭土受热能分解生成二氧化硅和氧化铝、以及水,故填:Al2O3;(2)加入NaOH溶液前需将烧渣粉碎,可以增大反应接触面积,加快反应速率,使反应更充分,故填:增大反应接触面积,加快反应速率,使反应更充分;(3)Na2SiO3和CO2气体反应生成偏硅酸沉淀和碳酸氢钠,故填:Na2SiO3+2CO2+2H2O=H2SiO3↓+2NaHCO3;(4)根据流程图可以看出,二氧化碳是可以循环利用的物质,故填:CO2。
2、我国化学家侯德榜发明的联合制碱法能制得产品纯碱和副产品氯化铵.工业上可以用食盐和石灰石为原料制取纯碱(Na2CO3),生产的关键是在沉淀池中让 NaCl、NH3、CO2和H2O尽可能多地转化成NaHCO3(固体沉淀物)和NH4Cl(溶液).主要生产流程如下:(已知2NH4CI+Ca(OH)2→CaCl2+2NH3↑+2H2O)①“煅烧炉”中发生反应的化学方程式是.②若在化学实验室里分离“设备(I)”中的混合物,用到的操作名称是.操作过程中需用到的玻璃仪器有烧杯、玻璃棒、.③在“设备(Ⅱ)”中固体A与水反应的化学方程式是.该反应属于反应(填写基本反应类型).④除水以外可在本流程中可循环利用的物质有(填写化学式).⑤举出副产品NH4Cl的一种用途.【答案】解:①“煅烧炉”中,高温条件下,碳酸钙分解生成氧化钙和二氧化碳,反应的化学方程式为:CaCO3CaO+CO2↑.故填:CaCO3CaO+CO2↑.②若在化学实验室里分离“设备(I)”中的混合物,用到的操作名称是过滤,操作过程中需用到的玻璃仪器有烧杯、玻璃棒、漏斗.故填:过滤;漏斗.③在“设备(Ⅱ)”中,固体A中的氧化钙和水反应生成氢氧化钙,反应的化学方程式为:CaO+H2O═Ca (OH)2,该反应属于化合反应.故填:CaO+H2O═Ca(OH)2;化合.④除水以外可在本流程中可循环利用的物质有氯化铵和氢氧化钙反应生成的氨气和碳酸氢钠分解生成的二氧化碳.故填:NH3、CO2.⑤副产品NH4Cl的一种用途是用作氮肥.故填:用作氮肥.3、工业上用闪锌矿(主要含ZnS,还含PbS等杂质)制备锌的流程如图1(部分产物略去):(1)X的化学式是,图1中用过量空气的目的是。
工艺流程题1.(安徽)我国制碱工业先驱侯德榜发明了“侯氏制碱法”。
其模拟流程如下:(1)反应①的化学方程式________________,反应②的基本反应类型为_______。
(2)工业上用分离液态空气 的方法制取氢气,属于_______变化(填“物理”或“化学”)。
(3)操作a 的名称是_____,实验室进行此操作所需的玻璃仪器有烧杯、玻璃棒、______。
(4)写出NH 4Cl 的一种用途________________。
(1)CaCO 3 =CaO+CO 2↑;分解反应。
(2)物理;(3)过滤;漏斗。
(4)做化肥或氮肥等。
2. (益阳)过氧化钙晶体﹝CaO 2·8H 2O ﹞较稳定,呈白色,微溶于水,广泛应用于环境杀菌、消毒。
以贝壳为原料制备CaO 2流程如下:(1)气体是CO 2,其名称是 二氧化碳 ;将过氧化钙晶体与溶液分离的方法是 过滤 。
(2)反应Y 需控制温度在0~5℃,可将反应容器放在 冰水混合物 中,该反应是化合反应,反应产物是CaO 2·8H 2O ,请写出化学方程式CaO 2+H 2O 2+7H 2O =CaO 2·8H 2O 。
获得的过氧化钙晶体中常含有Ca(OH)2杂质,原因是 CaO 或Ca(OH)2过量,且Ca(OH)2微溶 。
(3)CaO 2的相对分子质量为 72 ,过氧化钙晶体﹝CaO 2·8H 2O ﹞中H 、O 元素的质量比为 1∶10 。
(4)为测定制得的过氧化钙晶体中CaO 2·8H 2O 的质量分数,设计的实验如下:称取晶体样品50g ,加热到220℃充分反应(方程式为2CaO 2·8H 2O=====△2CaO +O 2↑+16H 2O ↑,杂质不发生变化),测得生成氧气的质量为3.2g ,请计算样品中CaO 2·8H 2O 的质量分数(CaO 2·8H 2O相对分子质量为216),写出必要的计算过程。
2020中考化学试题分类汇编——工艺流程题1.(安徽)我国制碱工业先驱侯德榜发明了“侯氏制碱法”。
其模拟流程如下:(1)反应①的化学方程式________________,反应②的基本反应类型为_______。
(2)工业上用分离液态空气的方法制取氢气,属于_______变化(填“物理”或“化学”)。
(3)操作a的名称是_____,实验室进行此操作所需的玻璃仪器有烧杯、玻璃棒、______。
(4)写出NH4Cl的一种用途________________。
(1)CaCO3 =CaO+CO2↑;分解反应。
(2)物理;(3)过滤;漏斗。
(4)做化肥或氮肥等。
2.(益阳)过氧化钙晶体﹝CaO2·8H2O﹞较稳定,呈白色,微溶于水,广泛应用于环境杀菌、消毒。
以贝壳为原料制备CaO2流程如下:(1)气体X是CO2,其名称是二氧化碳;将过氧化钙晶体与溶液分离的方法是过滤。
(2)反应Y需控制温度在0~5℃,可将反应容器放在冰水混合物中,该反应是化合反应,反应产物是CaO2·8H2O,请写出化学方程式CaO2+H2O2+7H2O=CaO2·8H2O 。
获得的过氧化钙晶体中常含有Ca(OH)2杂质,原因是CaO或Ca(OH)2过量,且Ca(OH)2微溶。
(3)CaO2的相对分子质量为72 ,过氧化钙晶体﹝CaO2·8H2O﹞中H、O元素的质量比为1∶10 。
(4)为测定制得的过氧化钙晶体中CaO2·8H2O的质量分数,设计的实验如下:称取晶体样品50g,加热到220℃充分反应(方程式为2CaO2·8H2O=====△2CaO+O2↑+16H2O↑,杂质不发生变化),测得生成氧气的质量为 3.2g,请计算样品中CaO2·8H2O的质量分数(CaO2·8H2O相对分子质量为216),写出必要的计算过程。
解:设样品中CaO2·8H2O的质量为x2CaO2·8H2O=====△2CaO+O2↑+16H2O↑432 32x 3.22.332432=x∴x =43.2(g )∴ 样品中CaO 2·8H 2O 的质量分数为%1005032.4 =86.4% 答:样品中CaO 2·8H 2O 的质量分数为=86.4%3. (呼和浩特)空气中氮气的含量最多,氮气在高温、高能量条件下可与某些物质发生反应。
工业流程专题训练1、用作牙膏摩擦剂的轻质碳酸钙可以用矿石A来制备,某化学兴趣小组设计了2种转化流程,如下图所示。
已知:a.二氧化碳持续通入氢氧化钙溶液发生如下反应:CO2+Ca(OH)2===CaCO3↓+H2O,CaCO3+ H2O + CO2===Ca(HCO3)2;b.碳酸氢钙微溶于水,微热易分解:Ca(HCO3)2===== CaCO3↓+H2O+ CO2↑;c.生石灰与水充分反应后可得到颗粒非常细小的熟石灰浆。
(1)小王主张用流程①、②、④和操作Ⅱ的设计,认为其工艺简单。
请写出反应①和④的化学方程式:①;④;操作Ⅱ包括等工序。
(2)制轻质碳酸钙时,D为(选填“悬浊液”或“溶液”或“乳浊液”),理由是:.(3)小李认为流程①、②、③和操作I比小王的主张更好,其理由是:_______________;操作I包括搅拌和微热等工序。
2、下面是某化工厂生产烧碱的工业流程图。
请根据以上信息回答下列问题:(1)请写出X物质在实验室中的一种用途。
(2)反应池中发生反应的化学方程式为。
(3)操作①的名称是,结晶得到的固体烧碱中可能含有少量的(写化学式)。
(4)滤液D可加入反应池循环再利用,目的是。
3、某实验小组利用废硫酸液制备K2SO4并研究CaSO4•2H2O加热分解的产物。
一、K2SO4的制备(1)将CaCO3研成粉末的目的是。
(2)上述流程中可循环使用的物质有CO2和(填写化学式)。
微热分离CaCO3CO2KClCO2NH3K2SO4晶体NH4Cl溶液M溶液反应ⅢCaSO4•2H2O CaSO4悬浊液反应Ⅱ过量CaCO3粉末废硫酸反应ⅠA B C D E(3)反应Ⅲ中相关物质的溶解度如下表。
你认为反应Ⅲ在常温下能实现的原因是。
(4)不用水而用饱和K2SO4溶液洗涤反应Ⅲ所得晶体的目的是;为检验此晶体是否洗涤干净,可取最后一次洗涤液,先加入(选填序号,下同),振荡、静置,再向上层清液中滴加,观察现象即可判断。
中考化学总复习《流程题》专项试题一、流程题1.有Mg 、Fe 、Cu 的混合粉末,分离并得到MgSO 4·7H 2O 过程如下:(1)固体B 是________.(2)操作②中用到的主要玻璃仪器有______、玻璃棒和烧杯等.(3)操作②主要包含蒸发浓缩、_____、过滤、洗涤烘干等.(4)实验中可选用适量的下列试剂中的______代替稀H 2SO 4(填标号)a CuSO 4溶液b FeSO 4溶液c 稀盐酸2.废弃金属是重要的可再生资源,利用化学工艺可回收处理大量废旧电器。
某品牌电器的废旧电路板中含有Fe 、Cu 、Ag 、Ni (镍,银白色金属)等金属,如图所示是某车间回收部分金属的工艺流程。
已知:22442Δ2Cu+O +2H SO 2CuSO +2H O ,Ni 与酸反应生成正二价离子。
根据信息回答下列问题:(1)操作②中加入足量稀硫酸的目的是______,滤液②中含有的金属阳离子是______ (填离子符号)。
(2)根据以上工艺流程,可以得出Ni 、Fe 的金属活动性强弱顺序是Ni______Fe (填“<”或“>”=)。
(3)滤渣②中含有的金属是______,固体A 除主要含有铜外,还含有一定量的铁,为了进一步提纯铜,可以向固体A 中加入______,当看到______的现象时,表明铁已完全除尽。
(4)相比于直接焚烧废旧电路板回收金属,该工艺流程的主要优点是______。
3.实验室有氧化铜和铁的混合粉末,为除去其中的铁得到纯净的铜,设计了如图所示流程:(1)溶液A 中溶质除了FeSO 4和CuSO 4外,还有____。
(2)步骤②中加入过量铁粉,能观察到有气泡产生且有红色固体析出,请写出有红色固体析出时发生反应的化学方程式______。
(3)步骤②和步骤②后都要经过____操作,其中玻璃棒的作用是________。
(4)选用一种物理方法分离滤渣B 中的两种物质,该方法是_______。
工业流程题1、实验结束时,同学们将含有CuSO4、ZnSO4、FeSO4的废液倒在废液缸里,如果将废液直接排放就会造成水污染.于是几位同学利用课余处理废液,回收工业重要原料硫酸锌和有关金属.实验过程如下:请回答:(1)操作1是,固体A的成分,(2)固体C是.滤液1和滤液2中溶质相同,该溶质是.(3)写出加入过量锌粉的其中一个反应的化学方程式;加入足量稀硫酸发生反应的化学方程式.【答案】解:(1)操作1把混合物分离成固体和滤液,所以,操作1为过滤操作;根据金属活动性锌>铁>铜,向含有CuSO4、ZnSO4、FeSO4的废液加入过量的锌粉,铁、铜被置换出来,因此过滤后所得固体A中含有铁、铜和未反应的锌;故答案为:过滤;Cu、Zn、Fe;(2)利用磁铁可以吸引铁的特点,可判断固体B、C为铁粉或铜粉与锌粉的混合物之一;由于固体B能与足量稀硫酸反应后可得到铜粉,可确定固体B为铜粉与锌粉的混合物,而固体C为铁粉;故答案为:Fe;根据金属的活动性锌>铁>氢>铜,向CuSO4、ZnSO4、FeSO4混合溶液中加入过量锌粉后过滤,所得滤液为ZnSO4溶液;把铜粉与锌粉的混合物放入足量稀硫酸中充分反应后过滤,所得滤液为ZnSO4溶液;故答案为:ZnSO4;(3)过量的锌粉与混合溶液中的硫酸铜反应,可置换出铜同时生成硫酸锌;与混合溶液中的硫酸亚铁反应,可置换出铁同时生成硫酸锌;铜粉与锌粉的混合物中的锌粉能与稀硫酸发生置换反应生成硫酸锌和氢气;故答案为:Zn+CuSO4=ZnSO4+Cu(或Zn+FeSO4=ZnSO4+Fe);Zn+H2SO4=ZnSO4+H2↑.2、某实验结束时,同学们将含有CuSO4、ZnSO4、FeSO4的废液倒在废液缸里,如果将废液直接排放就会造成水污染。
于是几位同学利用课余处理废液,回收工业重要原料硫酸锌和有关金属。
实验过程如下:请回答:(1)步骤①④的操作名称是;用到的玻璃仪器除了玻璃棒、烧杯,还有;固体A中含种物质。
(2)写出步骤①其中一个反应的化学方程式为;步骤④发生反应的化学方程式为。
(3)检验步骤④中加入的稀硫酸是否足量的方法是。
【答案】解:(1)由实验过程图可判断,操作1和操作4完成后原混合物分成了固体和滤液两部分;利用这一特点可判断操作1和操作4为过滤操,用的玻璃仪器有:玻璃棒、烧杯、漏斗;混合溶液为含有CuSO4、ZnSO4、FeSO4的废液,向混合溶液中加入过量的锌粉,锌可与硫酸铜、硫酸亚铁发生置换反应生成铁、铜和硫酸锌,所以固体A中含有生成的铁、铜及未反应完的锌;(2)过量锌粉与CuSO4、ZnSO4、FeSO4混合溶液中的CuSO4、FeSO4都可以发生置换反应,反应的化学方程式为:Zn+CuSO4=Cu+ZnSO4(或Zn+FeSO4=Fe+ZnSO4);加入足量稀硫酸,金属混合粉末中的锌粉可与稀硫酸发生置换反应,反应的化学方程式为:Zn+H2SO4=ZnSO4+H2↑;(3)固体C为锌、铜混合物加入的稀硫酸与锌反应而得到纯净的固体,因此,取反应后所得固体铜加入稀硫酸观察是否有气泡可检验向固体C中加入的稀硫酸是否足量,其操作的方法为:取滤渣于试管中加入少量稀硫酸,若有气泡产生则酸不足量,若无气泡产生则酸已足量;故答案为:(1)过滤漏斗 3;(2)①Zn+CuSO4=Cu+ZnSO4(或Zn+FeSO4=Fe+ZnSO4)④Zn+H2SO4=ZnSO4+H2↑;(3)取滤渣于试管中加入少量稀硫酸,若有气泡产生则酸不足量,若无气泡产生则酸已足量。
3、有一种工业废水,其中含有大量的硫酸亚铁,少量的硫酸铜以及污泥。
某同学设计了一个既经济又合理的方法回收铜和硫酸亚铁晶体。
方案流程如下:查阅资料得知硫酸亚铁晶体化学式为:FeSO4•7H2O,该物质受热易失去结晶水。
请回答:(1)步骤①②③中最后都需进行的实验操作是;(2)步骤②中需加入的物质是,发生反应的化学方程式是,固体的成分是;(3)步骤③中需加入稀硫酸,发生反应的化学方程式是;(4)步骤④的操作是。
【答案】解:(1)步骤①是将污泥与溶液分离,所以可用过滤,步骤②③都将固液分离,所以可用过滤;(2)要将硫酸铜与硫酸亚铁的混合溶液中回收铜,同时得到硫酸亚铁溶液,只能加入过量的铁置换硫酸铜溶液中的铜,化学方程式为:Fe+CuSO4=FeSO4+Cu;铁与硫酸铜反应生成铜和硫酸亚铁,因此经过步骤②之后得到的固体中含有生成的铜和剩余的铁;(3)步骤③中加入适量稀硫酸与铁反应生成硫酸亚铁,化学方程式为:Fe+H2SO4═FeSO4+H2↑;(4)将溶液2和3合在一起进行蒸发结晶即可得到硫酸亚铁晶体。
故答案为:(1)过滤(2)铁粉 Fe+CuSO4═FeSO4+Cu Fe和Cu(3)Fe+H2SO4═FeSO4+H2↑(4)蒸发。
4、分子筛(又称为沸石,主要成分为水和硅铝酸钠)可作为催化剂或吸附剂等,以高岭土[主要成分为Al2(Si2O5](OH)4].烧碱等为主要原料生产分子筛的工艺流程如图:(1)步骤①所得烧渣中主要含有两种固体氧化物,分别为SiO2和(写化学式)(2)步骤②加入NaOH溶液前需将烧渣粉碎,其目的是。
(3)步骤③发生的反应之一是Na2SiO3溶液和通入的CO2气体生成偏硅酸(H2SiO3)沉淀和碳酸氢钠,该反应的化学方程式为。
(4)上述流程中可以循环利用的物质(水除外)是。
【答案】解:(1)高岭土受热能分解生成二氧化硅和氧化铝、以及水,故填:Al2O3;(2)加入NaOH溶液前需将烧渣粉碎,可以增大反应接触面积,加快反应速率,使反应更充分,故填:增大反应接触面积,加快反应速率,使反应更充分;(3)Na2SiO3和CO2气体反应生成偏硅酸沉淀和碳酸氢钠,故填:Na2SiO3+2CO2+2H2O=H2SiO3↓+2NaHCO3;(4)根据流程图可以看出,二氧化碳是可以循环利用的物质,故填:CO2。
5、我国化学家侯德榜发明的联合制碱法能制得产品纯碱和副产品氯化铵.工业上可以用食盐和石灰石为原料制取纯碱(Na2CO3),生产的关键是在沉淀池中让 NaCl、NH3、CO2和H2O尽可能多地转化成NaHCO3(固体沉淀物)和NH4Cl(溶液).主要生产流程如下:(已知2NH4CI+Ca(OH)2→CaCl2+2NH3↑+2H2O)①“煅烧炉”中发生反应的化学方程式是.②若在化学实验室里分离“设备(I)”中的混合物,用到的操作名称是.操作过程中需用到的玻璃仪器有烧杯、玻璃棒、.③在“设备(Ⅱ)”中固体A与水反应的化学方程式是.该反应属于反应(填写基本反应类型).④除水以外可在本流程中可循环利用的物质有(填写化学式).⑤举出副产品NH4Cl的一种用途.【答案】解:①“煅烧炉”中,高温条件下,碳酸钙分解生成氧化钙和二氧化碳,反应的化学方程式为:CaCO3CaO+CO2↑.故填:CaCO3CaO+CO2↑.②若在化学实验室里分离“设备(I)”中的混合物,用到的操作名称是过滤,操作过程中需用到的玻璃仪器有烧杯、玻璃棒、漏斗.故填:过滤;漏斗.③在“设备(Ⅱ)”中,固体A中的氧化钙和水反应生成氢氧化钙,反应的化学方程式为:CaO+H2O═Ca(OH)2,该反应属于化合反应.故填:CaO+H2O═Ca(OH)2;化合.④除水以外可在本流程中可循环利用的物质有氯化铵和氢氧化钙反应生成的氨气和碳酸氢钠分解生成的二氧化碳.故填:NH3、CO2.⑤副产品NH4Cl的一种用途是用作氮肥.故填:用作氮肥.6、工业上用闪锌矿(主要含ZnS,还含PbS等杂质)制备锌的流程如图1(部分产物略去):(1)X的化学式是,图1中用过量空气的目的是。
(2)①~④中属于化合反应的是。
(3)Zn (填“能”或“不能”)与PbCl2溶被反应。
(4)写出反应③中生成ZnO的化学方程式。
(5)结合下表数据设计:从粗锌中分离出纯锌的方案是℃。
(6)反应②中固体质量随反应时间的变化图示如图,计算产生Y的质量。
(写出必要的计算过程)【答案】解:(1)焦炭在氧气充足时燃烧生成二氧化碳,图1中用过量空气是为了保证让碳完全反应,故填:CO2;使焦炭完全反应;(2)反应①是碳和氧气点燃生成二氧化碳,属于化合反应,反应②是碳和二氧化碳高温反应生成一氧化碳,属于化合反应,反应③是硫化锌与氧气高温反应生成氧化锌和二氧化硫,不是化合反应,反应④是氧化锌和一氧化碳反应生成锌和二氧化碳,不是化合反应,故填:①②;(3)锌的活动性强于铅,故锌能与氯化铅溶液反应,故填:能;(4)反应③中硫化锌与氧气高温反应生成氧化锌和二氧化硫,故填:2ZnS+3O22ZnO+2SO2;(5)根据表格提供的数据可以看出,锌的沸点比铅低,故可以将粗锌放在一容器中,保持温度907-1749℃,收集的锌蒸气,冷却后可得纯净的锌,故填:将粗锌放在一容器中,保持温度907-1749;收集的锌蒸气,冷却后可得纯净的锌;(6)设生成Y的质量为xC+CO22CO12 5630g xx=140g答:产生Y的质量为140g。
7、工业上炼铁、炼钢和轧制钢材的主要流程如图:(1)炉渣中含有硅酸钙(CaSiO3),其中硅元素的化合价是,在高炉中加入石灰石的目的是除去脉石(SiO2)生成炉渣CaSiO3,除去脉石的反应化学方程式是。
(2)反应:①Fe2O3 +3C2Fe+3CO↑,②Fe2O3 +3CO2Fe+3CO2,用于高炉炼铁的原理是,属于置换反应的是(填序号)。
(3)炼铁时将铁矿石粉碎的目的。
(4)炼钢就是将生铁“降碳除杂(硫、磷等)”,写出炼钢炉中降碳的反应化学方程式。
(5)轧制过程是变化(填“物理”或“化学”)。
【答案】解:(1)钙元素显+2价,氧元素显-2价,设硅元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+2)+x+(-2)×3=0,则x=+4价;在高温下碳酸钙发生分解生成氧化钙和二氧化碳,然后氧化钙与二氧化硅在高温下反应生成硅酸钙;(2)高炉炼铁的原理是一氧化碳与氧化铁在高温下反应生成铁和二氧化碳,置换反应的反应物和生成物都是一种单质和一种化合物;(3)炼铁的固体原料需经过粉碎,粉碎的目的是增大反应物接触面积,加快反应速率;(4)碳与氧气在点燃下反应生成二氧化碳,从而降低了生铁中的含碳量;(5)轧制过程中只是钢的形状发生改变,没有新的物质生成,属于物理变化。
答案为:(1)+4; CaCO3CaO+CO2↑,CaO+SiO2CaSiO3 。
(2)②;①;(3)增大反应物接触面积,加快反应速率(合理即可);(4)C+O2 CO2;(5)物理。
8、某粗盐样品中含有杂质氯化镁、氯化钙。
某同学设计了以下提纯方案(1)若方案中先除去的是氯化镁,接着除去氯化钙,回答:试剂a的化学式是,b的化学式是。