高考化学专题强化练试题热化学方程式、反应焓变的计算
- 格式:doc
- 大小:136.50 KB
- 文档页数:7

高中化学热化学方程式书写焓变计算练习题一、单选题1.标准状况下,气态分子断开1mol 化学键的焓变称为键焓。
已知H —H 键、H —O 键和O==O 键的键焓H ∆分别为1436kJ mol -⋅、1463kJ mol -⋅和1495kJ mol -⋅。
下列热化学方程式正确的是( ) A.12221H O(g)H (g)O (g)485kJ mol 2H -===+∆=-⋅B.12221H O(g)H (g)O (g)485kJ mol 2H -===+∆=+⋅C.12222H (g)O (g)2H O(g)485kJ mol H -+===∆=+⋅D.12222H (g)O (g)2H O(g)485kJ mol H -+===∆=-⋅2.含11.2g KOH 的稀溶液与1L0.1mol/L 的H 2SO 4溶液反应放出11.46kg 的热量,下列能正确表示中和热的热化学方程式是( )A.KOH(aq)+1/2H 2SO 4(aq)=1/2K 2SO 4+H 2O(l);ΔH =-11.46kJ/molB.2KOH(s)+H 2SO 4(aq)=K 2SO 4+2H 2O(l);ΔH =-114.6kJ/molC.2KOH(aq)+H 2SO 4(aq)=K 2SO 4+2H 2O(l);ΔH =+114.6kJ/molD.KOH(aq)+1/2H 2SO 4(aq)=1/2K 2SO 4+H 2O(l);ΔH =-57.3kJ/mol 3.根据热化学方程式:()()()122S l O g SO g H 293.23kJ mol ∆⋅-+==-,分析下列说法中正确的是( )A.硫和氧气反应放出293.23kJ 的热量B.一个硫原子和一个氧气分子完全反应放出293.23kJ 的热量C.1摩尔硫单质和1摩尔氧气完全反应生成1摩尔二氧化硫放出293.23kJ 的热量D.1摩尔液体硫磺和1摩尔气态氧气完全反应生成1摩尔二氧化硫气体放出293.23kJ 的热量 4.下列有关热化学方程式的叙述正确的是( )A.已知:2222H (g)O (g)2H O(g)483.6kJ /mol H +=∆=-,则氢气的燃烧热为241.8kJ/molB. 已知:4P (s ,红磷)===4P (s ,白磷)0H ∆>,则白磷比红磷稳定C. 含20.0 g NaOH 的稀溶液与稀硫酸完全中和,放出28.7kJ 的热量,则表示该反应中和热的热化学方程式为2424211NaOH(aq)H SO (aq)Na SO (aq)H O(l)57.4kJ /mol 22H +=+∆=-D. 已知:221C(s)O (g)CO (g)H +=∆,221C(s)O (g)CO(g)2H +=∆,则12H H ∆>∆5.下列说法中正确的是( )A. 在25℃、101kPa 时,1mol 纯物质完全燃烧时所放出的热量,叫作该物质的燃烧热B. 酸与碱发生中和反应生成1mol 水,这时的反应热叫做中和热C. 燃烧热和中和热都属于反应热D. 在稀溶液中,1mol 3CH COOH 与1mol NaOH 完全中和时放出的热量为57.3kJ 二、填空题6.0.3mol 的气态高能燃料乙硼烷(B 2H 6)在氧气中燃烧,生成固态的三氧化二硼和液态水,放出649.5kJ 热量,其热化学方程式为__________________________。

反应焓变计算公式
反应焓变(ΔH)的计算公式主要有两种表达方式:
1.宏观角度:ΔH = H生成物- H反应物。
其中,H生成物表示生成物的焓的总量,H反应物表示反
应物的焓的总量。
如果ΔH为“+”,则表示吸热反应;如果ΔH为“-”,则表示放热反应。
2.微观角度:ΔH = E吸收- E放出。
其中,E吸收表示反应物断键时吸收的总能量,E放出表示生成
物成键时放出的总能量。
同样,如果ΔH为“+”,则表示吸热反应;如果ΔH为“-”,则表示放热反应。
此外,还有其他常用的计算方法,如根据热化学方程式进行计算、根据反应物和生成物的总焓计算、依据反应物化学键断裂与生成物化学键形成过程中的能量变化计算,以及根据盖斯定律进行计算等。
焓是物体的一个热力学能状态函数,即热函,一个系统中的热力作用,等于该系统内能加上其体积与外界作用于该系统的压强的乘积的总和。
焓变即物体焓的变化量,其符号记为ΔH,单位为kJ/mol。
在等压且只做膨胀功的条件下,ΔH = ΔU + PΔV = Q,这表示在上述情况下,体系所吸收的热等于体系焓的增量。
以上信息仅供参考,如需更多信息,建议查阅相关文献或咨询专业化学家。

2022届高中化学一轮复习同步强化练习 反应热的计算(一)一、单选题(共14题)1.下列关于热化学方程式的说法正确的是( )A. ,则的燃烧热为()()()()4222CH g 2O g CO g 2H O g ++1Δ802kJ mol H -=-⋅4CH 1802kJ mol -⋅B. ,则该反应为放热反应()()33CH OH g CH OH l Δ0H <C.已知 ,则()()()2H aq OH aq H O l +-+1Δ57.3kJ mol H -=-⋅ ()()()()2NaOH aq HCl g NaCl aq H O 1++1Δ57.3kJ mol H -=-⋅D. ,则()()()2232SO g O g 2SO g + 1Δ196.6kJ mol H -=-⋅()()()3222SO 12SO g O g + 1Δ196.6kJ mol H ->+⋅2.已知:。
某些化学键的键能数据如表所示:122S (s)S (g)Δ 4.5kJ mol H -=+⋅化学键H —H Cl —Cl H —ClS=SH —S键能/()1kJ mol-⋅436243431255339下列说法正确的是( )A.与反应生成时放出370kJ 热量21mol H (g)22mol Cl (g)HCl(g)B.与反应生成的热化学方程式为2H (g)2S (s)2H S(g)12222H (g)S (s)2H S(g)Δ224.5kJ mol H -+=-⋅C.反应的焓变生成物的键能之和一反应物的键能之和ΔH =D.1mol 分解吸收的热量比1 mol 分解吸收的热量多,所以2H S(g)HCl(g)比稳定2H S(g)HCl(g)3.催化重整反应为。
42CH CO -422CH (g)CO (g)2CO(g)2H (g)ΔH ++已知:①1241C(s)2H (g)CH (g)Δ75kJ mol H -+=-⋅②1222C(s)O (g)CO (g)ΔH 394kJ mol -+=-⋅③1231C(s)O (g)CO(g)Δ111kJ mol 2H -+=-⋅则为( )ΔH A. B. C. D.1580kJ mol --⋅1+247kJ mol -⋅1+208kJ mol -⋅1430kJ mol --⋅4.已知:,下列有关热()()()()-14242NaHSO aq +NaOH aq Na SO aq +H O l ΔH=-57.3kJ mol =⋅化学方程式说法正确的是( )A.稀盐酸和稀氢氧化钠溶液的中和热为 -1 57.3kJ mol H ∆=-⋅B.稀硫酸和稀氢氧化钡溶液的中和热为 -1 57.3kJ mol H ∆=-⋅C.稀盐酸和氨水溶液的中和热为 -157.3kJ mol H ∆=-⋅D.稀醋酸和稀氢氧化钠溶液的中和热为-157.3kJ mol H ∆=-⋅5.常温常压下,1.5g 火箭燃料1,2-甲基肼完全燃烧生成()33H C NH NH CH ---二氧化碳气体和液态水时放出50kJ 热量,则该条件下1,2-二甲基肼的燃烧热为( )A. B. C. D.11000kJ mol -⋅11500kJ mol -⋅12000kJ mol -⋅13000kJ mol -⋅6.同温同压下,下列放热反应放出热量Q2>Q1的是( )A.2H2(g)+O2(g)=2H2O(g)△H=-Q1 kJ/mol 2H2(g)+O2(g)=2H2O(l)△H=-Q2 kJ/molB.S(g)+O2(g)=SO2(g)△H=-Q1 kJ/mol S(s)+O2(g)=SO2(g)△H=-Q2 kJ/molC.C(s)+O2(g)=CO2(g)△H=-Q1 kJ/mol C(s)+1/2O2(g)=CO(g)△H=-Q2 kJ/molD.H2(g)+Cl2(g)=2HCl(g)△H=-Q1 kJ/mol 1/2H2(g)+1/2Cl2(g)=HCl(g)△H=-Q2 kJ/mol7.已知2mol氢气完全燃烧生成水蒸气时放出能量484kJ,且氧气中1molO=O键完全断裂时吸收热量496kJ,水蒸气中1molH-O键形成时放出能量463kJ,则氢气中1molH-H键断裂时吸收热量为()A.920kJ B.557kJ C.436kJ D.188kJ8.某反应过程中的能量变化如图所示,下列说法正确的是( )A.改变催化剂,可改变该反应的活化能B.该反应为吸热反应,反应热等于HC.a 反应过程有催化剂参与D.在催化剂作用下,该反应的活化能等于12E E +9.某硝酸厂处理尾气中NO 的方法是在催化剂存在下,用将NO 还原为2H ,其热化学方程式为 ,其能量2N 12221NO(g)H (g)N (g)H O(g)ΔkJ mol 2H m -++=⋅变化过程如下(其中均为正值):a b c d 、、、下列说法正确的是( )A.过程②、④是吸热过程 B.1()2m a b c d =+--C. D.1()2m c a d b =+--1()2m c d a b =+--10.和的能量关系如图所示(M=Ca 、Mg ):3MgCO 3CaCO已知:离子电荷相同时,半径越小,离子键越强。

2020高考化学盖斯定律焓变的计算专攻试题【专题训练】1.化学反应的焓变既可以通过实验测定,也可以根据理论计算。
(1)一氧化碳还原氧化铁是工业炼铁的原理。
已知:①FeO(s)+3CO(g)===2Fe(s)+3CO(g)A H=-26.kj・mol-i2321②3FeO(s)+CO(g)===2FeO(s)+CO(g)A H=—50.8kJ•mol-i233422③FeO(s)+CO(g)===3FeO(s)+CO(g)A H=—36.5kJ•mol-i3423试写出CO气体还原固态FeO生成固态Fe和CO气体的热化学方程式:2(结果保留一位小数)。
⑵请根据表中的数据计算A H和A H。
i2CO(g)+4H(g)===CH(g)+2HO(g)的AH=kJ・mol-i;CH(g)+2242i4HO(l)===3H(g)+CO(g)的A H=kJ・mol-i。
222答案(i)FeO(s)+CO(g)===Fe(s)+CO(g)A H=+7.3kJ・mol-i2(2)-i70+250.i解析⑴根据盖斯定律,由(①X3—②一③X2)xj得FeO(s)+CO(g)===Fe(s)+CO(g)A H=(A H X3-A H-A H X2)xg~+7・3kJmol-i。
2i236(2)A H=2E(C===O)+4E(H—H)-4E(C—H)-4E(H—O)=(2X799+4X436i-4X413-4X465)kJ・mol-i=-i70kJ・mol-i。
根据燃烧热写出如下热化学方程式:CH(g)+20(g)===CO(g)+2H0⑴A H=-890・3kJ・mol-】;42223H(g)+^0(g)===H0(l)A H=-285.8kJ•mol-i;22224C0(g)+R(g)===C0(g)A H=-283・0kJ・mol-i。
2225故A H=A H-3A H-A H=(-890.3+3X285.8+283・0)kJ・mol-i=+2345250.1kJ•mol-i。
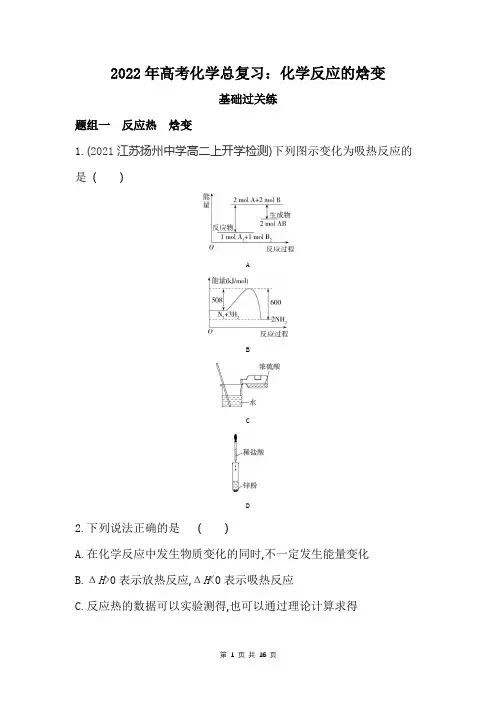

高考化学知识点复习《热化学反应方程式书写》十年真题汇总含答案1.(2017·浙江高考真题)根据能量变化示意图,下列热化学方程式正确的是( )A.N2(g)+3H2(g)=2NH3(g) ΔH=-(b-a)kJ/molB.N2(g)+3H2(g)=2NH3(g) ΔH=-(a-b)kJ/molC.2NH3(l)=N2(g)+3H2(g) ΔH=2(b+c-a)kJ/molD.2NH3(l)=N2(g)+3H2(g) ΔH=2(a+b-c)kJ/mol【答案】C【解析】焓变等于反应物断裂化学键吸收的能量减去形成化学键释放的能量,由图可知,1 2N2(g)+32H2(g)=NH3(g) △H=(a-b)kJ•mol-1,12N2(g)+32H2(g)=NH3(l) △H=(a-b-c)kJ•mol-1,据此分析判断。
A.12N2(g)+32H2(g)=NH3(g) △H=(a-b)kJ•mol-1,则N2(g)+3H2(g)=2NH3(g) △H=-2(b-a)kJ•mol-1,错误;B.12N2(g)+32H2(g)=NH3(g) △H=(a-b)kJ•mol-1,则N2(g)+3H2(g)=2NH3(g)△H═-2(b-a)kJ•mol-1,错误;C.12N2(g)+32H2(g)=NH3(l) △H=(a-b-c)kJ•mol-1,则N2(g)+3H2(g)=2NH3(l) △H=2(a-b-c)kJ•mol-1,则2NH3(1)=N2(g)+3H2(g)△H=2(b+c-a)kJ•mol-1,正确;D.12N2(g)+32H2(g)=NH3(l) △H=(a-b-c)kJ•mol-1,则N2(g)+3H2(g)=2NH3(l) △H=2(a-b-c)kJ•mol-1,则2NH3(1)=N2(g)+3H2(g)△H=2(b+c-a)kJ•mol-1,错误;故选C。
2.(2014·海南高考真题)标准状态下,气态分子断开1 mol化学键的焓变称为键焓。

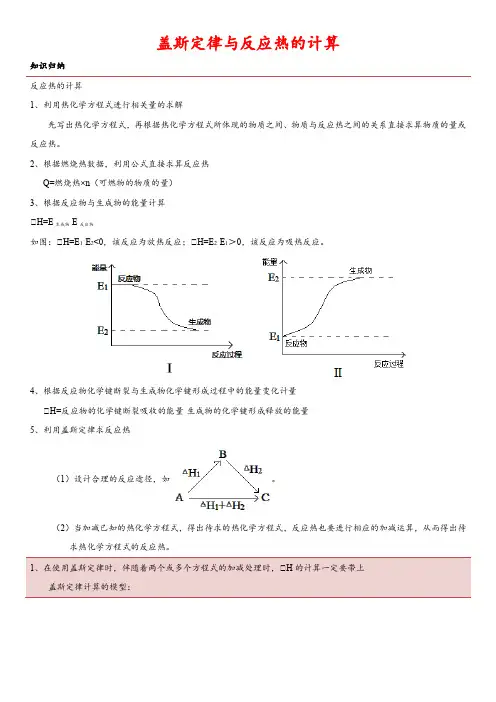
盖斯定律与反应热的计算知识归纳反应热的计算1、利用热化学方程式进行相关量的求解先写出热化学方程式,再根据热化学方程式所体现的物质之间、物质与反应热之间的关系直接求算物质的量或反应热。
2、根据燃烧热数据,利用公式直接求算反应热Q=燃烧热×n(可燃物的物质的量)3、根据反应物与生成物的能量计算△H=E生成物-E反应物如图:△H=E1-E2<0,该反应为放热反应;△H=E2-E1>0,该反应为吸热反应。
4、根据反应物化学键断裂与生成物化学键形成过程中的能量变化计量△H=反应物的化学键断裂吸收的能量-生成物的化学键形成释放的能量5、利用盖斯定律求反应热(1)设计合理的反应途径,如。
(2)当加减已知的热化学方程式,得出待求的热化学方程式,反应热也要进行相应的加减运算,从而得出待求热化学方程式的反应热。
1、在使用盖斯定律时,伴随着两个或多个方程式的加减处理时,△H的计算一定要带上盖斯定律计算的模型:(3)可燃物完全燃烧产生的热量=可燃物的物质的量×其燃烧热。
2、注意事项(1)反应热数值与各物质的化学计量数成正比,因此热化学方程式中各物质的化学计量数改变时,其反应热数值需同时作相同倍数的改变。
(2)热化学方程式中的反应热是指按所给形式完全进行时的反应热。
(3)正、逆反应的反应热数值相等,符号相反。
例题精讲例1、烟气(主要污染物SO2、NOx)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中SO2、NOx的含量。
O3氧化烟气中SO2、NOx的主要反应的热化学方程式为:NO(g)+O3(g)=NO2(g)+O2(g) △H=-200.9kJ·mol-1NO(g)+1/2O2(g)=NO2(g) △H=-58.2kJ·mol-1SO2(g)+O3(g)=SO3(g)+O2(g) △H=-241.6kJ·mol-1(1)反应3NO(g)+O3(g)=3NO2(g)的△H=_______mol·L-1。

2018年全国卷高考化学复习专题突破《反应热的计算与热化学斱程式的书写》一、反应热的计算斱法1.利用热化学斱程式进行有关计算根据已知的热化学斱程式、已知的反应物或生成物的物质的量、反应吸收或放出的热量,可以把反应热当作“产物”,计算反应放出或吸收的热量.2.根据燃烧热数据,计算反应放出的热量计算公式:Q=燃烧热×n(可燃物的物质的量).3.根据旧键断裂和新键形成过程中的能量差计算焓变若反应物旧化学键断裂吸收能量E1,生成物新化学键形成放出能量E2,则反应的ΔH=E1-E2.4.利用物质具有的能量计算:ΔH=∑E(生成物)-∑E(反应物).5.利用反应的互逆性关系计算:ΔH1=-ΔH2.6.利用盖斯定律计算:对于存在下列关系的反应:总结:根据盖斯定律计算ΔH的步骤和斱法1.计算步骤2.计算斱法二、热化学斱程式的书写与反应热大小的比较1.热化学斱程式书写的“六个注意”总结:热化学斱程式书写与正误判断的步骤2.反应热大小的比较斱法(1)利用盖斯定律比较,如比较ΔH1与ΔH2的大小的斱法.因ΔH1<0,ΔH2<0,ΔH3<0(均为放热反应),依据盖斯定律得ΔH1=ΔH2+ΔH3,即|ΔH1|>|ΔH2|,所以ΔH1<ΔH2.(2)同一反应的生成物状态不同时,如A(g)+B(g)=C(g)ΔH1 ;A(g)+B(g)=C(l)ΔH2,则ΔH1>ΔH2.(3)同一反应的反应物状态不同时,如A(s)+B(g)===C(g)ΔH1;A(g)+B(g)===C(g)ΔH2,则ΔH1>ΔH2.(4)两个有联系的反应相比较时,如C(s)+O 2(g)===CO 2(g) ΔH 1①;C(s)+12O 2(g)===CO(g) ΔH 2② 比较斱法:利用反应①(包括ΔH 1)乘以某计量数减去反应②(包括ΔH 2)乘以某计量数,即得出ΔH 3=ΔH 1×某计量数-ΔH 2×某计量数,根据ΔH 3大于0或小于0进行比较.总之,比较反应热的大小时要注意:①反应中各物质的聚集状态;②ΔH 有正负之分,比较时要连同“+”、“-”一起比较,类似数学中的正、负数大小的比较;③若只比较放出或吸收热量的多少,则只比较数值的大小,不考虑正、负号.真题练习1.已知下列反应:SO 2(g)+2OH -(aq)===SO 2-3(aq)+H 2O(l) ΔH 1ClO -(aq)+SO 2-3(aq)===SO 2-4(aq)+Cl -(aq) ΔH 2CaSO 4(s)===Ca 2+(aq)+SO 2-4(aq) ΔH 3则反应SO 2(g)+Ca 2+(aq)+ClO -(aq)+2OH -(aq)===CaSO 4(s)+H 2O(l)+Cl -(aq)的ΔH =________.[解析] 将题给三个热化学斱程式分别标号为Ⅰ、Ⅱ、Ⅲ,根据盖斯定律,由Ⅰ+Ⅱ-Ⅲ可得:SO 2(g)+Ca 2+(aq)+ClO -(aq)+2OH -(aq)===CaSO 4(s)+H 2O(l)+Cl -(aq),则有ΔH =ΔH 1+ΔH 2-ΔH 3.[答案] ΔH 1+ΔH 2-ΔH 32.(1)已知反应2HI(g)===H 2(g)+I 2(g)的ΔH =+11 kJ·mol -1,1 mol H 2(g)、1 mol I 2(g)分子中化学键断裂时分别需要吸收436 kJ 、151 kJ 的能量,则1 mol HI(g)分子中化学键断裂时需吸收的能量为________kJ.(2)甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分为CO 、CO 2和H 2)在催化剂作用下合成甲醇.发生的主要反应如下:①CO(g)+2H 2(g)===CH 3OH(g) ΔH 1 ②CO 2(g)+3H 2(g)===CH 3OH(g)+H 2O(g) ΔH 2③CO 2(g)+H 2(g)===CO(g)+H 2O(g) ΔH 3回答下列问题:C 由此计算ΔH 1=23[解析] (1)设1 mol HI(g)分子中化学键断裂吸收的能量为x ,则2x -436 kJ -151 kJ =+11 kJ,x =299 kJ.(2)根据键能与反应热的关系可知,ΔH 1=反应物的键能之和-生成物的键能之和=(1 076 kJ·mol -1+2×436 kJ·mol -1)-(413 kJ·mol -1×3+343 kJ·mol -1+465 kJ·mol -1)=-99 kJ·mol -1.根据质量守恒定律,由②-①可得:CO 2(g)+H 2(g)⇌CO(g)+H 2O(g),结合盖斯定律可得:ΔH 3=ΔH 2-ΔH 1=(-58 kJ·mol -1)-(-99 kJ·mol -1)=+41 kJ·mol -1.[答案] (1)299 (2)-99 +413.(1)已知:甲醇脱水反应:2CH 3OH(g)===CH 3OCH 3(g)+H 2O(g) ΔH 1=-23.9 kJ·mol -1甲醇制烯烃反应:2CH 3OH(g)===C 2H 4(g)+2H 2O(g) ΔH 2=-29.1 kJ·mol -1乙醇异构化反应:C 2H 5OH(g)===CH 3OCH 3(g) ΔH 3=+50.7 kJ·mol -1则乙烯气相直接水合反应C 2H 4(g)+H 2O(g)===C 2H 5OH(g)的ΔH =__kJ·mol -1.(2)二甲醚(CH 3OCH 3)是无色气体,可作为一种新型能源.由合成气(组成为H 2、CO 和少量的CO 2)直接制备二甲醚,其中的主要过程包括以下四个反应:甲醇合成反应:(ⅰ)CO(g)+2H 2(g)==CH 3OH(g) ΔH 1=-90.1 kJ·mol -1(ⅱ)CO 2(g)+3H 2(g)==CH 3OH(g)+H 2O(g) ΔH 2=-49.0 kJ·mol -1水煤气变换反应:(ⅲ)CO(g)+H 2O(g)==CO 2(g)+H 2(g) ΔH 3=-41.1 kJ·mol -1二甲醚合成反应:(ⅳ)2CH 3OH(g)==CH 3OCH 3(g)+H 2O(g) ΔH 4=-24.5 kJ·mol -1由H 2和CO 直接制备二甲醚(另一产物为水蒸气)的热化学斱程式为___________________.[解析](1)2CH 3OH(g)===CH 3OCH 3(g)+H 2O(g) ΔH 1=-23.9 kJ·mol -1 ①2CH 3OH(g)===C 2H 4(g)+2H 2O(g) ΔH 2=-29.1 kJ·mol -1 ②C 2H 5OH(g)===CH 3OCH 3(g) ΔH 3=+50.7 kJ·mol -1 ③根据盖斯定律,由①-②-③得:C 2H 4(g)+H 2O(g)===C 2H 5OH(g) ΔH =-45.5 kJ·mol -1.(2)写出由H 2和CO 直接制备二甲醚的化学斱程式:4H 2+2CO=== CH 3OCH 3+H 2O.由(ⅰ)得:2CO(g)+4H 2(g)===2CH 3OH(g) ΔH 1=(-90.1)×2 kJ·mol -1;由(ⅳ)得:2CH 3OH(g)===CH 3OCH 3(g)+H 2O(g) ΔH 4=-24.5 kJ·mol -1;以上两式相加得所求热化学斱程式的ΔH =(-90.1×2)kJ·mol -1+(-24.5) kJ·mol -1=-204.7 kJ·mol -1.故热化学斱程式为4H 2(g)+2CO(g)==CH 3OCH 3(g)+H 2O(g) ΔH =-204.7 kJ·mol -1.[答案] (1)-45.5 (2)4H 2(g)+2CO(g)===CH 3OCH 3(g)+H 2O(g) ΔH =-204.7 kJ·mol -14.室温下,将1 mol 的CuSO 4·5H 2O(s)溶于水会使溶液温度降低,热效应为ΔH 1,将1 mol 的CuSO 4(s)溶于水会使溶液温度升高,热效应为ΔH 2;CuSO 4·5H 2O 受热分解的化学斱程式为CuSO 4·5H 2O(s)=====△CuSO 4(s)+5H 2O(l),热效应为ΔH 3.则下列判断正确的是( )A .ΔH 2>ΔH 3B .ΔH 1<ΔH 3C .ΔH 1+ΔH 3=ΔH 2D .ΔH 1+ΔH 2>ΔH 3B [1 mol CuSO 4·5H 2O(s)溶于水会使溶液温度降低,为吸热反应,故ΔH 1>0,1 mol CuSO 4(s)溶于水会使溶液温度升高,为放热反应,故ΔH 2<0,1 mol CuSO 4·5H 2O(s)溶于水可以分为两个过程,先分解成1 mol CuSO 4(s)和5 mol 水,然后1 mol CuSO 4(s)再溶于水,CuSO 4·5H 2O 的分解为吸热反应,即ΔH 3>0,根据盖斯定律得到关系式ΔH 1=ΔH 2+ΔH 3,分析得到答案:ΔH 1<ΔH 3.]5.在1 200 ℃时,天然气脱硫工艺中会发生下列反应H 2S(g)+32O 2(g)===SO 2(g)+H 2O(g) ΔH 1 2H 2S(g)+SO 2(g)===32S 2(g)+2H 2O(g) ΔH 2 H 2S(g)+12O 2(g)===S(g)+H 2O(g) ΔH 3 2S(g)===S 2(g) ΔH 4则ΔH 4的正确表达式为( )A .ΔH 4=23(ΔH 1+ΔH 2-3ΔH 3)B .ΔH 4=23(3ΔH 3-ΔH 1-ΔH 2) C .ΔH 4=32(ΔH 1+ΔH 2-3ΔH 3) D .ΔH 4=32(ΔH 1-ΔH 2-3ΔH 3) A [根据盖斯定律找出各反应的反应热之间的关系.将前三个热化学斱程式分别标为①、②、③,根据盖斯定律,由23×①+23×②-2×③可得:2S(g)===S 2(g) ΔH 4=23(ΔH 1+ΔH 2-3ΔH 3).] 考点一:利用化学键计算反应热,热化学斱程式的书写1.已知:C(s)+H 2O(g)===CO(g)+H 2(g) ΔH =a kJ·mol -12C(s)+O 2(g)===2CO(g) ΔH =-220 kJ·mol -1 ,H —H 键、O===O 键和O —H 键的键能分别为436 kJ·mol -1、496 kJ·mol -1和462 kJ·mol -1,则a 为( )A .-332 B. -118C .+350 D. +130D [将两个热化学斱程式分别标为①、②,则根据盖斯定律可知②-①×2即得到热化学斱程式O 2(g)+2H 2(g)===2H 2O(g) ΔH =-(220+2a ) kJ/mol.由于反应热等于断键吸收的能量与形成新化学键所放出的能量的差值,则496 kJ/mol +2×436 kJ/mol -2×2×462 kJ/mol =-(220+2a ) kJ/mol,解得a =+130,答案选D.]2.已知:①破坏1 mol A —A 键、1 mol B —B 键、1 mol A —B 键时分别需要吸收436 kJ 、498 kJ 、463 kJ 的能量;②反应2A 2(g)+B 2(g)===2A 2B(g)的能量变化如图所示.下列说法中错误的是( )A .体系中A 2、B 2最活泼 B .E 1=1 370 kJ·mol -1C .ΔH =-482 kJ·mol -1D .该反应是放热反应A [由题图可以看出,反应物的总能量高于生成物的总能量,所以该反应是放热反应,D 正确;E 1表示断开反应物中化学键所吸收的能量(即反应的活化能),则E 1=2×436 kJ·mol -1+498 kJ·mol -1=1 370 kJ·mol -1,B 正确;E 2表示形成生成物中化学键所放出的热量,则E 2=2×2×463 kJ·mol -1=1 852 kJ·mol -1,ΔH =E 1-E 2=1 370 kJ·mol -1-1 852 kJ·mol -1=-482 kJ·mol -1,C 正确;图中A 和B 具有的能量最高,因此A 和B 最活泼,故A 错误.]3.燃料的使用和防止污染是社会发展中一个无法回避的矛盾话题.直接排放煤燃烧产生的烟气会引起严重的环境问题.煤燃烧产生的烟气含氮的氧化物,用CH 4催化还原NO x 可以消除氮氧化物的污染.(1)已知:①CH 4(g)+2NO 2(g)===N 2(g)+CO 2(g)+2H 2O(g) ΔH 1=-860.0 kJ·mol -1②2NO 2(g)⇌N 2O 4(g) ΔH 2=-66.9 kJ·mol -1写出CH 4催化还原N 2O 4(g)生成N 2和H 2O(g)、CO 2的热化学斱程式:______________________________________________________________.(2)如图为1 mol NO 2(g)和1 mol CO(g)反应生成NO(g)和CO 2(g)过程中的能量变化示意图.已知E 1=134 kJ/mol,E 2=368 kJ/mol(E 1、E 2为反应的活化能).若在反应体系中加入催化剂,反应速率增大,则E 1、ΔH 的变化分别是________、________(填“增大”“减小”或“不变”).写出该反应的热化学斱程式:________________________.[解析] (1)根据盖斯定律,反应①-反应②即可得热化学斱程式:CH 4(g)+N 2O 4(g)===N 2(g)+CO 2(g)+2H 2O(g)ΔH =-860.0 kJ·mol -1+66.9 kJ·mol -1=-793.1 kJ·mol -1.(2)E 1为该反应的活化能,加入催化剂能降低反应的活化能但不能改变反应热.ΔH =生成物总能量-反应物总能量=E 1-E 2,据此可写出反应的热化学斱程式.[答案] (1)CH 4(g)+N 2O 4(g)===N 2(g)+CO 2(g)+2H 2O(g) ΔH =-793.1 kJ·mol -1(2)减小 不变 NO 2(g)+CO(g)===NO(g)+CO 2(g) ΔH =-234 kJ·mol -14.参考下列图表和有关要求回答问题:(1)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:①CH 3OH(g)+H 2O(g)===CO 2(g)+3H 2(g) ΔH =+49.0 kJ·mol -1②CH 3OH(g)+12O 2(g)===CO 2(g)+2H 2(g) ΔH =-192.9 kJ·mol -1 又知:③H 2O(g)===H 2O(l) ΔH =-44 kJ·mol -1则甲醇燃烧生成液态水的热化学斱程式为___________________________.(2)已知1 mol 白磷(P 4)完全燃烧放热为d kJ,白磷及其完全燃烧的产物结构如图所示,则上表中x =________(用含有a 、b 、c 、d 的代数式表示).[解析] (1)②×3-①×2+③×2得CH 3OH(g)+32O 2(g)===CO 2(g)+2H 2O(l) ΔH =3×(-192.9 kJ·mol -1)-2×49.0 kJ·mol -1+(-44 kJ·mol -1)×2=-764.7 kJ·mol -1.(2)反应热=反应物键能总和-生成物键能总和,即6a +5c -(4x +12b )=-d ,解得x =-14(12b -d -6a -5c )或14(d +6a +5c -12b ). [答案] (1)CH 3OH(g)+32O 2(g)===CO 2(g)+2H 2O(l) ΔH =-764.7 kJ·mol -1 (2)-14(12b -d -6a -5c )或14(d +6a +5c -12b ) 考点二:盖斯定律及其应用1.用H 2可将工业废气中的NO 催化还原为N 2,其能量转化关系如图(图中计量单位为mol),则:NO(g)+H 2(g)===12N 2(g)+H 2O(g)的ΔH 为( )A .12(a +b -c -d ) kJ·mol -1B .12(c +a -d -b ) kJ·mol -1 C .12(c +d -a -b ) kJ·mol -1 D .12(c +d -a -b ) kJ·mol -1 A [由图中转化可知,断裂化学键吸收能量,形成化学键释放能量,发生2NO(g)+2H 2(g)===N 2(g)+2H 2O(g) ΔH =(a +b -c -d ) kJ·mol -1,又因为化学计量数与反应中的能量变化成正比,则NO(g)+H 2(g)===12N 2(g)+H 2O(g) ΔH =12(a +b -c -d ) kJ·mol -1.] 2.(2016·昆明重点中学测试四)氢气、铝、铁都是重要的还原剂.已知下列反应的热化学斱程式:2H 2(g)+O 2(g)===2H 2O(g) ΔH 13H 2(g)+Fe 2O 3(s)===2Fe(s)+3H 2O(g) ΔH 22Fe(s)+32O 2(g)===Fe 2O 3(s) ΔH 3 2Al(s)+32O 2(g)===Al 2O 3(s) ΔH 4 2Al(s)+Fe 2O 3(s)===Al 2O 3(s)+2Fe(s) ΔH 5下列关于上述反应焓变的判断正确的是( )A .ΔH 1<0,ΔH 3>0B .ΔH 5<0,ΔH 4<ΔH 3C .ΔH 1=ΔH 2+ΔH 3D .ΔH 3=ΔH 4+ΔH 5B [燃烧反应是放热反应,故ΔH 1<0,ΔH 3<0,A 错;铝热反应是放热反应,故ΔH 5<0,ΔH 5=ΔH 4-ΔH 3<0,即ΔH 4<ΔH 3,B 正确;ΔH 1=(ΔH 2+ΔH 3)×2/3,C 错;ΔH 3=ΔH 4-ΔH 5,D 错.]3.已知下列热化学斱程式:①2C(s)+O 2(g)===2CO(g) ΔH =-221.0 kJ·mol -1;②C(s)+O 2(g)===CO 2(g) ΔH =-393.5 kJ·mol -1;③2CO(g)+O 2(g)===2CO 2(g) ΔH =-566.0 kJ·mol -1;④CH 4(g)+2O 2(g)===CO 2(g)+2H 2O(g) ΔH =-890.0 kJ·mol -1.请回答下列问题:(1)CO 的燃烧热为_________________________________.(2)炽热的木炭与二氧化碳反应生成一氧化碳的反应为________(填“放热”或“吸热”)反应,理由是__________________________.(3)实验中测定甲烷与氧气反应生成CO 的反应热不易操作,原因是_____,写出甲烷与氧气反应生成CO 的热化学斱程式:______________________.[解析] (1)由热化学斱程式③可知CO 的燃烧热为-283.0 kJ·mol -1.(2)热化学斱程式①减去热化学斱程式②可得C(s)+CO 2(g)===2CO(g) ΔH =+172.5 kJ·mol -1,故该反应为吸热反应.(3)甲烷燃烧时,无法控制反应使其完全生成CO,一般生成CO 和CO 2的混合物,故甲烷与氧气反应生成CO 的反应热不易直接测定.根据盖斯定律,④×2-③即得新的热化学斱程式2CH 4(g)+3O 2(g)===2CO(g)+4H 2O(g) ΔH =-1 214.0 kJ·mol -1.[答案] (1)-283.0 kJ·mol -1 (2)吸热 由热化学斱程式①减去热化学斱程式②可得C(s)+CO 2(g)===2CO(g) ΔH =+172.5 kJ·mol -1 (3)不能保证甲烷全部生成CO 2CH 4(g)+3O 2(g)===2CO(g)+4H 2O(g) ΔH =-1 214.0 kJ·mol -14.运动会中的火炬一般采用丙烷为燃料.丙烷的热值较高,污染较小,是一种优良的燃料.试回答下列问题:(1)一定量的丙烷完全燃烧生成CO 2(g)和1 mol H 2O(l)过程中的能量变化曲线如图所示,请在图中的括号内填“+”或“-”.(2)写出表示丙烷燃烧热的热化学斱程式:______________________________________________________________.(3)二甲醚(CH 3OCH 3)是一种新型燃料,应用前景广阔.1 mol 二甲醚完全燃烧生成CO 2(g)和H 2O(l)时放出1 455 kJ 热量.若1 mol 丙烷和二甲醚的混合气体完全燃烧生成CO 2(g)和H 2O(l)时共放出1 645 kJ 热量,则混合气体中丙烷和二甲醚的物质的量之比为________.[解析] (1)一定量的丙烷完全燃烧生成CO 2(g)和1 mol H 2O(l)的过程放热,ΔH 为负值.(2)燃烧热是1 mol 物质完全燃烧生成稳定氧化物时放出的热量,所以表示丙烷燃烧热的热化学斱程式为C 3H 8(g)+5O 2(g)===3CO 2(g)+4H 2O(l) ΔH =-2 215.0 kJ·mol -1.(3)n (二甲醚)×1 455 kJ·mol -1+[1 mol -n (二甲醚)]×2 215.0 kJ·mol -1=1 645 kJ,解得n (二甲醚)=0.75 mol ,n (丙烷)=0.25 mol.[答案] (1)- (2)C 3H 8(g)+5O 2(g)===3CO 2(g)+4H 2O(l) ΔH =-2 215.0 kJ·mol -1 (3)1∶35.通常人们把断开1 mol 化学键所吸收的能量看成是该化学键的键能.已知N 2、O 2分子中化学键的键能分别是946 kJ·mol -1、497 kJ·mol -1.查阅资料知:①N 2(g)+O 2(g)===2NO(g) ΔH =+180 kJ·mol -1②2NO(g)+O 2(g)===2NO 2(g) ΔH =-112 kJ·mol -1③2C(s)+O 2(g)===2CO(g) ΔH =-221 kJ·mol -1④C(s)+O 2(g)===CO 2(g) ΔH =-393.5 kJ·mol -1(1)NO 分子中化学键的键能为_________________________.(2)CO 与NO 2反应的热化学斱程式为4CO(g)+2NO 2(g)===4CO 2(g)+N 2(g) ΔH =________.[解析] (1)N 2(g)+O 2(g)===2NO(g) ΔH =+180 kJ·mol -1,断开1 mol 反应物的化学键共吸收热量:946 kJ +497 kJ=1 443 kJ,则NO 分子中化学键的键能为1 443-1802kJ·mol -1=631.5 kJ·mol -1, (2)根据盖斯定律,由4×④-(2×③+①+②)可得4CO(g)+2NO 2(g)===4CO 2(g)+N 2(g) ΔH =-1 200 kJ·mol -1.[答案] (1)631.5 kJ·mol -1 (2)-1 200 kJ·mol -1。

反应热的计算课后练习(2)1.化学在能源开发与利用中起着十分关键的作用.(1)蕴藏在海底的“可燃冰”是高压下形成的外观象冰的甲烷水合物固体.甲烷气体燃烧和水汽化的热化学方程式如下:CH4(g)+2O2(g)===CO2(g)+2H2O(g)ΔH=-802.3 kJ·mol-1H2O(l)===H2O(g)ΔH=+44 kJ·mol-1则356 g“可燃冰”(分子式为CH4·9H2O)释放的甲烷气体完全燃烧生成液态水,放出的热量为____________________________________________________.(2)0.3 mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5 kJ热量,其热化学方程式为______________________________________(3)家用液化气中主要成分之一是丁烷.当丁烷完全燃烧并生成CO2和液态水时,放出热量50 kJ.试写出丁烷燃烧的热化学方程式______________________________.2.已知两个热化学方程式:2H2(g)+O2(g)==2H2O(l); △H= -571.6 kJ/molC3H8(g) +5O2(g)==3CO2(g)+4 H2O(l); △H= -2220kJ/mol实验测得H2和C3H8混合气体共5mol,完全燃烧时放热3847kJ,则混合气体中H2与C3H8的体积比为()A.1:3B.3:1C.1:4D.1:13. CO、CH4均为常见的可燃性气体。
(1)等体积的CO和CH4在相同条件下分别完全燃烧,转移的电子数之比是________。
(2)已知在101 kPa时,CO的燃烧热为283 kJ/mol。
相同条件下,若2 mol CH4完全燃烧生成液态水,所放出的热量为1 mol CO完全燃烧放出热量的6.30 倍,CH4完全燃烧反应的热化学方程式是____________________________________________________。

化学反应热的相关计算非选择题(共15题)1.随着世界工业经济的发展、人口的剧增,全球能源紧张及世界气候面临越来越严重的问题,如何降低大气中CO 2的含量及有效地开发利用CO 2引起了全世界的普遍重视。
(1)把煤作为燃料可通过下列两种途径:途径I :C(s)+O 2(g)=CO 2(g) △H 1<0①途径II :先制成水煤气:C(s)+H 2O(g)=CO(g)+H 2(g) △H 2>0②再燃烧水煤气:2CO(g)+O 2(g)=2CO 2(g) △H 3<0③2H 2(g)+O 2(g)=2H 2O(g) △H 4<0④则途径I 放出的热量___________(填“大于”“等于”或“小于”)途径II 放出的热量;△H 1、△H 2、△H 3、△H 4的数学关系式是___________。
(2)在25℃、101kPa 下,1克甲醇完全燃料放热22.68kJ ,写出甲醇燃烧热的热化学方程式___________。
(3)已知①()()()221CO g +O g =CO g ?ΔH =-283.0kJ 12/mol ②H 2(g)+12O 2(g)=H 2O(l) ΔH 2=-285.8kJ/mol③C 2H 5OH(l)+3O 2(g)=2CO 2(g)+3H 2O(l) ΔH 3=-1370kJ/mol试计算④2CO(g)+4H 2(g)=H 2O(l)+C 2H 5OH(l)的ΔH=___________。
(4)臭氧可用于净化空气、饮用水消毒,处理工业废物和作为漂白剂。
臭氧几乎可与除铂、金、铱、氟以外的所有单质反应。
如:6Ag(s)+O 3(g)=3Ag 2O(s) △H=-235.8kJ•mol -1 已知:2Ag 2O(s)=4Ag(s)+O 2(g) △H=+62.2kJ•mol -1;则O 3转化为O 2的热化学方程式为___________。
2. (1) 已知反应: ①C(s)+1/2O 2(g)= CO(g) ΔH 1=-110.5 kJ·mol -1②C(s)+O 2(g)===CO 2(g) ΔH2=-393.5 kJ·mol -1写出表示CO 燃烧热的热化学方程式______________________。
热化学方程式反应焓变的计算A组1.2014年9月3日,“创新征程——2014年新能源汽车万里行”上海站发车。
中国制造的燃料电池车进行“路考”,车辆只吸收氢气,污染为零。
已知在101 kPa、298 K条件下,2 mol H2(g)完全燃烧生成水蒸气放出484 kJ热量,下列热化学方程式正确的是( )O2(g) ΔH(298 K)=+242 kJ·mol-1A.H2O(g)H2(g)+12B.2H2(g)+O2(g)2H2O(l) ΔH(298 K)=-484 kJ·mol-1C.H2(g)+1O2(g)H2O(g) ΔH(298 K)=+242 kJ·mol-12D.2H2(g)+O2(g)2H2O(g) ΔH(298 K)=+484 kJ·mol-1解析:在判断热化学方程式时,应注意以下几点:①标明各物质的状态,B中H2O的状态标错,B错误。
②标明反应是吸热还是放热,C、D应为负值,故C、D错误。
③若反应逆向进行,ΔH应改变符号,但绝对值不变,故A正确。
答案:A2.下列各组热化学方程式中,化学反应的反应热ΔH前者大于后者的是( )①C(s)+O2(g)CO2(g) ΔH1O2(g)CO(g) ΔH2C(s)+12②C3H8(g)+5O2(g)3CO2(g)+4H2O(g) ΔH32C3H8(g)+10O2(g)6CO2(g)+8H2O(g) ΔH4③2H2O(g)2H2(g)+O2(g) ΔH5NaOH(aq)+HCl(aq)NaCl(aq)+H2O(l) ΔH6A.①B.①③C.②③D.①②③解析:等量的碳在氧气中完全燃烧生成二氧化碳放出的热量大于不完全燃烧生成一氧化碳放出的热量,但放热反应的ΔH为负值,所以放出的热量越多,ΔH越小,故①中ΔH前者小于后者;可燃物越多,放出的热量越多,②中前者是1molC3H8(g)燃烧,后者是2molC3H8(g)燃烧,所放出的热量后者较多,同样放热反应的ΔH为负值,所以②中ΔH前者大于后者;③中前者为吸热反应,后者为放热反应,吸热反应ΔH>0,放热反应ΔH<0,ΔH前者大于后者。
专题强化练(二) 热化学方程式、反应焓变的计算1.已知热化学方程式2H 2(g)+O 2(g)===2H 2O(l) ΔH 1=-571.6 kJ ·mol -1,则下列关于热化学方程式2H 2O(l)===2H 2(g)+O 2(g) ΔH 2的说法正确的是( )A .热化学方程式中的系数表示分子数B .该反应中ΔH 2>0C .该反应中ΔH 2=-571.6 kJ ·mol -1D .该反应与题述反应互为可逆反应解析:选B 热化学方程式中的系数表示物质的物质的量,不表示分子数。
该反应是2H 2(g)+O 2(g)===2H 2O(l) ΔH 1=-571.6 kJ ·mol -1逆向进行的反应,其反应热ΔH 2=+571.6 kJ ·mol -1,但该反应与题述反应不互为可逆反应,因为二者的反应条件不同。
2.S(单斜)和S(正交)是硫的两种同素异形体。
已知:①S(单斜,s)+O 2(g)===SO 2(g) ΔH 1=-297.16 kJ ·mol -1②S(正交,s)+O 2(g)===SO 2(g) ΔH 2=-296.83 kJ ·mol -1③S(单斜,s)===S(正交,s) ΔH 3下列说法正确的是 ( )A .ΔH 3=+0.33 kJ ·mol -1B .单斜硫转化为正交硫的反应是吸热反应C .S(单斜,s)===S(正交,s) ΔH 3<0,正交硫比单斜硫稳定D .S(单斜,s)===S(正交,s) ΔH 3>0,单斜硫比正交硫稳定解析:选C 由已知,反应③=①-②,则由盖斯定律可得三个反应的焓变关系为ΔH 3=ΔH 1-ΔH 2=(-297.16 kJ ·mol -1)-(-296.83 kJ ·mol -1)=-0.33 kJ ·mol -1,故A 错;反应③焓变小于零,为放热反应,S(单斜)所含能量高于S(正交)所含能量,能量越低越稳定,所以正交硫比单斜硫稳定,故B 、D 错,C 正确。
3.已知下列热化学方程式:Fe 2O 3(s)+3CO(g)===2Fe(s)+3CO 2(g) ΔH =-24.8 kJ ·mol -1;Fe 2O 3(s)+13CO(g)===23Fe 3O 4(s)+13CO 2(g) ΔH =-15.73 kJ ·mol -1; Fe 3O 4(s)+CO(g)===3FeO(s)+CO 2(g) ΔH =+640.4 kJ ·mol -1;则14 g CO 气体还原足量FeO 固体得到Fe 单质和CO 2气体时对应的ΔH 约为 ( )A .-218 kJ ·mol -1B .-109 kJ ·mol -1C .+218 kJ ·mol -1D .+109 kJ ·mol -1解析:选B 14 g CO 气体的物质的量为12 mol 。
该问题可以转化为12CO(g)+12FeO(s)===12Fe(s)+12CO 2(g) ΔH =?所以应用盖斯定律,若把已知给出的3个热化学方程式按照顺序编号为①、②、③,那么由已知反应①×14-②×14-③×16即可得到所求反应,再由盖斯定律即可得出结果。
4.下列关系式正确的是 ( )①H 2(g)+12O 2(g)===H 2O(g) ΔH 1=a kJ ·mol -1 ②2H 2(g)+O 2(g)===2H 2O(g) ΔH 2=b kJ ·mol -1③H 2(g)+12O 2(g)===H 2O(l) ΔH 3=c kJ ·mol -1 ④2H 2(g)+O 2(g)===2H 2O(l) ΔH 4=d kJ ·mol -1A .a <c <0B .b >d >0C .2a =b <0D .2c =d >0解析:选C ①和②、③和④中H 2、O 2、H 2O 的聚集状态分别相同,且②和④中各物质的化学计量数分别是①、③中的2倍,所以b =2a ,d =2c 。
①、②、③、④均为放热反应,a 、b 、c 、d 均小于零,所以选项B 、D 错误;由于H 2O(g)―→H 2O(l)这一过程放出热量,所以反应③中放出的热量比反应①多,即c 的绝对值比a 大,但由于a 、c 均小于零,所以c <a ,A 项错误。
5.下列说法或表示方法正确的是 ( )A .已知C(s)+O 2(g)===CO 2(g) ΔH 1;C(s)+12O 2(g)===CO(g) ΔH 2,则ΔH 1>ΔH 2 B .在稀溶液中,H +(aq)+OH -(aq)===H 2O(l) ΔH =-57.3 kJ ·mol -1,若将含0.5 mol H 2SO 4的浓硫酸与含1 mol NaOH 的溶液混合,放出的热量大于57.3 kJC .由C(石墨)(s)===C(金刚石)(s) ΔH =+1.90 kJ ·mol -1可知,金刚石比石墨稳定D .在101 kPa 时,2 g H 2 完全燃烧生成液态水,放出 285.8 kJ 热量,则表示氢气燃烧的热化学方程式为2H 2(g)+O 2(g)===2H 2O(l) ΔH =-285.8 kJ ·mol -1解析:选B A 项,1 mol 碳完全燃烧放出的热量应大于不完全燃烧放出的热量,因ΔH 1、ΔH 2均小于零,所以ΔH 1<ΔH 2,错误;B 项,浓硫酸稀释过程中要放热,因此放出的热量大于57.3 kJ ,正确;石墨转化为金刚石为吸热反应,则金刚石所具有的能量高于石墨所具有的能量,能量越高越不稳定,所以金刚石不如石墨稳定,错误;2 g 即1 mol H 2完全燃烧生成液态水,放出285.8 kJ 热量,所以热化学方程式中2 mol H 2反应对应的焓变应为-571.6 kJ ·mol -1,错误。
6.在101 kPa 298 K 条件下,气态分子断开1 mol 化学键的焓变称为键焓,H —H 、H —O 和O===O 键的键焓ΔH 分别为436 kJ ·mol -1、463 kJ ·mol -1和495 kJ ·mol -1。
下列热化学方程式正确的是( )A .H 2O(g)===H 2(g)+12O 2(g) ΔH =-485 kJ ·mol -1 B .H 2O(g)===H 2(g)+12O 2(g) ΔH =+485 kJ ·mol -1 C .2H 2(g)+O 2(g)===2H 2O(g) ΔH =+485 kJ ·mol -1D .2H 2(g)+O 2(g)===2H 2O(g) ΔH =-485 kJ ·mol -1解析:选D H 2O(g)===H 2(g)+12O 2(g)的ΔH =463 kJ ·mol -1×2-436 kJ ·mol -1-495 kJ ·mol -1×12=+242.5 kJ ·mol -1,A 、B 项错误;2H 2(g)+O 2(g)===2H 2O(g) ΔH =-485 kJ ·mol -1,C 项错误,D 项正确。
7.煤燃烧的反应热的利用有如下两条途径:Ⅰ.利用煤在充足的空气中直接燃烧产生的热量。
Ⅱ.先使煤气化,即将煤与水蒸气反应得到氢气和一氧化碳,然后使氢气和一氧化碳在充足的空气中燃烧。
这两个过程的热化学方程式分别为:Ⅰ.C(s)+O 2(g)===CO 2(g) ΔH 1=a kJ ·mol -1Ⅱ.C(s)+H 2O(g)===CO(g)+H 2(g) ΔH 2=b kJ ·mol -1H 2(g)+12O 2(g)===H 2O(g) ΔH 3=c kJ ·mol -1 CO(g)+12O 2(g)===CO 2(g) ΔH 4=d kJ ·mol -1 填写下列空白:(1)途径Ⅱ与途径Ⅰ相比有许多优点,其优点是 。
(2)上述四个热化学方程式中________大于零(填“ΔH 1”“ΔH 2”“ΔH 3”或“ΔH 4”)。
(3)等质量的煤分别按以上两个不同途径反应产生的反应热的正确关系是________。
A .Ⅰ比Ⅱ多B .Ⅰ比Ⅱ少C .Ⅰ与Ⅱ在理论上相同(4)依据能量守恒定律,ΔH 1、ΔH 2、ΔH 3、ΔH 4之间的关系为 。
解析:(1)煤作为燃料直接使用,不仅燃烧不充分,还会产生SO 2等污染性气体,将煤气化后,既便于管道输送,又能使煤燃烧充分,热效率高,还能除去硫,减少污染。
(2)只有碳和水蒸气的反应属于吸热反应,故ΔH 2>0。
(3)根据盖斯定律,将Ⅱ中的三个热化学方程式相加就能得到Ⅰ中方程式,因此C 正确。
(4)由(3)可知,ΔH 1=ΔH 2+ΔH 3+ΔH 4。
答案:(1)煤气化后便于管道输送,燃烧充分、利用率高,洁净 (2)ΔH 2 (3)C(4)ΔH1=ΔH2+ΔH3+ΔH41.碘在不同状态下(固态或气态)与氢气反应的热化学方程式如下所示:①H2(g)+I2(?)===2HI(g) ΔH=+9.48 kJ·mol-1②H2(g)+I2(?)===2HI(g) ΔH=-26.48 kJ·mol-1下列判断正确的是 ( ) A.①中的I2为气态,②中的I2为固态B.①的反应物总能量比②的反应物总能量低C.①的产物比②的产物热稳定性好D.1 mol 固态碘升华时将吸热17 kJ解析:选B 分析两个热化学方程式可知,①中反应物的总能量较②中反应物的总能量低,故①中I2为固态,②中I2为气态,A项错误,B项正确;两反应中生成物的状态相同,故热稳定性相同,C项错误;由①式-②式可知1 mol 固态碘升华时将吸热35.96 kJ,故D 项错误。
2.用CH4催化还原NO x可以消除氮氧化物的污染。
如:①CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1②CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g) ΔH=-1 160 kJ·mol-1下列说法中错误的是 ( ) A.等物质的量的CH4在反应①、②中转移电子数相同B.由反应①可推知:CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(l) ΔH>-574 kJ·mol-1C.4NO2(g)+2N2(g)===8NO(g) ΔH=+586 kJ·mol-1D.若用标准状况下4.48 L CH4把NO2还原为N2,整个过程中转移的电子总数为1.6N A 解析:选B A项,反应①、②中均有CH4~CO2~8e-,故等物质的量的CH4在反应①、②中转移电子数相同;B项,相同条件下,生成液态水比生成气态水放热多,故ΔH<-574 kJ·mol-1;C项,根据盖斯定律,由①-②可得4NO2(g)+2N2(g)===8NO(g) ΔH=+586 kJ·mol-1;D项,CH4最终全部转化为CO2,故转移的电子总物质的量为4.48 L22.4 L·mol-1×8=1.6 mol,即1.6N A。