选修5有机化学基础第二章第二节芳香烃
- 格式:ppt
- 大小:3.73 MB
- 文档页数:61





芳香烃教学设计一、基本说明1、教学内容所属模块:高中化学选修5《有机化学基础》2、年级:高二年级3、所用教材出版单位:人民教育4、所属章节:第二章第二节二、教学设计1、教学目标知识与技能①了解苯的同系物概念。
②学习掌握苯及苯的同系物的结构和性质。
③通过对苯环与甲基的相互影响了解苯与苯的同系物性质上的异同。
④初步掌握苯与苯的同系物的鉴别方法。
过程与方法①通过甲苯使酸性高锰酸钾褪色实验让学生体验反应的真实,培养学生实验设计和实验操作的能力。
②通过对苯环与甲基的相互影响,培养学生辨证思维及用联系的观点看问题的方法。
③通过对甲烷、乙烯、苯、苯的同系物的对比,培养学生分类对比学习的能力。
情感态度和价值观①通过探究实验培养学生严谨求实的科学态度。
②通过实验及分析对比让学生体验学习的乐趣及成就感。
2、内容分析芳香烃这部分内容是高中有机化学中讲完甲烷、苯、脂肪烃及有机化合物基础知识后的一节内容,是一类常见的有机物。
在后面学习有机推断和有机合成中,有重要作用。
重点:苯及苯的同系物的结构和化学性质。
难点:苯的同系物的结构和化学性质,基团间的相互影响。
3、学情分析在必修2第三章学习了苯,学生已经接触过了芳香烃,对芳香烃已不陌生,但还没有系统的学习芳香烃的结构和性质。
在必修2中学习过苯的取代反应和加成反应,但对苯及同系物的氧化反应还不系统不全面。
4、设计思路以学生为主体,先对比复习甲烷、乙稀和苯的结构和性质,让学生自主探究设计苯和甲苯的性质实验,体会基团的相互影响与性质的关系,最后总结归纳完成课堂练习,完成学习任务。
三、教学过程1.什么是芳香烃?2.什么是苯的同系物?【板书】1.芳香烃的概念:含有一个或多个苯环的烃叫芳香烃。
2.苯的同系物的概念:苯环上的氢原子被烷基取代的产物叫做苯的同系物。
苯与甲苯结构的结构比较【板书】苯:组成上高度不饱和,结构比较稳定。
甲苯:苯环与甲基相互影响。
小组实验1.在试管里加入2ml苯,再滴加3滴KMnO4酸性溶液。
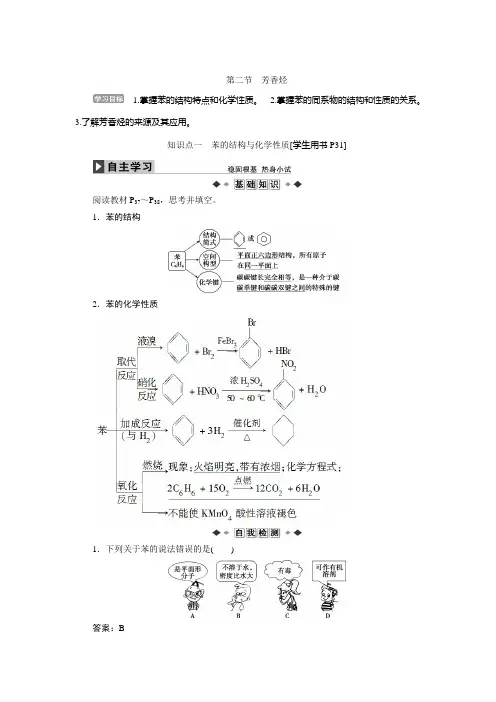
第二节芳香烃1.掌握苯的结构特点和化学性质。
2.掌握苯的同系物的结构和性质的关系。
3.了解芳香烃的来源及其应用。
知识点一苯的结构与化学性质[学生用书P31]阅读教材P37~P38,思考并填空。
1.苯的结构2.苯的化学性质1.下列关于苯的说法错误的是()答案:B2.能说明苯分子中的碳碳键不是单、双键交替的事实是()A.苯的一元取代物没有同分异构体B.苯的邻位二元取代物只有一种C.苯的间位二元取代物只有一种D.苯的对位二元取代物只有一种答案:B3.苯的结构简式可用来表示,下列关于苯的叙述正确的是()A.苯主要是以石油为原料而获得的一种重要化工原料B.苯中含有碳碳双键,所以苯属于烯烃C.苯分子中6个碳碳键完全相同D.苯可以与溴水、高锰酸钾酸性溶液反应而使它们褪色解析:选C。
苯分子中6个碳碳化学键完全相同;苯分子中不含有典型的碳碳双键,所以苯不属于烯烃;苯不能与溴水、高锰酸钾酸性溶液反应而使它们褪色;苯主要是以煤和石油为原料而获得的一种重要化工原料。
1.苯分子的特殊结构在性质方面的体现(1)苯不能使KMnO4酸性溶液和溴水褪色,由此可知苯在化学性质上与烯烃有很大差别。
(2)苯在催化剂(FeBr3)作用下与液溴发生取代反应,说明苯具有类似烷烃的性质。
(3)苯能与H2在催化作用下发生加成反应,说明苯具有烯烃的性质。
总之,苯易发生取代反应,能发生加成反应,难被氧化,其化学性质不同于烷烃、烯烃。
2.实验室制取溴苯如图所示,A 是制取溴苯的实验装置,B 、C 是改进后的装置。
请仔细分析,对比三个装置,回答以下问题。
(1)写出三个装置中共同发生的两个反应的化学方程式:________________________________________________________________________、 ________________________________________________________________________;写出装置B中右边试管所发生反应的化学方程式:________________________________________________________________________。

第二节芳香烃一、芳香烃1、定义:结构上由苯环和烷基组成的烃叫做芳香烃,包含苯2、苯的同系物:只含有一个苯环的芳香烃,不含苯芳香烃包含苯的同系物3、苯的同系物的基本概念通式:CnH2n-6结构特点:只含有一个苯环,以苯环为主体,烷基为侧链状态:液体或固体,一般都带有特殊气味4、代表物质:芳香烃:苯苯的同系物:甲苯【习题一】下列对有机化合物的分类结果正确的是()A.乙烯(CH2=CH2)、苯()、环己烷()都属于脂肪烃B.苯()、环戊烷()、环己烷()同属于芳香烃C.乙烯(CH2=CH2)、乙炔(CH≡CH)同属于烯烃D.、、同属于环烷烃【分析】A、含有苯环只有C和H两种元素构成的化合物属于芳香烃;B、只由C和H两种元素组成,含有苯环的为芳香烃;C、乙炔中含有碳碳三键,属于炔烃;D、饱和环烃为环烷烃,据此解答即可.【解答】解:A、含有苯环且只有C和H两种元素构成的化合物属于芳香烃,属于芳香烃,不是脂肪烃,故A错误;B、只由C和H两种元素组成,含有苯环的为芳香烃,环戊烷()、环己烷()不含有苯环,不属于芳香烃,属于脂肪烃,故B错误;C、乙炔中含有碳碳三键,属于炔烃,故C错误;D、饱和环烃为环烷烃,环戊烷、环丁烷、乙基环己烷均属于环烷烃,故D正确,故选:D。
二、苯1、基本结构化学式:C6H6 结构简式:(凯库勒式)或苯分子中并没有碳碳双键,不饱和度:42、物理性质无色,液体,带有特殊气味,密度比水小,难溶于水,易挥发,有毒3、化学性质1)氧化反应2C6H6+15O2 → 12CO2+6H2O (带浓烟)2)取代反应a、与液溴反应:需要加入少量铁粉,铁与液溴生成溴化铁,溴化铁可以催化苯的溴代+Br2 → +HBrb、与浓硝酸反应(硝化反应)反应需要浓硫酸催化和吸水+HO—NO2 → +H2O3)加成反应苯在一定条件下可与氢气加成,生成环己烷+3H2 →【习题二】能说明苯分子中碳碳键不是单双键交替的事实是()①苯不能使KMnO4溶液褪色;②苯环中碳碳键的键长均相等;③邻二氯苯只有一种;④在一定条件下苯与H2发生加成反应生成环己烷.A.①②③④ B.②③④ C.①②③ D.①②④【分析】①如果苯是单双键交替结构,则含碳碳双键,苯能使KMnO4溶液褪色;②苯环中碳碳键的键长均相等,说明苯环结构中的化学键只有一种;③如果苯的结构中存在单双键交替结构,苯的邻位二元取代物有两种;④苯在镍作催化剂的条件下也可与H2加成生成环己烷,不能证明苯分子中的碳碳键不是单双键交替.【解答】解:①苯不能使酸性高锰酸钾溶液褪色,说明苯分子中不含碳碳双键,可以证明苯环结构中不存在C-C单键与C=C双键的交替结构,故①正确;②苯环上碳碳键的键长相等,说明苯环结构中的化学键只有一种,不存在C-C 单键与C=C双键的交替结构,故②正确;③如果是单双键交替结构,苯的邻位二氯取代物应有两种同分异构体,但实际上只有一种结构,能说明苯环结构中的化学键只有一种,不存在C-C单键与CC 双键的交替结构,故③正确;④苯虽然并不具有碳碳双键,但在镍作催化剂的条件下也可与H2加成生成环己烷,所以不能说苯分子中碳碳键不是单、双键相间交替的事实,故④错误;故选:C。



高中化学人教版选修5《有机化学基础》【教学课题】《第二章第二节芳香烃》【教材背景】1、面向学生:高中二年级2、学科:化学3、课时:1课时;4、学生课前准备:(1)复习高中化学必修2“第三章有机化合物”中的有关甲烷,乙烯和苯的性质;(2)预习有关甲苯的知识;查阅资料了解苯及甲苯等芳香烃在生活中的实际用途;【教材分析】本节课的教学内容位于人教版高中《有机化学基础》(选修5),第二章的第二节的内容。
这部分内容是在学生已经学习了烷、烯等脂肪烃及苯的结构和性质的基础上进行的,学生已经了解了碳碳单键、碳碳双键的有关性质,并认识了苯作为芳香族化合物的母体结构的特殊类型化学键的性质,所以学好这一节的内容是前面知识的拓展和延伸,为学习更多的芳香族化合物及其衍生物的打基础。
【知识与技能】1.学习苯和苯的同系物的结构及化学性质;2.了解芳香烃的来源及其应用【过程与方法】1.归纳、比较法:归纳比较苯与脂肪烃及苯的同系物的结构和性质2.设计有关实验并探究有关物质的性质【情感、态度、价值观】1.通过探究分析,培养学生创新思维能力;2.通过实验,培养学生的实验能力;3.培养学生理论联系实际的思维、辨证思维能力及各事物间相互联系的观点;【重点难点】苯和苯的同系物的结构、性质【教学过程】【情景创设】播放视频“福建大田的苯泄露事件”【设计意图】(网络地址:/programs/view/1J8qfWY1Qnc/ )[师]:从视频中了解到了苯的哪些性质?通过视频引课,激发学生学习化学的兴趣,并感受化学与生活实际的紧密联系;【板书】一、比较认识甲烷、乙烯和苯的结构与性质:甲烷乙烯苯分子式CH4C2H4C6H6结构简式CH4CH2=CH2空间结构物理性质化学性质燃烧溴的CCl4溶液(H+)KMnO4溶液主要反应类型2、完成下列反应的化学方程式:1)苯与液溴:_________________________________________;2)苯与浓硝酸:_______________________________________;3)苯与氢气:_________________________________________;【展示模型】问:如果将苯分子中的一个氢原子换成甲基,这是什么物质?【板书】二、甲苯:1、甲苯的物理性质:(与苯相似)(网络学习:/view/106454.htm )【展示甲苯样品】学生归纳总结:无色有特殊气味的液体,不溶于水比水轻,易挥发;(与苯的物理性质相似)【板书】2、甲苯的结构:分子式:C7H8结构简式:问:至少有多少原子共面?最多有多少原子共面?问:这样的结构决定了怎样的化学性质呢?动画演示甲苯空间结构:复习基础知识,为学习甲苯的知识做好铺垫;自然过渡,并让学生从结构上感知苯和甲苯的相同与不同;直观观察,结学生直观的真实的印象;由学生观察甲苯的球棍模型得出,加强学生对甲苯的结构的认识,并感受苯与甲苯的共面问题;提出探究问题:根据甲苯的结构,推测甲苯的化学性质?并说出你推测的理由; 【指导探究】将学生分成三组,给出4分钟探究时间,并给学生提出探究要求和汇报要求;【指导学生】分组汇报探究结果,并做出评价;【演示实验】1、苯和甲苯的燃烧对比;2、苯和甲苯分别与溴的四氯化碳溶液反应对比;3、苯和甲苯分别与酸性高锰酸钾溶液反应对比;【归纳总结】3、甲苯的化学性质:1)燃烧氧化:2)与酸性高锰酸钾溶液:紫色褪去(苯环对甲基的影响)3)取代反应:(方程式略去)(甲基对苯环的影响)4)加成反应:【归纳总结】苯与甲苯的结构与性质比较苯甲苯分子式C6H6C7H8结构简式结构相同点结构不同点物理性质化学性质溴的CCl4 (H+)KMnO4主要反应类型问:苯是最简单的芳香烃,而甲苯是苯的同系物的代表,这两个概念如何区分?体现新课程理念,让学生探究知识的过程,并通过探究让学生学会合作,学会欣赏,通过谈讨增加学习的兴趣;学生分组汇报探究结果,给学生充分展示自己的平台,合理的给予肯定,让学生体验学习化学中的成功快乐,激发学习的热情;让学生感知比较学习的方法的重要性,并对本节课的内容做以总结;【板书】三、芳香烃(/view/170621.htm )1、芳香烃:含一个或多个苯环的烃;2、苯的同系物:(/view/1566836.htm )定义:苯环上的氢原子被烷基取代的产物;结构特点:一个苯环连一个或多个烷基苯苯的同系物结构特点有苯环苯环+烷基化学性质溴的CCl4不褪色不褪色(H+)KMnO4不褪色褪色主要反应类型取代加成氧化取代加成氧化练习1:下列芳香烃中属于苯的同系物的是( )练习2:既能用酸性高锰酸钾溶液鉴别,又能用溴的四氯化碳溶液鉴别的是()A.苯与甲苯B.己烯与甲苯C.乙烯与乙炔D.乙烯与乙烷【板书】四、芳香烃的来源与用途:【作业】课外探究:芳香烃的“功”与“过”;(知识拓展阅读:/wiki/%E8%8A%B3%E9%A6%99%E7%83%83 )阅读课本,让学生直接挖掘概念的重点,类比得出结论;继续体验比较的学习方法在学习化学中的重要性;练习对学习知识的反馈,也是对新掌握知识强化升华;学生自学课本,教会学生正确用书的自学能力;【教学反思】由于甲烷、乙烯、苯的基础知识安排在化学必修2的教材上,与这部分内容教学时间相距较长,所以教学中能明显感觉到学生对这部分知识遗忘较多,故课前复习这一环节一定要到位,在对苯的特殊的化学键清楚认知后再由此及彼,自然过渡到甲苯的结构与性质,比较认识苯及苯的同系物的相似性和特殊性,再结合教学过程的使用计算机模拟动画,同学分组探究,化学实验验证等方法,使得教学过程有“声”有“色”,使学生形成了有机化学知识体系;激发了学生学习化学的兴趣,也为学生持续学习化学奠定了基础。

课题:芳香烃基础自测苯的组成与结构1.三式平面正六边形,所有的原子都在同一平面上。
3.化学键苯分子中的碳碳键是一种介于碳碳单键和碳碳双键之间的独特的键。
苯的性质1.物理性质(1)燃烧现象:发出明亮火焰,产生浓黑烟。
(2)取代反应①在三溴化铁的作用下和溴单质发生取代反应的化学方程式为生成的二溴代物以邻位和对位取代产物为主。
②在60℃、浓硫酸作用下,和浓硝酸发生硝化反应:(3)加成反应在催化剂、加热条件下,与H2加成的化学方程式为(4)苯的特性①苯不与高锰酸钾酸性溶液和溴水反应,由此可知苯在化学性质上与烯烃有很大的差别。
②苯在催化剂(Fe或FeBr3)作用下与液溴发生取代反应,说明苯具有烷烃的性质。
③苯又能够与H2或Cl2分别在催化剂作用下发生加成反应,说明苯具有烯烃的性质。
④苯容易发生取代反应,而难于发生加成反应,难被氧化,其化学性质不同于烷烃、烯烃和炔烃。
溴苯、硝基苯的制备将反应后的液体倒入一个盛有冷水芳香烃的来源与苯的同系物1.芳香烃的来源(1)芳香烃最初来源于煤焦油中,现代主要来源于石油化学工业中的催化重整和裂化。
苯、乙苯和对二甲苯是应用最多的基本有机原料。
(2)工业上,乙苯、异丙苯主要通过苯与乙烯、丙烯反应获得。
苯与乙烯反应的化学方程式为。
2.苯的同系物(1)概念:苯环上的氢原子被烷基取代后的产物。
(2)结构特点:分子中只有1个苯环,侧链是烷烃基。
(3)通式:C n H2n-6(n≥7)。
苯的同系物与芳香烃的关系(1)分子式与苯(C6H6)相差一个或若干个“CH2”原子团的物质,如甲苯(C7H8)、二甲苯(C8H10)等都是苯的同系物,它们也都属于芳香烃。
(2)苯的同系物都是芳香烃,但芳香烃不一定是苯的同系物。
如属于芳香烃,但不是苯的同系物。
(3)苯的同系物的通式都为C n H2n-6(n≥7),但通式符合C n H2n-6的烃不一定是苯的同系物。
如的分子式为C10H14,它不属于苯的同系物。
选修5 《有机化学基础》同步练习第二章第二章《烃和卤代烃》第一节《脂肪烃》第一课时[基础题]1.下列事实、事件、事故中与甲烷有无关的是 A.天然气的主要成分 B.石油经过催化裂化及裂解后的产物 C.“西气东输”中气体 D.煤矿中的瓦斯爆炸2.二氟甲烷是性能优异的环保产品,它可替代某些会破坏臭氧层的“氟里昂”产品,用作空调、冰箱和冷冻库等中的致冷剂。
试判断二氟甲烷的结构简式()A.有4种 B.有3种 C.有2种 D.只有1种3.下列烷烃的一氯取代物中没有同分异构体的是()A.丙烷 B.丁烷 C.异丁烷 D.新戊烷4.甲烷在隔绝空气加强热时可分解为和,若有80%按上述形式分解,所得混合气体的密度是相同条件下氮气密度的倍数是()A.2 B.2.22 C.3.46 D.4.445.烯烃不可能具有的性质有A.能使溴水褪色 B.加成反应 C.取代反应D.能使酸性KMnO4溶液褪色6.与丙烯具有相同的碳、氢百分含量,但既不是同系物又不是同分异构体的是()A.环丙烷 B.环丁烷 C.乙烯 D.丙烷7.不能使酸性KMnO4溶液褪色的是A.乙烯 B.聚乙烯 C.丙烯 D.乙炔8.分子式为,分子结构中含有3个“—”原子团的烯烃共有A.2种 B.5种C.3种D.4种9.下列有机化合物有顺反异构体的是()A.CH3CH3 B.CH2=CH2 C.CH3CH=CH2 D.CH3CH=CHCH310.一定量的甲烷点燃后生成的CO2、CO和H2O的混和气体的质量为49.6 g,将此混和气体缓慢地通过无水氯化钙固体后,氯化钙的质量增加25.2 g,由此可推断混和气体中二氧化碳的物质的量为()A.0.5 mol B.0.3 mol C.13.2 mol D.17.6 mol[提高题]1.有的油田开采的石油中溶有一种碳氢化合物——金刚烷,它的分子立体结构如图5-7所示:(1)由图可知其分子式为:____________。
(2)它是由_________ 个六元环构成的六体的笼状结构,其中有__________个碳原子为三个环共有。
《芳香烃》说课稿尊敬的各位评委老师:大家好!今天我说课的内容是《芳香烃》。
下面我将从教材分析、学情分析、教学目标、教学重难点、教法与学法、教学过程以及教学反思这几个方面来展开我的说课。
一、教材分析《芳香烃》是高中化学选修 5《有机化学基础》中的重要内容。
在有机化学的学习中,烃是一类非常重要的有机化合物,而芳香烃则是具有特殊结构和性质的烃类。
通过对芳香烃的学习,学生可以进一步深化对有机物结构与性质关系的理解,为后续学习更复杂的有机化合物奠定基础。
本节课主要介绍了苯的结构、性质以及苯的同系物。
教材首先通过实验引出苯的物理性质和化学性质,然后通过对苯分子结构的探讨,揭示了苯的特殊稳定性。
在介绍苯的同系物时,教材重点强调了其与苯在结构和性质上的相似性和差异性,使学生能够形成对比和归纳的思维方式。
二、学情分析学生在之前的学习中已经掌握了烃的基本概念和一些简单烃类的性质,具备了一定的有机化学基础知识和实验操作能力。
但对于苯这种具有特殊结构和性质的芳香烃,学生可能会感到抽象和难以理解。
因此,在教学过程中,需要通过实验、模型等直观手段帮助学生突破难点,激发学生的学习兴趣。
三、教学目标1、知识与技能目标(1)了解苯的物理性质和化学性质,掌握苯的结构特点。
(2)理解苯的同系物的概念,掌握苯的同系物的性质。
(3)能够书写苯及其同系物的化学反应方程式。
2、过程与方法目标(1)通过实验探究,培养学生的观察能力、实验操作能力和分析问题的能力。
(2)通过对苯分子结构的探讨,培养学生的空间想象能力和逻辑思维能力。
3、情感态度与价值观目标(1)通过对芳香烃的学习,让学生感受有机化学的魅力,激发学生学习化学的兴趣。
(2)培养学生严谨的科学态度和创新精神。
四、教学重难点1、教学重点(1)苯的结构特点和化学性质。
(2)苯的同系物的性质。
2、教学难点(1)苯分子结构的特殊性。
(2)苯的加成反应和取代反应的原理。
五、教法与学法1、教法(1)实验探究法:通过实验让学生直观地感受苯的物理性质和化学性质,激发学生的学习兴趣。