7氧族
- 格式:ppt
- 大小:1.02 MB
- 文档页数:36
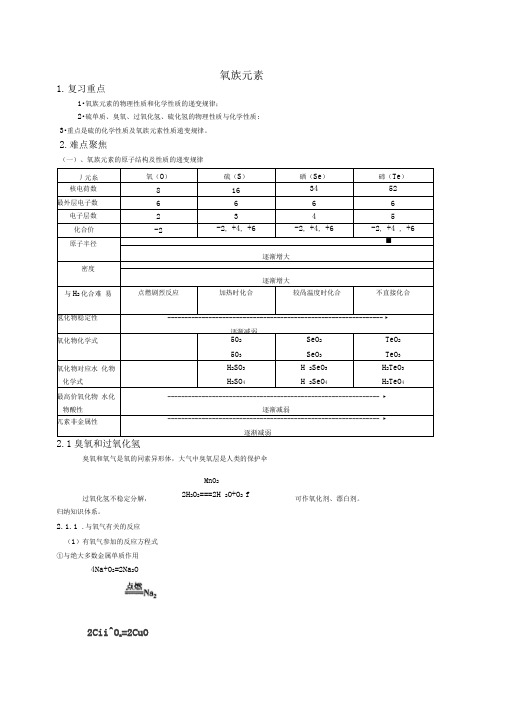
1.复习重点1•氧族元素的物理性质和化学性质的递变规律;2•硫单质、臭氧、过氧化氢、硫化氢的物理性质与化学性质; 3•重点是硫的化学性质及氧族元素性质递变规律。
2.难点聚焦(一)、氧族元素的原子结构及性质的递变规律丿元糸氧(O)硫(S)硒(Se)碲(Te)核电荷数8 16 34 52最外层电子数 6 6 6 6 电子层数 2 3 4 5化合价-2 -2, +4, +6 -2, +4, +6 -2, +4 , +6 原子半径■逐渐增大密度逐渐增大与H2化合难易点燃剧烈反应加热时化合较咼温度时化合不直接化合氢化物稳定性 --------------------------------------------------------------- ►逐渐减弱氧化物化学式502503SeO2SeO3TeO2TeO3氧化物对应水化物化学式H2SO3H2SO4H 2SeO3H 2SeO4H2TeO3H2TeO4最高价氧化物水化物酸性-------------------------------------------------------------- ►逐渐减弱兀素非金属性-------------------------------------------------------------- ►逐渐减弱2.1臭氧和过氧化氢臭氧和氧气是氧的同素异形体,大气中臭氧层是人类的保护伞过氧化氢不稳定分解,归纳知识体系。
2.1.1 .与氧气有关的反应(1)有氧气参加的反应方程式①与绝大多数金属单质作用4Na+O2=2Na2O2Cii^Oa=2CuO氧族元素MnO22H2O2===2H 2O+O2 f可作氧化剂、漂白剂。
②与绝大多数非金属单质作用2H 2S + O x 些25十汎0粹津2S0卫HyOPt4NHj *5® s^y^NO + 6^0高温4FeS 2+11O 22Fe 2O 2+8SO 2④与有机物作用料工佝+承H 』0(烽类物质慰爛:厢f 二耶峠 幡国滸就応FigiSr :%/芍皓評笫ESf 耳輕浑里恬晞点治样?空¥! :^n3E®HFiFrg|。


氧族元素知识归纳一、硫及其化合物转化关系图二、本章主要内容1.与氧气有关的反应(1)有氧气参加的反应方程式①与绝大多数金属单质作用4Na+O2=2Na2O②与绝大多数非金属单质作用③与非还原性化合物作用2NO+O2=2NO24FeS2+11O22Fe2O2+8SO2④与有机物作用⑤在空气中易被氧化而变质的物质a.氢硫酸或可溶性硫化物:2H2S+O2=2S↓+2H2Ob.亚硫酸及其可溶性盐2H2SO3+O2=2H2SO4,2Na2SO4+O2=2Na2SO4c.亚铁盐、氢氧化亚铁4Fe(OH)2+O2+2H2O=4Fe(OH)3d.苯酚e.氢碘酸及其可溶性碘化物4HI+O2=2H2O+2I2⑥吸氧腐蚀(如:铁生锈)负极:2Fe—4e—=2Fe2+正极:O2+4e—+2H2O=4OH—Fe2++2OH—=Fe(OH)2 4Fe(OH)2+O2+2H2O=4Fe(OH)32Fe(OH)3=Fe2O3+3H2O(2)生成氧气的反应方程式2.氧气和臭氧的比较3.硫元素的化学反应(1)硫单质的反应④S+Hg=HgS⑥S+2Ag=Ag2S ⑦3S+6KOH=2K2S+K2SO3+3H2O⑩S+6HNO3(浓)=H2SO4+6NO2↑+2H2O (2)H2S的反应①H2S H2+S↓②③H2S+X2=2HX+S↓(X2是指卤素单质,即Cl2,Br2,I2)④H2S+Pb(Ac)2=PbS↓+2HAc⑤H2S+CuSO4=CuS↓+H2SO4⑦FeS+2HCl=FeCl2+H2S↑(H2S的实验室制法)(3)SO2的反应①SO2+2H2S=3S↓+2H2O ②③SO2+Na2O=Na2SO3④SO2+Na2O2=Na2SO4⑤SO2+2NaOH=Na2SO3+H2O⑥Na2SO3+SO2+H2O=2NaHSO3⑦2NaHCO3+SO2=Na2SO3+2CO2+H2O⑧Na2CO3+SO2=Na2SO3+CO2⑨⑩SO2+X2+2H2O=H2SO4+2HX Na2SO3+X2+H2O=Na2SO4+2HX(X2=Cl2,Br2,I2)2FeCl3+SO2+2H2O=2FeCl2+2HCl+H2SO4SO2+NH3·H2O=NH4HSO3Na2SO3+H2SO4=Na2SO4+SO2↑+H2O2Na2SO3+O2=2Na2SO4(亚硫酸易被氧化而变质)(4)浓H2SO4有关反应(稀H2SO4具有酸的通性)4.硫化物的溶解性5.浓硫酸的氧化性和稀硫酸的氧化性的区别浓硫酸具有强氧化性,其氧化性是由硫酸分子中处于最高价态的+6价的硫产生的,加热能氧化许多金属、非金属及某些具有还原性的化合物,浓硫酸的还原产物一般为二氧化硫。

氧族元素知识复习总结相同点:最低化合价为-2价,正价为+4、+6价(氧元素除外)。
不同点:随着原子序数的递增元素原子获得电子的能力在减弱,非金属性依次减弱,金属性依次增强。
都能与多数金属反应。
(2)单质性质的异同:相同点:单质均可作氧化剂,每个原子可获得2个电子。
均有同素异形体。
不同点:单质颜色不同,密度依次增大,熔、沸点依次升高。
单质与2H 化合依次变难;单质氧化性依次减弱,还原性依次增强。
(3)氧化物有两种,3624O R O R ++和,其对应的水化物为含氧酸,均有酸的通性。
气态氢化物H 22R -;H 2S 、H 2Se 、H 2Te 其水溶液都显酸性,除H 2O外,氢化物都具有恶臭,有毒,溶于水形成无氧酸,具有还原性。
2.递变规律随着元素核电荷数的增加,电子层数依次增多,原子半径逐渐增大,核对外层电子的引力逐渐减弱,使原子得电子的能力逐渐减弱,而失电子的能力逐渐增强。
表现在性质上的递变规律是:单质的颜色由无色、淡黄、浅灰至呈银白色。
状态由气态到固态,熔、沸点也依次升高。
元素非金属性逐渐减弱,金属性逐渐增强。
单质的氧化性依次减弱。
含氧酸的酸性依次减弱,H 24R +O3、612R H ++O 4顺序氧化性增强。
气态氢化物的稳定性逐渐减弱,还原性增强。
二、臭氧1.结构:含有非极性键的极性分子,V 型结构2.物理性质:常温、常压下,O 3是一种有特殊臭味的淡蓝色气体,密度比氧气大,也比氧气易溶于水,液态呈深蓝色,沸点的-112.4℃,固态为紫黑色,熔点为-251℃3.化学性质:①不稳定性:常温下分解较慢,在受热、光照和MnO2等作用下迅速分解。
2O3 == 3O2②强氧化性:就氧化能力而言,它介于氧原子和氧分子之间。
能氧化在空气中不能氧化的金属。
臭氧分子与其它物质反应时,常产生氧气。
2Ag + 2O3 =Ag2O2 + 2O2 (常温下反应)O3 + 2KI + H2O = 2KOH + I2注:臭氧能使湿润的KI淀粉试纸变蓝,利用此性质可测定微量O3的含量,也可检验O3。


7主族元素口诀
7个主族(ⅠA、ⅡA、ⅢA、ⅣA、ⅤA、ⅥA、ⅦA)包含元素
第一主族,氢锂钠钾铷铯钫
IA:Li Na K Rb Cs Fr
第二主族,铍镁钙锶钡镭
ⅡA:Be Mg Ca Sr Ba Ra
第三主族,硼铝镓铟铊
ⅢA:B Al Ga In Tl
第四主族,碳硅锗锡铅
ⅣA:C Si Ge Sn Pb
第五主族,氮磷砷锑铋
ⅤA:N P As Sb Bi
第六主族,氧硫硒碲钋
ⅥA:O S Se Te Po
第七主族,氟氯溴碘砹
ⅦA:F Cl Br I At
化学元素记忆方法(谐音)
氢锂钠钾铷铯钫请李娜加入私访
铍镁钙锶钡镭媲美盖茨被累
硼铝镓铟铊碰女嫁音他
碳硅锗锡铅探归者西迁
氮磷砷锑铋蛋临身体闭
氧硫硒碲钋养牛西蹄扑
氟氯溴碘砹父女绣点爱
氦氖氩氪氙氡害耐亚克先动。
无机颜色表含部分元素化合物常温下物态、颜色、形态等物理化学性质卤族(英VIIA):Solid:I2 紫黑;ICl 暗红;IBr 暗灰;IF3 黄色;ICl3 橙;I2O5 白;I2O4 黄(离子晶体);I4O9 黄(离子晶体).Liquid:Br2 红棕;BrF3 浅黄绿;IBr3 棕;Cl2O6暗红;Cl2O7 无色油状;HClO4 无色粘稠状;(SCN)2 黄色油状.Gas:F2 浅黄;(CN)2无色;Cl2 黄绿;I2(g) 紫;BrF 红棕;BrCl 红;Cl2O 黄红;ClO2 黄色;Br2O 深棕;(SCN)n 砖红色固体.氧族(英VIA):Solid:S 淡黄;Se 灰,褐;Te 无色金属光泽;Na2S,(NH4)2S,K2S,BaS 白,可溶;ZnS 白↓;MnS 肉红↓;FeS 黑↓;PbS 黑↓;CdS 黄↓;Sb2S3 橘红↓;SnS 褐色↓;HgS 黑(沉淀),红(朱砂);Ag2S 黑↓;CuS 黑↓;Na2S2O3 白;Na2S2O4 白;SeO2 白,易挥发;SeBr2 红;SeBr4 黄;TeO2 白加热变黄;H2TeO3 白;TeBr2 棕;TeBr4 橙;TeI4 灰黑;PoO2 低温黄(面心立方),高温红(四方);SO3 无色;SeO3 无色易潮解;TeO3 橙色;H6TeO6 无色.Liquid:H2O 无色;纯H2O2 淡蓝色粘稠;CrO(O2)2(aq) 蓝;纯H2SO4 无色油状;SO32-(aq) 无色;SO42-(aq) 无色;SeO2(l) 橙;TeO2(l) 深红.Gas:O2 无色;O3 低浓度无色,高浓度淡蓝(鱼腥味);S2(g) 黄,上浅下深;H2S 无色;SO2 无色;H2Se 无色;H2Te 无色.卤化硫(未注明者均为无色):Liquid:SF6;S2F10;SCl4 淡黄;SCl2 红籗2Cl2 无色;S2Br2 红.Gas:SF4;SF2;S2F2.卤砜、卤化亚砜、卤磺酸:Liquid:SOCl2 白色透明;SO2Cl2 无色发烟.氮族(英VA):Solid:铵盐无色晶体;氮化金属白;N2O3 蓝色(低温);N2O5 白;P 白,红,黑;P2O3 白;P2O5 白;PBr3 黄;PI3 红;PCl5 无色;P4Sx 黄;P2S3 灰黄;P2S5 淡黄;H4P2O7 无色玻璃状;H3PO2 白;As 灰;As2O3 白;As2O5 白;AsI3 红;As4S4 红(雄黄);As4S6 黄(雌黄);As2S5 淡黄;Sb 银白;Sb(OH)3 白↓;Sb2O3 白(锑白,颜料);Sb2O5 淡黄;SbX3(XI) 白;SbI3 红;Sb2S3 橘红↓;Sb2S5 橙黄;Bi 银白略显红;Bi2O3 淡黄;Bi2O5 红棕;BiF3 灰白;BiCl3 白;BiBr3 黄;BiI3 黑↓;Bi2S3 棕黑.Liquid:N2H4 无色;HN3 无色;NH2OH 无色;发烟硝酸红棕;NO3^-(l)无色;王水浅黄,氯气味;硝基苯黄色油状;氨合电子(液氨溶液) 蓝;PX3 无色;纯H3PO4 无色粘稠状;AsX3(XI) 无色;.Gas:N2 无色;NH3 无色;N2O 无色甜味;NO 无色;NO2 红棕;PH3 无色;P2H6 无色;AsH3 无色;SbH3 无色;BiH3 无色.卤化氮(未注明者均为无色):Solid:NBr3•(NH3)6 紫,爆炸性;NI3•(NH3)6 黑,爆炸性;Liquid:NCl3;无色Gas:NF3;无色碳族(英IVA):Solid:C(金刚石) 无色透明;C(石墨) 黑色金属光泽;Si 灰黑色金属光泽;Ge 灰白;Sn 银白;Pb 暗灰;SiO2 无色透明;H2SiO3 无色透明胶状↓;Na2SiF6 白晶;GeO 黑;GeO2 白;SnO 黑;SnO2 白;Sn(OH)2 白↓;PbO黄或黄红;Pb2O3 橙;Pb3O4 红;PbO2 棕;CBr4 淡黄;CI4 淡红;GeI2 橙;GeBr2 黄;GeF4 白;GeBr4 灰白;GeI4 黄;SnF2 白;SnCl2 白;SnBr2 淡黄;SnI2 橙;SnF4 白;SnBr4 无色;SnI4 红;PbF2 无色↓;PbCl2 白↓;PbBr2 白;PbI2 金黄;PbF4 无色;GeS 红;GeS2 白;SnS 棕↓;SnS2 金黄(俗称“金粉”)↓;PbS 黑↓;PbS2 红褐;Pb(NO3)2 无色;Pb(Ac)2•3H2O 无色晶体;PbSO4 白↓;PbCO3 白↓;Pb(OH)2 白↓;Pb3(CO3)2(OH)2 铅白↓;PbCrO4 亮黄↓.Liquid:CCl4 无色;CS2 无色;GeCl4 无色;SnCl4 无色;PbCl4 无色.Gas:CO CO2 CH4 CF4 SiF4 SiH4 均为无色.硼族(英IIIA):Solid:B(无定型) 棕色粉末;B(晶体) 黑灰;Al 银白;Ga 银白(易液化);In 银灰;Tl 银灰;B2O3 玻璃状;H3BO3 无色片状;BN 白;Na2B4O7•10H2O 白色晶体;Cu(BO2)2 蓝↓;Ni(BO2)2 绿↓;NaBO2•Co(BO2)2 蓝↓;NaBO2•4H2O 无色晶体;无水NaBO2 黄晶;Al2O3 白晶;AlF3 无色;AlCl3 白;AlBr3 白;AlI3 棕;Al(OH)3 白↓;Ga2O3 白↓Ga(OH)3 白↓;GaBr3 白;GaI3 黄;In2O3 黄;InBr3 白;InI3 黄;TlOH 黄;Tl2O 黑;Tl2O3 棕黑;TlCl 白↓;TlBr 浅黄↓;TlI 黄↓(与银相似);TlBr3 黄;TlI3 黑.Liquid:BCl3 无色发烟.Gas:硼烷无色;BF3 无色(有窒息气味).碱土(英IIA):单质:银白焰色:Ca 砖红;Sr 洋红;Ba 绿.氧化物:均为白色固体.氢氧化物:白色固体Be(OH)2↓,Mg(OH)2↓.盐:多为无色或白色晶体;BeCl2 浅黄;BaCrO4 黄↓;CaF2 白↓.碱金属(英IA):单质:银白焰色:Li 红;Na 黄;K 紫;Rb 紫红;Cs 紫红.氧化物、过氧化物、超氧化物、臭氧化物:Li2O 白;Na2O 白;K2O 淡黄;Rb2O 亮黄;Cs2O 橙红;Na2O2 淡黄;KO2橙黄;RbO2深棕;CsO2 深黄;KO3 橘红.氢氧化物:白色,LiOH白↓.盐:多为无色或白色晶体且易溶于水.不溶盐↓(未注明者皆为白色晶体):LiF Li2CO3 Li3PO4 LiKFeIO6 Na[Sb(OH)6]NaZn(UO2)3(A c)9•6H2O 黄绿;M=K,Rb,Cs M3[Co(NO2)6] 亮黄;MBPh4 MClO4M2PtCl6 淡黄;CsAuCl4.铜副族(英IB):单质:Cu 紫红或暗红;Ag 银白;Au 金黄.铜化合物:焰色绿;CuF 红;CuCl 白↓;CuBr黄↓;CuI 棕黄↓;CuCN 白↓;Cu2O 暗红;Cu2S 黑;CuF2 白;CuCl2 棕黄(溶液黄绿);CuBr2 棕;Cu(CN)2 棕黄;CuO 黑↓;CuS黑↓;CuSO4 无色;CuSO4•5H2O 蓝;Cu(OH)2 淡蓝↓;Cu(OH)2•CuCO3 墨绿;[Cu(H2O)4]2+ 蓝;[Cu(OH)4]2- 蓝紫;[Cu(NH3)4]2+ 深蓝;[CuCl4]2- 黄;[Cu(en)2]2+ 深蓝紫;Cu2[Fe(CN)6] 棕红;炔铜红↓.银化合物:AgOH 白(常温分解);Ag2O 黑;新制AgOH 棕黄(混有Ag2O);蛋白银(AgNO3滴手上) 黑↓;AgF 白;AgCl 白↓;AgBr 淡黄↓;AgI 黄↓(胶体);Ag2S 黑↓;Ag4[Fe(CN)6] 白↓;Ag3[Fe(CN)6] 白↓;Ag+,[Ag(NH3)2]+,[Ag(S2O3)2]3-,[Ag(CN)2]- 无色.金化合物:HAuCl4•3H2O 亮黄晶体;KAuCl4•1.5H2O 无色片状晶体;Au2O3 黑;H[Au(NO3)4]•3H2O 黄色晶体;AuBr 灰黄↓;AuI 柠檬黄↓.锌副族(I英IB):单质:均为银白,Hg在水溶液中的沉淀为黑色.锌化合物:ZnO 白(锌白颜料)↓;ZnI2 无色;ZnS 白↓;ZnCl2 白色晶体(溶解度极大,水溶液酸性);K3Zn3[Fe(CN)6] 白;Zn3[Fe(CN)6]2 黄褐.镉化合物:CdO 棕灰↓;CdI2 黄;CdS 黄(镉黄颜料)↓;HgCl2(升汞) 白色;HgNH2Cl 白↓;Hg2Cl2(甘汞) 白↓.汞化合物:HgO 红(大晶粒)或黄(小晶粒)↓;HgI2 红或黄(微溶);HgS 黑或红↓;Hg2NI•H2O 红↓;Hg2(NO3)2 无色晶体.ZnS荧光粉:Ag 蓝;Cu 黄绿;Mn 橙.钪副族(英IIIB):略.钛副族(英IVB):钛化合物:Ti3+ 紫红;[TiO(H2O2)2]2+ 橘黄;H2TiO3 白色↓;TiO2 白(钛白颜料)或桃红(金红石)↓;(NH4)2TiCl6 黄色晶体;[Ti(H2O)6]Cl3 紫色晶体;[Ti(H2O)5Cl]Cl2•H2O 绿色晶体;TiCl4 无色发烟液体.锆、铪:MO2,MCl4 白.钒副族(英VB):钒化合物:V2+ 紫;V3+ 绿;VO2+ 蓝;V(OH)4^- 黄;VO4^3- 黄;VO 黑;V2O3 灰黑;V2S3 棕黑;VO2 蓝色固体;VF4 绿色固体;VCl4 暗棕色液体;VBr4 洋红色液体;V2O5 黄或砖红;水合V2O5 棕红;饱和V2O5溶液(微溶) 淡黄;[VO2(O2)2]3- 黄;[V(O2)3]3- 红棕.钒酸根缩聚:随着钒氧原子数之比的减少的,由浅黄~深红~淡黄.铌、钽:略.铬副族(英VIB):铬化合物:Cr2+ 蓝;Cr3+ 紫;Cr2O72- 橙红;CrO42- 黄;Cr(OH)4- 亮绿;Cr(OH)3灰蓝;Cr2O3 绿;CrO3 暗红色针状;[CrO(O2)2]OEt2 蓝;CrO2Cl2 深红色液体;Na2Cr2O7,K2CrO7 橙红;Ag2CrO4 砖红↓;BaCrO4 黄↓;PbCrO4 黄↓.紫红Cr2(SO4)3•18H2O——〉绿色Cr2(SO4)3•6H2O——〉桃红Cr2(SO4)3暗绿[Cr(H2O)4Cl2]Cl—冷却HCl—〉紫色[Cr(H2O)6]Cl3—乙醚HCl—〉淡绿[Cr(H2O)5Cl]Cl2[Cr(H2O)6]3+ 紫;[Cr(H2O)4(NH3)2]3+ 紫红;[Cr(H2O)3(NH3)3]3+ 浅红;[Cr(H2O)2(NH3)4]3+ 橙红;[Cr (NH3)5H2O]3+ 橙黄;[Cr(NH3)6]3+ 黄.钼、钨:MoO3 白;棕色MoCl3;绿色MoCl5;MoS3 棕色↓;(NH4)3[P(Mo12O40)]•6H2O 黄色晶状↓;WO3 深黄;H2WO4•xH2O 白色胶体.锰副族(英VIIB):锰化合物:Mn2+ 肉红;Mn3+ 紫红;MnO42- 绿;MnO4- 紫;MnO3+ 亮绿;Mn(OH)2 白↓;MnO(OH)2 棕↓;MnO2 黑↓;无水锰盐(MnSO4) 白色晶体;六水合锰盐(MnX2•6H2O, X=卤素,NO3,ClO4) 粉红;MnS•nH2O 肉红↓;无水MnS 深绿;MnCO3 白↓;Mn3(PO4)2 白↓;KMnO4 紫红;K2MnO4 绿;K2[MnF6] 金黄色晶体;Mn2O7 棕色油状液体.锝、铼:略.铁系(第四周期VIII族):铁化合物:Fe2+ 浅绿;[Fe(H2O)6]3+ 浅紫;[Fe(OH)(H2O)5]2+ 黄;FeO42- 紫红;FeO 黑;Fe2O3 暗红;Fe(OH)2 白↓;Fe(OH)3 棕红↓;FeCl3 棕红晶体;无水FeSO4 白;FeSO4•7H2O 绿;K4[Fe(CN)6](黄血盐) 黄色晶体;K3[Fe(CN)6](赤血盐) 红色晶体;Fe2[Fe(CN)6] 普鲁士蓝↓;Fe[Fe(CN)6] 黑↓;Fe(C5H5)2(二茂铁) 橙黄色晶体;M2Fe6(SO4)4(OH)12(黄铁矾,M=NH4,Na,K) 浅黄色晶体;Fe(CO)5 黄色液体.钴化合物:Co2+ 粉红;CoO 灰绿;Co3O4 黑;Co(OH)3 棕↓;Co(OH)2 粉红↓;Co(CN)2 红;K4[Co(CN)6] 紫色晶体;Co2(CO)8 黄色晶体;[Co(SCN)6]4- 紫;氯化钴脱水变色:粉红CoCl2•6H2O—325K—〉紫红CoCl2•2H2O—3l3K—〉蓝紫CoCl2•H2O—393K—〉蓝CoCl2.镍化合物:Ni2+ 亮绿;[Ni(NH3)6]2+ 紫;Ni(OH)2 绿↓;Ni(OH)3 黑↓;无水Ni(II)盐黄;Na2[Ni(CN)4] 黄;K2[Ni(CN)4] 橙;Ni(CO)4 无色液体.铂系元素(第五、六周期VIII族):Os 蓝灰色易挥发固体;Pd↓(aq) 黑;OsO4 无色有特殊气味气体;H2PtCl6 橙红色晶体;Na2PtCl6 橙黄色晶体;M2PtCl6(M=K,Rb,Cs,NH4) 黄色↓.镧系锕系元素:暂无.稀有气体元素:单质:He、Ne、Ar、Kr、Xe、Rn 无色,微溶于水;氪化合物:KrF2 无色,25℃分解;氙化合物:XeF2,XeF4,XeF6无色,熔沸点依次降低;XeOF4,XeO2F2,XeO2无色;XeO3 黄色,0℃爆炸;氙-金属配合物:XeF[RuF6],[Xe2F3][AsF6],XeF3[SbF6],XeF3[Sb2F11] 黄绿色固;XeF[Sb2F11]黄;XeF5[AsF6] 白固;XeF5[RuF6] 绿固。
17_氧族元素范文氧族元素是周期表中的第16族元素,包括氧、硫、硒、碲、钋和Livermorium。
它们在化学性质上有一些共同的特点,但也有一些明显的差异。
首先,氧族元素的电子组态为ns^2np^4,其中n表示主能级。
这意味着氧族元素有6个价电子,形成了-2的氧化态。
氧族元素的电子云形状为半球,因为它们的最外层电子对所形成的云是四面体排列的。
氧族元素的原子半径随着周期数的增加而增加。
这是因为周期表从上到下,原子核的电荷数增加,但是核外电子层数也增加,从而使得电子云半径增大。
氧族元素的电负性递减,从氧到碲,硫、硒和碲都是非金属元素,有着高的电负性和电离能。
氧具有最高的电负性,是自然界中第二电负性最高的元素,只次于氟。
它是一个非常活泼的元素,可以与许多其他元素形成化学键。
氧是地壳中最常见的元素之一,它占地壳质量的46.6%。
氧广泛应用于许多化学反应和产业中,包括燃烧、腐蚀、氧化还原反应等。
硫是氧族元素中最常见的元素之一,很多人熟悉它的味道,硫的气味有很强的刺激性。
硫广泛应用于许多工业领域,如制药、有机合成、橡胶制造、化肥和石油炼制。
硒是一种稀有元素,对生物体有极大的重要性。
它是一种必需的微量元素,对人体的健康和正常的免疫功能有益。
硒化物是一种重要的半导体材料,在光伏领域具有广泛应用。
碲是一种也比较稀有的元素,具有半导体的性质。
碲化物在红外光探测器和光电器件领域具有广泛应用。
钋是一种放射性元素,具有高毒性。
它是通过人工合成获得的,因此在自然界中是非常罕见的。
钋的用途相对较少,主要用于科学研究和工业领域。
Livermorium是最新发现的氧族元素。
它是通过合成反应获得的,只在实验室中制备和观察到。
Livermorium的性质和用途仍然在研究中。
总结来说,氧族元素在化学性质上有一些共同的特点,如有6个价电子和相似的电子云形状。
但它们也有明显的差异,如电负性的递减和元素特定的用途和性质。
通过研究氧族元素的性质和应用,可以深入了解这些元素在化学和生物领域中的重要性。