芳香性理论
- 格式:ppt
- 大小:292.00 KB
- 文档页数:17



有机化学基本理论主讲人:史达清3. 芳香性芳香性化合物的特点:(1)较高的碳/氢比例;(2)键长的平均化;(3)分子的共平面性;(4)共轭能;(5)特征光谱(在1H NMR 出现环电流,使环上质子化学位移移向低场);(6)化学性质(结构具有特殊稳定性,易被取代,不易被加成和氧化)。
芳香性的判据休克尔(Hückel)规则:在由sp2杂化碳原子组成的平面单环体系中,含有4n+2 个π 电子的体系将具有与惰性气体相类似的闭壳层结构,从而显示出芳香性。
在具体判断时,不能仅从4n+2 个π电子数进行判断。
一般要同时满足以下三个条件才具有芳香性:(1)闭环共轭体系;(2)成环的所有的原子在同一个平面上(即共平面) ;(3)4n+2 个π 电子举例:(1)环丙烯衍生物(2)环丁二烯衍生物(3)环戊二烯衍生物(4)环庚三烯衍生物(5)环辛四烯衍生物(6)轮烯类化合物其实对于单环共轭多烯,只有当成键轨道或非键轨道完全填充满电子时,才具有闭壳层结构。
如下图所示:(7)稠环芳烃一般,4n+2 规则只适用于平面单环体系,不适用于稠环体系。
对于稠环体系只能用分子轨道法经计算后确定成键轨道、非键轨道和反键轨道数目来看能否形成封闭的π 电子壳层而确定。
对较为简单的多环体系,其中没有三个以上的环所共用的原子,如果π 电子数为4n+2 ,则可以判别该体系是芳香性的。
(8)杂芳环化合物杂芳香性化合物是环上有杂原子取代的具有4n+2 个π 电子并显示芳香特点的化合物,它可以分为两类,一类是利用体系中杂原子上未共享电子对的一些化合物。
例如呋喃、噻吩、吡咯、噻唑、咪唑等。
这些化合物中的氧、氮或硫原子上的未共享电子对和二烯部分的四个π 电子结合得到一个 6 π 电子的4n+2 离域体系。
它们的芳香性大小是:噻吩>吡咯>呋喃。
另外一类是环上杂原子上的未共享电子对并未参与芳香性稳定化作用,例如吡啶、嘧啶等。
此外,还有一些以氮为中心原子的周边共轭体系,例如环[3.2.2]嗪、环[4.4.3]嗪也都是稳定的芳香性化合物。

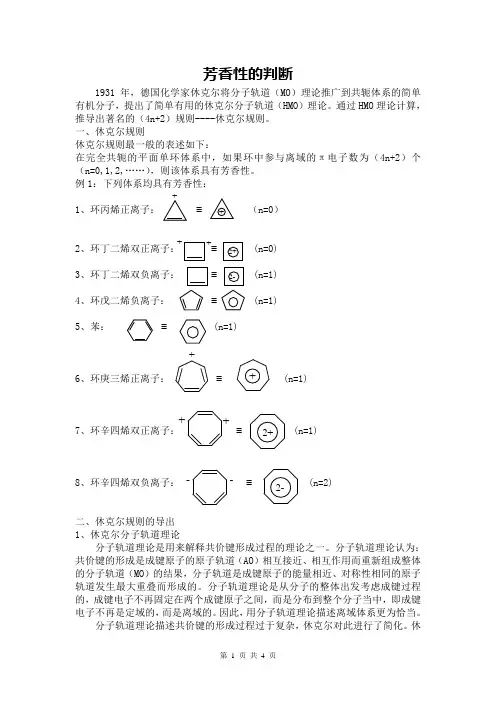
芳香性的判断1931年,德国化学家休克尔将分子轨道(MO )理论推广到共轭体系的简单有机分子,提出了简单有用的休克尔分子轨道(HMO )理论。
通过HMO 理论计算,推导出著名的(4n+2)规则----休克尔规则。
一、休克尔规则休克尔规则最一般的表述如下:在完全共轭的平面单环体系中,如果环中参与离域的π电子数为(4n+2)个(n=0,1,2,……),则该体系具有芳香性。
例1:下列体系均具有芳香性:1、环丙烯正离子:≡(n=0)2、环丁二烯双正离子:≡3、环丁二烯双负离子:≡4、环戊二烯负离子:≡5、苯:≡6、环庚三烯正离子: ≡7、环辛四烯双正离子: ≡8、环辛四烯双负离子: ≡二、休克尔规则的导出1、休克尔分子轨道理论分子轨道理论是用来解释共价键形成过程的理论之一。
分子轨道理论认为:共价键的形成是成键原子的原子轨道(AO )相互接近、相互作用而重新组成整体的分子轨道(MO )的结果,分子轨道是成键原子的能量相近、对称性相同的原子轨道发生最大重叠而形成的。
分子轨道理论是从分子的整体出发考虑成键过程的,成键电子不再固定在两个成键原子之间,而是分布到整个分子当中,即成键电子不再是定域的,而是离域的。
因此,用分子轨道理论描述离域体系更为恰当。
分子轨道理论描述共价键的形成过程过于复杂,休克尔对此进行了简化。
休+ - - + + + - -克尔认为:在离域体系中,σ键是定域于两个成键原子之间的,但π键是离域的,而化学性质主要与π键有关,这样我们就可以只关注由p 原子轨道组合形成的π分子轨道得到的π键。
这种只考虑π键的分子轨道理论就称为休克尔分子轨道理论(HMO )。
也就是说,HMO 为简化了的MO 。
例如,苯分子形成过程的休克尔分子轨道能级图如下:*6π*4π *5π6个p 轨道(AO ) 2π3π1π基态时,6个p 电子分成3对,分别填入3个能量较低的成键分子轨道1π、2π和3π中,而3个能量较高的反键分子轨道是全空的。

竞赛辅导讲义芳香性及其理论1865年,德国化学家凯库勒提出了著名的苯分子的正六边形环状结构式,并正式引入“芳香性”这一概念来描述苯及与苯有关的化合物的物理、化学性质。
此后芳香化学引起了人们极大的兴趣。
随着测试技术和量子化学的发展,人们对芳香性的认识逐步深化。
有关芳香性理论的研究一直是有机化学家、结构化学家和理论化学家的主要研究课题之一。
一、芳香性的涵义芳香性(aromaticity)是一个理论概念,其涵义随理论的发展而不断深化。
芳香性是有机化学中最难准确表述的概念之一。
一般所谓的芳香性分子具有以下几个特点:1、C/H比例高芳香性分子大多具有较高的C/H原子比。
从C/H原子比来看,芳香性分子属于高度不饱和分子。
例如:苯(C6H6)的C/H原子比为1﹕1;萘(C10H8)的C/H原子比为1.25﹕1;富勒烯(C60、C70)的C/H原子比甚至为∞。
而脂肪族分子,除乙炔(C2H2)、丁二炔(C4H2)等少数几个以外,绝大多数C/H原子比教低。
2、键长均一化芳香性分子中碳碳单键与碳碳双键键长有趋于一致的倾向,极端情况为苯分子。
X-射线衍射测定表明苯分子中碳碳键并无单双键之别,所有的碳碳键长均为0.1395nm,介于普通的碳碳单键键长(0.154nm)和碳碳双键键长(0.135nm)之间。
3、分子平面化芳香性分子的一个显著特征就是芳环上的组成原子都处在一个平面或接近一个平面内。
虽然平面分子不一定就是芳香性分子,但芳香性分子总是要求分子具有一定程度的平面性。
4、化学性质“反常”化不饱和分子的典型化学性质就是容易发生加成反应。
芳香性分子虽然属高度不饱和分子,却表现出“反常”的化学性质,即难以进行加成反应,更发生易取代反应,而后者正是饱和分子的典型化学性质。
5、π电子离域化通过氢化热或燃烧热的测定,芳香性分子的能量比非芳香性分子的能量低得多,即芳香性分子具有特殊的稳定性。
人们引入离域能DE(delocalization energy)或共振能RE(resonance energy)的概念来定量地表示芳香性的强弱:DE=E定域-E离域式中,E定域代表假想的定域的环多烯分子的能量,E离域代表离域的芳香性分子的能量。




第六章芳香性第一节芳香性的一般讨论芳香化合物的特点1.较高的C/H比苯C6H6,萘C10H8,蒽C14H102.共平面、键长均等化3.分子共平面组成芳香环的原子都在一个平面或接近一个平面里。
4.芳香性分子稳定程度—共轭能(离域能)大小例如苯的共轭能为150.7kJ/mol ,可以借助氢化热或燃烧热来求得。
比较1mol苯和3mol环已烯的氢化热,计算得苯的共轭能约为(3×119.7-208.5)= 150.7kJ/mol 。
对离域能定量计算REPE(每一个电子的离域能)=离域能/NREPE ﹥0 化合物有芳香性REPE =0 化合物非芳香性REPE ﹤0 化合物反芳香性REPE计算:1)求出离域能离域能=E非定域—E定域2)REPE计算REPE =离域能/nREPE(每一个电子的离域能)的正值越大,则相应的化合物的芳香性越强。
用REPE与这些化合物的性质进行联系、比较后得出结论:REPE可以作为判断环状多烯是否具有芳香性的指标。
5.化学性质特征芳香化合物与一般高度不饱和的脂肪族化合物不同,不易发生加成反应,较难发生氧化反应,易于发生取代反应,尤其是芳烃易发生亲电取代反应。
6.π电子数目:4n+2在环状多烯体系中,当π电子数为4n+2时,为芳香性分子;当π电子数为4n时,体系若比相应的多烯模型化合物稳定性降低,则具有反芳香性;体系若与相应的多烯模型化合物稳定性相近,则为非芳香性。
如:苯是典型的芳香性,环辛四烯为非芳香性体系,环丁二烯则为反芳香性,其化学性质很活泼,甚至比环丁烷还活泼。
芳香性是不是是是是是4n+2规则只能作为环状多烯的体系是否具有芳香性的定性依据,要描述芳香性分子稳定到什么程度,即芳香性强度,必须按HMO法对离域能进行定量的计算。
7.波谱特征芳香性化合物大多都具有特征的光谱。
NMR:芳环呈现反磁环流,环平面上下有屏蔽效应,环内有去屏蔽效应。
第二节带电荷环的芳香性环上带有电荷而具有芳香性的物质很多,它们是一类重要的非苯芳烃。
综述:芳香性概述“芳香性”是用于描述一些环状化合物特殊稳定性的概念。
在有机化学中, 尤其是针对不饱和环体系、多环体系研究中居重要地位。
自1825年Michael Faraday从煤焦油中分离出苯开始, 芳香化学至今已有近200年的历史。
为了深入了解“芳香性”及其在自然学科中产生的深远影响, 本文简述了其发展历史与本质, 并对芳香性的判断方法进行归类总结。
除了列举实例, 进一步对芳香化合物进行分类以外, 还基于本课题组近年的研究成果, 提出一些新观点。
芳香性的含义“芳香性”一词自使用以来, 科学家们不断发现具备该性质的化合物的各种特征, 并进行了总结与归纳。
这些特征, 一部分是规律的总结, 例如[4n+2]规则; 另一部分则是对化合物本身特征的描述, 例如平面性、键长平均化等。
随着科学研究的不断推进, 其中一些观点被修正甚至推翻, 但仍有一些经典的描述被保留并沿用至今。
仔细考察芳香性的历史, 我们发现“芳香性”事实上是用于描述化合物的特殊稳定性的概念。
换句话说,“芳香性”是一个描述行为特征, 而非表达理论规律的术语。
因此, “芳香性”应该由此类化合物的本质属性决定, 而“芳香性”规律则是对芳香化合物普遍性质的总结。
本文就“传统芳香化合物”的行为特征进行了总结(指Hückel 平面芳香性), 并列于下表中。
另外, 对近年发展的一些芳香性的独特类型, 本文也将结合实例逐一介绍。
通常, 芳香环由于其特殊的稳定性, 化学反应性相对其他非芳香环系要弱得多。
早在1866 年, Erlenmeyer就已经提出了芳香性的反应性判据。
在一般不饱和体系极易发生的反应, 如加成、开环反应中, 在芳香体系均较难实现。
通常芳香环更容易发生取代反应。
核磁共振化学位移(NMR Chemical Shift)芳香化合物产生的独特抗磁环电流, 会导致周围的磁场环境发生变化。
例如苯分子的6个H 原子均处于抗磁环电流的去屏蔽区域,因此其1H NMR 的化学位移值会向低场移动(δ=7。
芳香性是一种化学性质,有芳香性的分子中,由不饱和键、孤对电子和空轨道组成的共轭系统具有特别的、仅考虑共轭时无法解释的稳定作用。
可以将芳香性看作是环状离域和环共振的体现。
一般认为在这些体系中的电子,可以自由在由原子组成的环形结构上运动(离域),这些环形结构含有单键和双键相间,离域的结果是环键的键级趋于均化,给予体系稳定作用。
芳香性的理论最初由凯库勒发展出来,是以六元的苯分子为原型建立起来。
理论中的苯有两个共振形态,并有单键和双键相间,但理论上的两种苯(环己三烯)衍生物的这类异构体在实际上无法检测或分离出来,苯事实上是这两个异构体的“杂化体”,并且具有不考虑电子离域时无法解释的稳定性。
右上图中的双箭头于化学中代表共振的意思,但不代表该分子会变成那两个形态,反而是指该分子处于该两个形态的混合状态。
事实上,那两个形态都不能代表分子实际的形态,但指出了电子大概的分布。
由此可见,分子真实的形态就是那两个形态的融合,而它所发出的电磁波波长就是该两个形态所发出的平均长度。
用组成π键的电子密度分布的位置,来更准确地解释就是电子分布在分子的环的上、下。
数量必定是4n+2的定律,和肯定芳香族分子的环必定是平面。
芳香性化合物的特征[编辑]被分类为芳香性的化合物通常有以下的条件:1. 有一些离域电子组成一些π键,并且令整个环系统可以当成单与双键的组合;2. 给出离域电子形成π键的原子需处于同一个平面;3. 原子需组成一个环;4. 组成π键的电子总数需为4n+2,即不是4的倍数的双数(休克尔规则);5. 可进行亲电芳香取代反应和亲核芳香取代反应。
苯就是一个较好的例子,它适合以上所有条件,并且有6个离域电子(即n=1)。
有4n+2个π电子的化合物通常都是芳香性的。
环丁二烯只有4个离域电子,所以不属于芳香性化合物。
这些只有4n个π电子而又具近似平面结构的环状化合物称为反芳香性化合物。
非芳香族的有机物就叫做脂肪族,脂肪族没有芳香族具有的特殊的共振稳定作用。