5004聚酯、铝、聚乙烯药品包装用复合膜、袋质量标准
- 格式:doc
- 大小:30.00 KB
- 文档页数:3

食品和药品包装用复合膜、袋标准及其检测广州市冠誉铝箔包装材料有限公司廖启忠Tel:E-mail:目前药品包装用复合膜、袋有行业标准YBB00132002《药品包装用复合膜袋通则》、YBB00172002《聚酯/铝/聚乙烯药品包装用复合膜、袋》、YBB00182002《聚酯/低密度聚乙烯药品包装用复合膜、袋》、YBB00192002《双向拉伸聚丙烯/低密度聚乙烯药品包装用复合膜、袋》,相关的行业标准、国家标准和外国标准有YBB00142002《药品包装材料与药品相溶性试验指导试验指导原则》、GB/T10005-1998《双向拉伸聚丙烯(BOPP)/低密度聚乙烯(LDPE)复合膜、袋》、GB/T10004-1998《耐蒸煮复合膜、袋》、JIS Z1707-1995《食品包装用塑料膜》。
药品包装用复合膜、袋的性能指标主要有:外观尺寸、密封阻隔性能、机械性能、卫生性能和其它特种性能等五大类。
一、外观外观一般不允许有穿孔、异物、异味、粘连、复合层间分离及明显的损伤、气泡、皱纹、脏污等缺陷,复合袋的热封部位还应平整,无虚封。
对于印刷的文字和图案应清晰,完整,色彩均匀,无明显色差。
套印精度一般用精度为0.1mm的20倍刻度放大镜检验不0.5mm。
印刷质量详细的标准及检测可参考GB/T7707-1987《凹版装潢印刷品》。
对于卷膜还应紧实,卷面不允许有明显突起和凹陷的暴筋,卷膜两端应平整,端面不平整度一般不得超过2mm。
外观检验一般以目测为主,其质量标准不同厂家有较大差异。
二、尺寸偏差一般袋的长度和宽度允许有±1.5mm的偏差,偏差太大会影响袋的容积,瓶盖用封口膜由于要放置在瓶盖内其尺寸精度要求较高,一般允许偏差不超过±2%。
厚度偏差及平均厚度偏差一般要求不超过±10%,制袋产品,热封宽度也不能偏差过大,热封边的大小不仅会影响袋的强度,还会影响其容积,一般要求热封边的宽度偏差不超过20%作为袋,还有一个要控制的尺寸是热封边与袋边的距离,一般不超过4mm,最好有控制在3mm以内,过大会影响袋的容积,可能装不下被包装物。
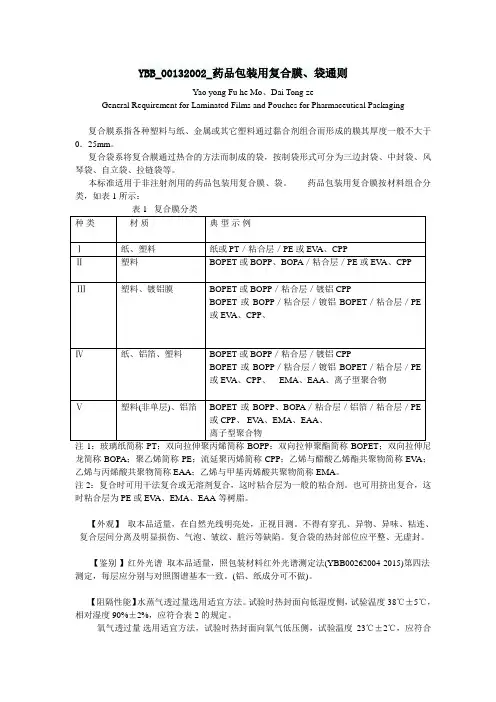
YBB_00132002_药品包装用复合膜、袋通则Yao yong Fu he Mo、Dai Tong zeGeneral Requirement for Laminated Films and Pouches for Pharmaceutical Packaging复合膜系指各种塑料与纸、金属或其它塑料通过黏合剂组合而形成的膜其厚度一般不大于0.25mm。
复合袋系将复合膜通过热合的方法而制成的袋,按制袋形式可分为三边封袋、中封袋、风琴袋、自立袋、拉链袋等。
本标准适用于非注射剂用的药品包装用复合膜、袋。
药品包装用复合膜按材料组合分类,如表1所示:注1:玻璃纸简称PT;双向拉伸聚丙烯简称BOPP:双向拉伸聚酯简称BOPET;双向拉伸尼龙简称BOPA;聚乙烯简称PE;流延聚丙烯简称CPP;乙烯与醋酸乙烯酯共聚物简称EV A;乙烯与丙烯酸共聚物简称EAA;乙烯与甲基丙烯酸共聚物简称EMA。
注2:复合时可用干法复合或无溶剂复合,这时粘合层为一般的粘合剂。
也可用挤出复合,这时粘合层为PE或EV A、EMA、EAA等树脂。
【外观】取本品适量,在自然光线明亮处,正视目测。
不得有穿孔、异物、异味、粘连、复合层间分离及明显损伤、气泡、皱纹、脏污等缺陷。
复合袋的热封部位应平整、无虚封。
【鉴别】红外光谱取本品适量,照包装材料红外光谱测定法(YBB00262004-2015)第四法测定,每层应分别与对照图谱基本一致。
(铝、纸成分可不做)。
【阻隔性能】水蒸气透过量选用适宜方法。
试验时热封面向低湿度侧,试验温度38℃±5℃,相对湿度90%±2%,应符合表2的规定。
氧气透过量选用适宜方法,试验时热封面向氧气低压侧,试验温度23℃±2℃,应符合表2的规定。
【机械性能】内层与次内层剥高强度取膜、袋适量,照剥离强度测定法(YBB001020003-2015)测定,纵、横向剥离强度平均值应符合表3规定。

聚酯/纸张/粒子/铝/聚乙烯复合膜、袋1范围本文件规定了聚酯/纸张/粒子/铝/聚乙烯复合膜、袋的术语和定义、原材料和添加剂、技术要求、试验方法、检验规则、标志、包装、运输及贮存。
本文件适用于聚酯、纸张、粒子、铝和聚乙烯通过粘合剂复合而成的食品包装用复合膜、袋。
2规范性引用文件下列文件中的内容通过文中的规范性引用而构成本文件必不可少的条款。
其中,注日期的引用文件,仅该日期对应的版本适用于本文件﹔不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T1037塑料薄膜与薄片水蒸气透过性能测定杯式增重与减重法GB/T1038塑料薄膜和薄片气体透过性试验方法压差法GB/T1040.3塑料拉伸性能的测定第3部分:薄膜和薄片的试验条件GB/T2828.1计数抽样检验程序第1部分:按接收质量限(AQL)检索的逐批检验抽样计划GB2918塑料试样状态调节和试验的标准环境GB4806.1食品安全国家标准食品接触性材料及制品通用安全要求GB4806.7食品安全国家标准食品接触用塑料材料及制品GB/T6672塑料薄膜和薄片厚度测定机械测量法GB/T6673塑料薄膜和薄片长度和宽度的测定GB/T7707凹版装潢印刷品GB/T8808软质复合塑料材料剥离试验方法GB9683复合食品包装袋卫生标准GB9685食品容器、包装材料用添加剂使用卫生标准GB/T8809塑料薄膜抗摆锤冲击试验方法GB/T10004包装用塑料复合膜、袋干法复合、挤出复合GB12904商品条码零售商品编码与条码表示GB/T14257商品条码条码符号放置指南GB/T17497.2柔性版装潢印刷品第2部分:塑料与金属箔类GB/T23508—2009食品包装容器及材料术语GB31604.2食品安全国家标准食品接触性材料及制品高锰酸钾消耗量的测定GB31604.8食品安全国家标准食品接触性材料及制品总迁移量的测定GB31604.9食品安全国家标准食品接触性材料及制品食品模拟物中重金属的测定GB31604.23食品安全国家标准食品接触性材料及制品复合食品接触性材料中二氨基甲苯的测定QB/T1130—1991塑料直角撕裂性能试验方法QB/T2358塑料薄膜包装袋热合强度试验方法3术语和定义GB/T23508—2009界定的以及下列术语和定义适用于本文件。

聚酯铝聚乙烯药品包装用复合膜、袋——YBB00172002(word版)国家药品监督管理局国家药品包装容器(材料)标准(试行)YBB00172002聚酯/铝/聚乙烯药品包装用复合膜、袋Juzhi/lvbo/JuyixiYaopinbaozhuangyong Fuhemo、DaiLaminated Films and Pouches (PET/AI/PE)for Pharmaceutical Packaging 本品系指聚酯(PET)与铝箔(AI)及聚乙烯(PE)通过黏合剂复合而成的膜。
本品的袋系将上述膜通过热合的方法制成。
本标准适用于固体药品包装用的复合膜、袋。
【外观】取本品适量,照药品包装用复合膜、袋通则(试行)(YBB00132002)外观项下的方法检查,应符合规定。
【鉴别】红外光谱取本品适量,采用内表面反射方法,照分光光度法(中华人民共和国药典2000年版附录IV C)测定,PET及PE层应分别与对照图谱基本一致。
【阻隔性能】水蒸气透过量照塑料薄膜和片材透水蒸气性试验方法杯式法(GB1037-88)的规定进行。
试验时PE层向湿度低的一侧,试验温度(38?2)?,相对湿2度(90?5)%,不得过0.5(g/m?24h)。
氧气透过量照塑料薄膜和薄片气体透过性试验方法压差法(GB/T1038-2000)的规32定进行。
试验时PE层向氧气低压侧,试验温度为(23?2)?,不得过0.5cm/(m?24h?0.1MPa)。
【机械性能】 PE层与AI层剥离强度照药品包装用复合膜、袋通则(试行)(YBB00132002)内层与次内层剥离强度项下的方法检查,纵、横向剥离强度平均值不得低于2.5N/15mm。
【热合强度】膜除另有规定外,裁取100mm×100mm试片四片,将任意两个试片PE面叠合,置热封仪上进行热合,热合温度150?~170?,压力0.2~0.3MPa,时间1秒。
从热合的中间部位各裁取3条15mm宽的试样,进行试验。
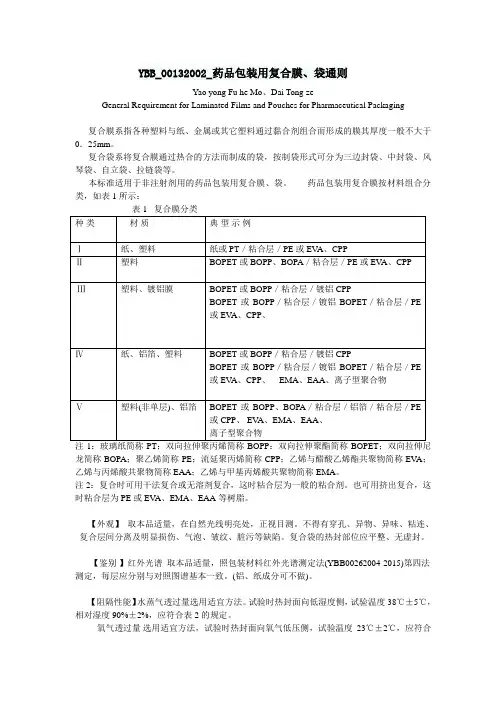
YBB_00132002_药品包装用复合膜、袋通则Yao yong Fu he Mo、Dai Tong zeGeneral Requirement for Laminated Films and Pouches for Pharmaceutical Packaging复合膜系指各种塑料与纸、金属或其它塑料通过黏合剂组合而形成的膜其厚度一般不大于0.25mm。
复合袋系将复合膜通过热合的方法而制成的袋,按制袋形式可分为三边封袋、中封袋、风琴袋、自立袋、拉链袋等。
本标准适用于非注射剂用的药品包装用复合膜、袋。
药品包装用复合膜按材料组合分类,如表1所示:注1:玻璃纸简称PT;双向拉伸聚丙烯简称BOPP:双向拉伸聚酯简称BOPET;双向拉伸尼龙简称BOPA;聚乙烯简称PE;流延聚丙烯简称CPP;乙烯与醋酸乙烯酯共聚物简称EV A;乙烯与丙烯酸共聚物简称EAA;乙烯与甲基丙烯酸共聚物简称EMA。
注2:复合时可用干法复合或无溶剂复合,这时粘合层为一般的粘合剂。
也可用挤出复合,这时粘合层为PE或EV A、EMA、EAA等树脂。
【外观】取本品适量,在自然光线明亮处,正视目测。
不得有穿孔、异物、异味、粘连、复合层间分离及明显损伤、气泡、皱纹、脏污等缺陷。
复合袋的热封部位应平整、无虚封。
【鉴别】红外光谱取本品适量,照包装材料红外光谱测定法(YBB00262004-2015)第四法测定,每层应分别与对照图谱基本一致。
(铝、纸成分可不做)。
【阻隔性能】水蒸气透过量选用适宜方法。
试验时热封面向低湿度侧,试验温度38℃±5℃,相对湿度90%±2%,应符合表2的规定。
氧气透过量选用适宜方法,试验时热封面向氧气低压侧,试验温度23℃±2℃,应符合表2的规定。
【机械性能】内层与次内层剥高强度取膜、袋适量,照剥离强度测定法(YBB001020003-2015)测定,纵、横向剥离强度平均值应符合表3规定。

药品包装用复合膜标准药品包装用复合膜是一种在医药行业中广泛使用的包装材料,其质量标准对于保障药品的质量和安全具有重要意义。
本标准旨在规定药品包装用复合膜的技术要求、试验方法、检验规则和标志、包装、运输、贮存等要求,以确保药品包装用复合膜的质量和安全性,保障药品的有效性和稳定性。
一、技术要求。
1. 外观质量,药品包装用复合膜应具有良好的透明度和光泽,无色差、气泡、皱纹、污渍等缺陷。
2. 物理性能,药品包装用复合膜应具有一定的拉伸强度、撕裂强度和破裂伸长率,以确保其在包装过程中不易损坏。
3. 化学性能,药品包装用复合膜应符合相关的卫生标准,不得含有对人体有害的物质,如重金属、有机溶剂等。
4. 热封性能,药品包装用复合膜应具有良好的热封性能,确保包装的密封性和防潮性。
5. 印刷性能,药品包装用复合膜应能够满足药品包装的印刷要求,印刷图案清晰、色彩饱满、不易脱落。
二、试验方法。
1. 外观检验,采用目测和光源透视等方法进行外观检验,确保药品包装用复合膜的外观质量符合要求。
2. 物理性能测试,采用拉伸试验机进行拉伸强度、撕裂强度和破裂伸长率的测试,确保其符合相关标准。
3. 化学性能测试,采用化学分析方法对复合膜中的有害物质进行检测,确保其不含有对人体有害的物质。
4. 热封性能测试,采用热封试验机对复合膜的热封性能进行测试,确保其能够满足包装的密封要求。
5. 印刷性能测试,采用印刷设备对复合膜进行印刷,检验其印刷效果是否符合要求。
三、检验规则和标志。
1. 对于合格的药品包装用复合膜,应在其包装上标注相关的质量标志,以示其合格性。
2. 对于不合格的药品包装用复合膜,应及时予以淘汰,并进行相应的处理,以免影响药品的质量和安全。
四、包装、运输、贮存。
1. 药品包装用复合膜应在包装过程中注意防潮、防晒、防污染,确保其质量不受影响。
2. 在运输和贮存过程中,应避免受潮、受热、受压,以免影响其使用性能和质量。
综上所述,药品包装用复合膜标准对于保障药品的质量和安全具有重要意义,各相关企业应严格按照标准要求进行生产和使用,以确保药品的有效性和稳定性,保障人民群众的用药安全。

(完整版)药品内包装用聚乙烯复合膜、袋检验标准操作规程编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望((完整版)药品内包装用聚乙烯复合膜、袋检验标准操作规程)的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为(完整版)药品内包装用聚乙烯复合膜、袋检验标准操作规程的全部内容。
(完整版)药品内包装用聚乙烯复合膜、袋检验标准操作规程编辑整理:张嬗雒老师尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布到文库,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是我们任然希望 (完整版)药品内包装用聚乙烯复合膜、袋检验标准操作规程这篇文档能够给您的工作和学习带来便利.同时我们也真诚的希望收到您的建议和反馈到下面的留言区,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请下载收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为 <(完整版)药品内包装用聚乙烯复合膜、袋检验标准操作规程> 这篇文档的全部内容。
标准操作规程目的:建立药品内包装用聚乙烯复合膜、袋的验收标准。
范围:用于中间体或原料包装用聚乙烯复合膜、袋。
责任者:采供部、仓管员、 QA、QC。
规程:1.分类和规格本标准使用于中间体、或原料药包装用聚乙烯复合膜、袋。
2.进厂聚乙烯复合膜必须核对厂家、批号,只能重经过供应商审计确认的生产厂家购入。
3。
重金属精密量取水浸液20ml,加醋酸盐缓冲液(pH3。
5)2ml,依法检查(中国药典2000年版二部附录VIII H 第一法),含重金属不得过1ppm.4.易氧化物精密量取水浸液20ml,精密加入高锰酸钾滴定液(0。

药品包装用复合膜标准药品包装用复合膜是指用于包装药品的薄膜材料,其质量直接关系到药品的保质期和安全性。
为了保障药品包装用复合膜的质量和安全性,国家对其进行了一系列的标准规定,以确保药品包装用复合膜的生产、使用和监管符合国家的相关法律法规,保障药品的质量和安全。
首先,药品包装用复合膜的材料应符合国家相关的标准要求。
复合膜的材料应具有良好的耐热性、耐湿性和防潮性,以保证药品在包装过程中不受外界环境的影响,保持药品的质量稳定。
同时,复合膜的材料应符合国家对食品接触材料的卫生安全要求,保证药品包装用复合膜不会对药品产生污染,确保药品的安全性。
其次,药品包装用复合膜的生产工艺应符合国家相关的标准规定。
生产工艺应严格控制复合膜的厚度、拉伸性能、热封性能等关键指标,以确保复合膜的质量稳定。
同时,生产过程中应加强对原材料的检验和控制,确保原材料的质量符合要求,进一步保障复合膜的质量。
另外,药品包装用复合膜的使用应符合国家相关的标准要求。
在药品包装过程中,应严格按照复合膜的使用说明进行操作,确保复合膜的性能得到充分发挥,保障药品包装的质量和安全。
同时,对于复合膜的储存和运输也应符合国家相关的标准规定,避免复合膜在储存和运输过程中受到损坏,影响其性能和质量。
最后,药品包装用复合膜的监管应加强,确保复合膜的质量和安全。
生产企业应建立健全的质量管理体系,加强对复合膜质量的监控和管理,及时发现和处理质量异常,保障复合膜的质量稳定。
监管部门应加强对药品包装用复合膜的监督检查,确保复合膜的生产、使用和监管符合国家相关的标准要求,保障药品的质量和安全。
总之,药品包装用复合膜标准的制定和执行,对保障药品的质量和安全具有重要意义。
各相关方应严格按照国家相关的标准要求执行,确保药品包装用复合膜的质量和安全,为人民群众的健康提供有力保障。
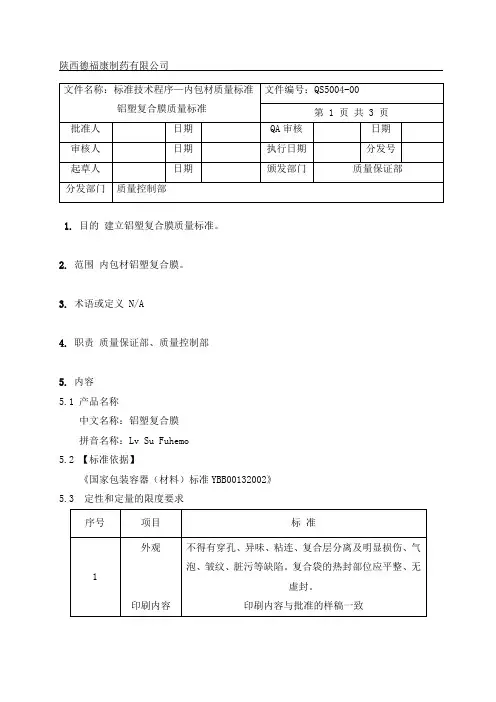
陕西德福康制药有限公司________________
1.目的建立铝塑复合膜质量标准。
2.范围内包材铝塑复合膜。
3.术语或定义 N/A
4.职责质量保证部、质量控制部
5.内容
5.1 产品名称
中文名称:铝塑复合膜
拼音名称:Lv Su Fuhemo
5.2 【标准依据】
《国家包装容器(材料)标准YBB00132002》
5.3定性和定量的限度要求
5.4【批准的供应商】生产商--
5.5 取样、检验方法或相关操作规程编号:检验方法见《铝塑复合膜(药用)标准检验操作规程》(SOP-QC5004-00),取样方法见《取样标准操作规程》(SOP-QA001-00)。
5.6【贮存条件和注意事项】密闭保存。
5.7 【复验期】二年
6.附件
N/A
7.参考或引用文件
7.1 《取样标准操作规程》SOP-QA001-00
7.2 《铝塑复合膜检验操作规程》SOP-QC5004-00
8.文件变更记载。

食品和药品包装用复合膜、袋标准及其检测广州市冠誉铝箔包装材料有限公司廖启忠Tel:E-mail:目前药品包装用复合膜、袋有行业标准YBB00132002《药品包装用复合膜袋通则》、YBB00172002《聚酯/铝/聚乙烯药品包装用复合膜、袋》、YBB00182002《聚酯/低密度聚乙烯药品包装用复合膜、袋》、YBB00192002《双向拉伸聚丙烯/低密度聚乙烯药品包装用复合膜、袋》,相关的行业标准、国家标准和外国标准有YBB00142002《药品包装材料与药品相溶性试验指导试验指导原则》、GB/T10005-1998《双向拉伸聚丙烯(BOPP)/低密度聚乙烯(LDPE)复合膜、袋》、GB/T10004-1998《耐蒸煮复合膜、袋》、JIS Z1707-1995《食品包装用塑料膜》。
药品包装用复合膜、袋的性能指标主要有:外观尺寸、密封阻隔性能、机械性能、卫生性能和其它特种性能等五大类。
一、外观外观一般不允许有穿孔、异物、异味、粘连、复合层间分离及明显的损伤、气泡、皱纹、脏污等缺陷,复合袋的热封部位还应平整,无虚封。
对于印刷的文字和图案应清晰,完整,色彩均匀,无明显色差。
套印精度一般用精度为0.1mm的20倍刻度放大镜检验不0.5mm。
印刷质量详细的标准及检测可参考GB/T7707-1987《凹版装潢印刷品》。
对于卷膜还应紧实,卷面不允许有明显突起和凹陷的暴筋,卷膜两端应平整,端面不平整度一般不得超过2mm。
外观检验一般以目测为主,其质量标准不同厂家有较大差异。
二、尺寸偏差一般袋的长度和宽度允许有±1.5mm的偏差,偏差太大会影响袋的容积,瓶盖用封口膜由于要放置在瓶盖内其尺寸精度要求较高,一般允许偏差不超过±2%。
厚度偏差及平均厚度偏差一般要求不超过±10%,制袋产品,热封宽度也不能偏差过大,热封边的大小不仅会影响袋的强度,还会影响其容积,一般要求热封边的宽度偏差不超过20%作为袋,还有一个要控制的尺寸是热封边与袋边的距离,一般不超过4mm,最好有控制在3mm以内,过大会影响袋的容积,可能装不下被包装物。

食品和药品包装用复合膜、袋标准及其检测广州市冠誉铝箔包装材料有限公司廖启忠Tel:E-mail:目前药品包装用复合膜、袋有行业标准YBB00132002《药品包装用复合膜袋通则》、YBB00172002《聚酯/铝/聚乙烯药品包装用复合膜、袋》、YBB00182002《聚酯/低密度聚乙烯药品包装用复合膜、袋》、YBB00192002《双向拉伸聚丙烯/低密度聚乙烯药品包装用复合膜、袋》,相关的行业标准、国家标准和外国标准有YBB00142002《药品包装材料与药品相溶性试验指导试验指导原则》、GB/T10005-1998《双向拉伸聚丙烯(BOPP)/低密度聚乙烯(LDPE)复合膜、袋》、GB/T10004-1998《耐蒸煮复合膜、袋》、JIS Z1707-1995《食品包装用塑料膜》。
药品包装用复合膜、袋的性能指标主要有:外观尺寸、密封阻隔性能、机械性能、卫生性能和其它特种性能等五大类。
一、外观外观一般不允许有穿孔、异物、异味、粘连、复合层间分离及明显的损伤、气泡、皱纹、脏污等缺陷,复合袋的热封部位还应平整,无虚封。
对于印刷的文字和图案应清晰,完整,色彩均匀,无明显色差。
套印精度一般用精度为0.1mm的20倍刻度放大镜检验不0.5mm。
印刷质量详细的标准及检测可参考GB/T7707-1987《凹版装潢印刷品》。
对于卷膜还应紧实,卷面不允许有明显突起和凹陷的暴筋,卷膜两端应平整,端面不平整度一般不得超过2mm。
外观检验一般以目测为主,其质量标准不同厂家有较大差异。
二、尺寸偏差一般袋的长度和宽度允许有±1.5mm的偏差,偏差太大会影响袋的容积,瓶盖用封口膜由于要放置在瓶盖内其尺寸精度要求较高,一般允许偏差不超过±2%。
厚度偏差及平均厚度偏差一般要求不超过±10%,制袋产品,热封宽度也不能偏差过大,热封边的大小不仅会影响袋的强度,还会影响其容积,一般要求热封边的宽度偏差不超过20%作为袋,还有一个要控制的尺寸是热封边与袋边的距离,一般不超过4mm,最好有控制在3mm以内,过大会影响袋的容积,可能装不下被包装物。
1目的:明确药品包装用铝膜质量标准,确定质量、生产、采供质控依据。
2 范围:药品包装用铝膜。
3 责任者:质量部、生产部、采供部。
4 内容:
4.1 基本信息
4.1.1 物料代码:药品包装用复合铝膜B19。
4.1.2 供应商:西安久志工贸有限公司。
4.2 取样、检验方法或相关操作规程编号
4.2.1 取样管理规程SOP-QA-1005-00。
4.2.2 检验方法或相关操作规程编号
药品包装用复合铝膜检验操作规程SOP-QC-8019-00。
4.3 标准内容
4.3.1 外观质量:不允许有穿孔、异物、异味、粘连、涂层不均匀,复合层间分离及明显损伤、气泡、皱纹、脏污等缺陷。
4.3.2 规格尺寸:应符合附表1规定。
4.4 贮存:清洁、通风、干燥处存放。
4.5 印刷包装材料的实样或样稿(样稿见附表2)
5 文件的培训:
5.1 内部培训讲师:人力资源部指定人员。
5.2 文件培训对象:质量部、生产部、采供部。
5.3 文件培训课时:0.5~1小时。
6 文件变更历史:
附表1。
(一)聚酯/铝/聚乙烯药品包装用复合膜、袋来源国家药品监督管理局YBB00172002本品系指聚酯(PET)与铝箔(Al)及聚乙烯(PE)通过黏合剂复合而成的膜。
本品的袋系将上述膜通过热合的方法制成。
本标准适用于固体药品包装用的复合膜、袋。
[外观]取本品适量,照药品包装用复合膜、袋通则(试行)(YBB00132002)外观项下的方法检查,应符合规定。
[鉴别]红外光谱取本品适量,采用内表面反射方法,照分光光度法(中华人民共和国药典2000年版附录ⅣC)测定,PET及PE层应分别与对照图谱基本一致。
[阻隔性能]水蒸气透过量照塑料薄膜和片材透水蒸气性试验方法杯式法(GBl037-88)的规定进行。
试验时PE 层向湿度低的一侧,试验温度(38±2)℃,相对湿度(90±5)%,不得过0.5(g/m2·24h)。
氧气透过量照塑料薄膜和薄片气体透过性试验方法压差法(GB/T 1038-2000)的规定进行。
试验时PE层向氧气低压侧,试验温度为(23±2)℃,不得过0.5cm3/(m2·24h·0.1MPa)。
[机械性能] PE层与A1层剥离强度照药品包装用复合膜、袋通则(试行)(YBB00132002)内层与次内层剥离强度项下的方法检查,纵、横向剥高强度平均值均不得低于2.5N/15mm。
[热合强度]膜除另有规定外,裁取100mm×100mm试片四片,将任意两个试片PE面叠合,置热封仪上进行热合,热合温度150℃~170℃,压力0.2~0.3MPa,时间1秒。
从热合的中间部位各裁取3条15mm宽的试样,进行试验。
试样应在温度23℃±2℃,相对湿度50%±5%的环境中,放置4小时以上,并在上述条件下进行试验。
以热合部位为中心线,打开呈180度,把试样的两端夹在试验机的两个夹具上,试样轴线与上下夹具中心线相重合,并松紧适宜,夹具间距离为50mm,试验速度为(300±30)mm/min,读取试样断裂时的最大载荷,平均值不得低于12N/15mm。
包装用塑料袋质量标准包装用塑料袋是一种常见的包装材料,广泛应用于各种商品的包装和运输中。
然而,由于市场上存在着各种质量参差不齐的塑料袋,因此有必要对包装用塑料袋的质量标准进行规范和要求,以保障商品包装的安全性和质量,同时减少对环境的影响。
本文将就包装用塑料袋的质量标准进行探讨,以期为相关行业提供参考和指导。
首先,包装用塑料袋的质量标准应当包括对原材料的要求。
塑料袋的原材料应选择优质的聚乙烯或聚丙烯等塑料材料,具有一定的韧性和耐磨性,能够承受一定的重量和压力。
原材料应符合国家相关标准,不得含有有害物质,如重金属、致癌物质等,以确保塑料袋对商品和环境的安全。
其次,包装用塑料袋的质量标准还应包括对生产工艺的要求。
生产塑料袋的工艺应先进、成熟,能够确保塑料袋的尺寸稳定、封口牢固,不易破损。
生产过程中应避免使用劣质原料和回收料,以免影响塑料袋的质量和使用寿命。
同时,生产工艺应符合环保要求,避免产生大量的废气、废水和固体废弃物,减少对环境的污染。
此外,包装用塑料袋的质量标准还应包括对印刷和装饰的要求。
在塑料袋上印刷文字、图案等装饰应清晰、牢固,不易脱落和模糊,以确保商品包装的美观和宣传效果。
印刷油墨应选用环保型材料,不含有害物质,符合食品包装卫生标准,以保障商品的安全和卫生。
最后,包装用塑料袋的质量标准还应包括对成品的要求。
成品塑料袋应符合相关的尺寸、厚度、承重等要求,能够满足商品包装的需要。
同时,成品塑料袋应进行严格的质量检验,确保没有破损、漏气等质量问题,以免影响商品的包装和运输。
综上所述,包装用塑料袋的质量标准应包括对原材料、生产工艺、印刷和装饰以及成品的要求。
只有严格制定和执行这些质量标准,才能保障包装用塑料袋的质量和安全,减少对环境的影响,为商品包装和运输提供保障。
希望相关行业能够重视包装用塑料袋的质量标准,不断提升产品质量,推动行业的健康发展。
药品包装用复合膜、袋通YBB00132002复合膜系指各种塑料与纸、金属或其它塑料通过黏合剂组合而形成的膜其厚度一般不大于0.2 5mm。
复合袋系将复合膜通过热合的方法而制成的袋,按制袋形式可分为三边封袋、中封袋、风琴袋、自立袋、拉链袋等。
本标准适用于非注射剂用的药品包装用复合膜、袋。
药品包装用复合膜按材料组合分类,如表1所示:表1 复合膜分类种类材质典型示例Ⅰ纸、塑料纸或PT/粘合层/PE或EVA、CPPⅡ塑料BOPET或BOPP、BOPA/粘合层/PE或EVA、CPPⅢ塑料、镀铝膜BOPET或BOPP/粘合层/镀铝CPPBOPET或BOPP/粘合层/镀铝BOPET/粘合层/PE或EVA、CPP、EMA、EAA、离子型聚合物Ⅳ纸、铝箔、塑料纸或PT/粘合层/铝箔/粘合层/PE或EVA、CPP、EMA、EAA、离子型聚合物涂层/铝箔/粘合层/PE或CPP、EVA、EMA、EAA、离子型聚合物Ⅴ塑料(非单层)、铝箔BOPET或BOPP、BOPA/粘合层/铝箔/粘合层/PE或CPP、EVA、EMA、EAA、离子型聚合物注1:玻璃纸简称PT;双向拉伸聚丙烯简称BOPP:双向拉伸聚酯简称BOPET;双向拉伸尼龙简称BOPA;聚乙烯简称PE;流延聚丙烯简称CPP;乙烯与醋酸乙烯酯共聚物简称EVA;乙烯与丙烯酸共聚物简称EAA;乙烯与甲基丙烯酸共聚物简称EMA。
注2:复合时可用干法复合或无溶剂复合,这时粘合层为一般的粘合剂。
也可用挤出复合,这时粘合层为PE或EVA、EMA、EAA等树脂。
[鉴别] 红外光谱选取适宜方法,取每层材料,照分光光度法(中华人民共和国药典2000年版附录ⅣC)测定,应符合规定。
(铝、纸成分可不做)。
[外观]取本品适量,在自然光线明亮处,正视目测。
不得有穿孔、异物、异味、粘连、复合层间分离及明显损伤、气泡、皱纹、脏污等缺陷。
复合袋的热封部位应平整、无虚封。
[阻隔性能] 水蒸气透过量照塑料薄膜和片材透水蒸气性试验方法杯式法(GBl037-88)的规定进行。
聚酯低密度聚乙烯药品包装用复合膜、袋(YBB00182002) 国家药品监督管理局国家药品包装容器(材料)标准(试行)YBB00182002聚酯/低密度聚乙烯药品包装用复合膜、袋Laminated Films and Pouches (PET/LDPE) for Pharmaceutical Packaging 本品系指聚酯(PET)与聚乙烯(LDPE)通过黏合剂复合而成的膜。
本品的袋系将上述膜通过热合的方法制成。
本标准适用于固体药品包装用的复合膜、袋。
【外观】取本品适量,照药品包装用复合膜、袋通则(试行)(YBB00132002)外观项下的方法检查,应符合规定。
【鉴别】红外光谱取本品适量,采用内表面反射方法,照分光光度法(中华人民共和国药典2000年版附录IV C)测定,PET及LDPE层应分别与对照图谱基本一致。
【阻隔性能】水蒸气透过量照塑料薄膜和片材透水蒸气性试验方法杯式法(GB1037-88的规定进行。
试验时LDPE层向湿度低的一侧,试验温度(38?2)?,相对湿度(90?5)%,不得过25.5(g/m?24h)。
氧气透过量照塑料薄膜和薄片气体透过性试验方法压差法(GB/T 1038—2000)的规定进行。
32试验时LDPE层向氧气低压侧,试验温度为23??2?,不得过1500cm/( m?24h?0.1Mpa).【机械性能】 PET层与LDPE层剥离强度照药品包装用复合膜、袋通则(试行)(YBB00132002)内层与次内层剥离强度项下的方法检查,纵、横向剥离强度平均值不得低于1.0N/15mm。
【热合强度】膜除另有规定外,裁取100mm×100mm试片四片,将任意两个试片LDPE面叠合,置热封仪上进行热合,热合温度145?-160?,压力0.2-0.3Mpa,时间1秒。
从热合的中间部位各裁取3条15mm宽的试样,进行试验。
试样应在温度23??2?,相对湿度50%?5%的环境中,放置4小时以上,并在上述条件下进行试验。
5004聚酯、铝、聚乙烯药品包装用复合膜、袋质量标准陕西德福康制药有限公司 ________________文件名称:标准技术程序—内包材质量标准文件编号:STP-QS5004-00 聚酯、铝、聚乙烯药品包装用复合膜、袋质量第 1 页共 3 页标准批准人日期 QA审核日期审核人日期执行日期分发号起草人日期颁发部门质量保证部分发部门质量控制部1. 目的建立聚酯、铝、聚乙烯药品包装用复合膜、袋质量标准。
2. 范围内包材聚酯、铝、聚乙烯药品包装用复合膜、袋。
3. 术语或定义3.1 包装材料:药品包装所用的材料,包括与药品直接接触的包装材料和容器、印刷包装材料,但不包括发运用的外包装材料。
3.2 药品质量标准:是国家对药品质量、规格及检验方法所作的技术规定,是药品生产、供应、使用、检验和药政管理部门共同遵循的法定依据。
4. 职责4.1 质量控制部负责起草审核质量标准。
4.2 质量保证部负责审批质量标准。
5. 内容5.1 产品名称中文名称:聚酯、铝、聚乙烯药品包装用复合膜、袋拼音名称:Juzhi、lv、Julvyixi Yaopin Baozhuangyong Fuhemo、dai 5.2 【标准依据】《国家包装容器(材料)标准YBB00172002》5.3 定性和定量的限度要求序号项目标准1 外观不得有穿孔、异物、异味、粘连、复合层间分离及明显损伤、气reduction in property value. Find warning signals, timely reporting or warning, develop and implement measures against customer transfers and other acts leading to loss or increase the difficulty of clearing. Personal credit business of late, agencies should be timely collection, if necessary, ask the right institutions to bring proceedings. Non-approved by head office, agencies at all levels shall not without the following: give文件名称:文件编号管理规程文件编号:SMP—PMP 001 01 第 2 页共 3 页泡、皱纹、脏污等缺陷。
1.目的建立聚酯、铝、聚乙烯药品包装用复合膜、袋质量标准。
2.范围内包材聚酯、铝、聚乙烯药品包装用复合膜、袋。
3.术语或定义
3.1 包装材料:药品包装所用的材料,包括与药品直接接触的包装材料和容器、印刷包装材料,但不包括发运用的外包装材料。
3.2 药品质量标准:是国家对药品质量、规格及检验方法所作的技术规定,是药品生产、供应、使用、检验和药政管理部门共同遵循的法定依据。
4.职责
4.1 质量控制部负责起草审核质量标准。
4.2 质量保证部负责审批质量标准。
5.内容
5.1 产品名称
中文名称:聚酯、铝、聚乙烯药品包装用复合膜、袋
拼音名称:Juzhi、lv、JulvyixiYaopin Baozhuangyong Fuhemo、dai
5.2【标准依据】《国家包装容器(材料)标准YBB00172002》
5.3定性和定量的限度要求
5.4【批准的供应商】生产商—西安昊宇医药包装有限公司
5.5 取样、检验方法或相关操作规程编号:检验方法见《聚酯、铝、聚乙烯药品包装用复合膜、袋检验标准操作规程》(SOP-QC5004-00),取样方法见《取样标准操作规程》
(SOP-QA001-00)。
5.6【贮藏】密闭保存。
5.7 【注意事项】N/A
5.8 【复验期】二年
6.附件N/A
7.参考或引用文件
7.1《取样标准操作规程》SOP-QA001-00
7.2《聚酯、铝、聚乙烯药品包装用复合、袋检验标准操作规程》SOP-QC5004-00
8.文件变更记载。