气体性质计算题简编 含答案
- 格式:docx
- 大小:71.68 KB
- 文档页数:4

气体的性质1.如下图所示,一气缸内充满1标准大气压的空气,缸内有一个空心的铁球,其质量m =10克,半径为2厘米,此时缸内的温度是0℃,气缸顶上有一面积S=100厘米2的重力可以忽略的活塞,活塞可以无摩擦地上下自由移动,为了使铁球离开缸底,在活塞上至少要加多大的外力?(大气压强P o=10牛/厘米2,空气的摩尔质量M=29克/摩尔)2.如下图所示,一根一端封闭的玻璃管,长为l=96厘米,内有一段长为h=20厘米的水银柱,当温度为27℃时,开口端竖直向上,被封闭气体长度为H=60厘米,问温度至少升至多高时,水银才能从管中全部溢出(大气压P o=76厘米汞柱)?3.如下图所示,水平固定的圆筒由足够长的粗筒和细筒相接而成,筒中有直径不同的两个活塞A、B,用一根细绳相线,活塞B通过水平细绳,定滑轮与一质量为2.0kg的重物C连接,A、B两活塞的横截面积分别为20cm2和10cm2。
当两活塞封闭的空气柱温度为327℃时,两活塞保持静止,此时两活塞分别与大小圆筒的相接面的距离均为l。
已知大气压强为1 .0×105P a,活塞与筒壁,滑轮与轮轴间的摩擦均可忽略不计,取g=10m/s2求:(1)此时筒内两活塞间气柱的压强多大?(2)当筒内气体的温度缓慢降至27℃时,活塞A能否向右移距离l?试说明理由。
(3)当气柱温度降至27℃时,筒内气体的压强为多大?(在整个变化过程中,A、B间绳子始终有张力)4.如右图所示,长为2l的圆筒形气缸可沿动摩擦因数为 的水平面滑动,在气缸中央有一截面积为S的活塞,气缸内气体的温度为T o,压强为P o(大气压也为P o),在墙壁与活塞之间装有劲度系数为K的弹簧,当活塞处于图中所示位置时,弹簧恰在原长位置,今使气缸内气体体积增加1倍,问气体的温度应达多少?(气缸内壁光滑,活塞和气缸总质量为m)。
5.一根内径均匀,一端封闭,另一端开口的直玻璃管,长l=100cm,用一段长h=25cm的水银柱将一部分空气封在管内,将其开口朝上竖直放置,被封住的气柱长l0=62.5cm。

一、填空题1.温度为400K ,体积为2m 3的容器中装有2mol 的理想气体A 和8mol 的理想气体B ,则该混合气体中B 的分压力p B =( )KPa 。
13.3022.在300K ,100KPa 下,某理想气体的密度ρ=80.8275×10-3kg ·m -3。
则该气体的摩尔质量M=( )。
3.恒温100°C 下,在一带有活塞的气缸中装有3.5mol 的水蒸气H 2O (g ),当缓慢地压缩到压力p=( )KPa 是才可能有水滴H 2O (l )出现。
4.恒温下的理想气体,其摩尔体积随压力的变化率Tmp V ⎪⎪⎭⎫ ⎝⎛∂∂ =( )。
5,一定的范德华气体,在恒容条件下,其压力随温度的变化率()=∂∂V T /p .6.理想气体的微观特征是:( )7. 在临界状态下,任何真实气体的宏观特征为:( )8. 在n,T 在一定的条件下,任何种类的气体当压力趋近于零时均满足:()=→pV p lim 0( ).9.实际气体的压缩因子定义为Z=( )。
当实际气体的Z>1时,说明该气体比理想气体( )三、问答题理想气体模型的基本假设是什么?什么情况下真实气体和理想气体性质接近?增加压力真实气体就可以液化,这种说法对吗,为什么?第二章 热力学第一定律――附答案一、填空题1. 理想气体向真空膨胀过程 , 下列变量中等于零的有 : 。
2. 双原子理想气体经加热内能变化为 ,则其焓变为 。
3. 在以绝热箱中置一绝热隔板,将向分成两部分,分别装有温度,压力都不同的两种气体,将隔板抽走室气体混合,若以气体为系统,则此过程 。
4. 绝热刚壁容器内发生CH 4+2O 2=CO 2+2H 2O 的燃烧反应,系统的 Q ___ 0 ; W ___ 0 ;∆U ___ 0;∆H ___ 05. 某循环过程 Q = 5 kJ, 则 ∆U + 2W + 3 ∆(pV) = __________.6. 298K 时, S 的标准燃烧焓为-296.8 kJ ⋅mol -1, 298K 时反应的标准摩尔反应焓 ∆r H m = ________ kJ ⋅mol -1 .7. 已知 的 , 则 的 。
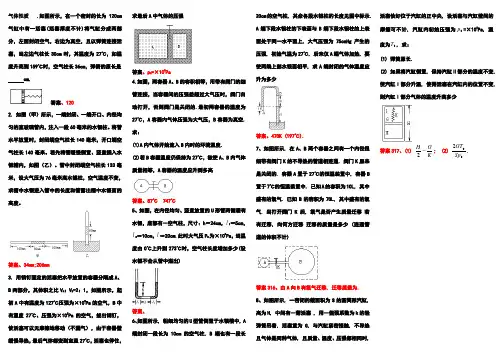
气体性质 .如图所示,在一个密封的长为120cm 气缸中有一活塞(活塞厚度不计)将气缸分成两部分,左面封闭空气,右边为真空,且以弹簧连接活塞,当左边气柱长30cm时,其温度为27℃,如温度升高到159℃时,空气柱长36cm,弹簧的原长是 cm.答案、1202. 如图(甲)所示,一端封闭、一端开口、内径均匀的直玻璃管内,注入一段60毫米的水银柱。
将管水平放置时,封闭端空气柱长140毫米,开口端空气柱长140毫米。
若先将管缓慢倒置、竖直插入水银糟内,如图(乙)。
管中封闭端空气柱长133毫米,设大气压为76毫米高水银柱,空气温度不变,求槽中水银进入管中的长度和管露出槽中水银面的高度。
答案、34mm;206mm3. 用销钉固定的活塞把水平放置的容器分隔成A、B两部分,其体积之比V A:V B=2:1,如图所示,起初A中有温度为127℃压强为×105Pa的空气,B中有温度27℃、压强为×105Pa的空气,拔出销钉,使活塞可以无摩擦地移动(不漏气),由于容器壁缓慢导热,最后气体都变到室温27℃,活塞也停住,求最后A中气体的压强答案、p A=×105Pa4.如图,两容器A、B的容积相等,用带有阀门的细管连接,当容器间的压强差超过大气压时,阀门自动打开,否则阀门是关闭的.最初两容器的温度为27℃,A容器内气体压强为大气压,B容器为真空.求:(1)A内气体开始流入B内时的环境温度.(2)若B容器温度仍保持为27℃,欲使A、B内气体质量相等,A容器的温度应升到多高答案、87℃ 747℃5、如图,在内径均匀、竖直放置的U形管两侧灌有水银,底部有一空气柱,尺寸:h=24cm,l1=5cm,l2=10cm,l=20cm.此时大气压P0为×105Pa,当温度由0℃上升到273℃时,空气柱长度增加多少(设水银不会从管中溢出)答案、6、如图所示, 粗细均匀的U型管倒置于水银槽中, A端封闭一段长为10cm的空气柱, B端也有一段长20cm的空气柱, 其余各段水银柱的长度见图中标示.A端下段水银柱的下表面与B端下段水银柱的上表面处于同一水平面上, 大气压强为75cmHg产生的压强, 初始气温为27℃, 后来仅A端气体加热, 要使两端上部水银面相平, 求A端封闭的气体温度应升为多少答案、470K (197℃).7、如图所示, 在A、B两个容器之间有一个内径很细带有阀门K的不导热的管道相连通. 阀门K原来是关闭的. 容器A置于27℃的恒温装置中, 容器B置于7℃的恒温装置中. 已知A的容积为10L, 其中盛有的氧气. 已知B的容积为70L, 其中盛有的氧气. 当打开阀门K后, 氧气是否产生质量迁移若有迁移, 向何方迁移迁移的质量是多少 (连通管道的体积不计)答案316、由A向B有氧气迁移, 迁移质量为.8、如图所示, 一密闭的截面积为S的圆筒形汽缸,高为H, 中间有一薄活塞 , 用一倔强系数为k的轻弹簧吊着, 活塞重为G, 与汽缸紧密接触, 不导热且气体是同种气体, 且质量、温度、压强都相同时,活塞恰好位于汽缸的正中央, 设活塞与汽缸壁间的摩擦可不计, 汽缸内初始压强为p=×105Pa, 温度为T, 求:(1) 弹簧原长.(2) 如果将汽缸倒置, 保持汽缸Ⅱ部分的温度不变,使汽缸Ⅰ部分升温, 使得活塞在汽缸内的位置不变,则汽缸Ⅰ部分气体的温度升高多少答案317、(1)KGH2; (2)2SpGT.气体性质 . 如图所示,在一个密封的长为120cm气缸中有一活塞(活塞厚度不计)将气缸分成两部分,左面封闭空气,右边为真空,且以弹簧连接活塞,当左边气柱长30cm时,其温度为27℃,如温度升高到159℃时,空气柱长36cm,弹簧的原长是cm.2. 如图(甲)所示,一端封闭、一端开口、内径均匀的直玻璃管内,注入一段60毫米的水银柱。

气体的PVT性质习题一、简答题1、物质的聚集状态分为哪三种,用符号怎么表示?2、名词解释:气体的压强、体积、温度3、理想气体存在吗?真实气体的pVT行为在何种条件下可用pV=nRT来描述?4、理想气体的微观模型是什么?5、分压和分体积定律只适用于理想气体混合物吗?能否适用于真实气体?6、范德华方程式是根据哪两个因素来修正理想气体状态方程的?7、实际气体与理想气体的差异是什么?8、不同气体的压缩因子z值在定温下随压力P是如何变化的?二、计算题1、混合气体中各组分的物质的量分数分别为:氯乙烯0.72、氯化氢0.10和乙烯0.18。
在保持压力101.325kPa不变的条件下,用水洗去氯化氢枯燥,求剩余干气体中各组分的分压力。
2、30℃时,在一个10.0L的容器中,O2,N2和CO2混合物的总压为93.3kPa。
分析结果得p(O2)=26.7kPa,CO2的含量为5.00g,求容器中:a. p(CO2);b.p(N2);c.O2的摩尔分数。
3、 10.0 mol C2H6气体在300K充入4.86×10-3m3的容器中,测得其压力为3.445 MPa。
分别用〔1〕理气状态方程〔2〕范德华方程计算容器内气体的压力〔a=0.5562 Pa·m3/mol2;b=6.380×10-3 m3/mol〕。
气体的PVT性质习题参考答案一、简答题1、物质的聚集状态分为哪三种,用符号怎么表示?答:物质的聚集状态分为气体、液体和固体,分别用符号g,l,s表示。
2、名词解释:气体的压强、体积、温度答:由于分子的热运动,气体分子不断地与容器壁碰撞,对器壁产生作用力。
单位面积器壁上所受的力称为压强,用符号p表示,法定计量单位是Pa(帕斯卡)。
气体的体积即它们所占空间的大小,用符号V 表示。
由于气体能充满整个容器,所以气体的体积就是气体容器的容积,单位是m3(立方米)。
气体的温度是定量反映气体冷热程度的物理量。

物理化学气体性质习题答案物理化学气体性质习题答案气体是物理化学中一个重要的研究对象,其性质和行为对于我们理解自然界和应用科学原理具有重要意义。
在学习物理化学的过程中,我们经常会遇到一些关于气体性质的习题。
下面,我将为大家提供一些常见气体性质习题的答案,希望能对大家的学习有所帮助。
1. 问题:一定体积的气体在恒定温度下,压强与摩尔数成正比。
如果将气体的摩尔数增加一倍,压强会发生什么变化?答案:根据查理定律,一定体积的气体在恒定温度下,压强与摩尔数成正比。
因此,当气体的摩尔数增加一倍时,压强也会增加一倍。
2. 问题:一定质量的气体在恒定温度下,体积与压强成反比。
如果将气体的压强减小一半,体积会发生什么变化?答案:根据波义耳定律,一定质量的气体在恒定温度下,体积与压强成反比。
因此,当气体的压强减小一半时,体积会增加两倍。
3. 问题:一定质量的气体在恒定温度下,体积与摩尔数成正比。
如果将气体的摩尔数减少一半,体积会发生什么变化?答案:一定质量的气体在恒定温度下,体积与摩尔数成正比。
因此,当气体的摩尔数减少一半时,体积也会减少一半。
4. 问题:一定质量的气体在恒定温度下,压强与体积成正比。
如果将气体的体积增加一倍,压强会发生什么变化?答案:根据阿伏伽德罗定律,一定质量的气体在恒定温度下,压强与体积成正比。
因此,当气体的体积增加一倍时,压强也会减少一倍。
5. 问题:一定质量的气体在恒定温度下,压强与摩尔数成正比。
如果将气体的摩尔数减少一半,压强会发生什么变化?答案:一定质量的气体在恒定温度下,压强与摩尔数成正比。
因此,当气体的摩尔数减少一半时,压强也会减少一半。
以上是一些常见的物理化学气体性质习题的答案。
通过解答这些习题,我们可以更好地理解气体的性质和行为。
当然,除了这些基本的性质关系,气体还有很多其他的性质和行为,例如气体的扩散性、气体的溶解度等等。
希望大家在学习和应用物理化学的过程中,能够深入理解气体的性质,掌握相关的理论知识,并能够灵活运用于实际问题的解决中。

化学气体的理想气体定律练习题及解答化学气体的理想气体定律练习题及解答1. 问题一:理想气体定律的表达式是什么?请简要说明每个符号的含义。
理想气体定律的表达式为PV = nRT,其中:- P代表气体的压强(单位为帕斯卡)- V代表气体的体积(单位为立方米)- n代表气体的物质的量(单位为摩尔)- R代表气体常数(单位为焦耳·摩尔^-1·开尔文^-1)- T代表气体的温度(单位为开尔文)2. 问题二:根据理想气体定律回答以下问题:a) 一个由1摩尔氧气组成的气体在温度为300K下,占据1升的体积,求气体的压强。
根据理想气体定律,我们有PV = nRT。
将已知值代入计算得到:P = (1 mol)(8.314 J·mol^-1·K^-1)(300 K)/(1 L) = 24.942 J·L^-1·mol^-1因此,气体的压强为24.942 J·L^-1·mol^-1。
b) 一气缸中装有4摩尔氢气,并且体积为5升。
如果气缸的温度是350K,求气体的压强。
同样地,根据理想气体定律,我们有PV = nRT。
将已知值代入计算得到:P = (4 mol)(8.314 J·mol^-1·K^-1)(350 K)/(5 L) = 233.392 J·L^-1·mol^-1因此,气体的压强为233.392 J·L^-1·mol^-1。
c) 一气缸中装有2摩尔二氧化碳气体,并且温度为400K。
如果气体的压强为80 J·L^-1·mol^-1,求气体的体积。
根据理想气体定律,我们有PV = nRT。
将已知值代入计算得到:V = (2 mol)(8.314 J·mol^-1·K^-1)(400 K)/(80 J·L^-1·mol^-1) = 41.57 L 因此,气体的体积为41.57升。

气体性质计算题简编含答案SANY标准化小组 #QS8QHH-HHGX8Q8-GNHHJ8-HHMHGN#3-3气体性质计算题简编1.如图所示,活塞把密闭气缸分成左、右两个气室,每室各与U 形管压强计的一臂相连,压强计的两壁截面处处相同,U 形管内盛有密度为32/105.7m kg ⨯=ρ的液体。
开始时左、右两气室的体积都为320102.1M V -⨯=,气压都Pa p 30100.4⨯=,且液体的液面处在同一高度,如图19-2所示,现缓慢向左推进活塞,直到液体在U 形管中的高度差h=40cm ,求此时左、右气室的体积1V 、2V ,假定两气室的温度保持不变,计算时可以不计U 形管和连接管道中气体的体积,g 取2/10s m 。
2.某房间的容积为20m 3,在温度为17℃,大气压强为74 cm Hg 时,室内空气质量为25kg ,则当温度升高到27℃,大气压强变为76 cm Hg 时,室内空气的质量为多少千克3.向汽车轮胎充气,已知轮胎内原有空气的压强为个大气压,温度为20℃,体积为20L ,充气后,轮胎内空气压强增大为个大气压,温度升为25℃,若充入的空气温度为20℃,压强为1个大气压,则需充入多少升这样的空气(设轮胎体积不变).4.如图13-60所示,气缸A 和容器B 由一细管经阀门K 相连,A 和B 的壁都是透热的,A 放在27℃、1标准大气压的大气中,B 浸在127℃的恒温槽内,开始时K 是关断的,B 内没有气体,容积V B =2.4L ,A 内装有气体,体积V A =4.8L ,打开K ,使气体由A 流入B ,等到活塞D 停止移动时,A 内气体体积是多大假设活塞D 与气缸壁之间没有摩擦,细管的容积忽略不计.5.如下图所示,粗细均匀的U 形玻璃管竖直放置,两臂长为50cm.在两管中注入10cm 高的水银后,封闭左管口,求继续向右管中注入多高的水银,可使左管水银面上升4cm ,设整个过程中温度保持不变,且大气压强P 0=760mmHg.6.如下图所示,活塞A 将一定质量的气体封闭在汽缸B 内,当汽缸竖直放置时,活塞到缸底的距离为60cm ,活塞与汽缸间摩擦不计,大气压强为×105Pa.现将汽缸平放在水平地面上,测得活塞A 到缸底的距离为100cm ,并测得汽缸B 的截面积S =100cm 2,求活塞A 的质量.7.如下图所示中一个横截面积为10cm 2的容器内,有一个用弹簧和底面相连的活塞,当温度为27℃,内外压强都是×105Pa 时,活塞和底面相距10cm ,在活塞上放质量为40kg 的物体,活塞下降5cm ,温度仍为27℃(活塞质量不计,g 取9.8m/s 2),求:(1)弹簧劲度系数k;(2)如把活塞内气体加热到57℃,为保持活塞位置仍下降5cm ,活塞上应再加的物体质量为多少8.如下图所示,气缸内底部面积为0.02米2,被活塞封闭在气缸内的空气温度为-5℃,活塞质量为8千克,当气缸缸筒与水平面成60°角时,活塞距缸底L ,现将气缸直立,如图所示.欲使活塞距缸底仍为L ,应使缸内气体升高到多少摄氏度(大气压强p 0=×105帕,g =10m/s 2)9.如图所示,水平放置的密封气缸的活塞被很细的弹簧拉住,气缸内密封一定质量的气体.当缸内气体温度为27℃,弹簧的长度为30cm 时,气缸内气体压强为缸外大气压的倍.当缸内气体温度升高到127℃时,弹簧的长度为36cm.求弹簧的原长(不计活塞与缸壁的摩擦)10.如下图所示,一圆柱形气缸直立在水平地面上,内有质量不计的可上下移动的活塞,在距缸底高为2H 0的缸口处有固定的卡环;使活塞不会从气缸中顶出,气缸壁和活塞都是不导热的,它们之间没有摩擦.活塞下方距缸底高为H 0处还有一固定的可导热的隔板,将容器分为A 、B 两部分,A 、B 中各封闭同种的理想气体,开始时A 、B 中气体的温度均为27℃,压强等于外界大气压强P 0,活塞距气缸底的高度为,现通过B 中的电热丝缓慢加热,试求:(1)当B 中气体的压强为时,活塞距缸底的高度是多少 (2)当A 中气体的压强为时,B 中气体的温度是多少11.如图所示,内径均匀的U 型细玻璃管一端开口,竖直放置,开口端与一个容积很大的贮气缸B 连通,封闭端由水银封闭一段空气A ,已知-23℃时空气柱A 长62cm ,右管水银面比左管水银面低40cm ,当气温上升到27℃时,水银面高度差变化4cm ,B 贮气缸左侧连接的细管的体积变化不计.(1)试论证当气温上升到27℃时,水银面高度差是增大4cm 还是减小4cn (2)求-23℃时贮气缸B 中气体的压强.参考答案1.解 以1p 、1V 表示压缩后左室气体的压强和体积,2p 、2V 表示这时右室气体的压强和体积,0p 、0V 表示初态两室气体的压强和体积。

气体的性质1.如下图所示,有一个圆筒形容器,长为3L ,其中装有两个可移动的活塞,分别把两部分气体封闭在圆筒的两部分A 和B 中,A 和B 中为等质量的同种气体,两活塞之间有一被压缩的弹簧且为真空,其自然长为2L ,劲度系数为K ,当AB 两部分气温为T 1开时,弹簧的长为L ,整个系统保持平衡。
现使气温都下降为T 2开,弹簧的长度变为1.5L ,则12T T = 。
1.3/82.如下图所示为0.2摩尔的某种气体的压强与温度的关系,图中P 0为标准大气压, 气体在B 状态时的体积是 。
2.5.6升3.使一定质量的理想气体如下图中箭头所示的顺序变化,图线BC 是一段以纵轴和横轴为渐近线的双曲线,已知气体在状态A 的温度T A =300K ,则气体在状态B 、C 和D 的温度 T B = ,T C = ,T D = 。
3.T B =T C =600k ;T D =300k4.在圆形容器内有一弹簧,上端固定,下端连一重力不计的活塞,活塞与容器内壁 之间不漏气且不计摩擦,容器内活塞上面部分为真空,当弹簧自然伸长时,活塞刚好能触及到容器底部,如果活塞下面充入一定质量的温度为T的某种气体,使活塞下面气柱的高度为h ,如右图所示,当容器内气体温度升高到T 1时,则气柱的高度h 1= 。
4. T T h /15.用注射器验证玻—马定律实验中,因活塞不便从注射器上拆下,为了知道活塞压 气体时产生的附加压强ΔP ,一位学生采用了这样的方法:先使注射器如图(a)竖直放置,读出封闭气体体积V 1=36毫升,然后把注射器倒转180°,如下图(b)放置,读出封闭气体体积 V 2=38毫升,已知大气压为P o =76厘米汞柱,则由活塞重力对气体产生的附加压强为 。
5.2.05cmHg6.潜水艇的贮气筒与水箱相连,当贮存的空气压入水箱后,水箱就排出水使潜水艇 浮起。
某潜水艇贮气筒的容积为2米3,贮有压强为2.00×107帕的压缩气体。


气体性质推断题汇总及答案
题目1:
一瓶氧气和一瓶氮气,它们外形一样,重量一样,在正常大气压下,它们吸收热量的多少一样吗?
答案:一样。
因为它们在相同的温度下,吸收的热量由内能决定,与它们的化学成分和分子大小无关。
题目2:
同一质量的同种气体在相等的体积和温度下混合时,混合气的分压强度增大了吗?
答案:不一定,与两种气体的分子之间作用有关。
如果气体A 和气体B之间相互作用力小于气体A内分子间作用力和气体B内分子间作用力,则以该温度下,气体A与气体B混合的分压强度之和小于两者分别各自的分压强度之和;如果相互作用力大于两气体内部的作用力,则混合气的分压强度之和大于各自的分压强度之和。
题目3:
在常压下,1L氧气(O2)在25℃下可以溶解0.04克,而1L
二氧化碳(CO2)在25℃下只能溶解0.02克,暗示氧气比二氧化
碳
A.分子量大
B.游离能低
C.化学活性强
D.分子之间缔合力小
答案:D。
氧气分子之间缔合力弱,容易吸附在水等介质的表面,而二氧化碳分子之间缔合力较强,容易形成络合物而难以溶解。
题目4:
一个二つ相等、内装气体的温度计,它的校准是在1大气压下的,如果该温度计被带到了2000米高度,此时读数偏向哪里了?
答案:读数偏低。
因为气压减小,导致液柱下降,读数偏低。

理想气体练习题详解理想气体是物理学中常用的一种模型,它具有一些特殊的性质和行为规律,是研究气体性质和动力学过程的基础。
本文将通过解析几个典型的理想气体练习题,帮助读者更好地理解理想气体的基本概念和计算方法。
1. 练习题一在标准大气压下,体积为1L的理想气体中,某物质的质量为5g,求该气体的摩尔质量。
解析:根据理想气体的摩尔质量公式:摩尔质量 = 质量 / 物质的摩尔数,其中物质的摩尔数可以通过气体的体积和标准状态下每个摩尔气体的体积得到。
在标准状态下,1摩尔理想气体的体积为22.4L。
所以,该气体的摩尔质量为:摩尔质量 = 5g /(1L / 22.4L)= 112g/mol2. 练习题二某容器中有一理想气体,初始状态下容器内的气体温度为300K,体积为5L,压强为2 atm。
若气体发生等温压缩,最终体积为2L,求气体的最终压强。
解析:根据理想气体状态方程:P1V1 = P2V2,其中P1和P2为气体的初始和最终压强,V1和V2为气体的初始和最终体积。
带入已知条件,可得:2 atm × 5 L = P2 × 2 L解得最终压强 P2 = 5 atm3. 练习题三某理想气体在一定条件下发生等温膨胀,初始状态下体积为5L,压强为2 atm。
若气体最终体积为10L,求气体的最终压强。
解析:同样根据理想气体状态方程:P1V1 = P2V2带入已知条件,可得:2 atm × 5 L = P2 × 10 L解得最终压强 P2 = 1 atm通过以上三个练习题的解析,我们对理想气体的基本性质和计算方法有了更加清晰的认识。
理想气体模型采用简化的假设,忽略了气体分子之间的相互作用力,使得计算更加方便。
然而,在实际气体中,分子之间的作用力是不可忽略的,在高压、低温条件下,理想气体模型的假设误差会显著增大。
因此,在实际问题中,需要根据具体条件选择合适的气体模型进行计算。
希望本文的练习题详解能够帮助读者更好地理解和掌握理想气体的基本概念和计算方法。
第1章气体的pVT性质思考题1.如何使一个尚未破裂而被打瘪的乒乓球恢复原状?采用了什么原理?2.在两个密封、绝热、体积相等的容器中,装有压力相等的某理想气体。
试问这两容器中气体的温度是否相等?3.两个容积相等的玻璃球内充满N2(g),两球中间用一玻管相通,管中间有一水银滴将两边的气体分开。
当左球的温度为273K,右球的温度为293K时,水银滴处在中间达成平衡。
试问:(1)若将左球的温度升高10K,中间水银滴向哪边移动?(2)若两球同时都升高10K,水银滴向哪边移动?4.在大气压力下,将沸腾的开水迅速倒入保温瓶中,达该瓶容积的70%左右,迅速塞上软木塞防止漏气,然后放开手,请估计会发生什么现象?5.当纯物质的气、液两相处于平衡时,不断升高平衡温度,这时处于平衡状态的气液两相的摩尔体积V m(l)和V m(g)将如何变化?6.如何定义气体的临界温度和临界压力?7.处于临界点的各物质有何共同特性?概念题1.在温度、容积恒定的容器中,含有A和B两种理想气体,这时A的分压和分体积分别为p A和V A。
若在容器中再加入一定量的理想气体C,问p A和V A的变化。
(A)p A,V A都变大(B)p A,V A都变小(C)p A不变,V A变小(D)p A变小,V A不变2.在温度T、容积V恒定的容器中,含有A和B两种理想气体,它们的物质的量、分压和分体积分别为能n A,p A,V A和n B,p B,V B,容器中的总压力为p。
试判断下列公式中哪个是正确的?(A)p A V=n A RT(B)pV B=(n A+n B)RT(C)p A V A=n A RT(D)p B V B= n B RT3.已知H2(g)的临界温度和压力分别为T c=33.3K,p c=1.297×106Pa。
有一氢气钢瓶,在298K时瓶内的压力为98.0×106Pa,问这时氢气的状态。
(A)液态(B)气态(C)气—液两相平衡(D)无法确定4.在一个绝热真空容器中,灌满373K和压力为101.325kPa的纯水,不留一点空隙,这时水的饱和蒸气压为多少?(A)等于零(B)大于101.325kPa(C)小于101.325kPa(D)等于101.325kPa5.真实气体在下述哪个条件下可近似作为理想气体处理?(A)高温高压(B)低温低压(C)高温低压(D)低温高压6.真实气体液化的必要条件是什么?(A)压力大于p c(B)温度低于T c(C)体积等于V m,c(D)同时升高温度和压力7.在一个恒温、容积为2dm3的真空容器中,依次充入温度相同始态为100kPa,2dm3的N2(g)和200kPa,1dm3的Ar(g),设两者形成理想气体混合物,则容器中的总压力为多少?(A)100kPa(B)150kPa(C)200kPa(D)300kPa8.在298K时,往容积相等的A、B两个抽空容器中分别灌入100g和200g水,当达到平衡时,两容器中的水蒸气压力分别为p A和p B,则两者的关系为?(A)p A<p B(B)p A>p B(C)p A=p B (D) 无法确定9.在273K,101.325kPa时,摩尔质量为154g·mol-1的CCl4(l)的蒸气可近似看作理想气体,则气体的密度是多少(单位为g·dm-3)?(A)6.87(B)4.52(C)3.70(D)3.4410.某体积恒定的容器中装有一定量温度为300K的气体,现保持压力不变,要将气体赶出1/6,需将容器加热到的温度为多少?(A)350K(B)250K(C)300K(D)360K概念题:1。
气体的性质水平预测双基型★1.下列说法中正确的是( ).(A)一定质量的气体的体积是不会改变的(B)气体的体积等于所有分子的体积之和(C)所有气体的压强都是由气体受重力引起的(D)密闭容器内气体对各个方向上器壁的压强大小相同答案:D★2.一定质量的理想气体发生状态变化时,其状态参量p、V、T、的变化情况可能是( ).(1995年上海高考试题)(A)p、V、T都增大(B)p减小,V和T增大(C)p和V减小,T增大(D)p和T增大,V减小答案:ABD★★3.如图所示各图中,p表示气体的压强,V表示体积,T表示热力学温度,t表示摄氏温度,则正确描述一定质量理想气体等压变化规律的是图( ).(2002年上海高考试题)答案:AC纵向型★★4.如图所示,竖直插入水银槽的细长玻璃管内外两个水银面高度差为70cm,当时大气压为标准大气压.现保持温度不变,将玻璃管向上提起一些,管内水银面将( ).(A)向上移动(B)向下移动(C)不移动(D)先向下移动,然后再向上移动答案:A★★5.一定质量的理想气体可经不同的过程从一种状态(p1、V1、T1)变到另一种状态(p2、V2、T2),已知T2>T1,则在这些过程中( ).(1990年全国高考试题) (A)气体一定从外界吸收热量(B)气体和外界交换的热量都是相等的(C)外界对气体所做的功都是相等的(D)气体内能的变化都是相等的答案:D★★6.某同用同一个注射器做了两次验证玻意耳定律的实验,操作完全正确.根据实验数据却在如图所示的p-V图上画出了两条不同的双曲线,造成这种情况的可能原因是( ).(2001年上海高考试题)(A)两次实验中空气质量小同(B)两次实验中温度不同(C)两次实验中保持空气质量、温度相同,但所取的气体压强的数据不同(D)两次实验中保持空气质量、温度相同,但所取的气体体积的数据不同答案:AB★★★7.一绝热隔板将一绝热长方形容器隔成两部分,两边分别充满气体,隔板可无摩擦移动.开始时,左边的气体的温度为0℃,右边的气体的温度为20℃,隔板处于静止状态,当左边的气体加热到20℃,右边的气体加热到40℃时,则达到平衡状态时隔板的最终位置( ).(2000年全国高考理科综合试题)(A)保持不动(B)在初始位置右侧(C)在初始位置左侧(D)决定于加热过程答案:B★★★8.如图所示,一端封闭的U形玻璃管竖直放置,左管中封闭有20cm长的空气柱,两管水银面相平,水银柱足够长.现将阀门S打开,流出部分水银,使封闭端水银面下降18cm,则开口端水银面将下降___cm(设此过程中气体温度保持不变,大气压强为76cmHg).答案:54★★★9.已知高山上某处的气压为0.40atm,气温为-30℃,则该处1cm3大气中的分子数约为____________个.(在标准状态下1mol气体的体积为22.4L).(1991年全国高考试题)答案:1.2×1019横向型★★★10.A、B为两个相同的固定在地面上的气缸,内部有质量相等的同种气体,且温度相同,C、D为两重物,质量m C>m D,按如图所示方式连接并保持平衡.现使它们的温度都升高10℃,不计活塞质量及滑轮系统的摩擦,则系统重新平衡后( ).(A)C下降的高度比D下降的多(B)C下降的高度比D下降的少(C)C、D下降的高度一样多(D)A、B气缸内气体的最终压强与初始压强不相同答案:A★★★★11.如图所示,竖直放置的气缸内盛有气体,上面被一活塞盖住,活塞通过劲度系数k=600N/m的弹簧与气缸相连接,系统处于平衡状态.已知此时外界大气压强p0=1.00×105N/m?,活塞到缸底的距离t=0.500m,缸内横截面积S=1.00×10-2m2.今在等温条件下将活塞缓慢上提到距缸底为2l处,此时提力为F=500N.弹簧的原长l0应为多少?若提力为F=700N,弹簧的原长l0又应为多少(不计摩擦及活塞和弹簧的质量,并假定在整个过程中,气缸不漏气,弹簧都遵从胡克定律)?(2002年北京春季高考试题)答案:1.5m,0.833m★★★★★12.一球形热气球,其隔热很好的球皮连同吊篮等装载物的总质量为300㎏.经加热后,气球膨胀到最大体积,此时它的直径为18m,球内外气体成分相同,而球内气体压强则稍稍高过大气压,试求出刚好能使热气球上升时球内空气的温度.已知此时大气温度为27℃,压强为1atm,在标准状况下空气的密度为1.3㎏/m3.(第九届全国中学生物理竞赛决赛试题)答案:54℃阶梯训练气体的状态和状态参量双基训练★1.关于气体的体积,下列说法中正确的是( ).【1】(A)气体的体积与气体的质量成正比(B)气体的体积与气体的密度成反比(C)气体的体积就是所有气体分子体积的总和(D)气体的体积是指气体分子所能达到的空间答案:D★2.对于一定量的气体,下列说法中正确的是( ).(2000年全国高考试题)【1】(A)当分子热运动变剧烈时,压强必变大(B)当分子热运动变剧烈时,压强可以不变(C)当分子间的平均距离变大时,压强必变小(D)当分子间的平均距离变大时,压强必变大答案:B★3.在研究气体的热学性质时,描述气体的热力学状态的参量有_________.对于一定质量的气体,若这三个参量都不变,则气体状态________(选填”变化”或”不变”).若该气体状态发生改变,则至少有______个参量发生广变化.【1】答案:气体的温度、体积和压强,不变,两★4.据报道,美国的一个研究小组利用激光制冷技术,将铯原子冷却到了290nK的极低温度,这一温度是______K.某人体温是36.5℃,也可以说体温为__________K.某人体温升高 1.5℃,也可以说体温升高了_________K.【1.5】答案:2.9×10-7,309.5,1.5★★5.有一房间,上午10时温度为15℃,下午2时的温度为25℃,假定大气压强无变化,则下午2时与上午10时相比较,房间内的( ).【1.5】(A)空气密度增大(B)空气分子的平均动能增大(C)空气分子的速率增大(D)空气质量增大答案:B纵向应用★★6.如图所示,粗细均匀的U形管竖直放置,管内由水银柱封住一段空气柱.如果沿虚线所示的位置把开口一侧的部分截掉,保持弯曲部分管子位置不动,则封闭在管内的空气柱将( ).【2】(A)体积变小(B)体积变大(C)压强变小(D)压强不变答案:A★★7.对于一定质量的气体,下列说法中上正确的是( ).【2】(A)如果体积V减小,气体分子在单位时间内作用于器壁单位面积的总冲量一定增大(B)如果压强p增大,气体分子在单位时间内作用于器壁单位面积的总冲量一定增大(C)如果温度T不变,气体分子在单位时间内作用于器壁单位面积的总冲量一定不变(D)如果密度ρ不变,气体分子在单位时间内作用于器壁单位面积的总冲量一定不变答案:B★★8.如图所示,水平放置的一根玻璃管和几个竖直放置的U形管内都有一段水银柱,封闭端里有一定质量的气体,图(a)中的水银柱长度和图(b)、(c)、(d)中U 形管两臂内水银柱高度差均为h=10cm,外界大气压强p 0=76cmHg,则四部分气体的压强分别为p a =________cmHg,p b =__________cmHg,p c =_______cmHg,p d =_________cmHg.【3】 答案:76,86,66,86★★★9.如图所示,一个横截面积为S 的圆筒形容器竖直放置.金属圆板A 的上表面是水平的,下表面是倾斜的,下表面与水平面的夹角为θ,圆板的质量为M.不计圆板与容器内壁之间的摩擦.若大气压强为p 0,则被圆板封闭在容器中的气体的压强p 等于( ).(1994年全国高考试题)>>p.147【3】 (A)S Mgcos p 0θ+ (B)θθScos Mg cos p 0+ (C)S Mgcos p 20θ+ (D)S Mg p 0+答案:D★★★10.如图所示,一气竖直倒放,气缸内有一质量不可忽略的活塞,将一定量的理想气体封在气缸内,活塞与气缸擘无摩擦,气体处于平衡状态.现保持温度不变把气缸稍微倾斜一点.在气缸达到平衡后,与原来相比,则( ).(2000年广东高考试题)【3】(A)气体的压强变大 (B)气体的压强变小(C)气体的体积变大 (D)气体的体积变小答案:AD★★★11.关于大气压的存在,有个科学史上传为美谈的”马德堡半球”实验:1645年,德国的马德堡有个叫格里克的人做了两个中空的金属半球,直径均为1.2英尺(约0.37m),如图所示.把它们扣在一起,然后抽去其中的空气,这两个半球靠大气的压力紧密地连在一起,用16匹马方才拉开.试估算要把此马德堡半球分开,这16匹马对每个半球作用的拉力约为_________N.【4】答案:1.1×104横向拓展★★★12.如图所示,用弹簧秤拉着一支薄壁平底玻璃试管,将它的开口向下插在水银槽中,由于管内有一部分空气,此时试管内水银面比管外水银面高h.若试管本身的重力与管壁的厚度均不计,此时弹簧秤的示数等于( ).【3】(A)进入试管内的H 高水银柱的重力(B)外部大气与内部空气对试管平底部分的压力之差(C)试管内高出管外水银面的h 高水银柱的重力(D)上面(A)(C)所述的两个数值之差答案:BC★★★13.如图所示,一圆柱形容器上部圆筒较细,下部的圆筒较粗且足够长,容器的底是一个可以沿下部圆筒无摩擦移动的活塞S,用细绳通过测力计F将活塞提着,容器中盛水.开始时,水面与上圆筒的开口处在同一水平面上,在提着活塞的同时使活塞缓慢地下移,在这个过程中,测力计的示数是( ).【4】(A)先变小,然后保持不变(B)一直保持不变(C)先变大,然后变小(D)先变小,然后变大答案:A★★★★14.如图所示是医院给病人输液的部分装置示意图.在输液过程中( ).【5】(A)A 瓶中的药液先用完(B)B 瓶中的药液先用完(C)随着液面下降,A 瓶内C 处气体压强逐渐增大(D)随着液面下降,A 瓶内C 处气体压强保持不变答案:AC★★★★15.如图所示.粗细均匀的U 形细管水平部分长为L,管中盛有一定质量的液体,当U 形管以加速度a 向右运动时,两管中液面的高度差Δh=_______.【5】 答案:g La ★★★★16.如图所示,粗细均匀的试管,横截面积为S,质量为m 的活塞可在其内部无摩擦地滑动,它封闭了一段气柱.现使试管在水平面内以角速度ω绕轴OO′匀速转动,此时活塞和转轴的距离为L.活塞不漏气,运动中封闭气体的温度不变,大气压强为p 0,.则此时封闭气体的压强为多少?>>p.148【6】答案:SL m p 20ω= ★★★★★17.如图所示,芹边容器里液体的密度为ρ1,右边容器里液体的密度为ρ2,a 、b 两管液柱的高度差为h,容器A 中气体的压强为_______(已知大气压强为p 0).(第四届全国力学竞赛试题)【l0】答案:12210A gh p p ρρρρ--= 气体实验定律双基训练★1.关于温度,下列说法中正确的是( ).【1】(A)气体的温度升高1℃,也可以说温度升高1K;温度下降5K,也就是温度下降5℃(B)温度由摄氏温度t升至2t,对应的热力学温度由T升至2T(C)绝对零度就是当一定质量的气体体积为零时,用实验方法测出的温度(D)随着人类制冷技术的不断提高,总有一天绝对零度会达到答案:A★2.一定质量的气体在等温变化过程中,下列物理量中将发生变化的是( ).【1】(A)分子的平均动能(B)单位体积内的分子数(C)气体的压强(D)分子总数答案:BC★★3.一定质者的气体在等容变化过程中.温度每升高1℃,压强的增加等于它在300K时压强的( ).【2】(A)1/27 (B)1/273 (C)1/300 (D)1/573答案:C★★4.下列关于盖·吕萨克定律的说法中正确的是( ).【2】(A)对于一定质量的理想气体,在保持压强不变的情况下,温度每升高1℃时,其体积的增量是温度升高前体积的1/273(B)对于一定质量的理想气体.在保持压强不变的情况下,温度每升高1℃时,其体积的增量是它在0℃时体积的1/273(C)对于一定质量的气体,在保持压强不变的情况下,其体积与温度成止比(D)对于一定质量的气体,在保持压强不变的情况下,其体积与热力学温度成正比答案:BD★★5.如图所示,将一只倒置的试管竖直地插入容器内,试管内原有的空气被压缩,此时,试管内外水面的高度差为h,若使试管插入水中的深度增大一些,则试管内外水面的高度差将( ).(1990年上海高考试题)【2.5】(A)增大(B)减少(C)保持不变(D)无法确定答案:A★★6.如图所示,密封的U形管中装有水银,左、右两端都封有空气,两水银面的高度差为h.把U形管竖直浸没在热水中,高度差将( ).【3】(A)增大(B)减小(C)不变(D)两侧空气柱的长度未知,不能确定答案:A纵向应用★★7.在冬季,剩有半瓶热水的暖水瓶经过一个夜晚,第二天拔瓶口的软木塞时觉得很紧,不易拔出来,主要原因是( ).(2001年上海理科综合试题)【2】(A)软木塞受潮膨胀(B)瓶口因温度降低而收缩变小(C)白天气温升高,大气压强变大(D)瓶内气体因温度降低而压强减小答案:D★★8.人们常常用充气泵为金鱼缸内的水补充氧气,右图所示为充气泵气室的工作原理图.没大气压强为p0,气室中的气体压强为p,气通过阀门S1、S2与空气导管相连接,下列选项中正确的是( ).(2002年上海春季高考理科综合试题)【2.5】(A)当橡皮碗被拉伸时,p>p0,S1关闭S2开通(B)当橡皮碗被拉伸时,p<p0,S1关闭,S2开通(C)当橡皮碗被压缩时,p>p0,S1关闭,S2开通(D)当橡皮碗被压缩时,p <p 0,S 1关闭,S 2开通答案:C★★9.我国民间常用”拔火罐”来治疗某些疾病,即用一个小罐将纸燃烧后放入罐内,然后迅速将火罐开口端紧压在人体的皮肤上,待火罐冷却后,火罐就紧紧地被”吸”在皮肤上,试用气体的有关性质解释这个现象.【4】答案:火罐内的气体体积一定,冷却后气体的温度降低,压强减小,故在大气压力作用下被”吸’’在皮肤上.★★★10.如图所示,轻弹a 管(上端封闭,下端开口).使两段水银柱及被两段水银柱封闭的空气柱合在一起.若此过程中温度不变,水银柱与管壁密封很好,则b 管水银柱的下端而A′与原来a 管水银柱的下端面A 相比,将( ).【4】(A)在同一高度 (B)稍高(C)稍低 (D)条件不足,无法判断答案:C★★★11.气压式保温瓶内密封空气体积为V,瓶内水面与出水口的高度差为h,如图所示.设水的密度为ρ,大气压强为p 0,欲使水从出水口流出,瓶内空气压缩量ΔV 至少为__________.【4】 答案:gh p ghV 0ρρ+★★★12.房间里气温升高3℃时,房间内的空气将有1%逸出到房间外,由此可计算出房间内原来的温度是________℃.【4.5】答案:24★★★13.活塞式气泵是利用气体体积膨胀来降低气体压强的.已知某贮气筒的容积为V,气泵每抽一次,抽出的气体体积为V′=V/2.设抽气过程中温度不变,贮气筒内原来气体的压强为p 0,则对它抽气三次后,贮气筒内气体压强变为多少?【5】答案:278p 0 ★★★14.氧气瓶在车间里充气时,压强达1.5×107Pa,运输到工地上发现压强降为1.35×107Pa,已知车间里的温度为27℃,工地上的温度为-3℃,试判断氧气瓶在运输途中是否漏气(氧气瓶本身的热膨胀忽略不计).【5】答案:不漏气★★★15.一个容积为5L 的没有气的篮球,用横截面积为5cm 2、冲程为25cm 的打气筒打气,在打第81次时,打气筒中活塞至少下压多少才能使空气进入篮球(设打气过程中气体的温度保持不变,p 0=76cmHg)?【6】答案:12.5cm★★★16.如图所示,圆柱形气缸倒置在水平粗糙的地面上,气缸内部封有一定质量的空气,气缸质量为10㎏,缸壁厚度可不计,活塞质量为5㎏,其横截面积为50cm 2,活塞与缸壁间的摩擦不计.当缸内气体温度为27℃时,活塞刚好与地面相接触,但对地面无压力.现对气缸传热,使缸内气体温度升高.问:当气缸对地面无压力时,缸内气体温度是多少℃(已知大气压强p 0=1.0×105Pa)?【6】答案:127℃★★★17.如图所示,上端开口的圆柱形气缸竖直放置,横截面积为0.2m 2的活塞将一定质量的气体和一形状不规则的固体A 封闭在气缸内.温度为300K时,活塞离气缸底部的高度为0.6m.将气体加热到330K 时,活塞上升了0.05m,不计摩擦力及固体体积的变化.求物体A 的体积.(2002年上海高考试题)【7】答案:0.02m 3★★★18.验证查理定律的实验装置如图所示,在这个实验中测得压强和温度的数据中,必须测出的一组数据是_________和______.首先要在环境温度条件下调节A 、B 管中水银面_______________,此时烧瓶中空气压强为____________.再把烧瓶放进盛着冰水混合物的容器里,瓶中空气温度下降至冰水混合物的温度一样,此时烧瓶中空气温度为_________K,B 中水银面将_____________________,再将A 管_________,使B 管中水银___________面____________,这时瓶内空气压强等于__________.【10】答案:当时的大气压,温度,等高,大气压,273,上移,下降,回复到原来的位置,大气压强减去A 、B 管中水银面高度差★★★19.有一组同学对温度计进行了专题研究.他们通过查阅资料得知17世纪时伽利略曾设计过一个温度计,其结构为:一麦秆粗细的玻璃管,一端与一鸡蛋大小的玻璃泡相连,另一端竖直插在水槽中,并使玻璃管内吸入一段水柱.根据管中水柱高度的变化可测出相应的温度.为了研究”伽利略温度计”,同学们按照资料中的描述自制了如图所示的测温装置,图中A 为一小塑料瓶,B 为一吸管,通过软木塞与A 连通,管的下端竖直插在大水槽中,使管内外水面有一高度差h,然后进行实验研究:(1)在不同温度下分别测出对应的水柱高度h,记录的实验数据 如下表所示. 温度(0℃) 17 19 21 23 25 27 h(cm)30.0 24.9 19.7 14.6 9.4 4.2 Δh=h n-1-h n 5.1根据表中数据计算相邻两次测量水柱的高度差,并填入表内的空格.由此可得结论:①当温度升高时,管内水柱高度h 将_______(选填”变大”、”变小”或”不变”).②水柱高度h 随温度的变化而______(选填”均匀”或”小均匀”)变化.试从理论上分析并证明结沧②的正确性(提示:管内水柱产生的压强远远小于一个大气压).__________________________________________________________________________.(2)通过实验,同学们发现用”伽利略温度计”来测温度,还存在一些不足之处,其中主要的不足之处有:①_________________________________________________.②_________________________________________________.(2002年上海高考试题)【12】 答案:(1)5.2,5.1,5.2,5.2①变小②均匀,封闭气体近似作等压变化k T V T V =∆∆=(k 为常数),ΔV=kΔT=kΔt,St k S V h ∆=∆=∆,即h 随温度的变化而均匀变化(S 为管的截面积)(2)①测量温度范围小②温度读数受大气压影响★★★20.大气压强对许多物理实验和化学实验有着重要的影响.现用”验证玻意耳定律”的仪器来测量大气压强p 0.注射器针筒已被固定在竖直方向上,针筒上所标刻度是注射器的容积,最大刻度V max =10ml.注射器活塞已装上钩码框架,如图所示.此外,还有一架托盘天平、若干钩码、一把米尺、一个针孔橡皮帽和少许润滑油.下面是实验步骤,试填写所缺的③和⑤.①用米尺测出注射器针筒上全部刻度的长度L.②_____________________________________.③把适量的润滑油抹在注射器的活塞上,将活塞插入针筒中,上下拉动活塞,使活塞与针筒的间隙内均匀地涂上润滑油.④将活塞插到适当的位置.⑤__________________________________________.⑥在钩码框架两侧挂上钩码,记下挂上的钩码质量m 1.在达到平衡后,记下注射器中空气柱的体积V 1.在这个过程中,不要用手接触注射器以保证空气柱温度不变.⑦增加钩码的个数,使钩码的质量增大为m 2,达到平衡后,记下空气柱的体积V 2.(2)求出计算大气压强p 0的公式(用已给的和测得的物理量表示).(2002年全国高考理科综合试题)【12】 答案:(1)②称出活塞和钩码框架的总质量M ⑤将注射器针筒上的小孔用橡皮帽堵住(2)⎪⎪⎭⎫ ⎝⎛---=M V V V m V m V Lg p 211122m 0 横向拓展★★★★21.宇宙飞船密封舱内有一水银气压计,起飞时舱内温度为0℃,气压计示数相当于76cmHg 所产生的压强,在飞船以a=9.8m/s 2匀加速上升过程中(飞船离地面尚不太高),舱内温度为27.3℃,压强计示数相当于________cm 高水银柱所产生的压强.【7】答案:41.8★★★★22.如图所示,一个粗细均匀的圆筒.B 端用塞子塞住,A 端可用一无摩擦滑动的活塞封闭,筒壁C 处有一小孔,小孔距B 端25cm.现向B 端缓慢移动活塞,若大气压强为1.0×105Pa,筒内壁的横截面积为1.2cm 2,塞子与筒壁间的最大静摩擦力为18N,温度保持不变.要使塞子不会被顶出,活塞推到离B 端的距离不得小于多少?【6】答案:10cm★★★★23.如图所示为测定肺活量的装置示意图,图中A 为倒扣在水中的开口圆筒,测量前尽量排尽其中的卒气.测量时被测者尽力吸足空气,再通过B 将空气呼出,呼出的空气通过气管进入A 内,使A 浮起.已知圆筒A 的质量为,m 、横截面积为S 、大气压强为p 0,水的密度为ρ,圆筒浮出水面的高度为h,则被测者的肺活量有多大?【8】答案:⎪⎪⎭⎫⎝⎛+⎪⎪⎭⎫ ⎝⎛+=S m h p mg S V 0ρ ★★★★24.如图所示,截面均匀的U 形玻璃细管两端都开口,玻璃管足够长,管内有两段水银柱封闭着一段空气柱.若气体温度是27℃时,空气柱在U 形管的左侧.A 、B 两点之间封闭着的空气柱长为15cm,U 形管底长CD=10cm,AC 高为5cm.已知此时的大气压强为75cmHg.(1)若保持气体的温度不变,从U 形管左侧管口处缓慢地再注入25cm 长的水银柱,则管内空气柱长度为多少?(2)为了使这段空气柱长度恢复到15cm,且回到A 、B 两点之间.可以向U形管再注入一些水银,且可改变气体的温度,应从哪一侧管口注人多长水银柱?气体的温度变为多少?【10】答案:(1)12cm(2)右侧,25cm,375K★★★★25.图中的竖直圆筒是固定不动的,粗筒横截面积是细筒的4倍,细筒足够长.粗筒中A、B两轻质活塞间封有空气,气柱长l=20cm.活塞A上方的水银深H=10cm,两活塞与筒壁间的摩擦不计.用外力向上托住活塞B,使之处于平衡状态.水银面与粗筒上端相平.现使活塞B缓慢上移,直至水银的一半被推入细筒中,求活塞B上移的距离.设在整个过程中气柱的温度不变,大气压强p0=75cmHg.(1997年全国高考试题)【12】答案:8cm★★★★26.活塞把密闭气缸分成左、右两个气室,每窒各与U形管压强计的一臂相连,压强计的两臂截面处处相同.U形管内盛有密度为ρ=7.5×102㎏/m3的液体.开始时左、右两气室的体积都为V0=1.2×10-2m3.,压强都为p0=4.0×103Pa,且液体的液面处在同一高度,如图所示.现缓缓向左推进活塞,直到液体在U形管中的高度差h=40cm.求此时左、右气室的体积V1、V2.假定两气室的温度保持不变,计算时可以不计U形管和连接管道中气体的体积,g取10m/s2.(1998年全国高考试题)【14】答案:8.0×10-3m3,1.6×10-2m3★★★★27.如图所示,气缸由两个横截面不同的圆筒连接而成.活塞A、B被轻质刚性细杆连接在一起,可无摩擦移动.A、B的质量分别为m A=12㎏,m B=8.0㎏,横截面积分别为S A=4.0×10-2m.,S H=2.0×10-2m2.一定质量的理想气体被封闭在两活塞之间,活塞外侧大气压强p0=1.0×l05Pa.(1)气缸水平放置达到如图(a)所示的平衡状态,求气体的压强.已知此时气体的体积V1=2.0×10-2m3.现保持温度不变,将气缸竖直放置,达到平衡后如图(b)所示.与图(a)相比,活塞在气缸内移动的距离l为多少?重力加速度g取10m/s2.(1999年全国高考试题)【14】答案:(1)1.0×105Pa(2)9.1×10-2m★★★★28.在如图所示的装置中,A、B和C为内径相等的玻璃管,它们都处于竖直位置.A、B两管的上端等高,管内装有水,A管上端封闭,管内密封部分气体,B管上端开口,C管中水的下方有活塞顶住.A、B、C三管由内径很小的细管连接在一起.开始时,A管中气柱长度L A=3.0m,B管中气柱长度L B=2.0m,C管中水柱长度L0=3.0m,整个装置处于平衡状态.现将活塞缓慢向上顶,直到C管中的水伞部被顶到上面的管中,求此时A管小气柱的长度.已知大气压强p0=1.0×105Pa,计算时重力加速度g取10m/s2.【12】答案:2.62m★★★★29.麦克劳真空计是一种测量极稀薄气体压强的仪器,其基本部分是一个玻璃连通器,其上端玻璃管A与盛有待测气体的容器连接,其下端D经过橡皮软管与水银容器R相通,如图所示.图中K1、K2是相互平行的竖直毛细管,它们的内径皆为d,K1顶端封闭,在玻璃泡B与管C相通处刻有标记m,测量时先降低R使水银面低于m,如图(a)所示,逐渐提升R,直至K 2中水银面与K 1,顶端等高,这时K 1中水银面比顶端低h,如图(b)所示.设待测容器较大,水银面升降不影响其中压强,测量过程中温度不变.已知B(m 以上)的容积为V,K 1的容积远小于V,水银的密度为ρ.(1)试导出上述过程中计算待测压强ρ的表达式.(2)已知V=628cm 3,毛细管的直径d=0.3mm,水银密度ρ=13.6×103㎏/m 3.,h=40mm,算出待测压强p(计算时g 取10m/s 2.,结果保留两位有效数字).(1999年广东高考试题)【15】答案:(1)4V d gh p 22πρ=(2)2.4×10-2pa★★★★30.如图所示,有一个直立的气缸,气缸底到气缸口的距离为L 0(cm),用一厚度和质量均可忽略不计的刚性活塞A,把一定质量的空气封在气缸内,活塞与气缸间的摩擦可忽略.平衡时活塞上表面与气缸U 的距离很小(计算时可忽略不计),周围大气的压强为H 0(cmHg).现把盛有水银的一个瓶子放在活塞上(瓶子的质量可忽略),平衡时活塞到气缸底的距离为L(cm).若不是把这瓶水银放在活塞上,而是把瓶内水银缓缓不断地倒在活塞上方,这时活塞向下移,压缩气体,直到活塞不再下移.求此时活塞在气缸内可能的位置以及与之相对应的条件(即题中给出量之间应满足的关系).设气体的温度不变.(1996年全国高考试题)【16】答案:若L≥H 0,则L′=L;若L <H 0,则L′=H 0★★★★★31有一内径均匀,两支管等长且大于78cm 的、一端开口的U 形管ACDB.用水银将一定质量的理想气体封闭在A 端后,将管竖直倒立.平衡时两支管中液面高度差为2cm,此时闭端气柱的长度为l 0=38cm,如图所示.已知大气压强相当于h 0=76cmHg.若保持温度不变,不考虑水银与管壁的摩擦,当轻轻晃动一下U 形管,使左端液面上升或下降Δh(Δh <2cm)时,将出现什么现象?试加以讨论并说明理由.(第八届全国中学生物理竞赛预赛试题)【20】答案:若晃动幅度小于1cm,水银柱将在最初的平衡位置附近作振动;若晃动幅度大于1cm,水银柱最终将会有一部分从开口端流出;若晃动幅度恰好等于1cm,从理论上讲,这时左、右液面恰好相平,但由于这是一种不稳定平衡,因而这种状态实际上不会出现★★★★★32.在一个横截面积为S 的密闭容器中,有一个质量为m 的活塞把容器中的气体分成两部分.活塞可在容器中无摩擦地滑动,当活塞处于平衡时,活塞两边气体的温度相同,压强都是p,体积分别为V 1,和V 2,如图所示.现用某种方法使活塞稍许偏离平衡位置,然后放开,活塞将在两边气体的压力作用下来回运动.整个系统可看作是恒温的.(1)求活塞的运动周期,将结果用p 、V 1、V 2、m 和S 表示.(2)求气体温度t=0℃时的周期T 和气体温度t′=30℃时的周期T′的比值.(第二届全国中学生物理竞赛决赛试题)【20】答案:(1)()21221V V pS V mV 2+π(2)0.95 ★★★★★33.正确使用高压锅的方法是:将已盖好密封锅盖的压力锅加热,如图(a)所示,当锅内水沸腾时再加盖压力阀S,此时可认为锅内只有水的饱和蒸汽,空气已全部排除.然。
高中物理选修3-3气体大题训练(带答案)本文为物理专业内部资料,包含了几道气体计算题,需要注意格式和表述的准确性。
1.题目描述:一个圆柱形气缸内有一个活塞,气缸上部有挡板,内部高度为d。
活塞封闭一定量的理想气体,开始时活塞离底部加热。
求:①当活塞刚好到达气缸口时,气体的温度;②气体温度达到387℃时,活塞离底部的高度和气体的压强。
2.题目描述:一个U形管,左端封闭着水银和气体,右端开口,两管的气体温度始终不变。
现在用小活塞封住开口端,并缓慢推动活塞,使两管液面相平。
求:①粗管中气体的最终压强;②活塞推动的距离。
3.题目描述:一个U形玻璃管,左端封闭着理想气体,右端开口。
封闭气体的温度为T=312K时,两管水银面的高度差△h=4cm。
现对封闭气体缓慢加热,直到两管水银面相平。
设外界大气压p=76cmHg。
①求左、右两管中的水银面相平时封闭气体的温度;②若保持气体温度不变,从右管的开口端缓慢注入水银,直到右侧管的水银面比左侧管的高△h′=4cm,求注入水银柱的长度。
4.题目描述:一个由三个粗细不同的同轴绝热圆筒组成的气缸,两活塞之间密封有温度为T的空气。
开始时,两活塞静止在图示位置。
现对气体加热,使其温度缓慢上升,两活塞缓慢移动。
求:①加热前被封闭气体的压强和细线中的拉力;②气体温度上升到多少时,其中一活塞恰好移至其所在圆筒与b圆筒连接处;③气体温度上到时,封闭气体的压强。
5.题目描述:一个圆柱形气缸内有一个活塞,活塞封闭一定质量的气体,活塞与汽缸间无摩擦且不漏气。
总质量为m2的砝码盘通过左侧竖直的细绳与活塞相连。
当环境温度为T 时,活塞离缸底的高度为h。
现使活塞离缸底的高度为0.求:当活塞再次平衡时,环境温度是多少?10.在光滑水平面上放置一个质量为2m的气缸,内外壁都光滑,气缸内有一质量为m、横截面积为s的活塞密封住一定质量的理想气体。
大气压强为p,不考虑环境温度变化。
问题如下:①现在对气缸施加一个水平向左的恒力F(如图A),稳定后封闭气柱长为l1,求此时气缸的加速度a和气体的压强p1.②若用大小仍为F的XXX水平向左推活塞,如图B,求稳定后封闭气柱的长度l2.11.如图,高度足够大、导热的圆柱形汽缸A、B竖直放置,其内部的横截面积分别为Sa = 4×10^3 m^2、Sb =1.0×10^-3 m^2,两气缸底部用容积不计的细管连通。
气体性质一、物体由大量分子组成的1. 阿伏加德罗常数:1摩尔任何物质含有的微粒都是N A =6.02×1023mol -1。
2. 分子小而轻:一般分子直径的数量级为10-10m ;质量的数量级为10-26㎏。
3. 油膜法测定分子直径:先测出纯油酸体积V ,再测出它在水面散开面积S ,则单分子油膜的厚度即为分子直径:d=V/S4. 分子直径大小的计算题:会利用公式计算一个分子的质量,体积。
表示摩尔数)表示总分子数,表示密度,表示总体积,表示总质量,为分子体积,为分子质量,为气体摩尔体积,为摩尔质量,,(此公式只适用于气体,(此公式只适用于气体=(普遍适用)=,(普遍适用)n V M v m V ( )N *V V)v V N N *M MN *n N mol A mol A A molA mol N M M V N m M N mol mol molmol A ρρ==== 二、分子的热运动分子永不停息的作无规则运动,且跟温度有关,所以把分子的运动叫热运动。
1. 布朗运动并不是分子的运动,布朗运动反映了液体内部分子的运动,是液体分子不断地撞击颗粒的结果。
2. 布朗运动的特点:①永不停息;②无规则;③颗粒越小,现象越明显;④温度越高,运动越激烈。
3. 扩散现象说明:墨水的扩散实际上是墨水微粒在水中被水分子撞击而运动的结果,反映了液体分子在作永不停息的无规则运动。
温度越高,分子运动越激烈,被撞击的墨水微粒扩散越快。
三、分子间存在相互作用力1、分子间的引力和斥力是同时存在的,且都随分子间距的增大而减小。
实际表现出来的分子力是引力和斥力的合力。
理解分子力做正功,分子势能减小;分子力做负功,分子势能增加。
2、分子间的作用力与分子间的关系: ① r =r 0时:f 引=f 斥,分子力F =0② r <r 0时:f 引<f 斥,分子力表现为斥力 ③ r >r 0时:f 引>f 斥,分子力表现为引力 ④ r >10 r 0时:f 引→0,f 斥→0,分子力F→0。
3-3气体性质计算题简编1.如图所示,活塞把密闭气缸分成左、右两个气室,每室各与U 形管压强计的一臂相连,压强计的两壁截面处处相同,U 形管内盛有密度为32/105.7m kg ⨯=ρ的液体。
开始时左、右两气室的体积都为320102.1M V -⨯=,气压都Pa p 30100.4⨯=,且液体的液面处在同一高度,如图19-2所示,现缓慢向左推进活塞,直到液体在U 形管中的高度差h=40cm ,求此时左、右气室的体积1V 、2V ,假定两气室的温度保持不变,计算时可以不计U 形管和连接管道中气体的体积,g 取2/10s m 。
2.某房间的容积为20m 3,在温度为17℃,大气压强为74 cm Hg 时,室内空气质量为25kg ,则当温度升高到27℃,大气压强变为76 cm Hg 时,室内空气的质量为多少千克?3.向汽车轮胎充气,已知轮胎内原有空气的压强为1.5个大气压,温度为20℃,体积为20L ,充气后,轮胎内空气压强增大为7.5个大气压,温度升为25℃,若充入的空气温度为20℃,压强为1个大气压,则需充入多少升这样的空气(设轮胎体积不变).4.如图13-60所示,气缸A 和容器B 由一细管经阀门K 相连,A 和B 的壁都是透热的,A 放在27℃、1标准大气压的大气中,B 浸在127℃的恒温槽内,开始时K 是关断的,B 内没有气体,容积V B =2.4L ,A 内装有气体,体积V A =4.8L ,打开K ,使气体由A 流入B ,等到活塞D 停止移动时,A 内气体体积是多大?假设活塞D 与气缸壁之间没有摩擦,细管的容积忽略不计.5.如下图所示,粗细均匀的U 形玻璃管竖直放置,两臂长为50cm.在两管中注入10cm 高的水银后,封闭左管口,求继续向右管中注入多高的水银,可使左管水银面上升4cm ,设整个过程中温度保持不变,且大气压强P 0=760mmHg.6.如下图所示,活塞A 将一定质量的气体封闭在汽缸B 内,当汽缸竖直放置时,活塞到缸底的距离为60cm ,活塞与汽缸间摩擦不计,大气压强为1.0×105Pa.现将汽缸平放在水平地面上,测得活塞A 到缸底的距离为100cm ,并测得汽缸B 的截面积S =100cm 2,求活塞A 的质量.7.如下图所示中一个横截面积为10cm 2的容器内,有一个用弹簧和底面相连的活塞,当温度为27℃,内外压强都是1.01×105Pa 时,活塞和底面相距10cm ,在活塞上放质量为40kg 的物体,活塞下降5cm ,温度仍为27℃(活塞质量不计,g 取9.8m/s 2),求:(1)弹簧劲度系数k;(2)如把活塞内气体加热到57℃,为保持活塞位置仍下降5cm ,活塞上应再加的物体质量为多少?8.如下图所示,气缸内底部面积为0.02米2,被活塞封闭在气缸内的空气温度为-5℃,活塞质量为8千克,当气缸缸筒与水平面成60°角时,活塞距缸底L ,现将气缸直立,如图所示.欲使活塞距缸底仍为L ,应使缸内气体升高到多少摄氏度?(大气压强p 0=1.0×105帕,g =10m/s 2)9.如图所示,水平放置的密封气缸的活塞被很细的弹簧拉住,气缸内密封一定质量的气体.当缸内气体温度为27℃,弹簧的长度为30cm 时,气缸内气体压强为缸外大气压的1.2倍.当缸内气体温度升高到127℃时,弹簧的长度为36cm.求弹簧的原长?(不计活塞与缸壁的摩擦)10.如下图所示,一圆柱形气缸直立在水平地面上,内有质量不计的可上下移动的活塞,在距缸底高为2H 0的缸口处有固定的卡环;使活塞不会从气缸中顶出,气缸壁和活塞都是不导热的,它们之间没有摩擦.活塞下方距缸底高为H 0处还有一固定的可导热的隔板,将容器分为A 、B 两部分,A 、B 中各封闭同种的理想气体,开始时A 、B 中气体的温度均为27℃,压强等于外界大气压强P 0,活塞距气缸底的高度为1.6H 0,现通过B 中的电热丝缓慢加热,试求:(1)当B 中气体的压强为1.5P 0时,活塞距缸底的高度是多少? (2)当A 中气体的压强为1.5P 0时,B 中气体的温度是多少?11.如图所示,内径均匀的U 型细玻璃管一端开口,竖直放置,开口端与一个容积很大的贮气缸B 连通,封闭端由水银封闭一段空气A ,已知-23℃时空气柱A 长62cm ,右管水银面比左管水银面低40cm ,当气温上升到27℃时,水银面高度差变化4cm ,B 贮气缸左侧连接的细管的体积变化不计.(1)试论证当气温上升到27℃时,水银面高度差是增大4cm 还是减小4cn? (2)求-23℃时贮气缸B 中气体的压强.参考答案1.解 以1p 、1V 表示压缩后左室气体的压强和体积,2p 、2V 表示这时右室气体的压强和体积,0p 、0V 表示初态两室气体的压强和体积。
课外习题参考答案•第八章气体的性质1.甲76cm,乙86cm,丙76cm, 丁76cm,戊83cm,己69cm,庚60cm,辛92cm.2.(4)・3.水银全部落下.4. 5. 98X106Pa.5.20m.6.(3)・7. 5. 6X105Pa.8.9. 21X105Pa.9. 1.05m3,提示:可将排出的气体仍看作与贮气筒相通,只是气体的体积变大,再将增大部分的气体折合成压强为2. 00X107pa的气体,求出体积.10.(2).11. 1. 15 倍.12.34. 5°C.13.不能.14. 1.07m3.15.-78°C.16.-87°C.17.607°C.18.16 T.提示:可将打n次气看作将体积为nX400cm3、压强为lXl()5pa、温度为300K的气体一次打入.19.UO°C.20.760. 3mm.21.向左移动.22.11.95cm.提示:气柱长度超过11cm后,水银将从开口端流出,气柱每增加xcm,柱内气压也增加相当xcm水银柱产生的压强.23. 3 倍.24.16.25.(4) , (5).*26. 4. 9X106J.*27. 4. 7X107J.*29.温度低于露点时.*30. 1. 742X103Pa.*31. 61.6%.*32.能.*33.低于-2°C.*34. (3).一些常用数据mt P*g - z Wt P4« • Zia21J x IO3«N»2J6X IO3金193 x 10s M25X IO3113 x IO3«a±22x UpULJx IO32Jx IO3«x «P»HX UP蛛ft75X UP 白磷IA IO3mt70X呻B 1.4- 14 X IO349X IO3*09X呻«17X IO3ffi09X IO327x IO30L4X 11Pvut・Z mt P—・ k313J6X 103OJX 10?MR IJ8X Up AM OJDX IO3IJQ3X IO3HM0J8X Up钮IJ03X Up an0J8x UpH*IJOX up0.71 x 呻一11,作曲密度CP・LU X 压强tut<>■ ■ Bf3ttfl■・'A 3.2112Srwui 1.98jMTVunf040ft 1.43童O.!8sn l.»OJO0AWMAtt比悠容cfl • »81•C1cfl ・V • K1*419 x IO3ft461 X IO2 2<Jx UP MH394 x IO22I4X Up fl WX W?株2fl9x IO3M130X IO2 S.WX IO2 1.38 x IO2 w5J02X IO? 1.30 x IO2木在不■£度下邮化埴Iff: 0 30100 1»m230noWJ -版.又1伊x i(fi2% x呻112X邮5IMl.?l*1/。
3-3气体性质计算题简编
1.如图所示,活塞把密闭气缸分成左、右两个气室,每室各与U 形管压强计的一臂相连,压强计的两壁截面处处相同,U 形管内盛有密度为32/105.7m kg ⨯=ρ的液体。
开始时左、右两气室的体积都为32010
2.1M V -⨯=,气压都Pa p 30100.4⨯=,且液体的液面处在同一高度,如图19-2所示,现缓慢向左推进活塞,直到液体在U 形管中的高度差h=40cm ,求此时左、右气室的体积1V 、2V ,假定两气室的温度保持不变,计算时可以不计U 形管和连接管道中气体的体积,g 取2/10s m 。
2.某房间的容积为20m 3,在温度为17℃,大气压强为74 cm Hg 时,室
内空气质量为25kg ,则当温度升高到27℃,大气压强变为76 cm Hg 时,室内空气的质量为多少千克
3.向汽车轮胎充气,已知轮胎内原有空气的压强为个大气压,温度为20℃,体积为20L ,充气后,轮胎内空气压强增大为个大气压,温度升为25℃,若充入的空气温度为20℃,压强为1个大气压,则需充入多少升这样的空气(设轮胎体积不变).
4.如图13-60所示,气缸A 和容器B 由一细管经阀门K 相连,A 和B 的壁都是透热的,A 放在27℃、1标准大气压的大气中,B 浸在127℃的恒温槽内,开始时K 是关断的,B 内没有气体,容积V B =2.4L ,A 内装有气体,体积V A =
4.8L ,打开K ,使气体由A 流入B ,等到活塞D 停止移动时,A 内气体体积是多大假设活塞D 与气缸壁之间没有摩擦,细管的容积忽略不计.
5.如下图所示,粗细均匀的U 形玻璃管竖直放置,两臂长为50cm.
在两管中注入10cm 高的水银后,封闭左管口,求继续向右管中注入多高的水银,可使左管水银面上升4cm ,设整个过程中温度保持不变,且大气压强P 0=760mmHg.
6.如下图所示,活塞A 将一定质量的气体封闭在汽缸B 内,当汽缸竖直放置时,活塞到缸底的距离为60cm ,活塞与汽缸间摩擦不计,大气压强为×105Pa.现将汽缸平放在水平地面上,测得活塞A 到缸底的距离为100cm ,并测得汽缸B 的截面积S =100cm 2,求活塞A 的质量.
7.如下图所示中一个横截面积为10cm 2的容器内,有一个用弹簧和
底面相连的活塞,当温度为27℃,内外压强都是×105Pa 时,活塞和底面相距10cm ,在
活塞上放质量为40kg 的物体,活塞下降5cm ,温度仍为27℃(活塞质量不计,g 取9.8m/s 2
),求:
(1)弹簧劲度系数k;
(2)如把活塞内气体加热到57℃,为保持活塞位置仍下降5cm ,活塞上应再加的物体质量为多少
8.如下图所示,气缸内底部面积为0.02米2,被活塞封闭在气缸内的空气温度为-5℃,活塞质量为8千克,当气缸缸筒与水平面成60°角时,活塞距缸底L ,现将气缸直立,如图所示.欲使活塞距缸底仍为L ,应使缸内气体升高到多少摄氏度(大气压强p 0=×105帕,g =10m/s 2)
9.如图所示,水平放置的密封气缸的活塞被很细的弹簧拉住,气缸内密封一定质量的气体.当缸内气体温度为27℃,弹簧的长度为30cm 时,气缸内气体压强为缸外大气压的倍.当缸内气体温度升高到127℃时,弹簧的长度为36cm.求弹簧的原长(不计活塞与缸壁的摩擦)
10.如下图所示,一圆柱形气缸直立在水平地面上,内有质量不计的可上下移动的活塞,在距缸底高为2H 0的缸口处有固定的卡环;使活塞不会从气缸中顶出,气缸壁和活塞都是不导热的,它们之间没有摩擦.活塞
下方距缸底高为H 0处还有一固定的可导热的隔板,将容器分为A 、B 两部分,A 、B 中各封闭同种的理想气体,开始时A 、B 中气体的温度均为27℃,压强等于外界大气压强P 0,活塞距气缸底的高度为,现通过B 中的电热丝缓慢加热,试求:
(1)当B 中气体的压强为时,活塞距缸底的高度是多少 (2)当A 中气体的压强为时,B 中气体的温度是多少
11.如图所示,内径均匀的U 型细玻璃管一端开口,竖直放置,开口端与一个容积很大的贮气缸B 连通,封闭端由水银封闭一段空气A ,已知-23℃
时空气柱A 长62cm ,右管水银面比左管水银面低40cm ,当气温上升到27℃时,水银面高度差变化4cm ,B 贮气缸左侧连接的细管的体积变化不计.
(1)试论证当气温上升到27℃时,水银面高度差是增大4cm 还是减小4cn (2)求-23℃时贮气缸B 中气体的压强.
参考答案
1.解 以1p 、1V 表示压缩后左室气体的压强和体积,2p 、2V 表示这时右室气体的压强和体积,0p 、0V 表示初态两室气体的压强和体积。
由玻意耳定律得
由题述可知体积关系0212V V V =+ 两气室压强关系gh p p ρ=-21 解以上四式得
解方程并选择物理意义正确的解得 代入数值,得331100.8m V -⨯=
2.解析:以房间内的空气为研究对象,是属于变质量问题,应用克拉珀龙方程求解,设原质量为m ,变化后的质量为m ′,由克拉珀龙方程
3.解析:以充气后轮胎内的气体为研究对象,这些气体是由原有部分加上充入部分气体所混合构成.
轮胎内原有气体的状态为:p 1= atm ,T 1=293K ,V 1=20L . 需充入空气的状态为:p 2=1atm ,T 2=293K ,V 2=
充气后混合气体状态为:p =,T =298K ,V =20L 4.解:3L
5.解:1
6.40mm (提示:设右管中注入水银后比左管高出xmm ,而此时左管封闭气体体积V 2,由玻意耳定律得P 1V 1=P 2V 2,760×40=P 2·36①,P 2=760+x ②,由①②得x=(mm),故共注入+2×4=16.40mm 水银)
6.解:66.7kg [提示:设活塞A 质量为m.封闭气体初态:P 1=P 0+S
mg
,V 1=60S ;末态P 2=P 0,V 2=100S ,由P 1V 1=P 2V 2得(P 0+
S
mg
)60S=P 0·100S ,∴m=66.7kg ] 7.解:.K=6×103N/m ;△m=1kg
提示:(1)Ⅰ状态:P 1=P 0,l 1=10cm ,T 1=300k ;Ⅱ状态:P 2=P 0+s
kx
mg -,l 2=5cm ,T 2=300K ,x=5cm ,由P 1l 1s=P 2l 2s ,得:k=
x
S
P mg 0-=6×103N/m (2)Ⅲ状态:P 3,V 3=l 2s ,T 3=330K ,由
33T P =22T P 得P 3=2
3T T
P 2=,△mg/s=P 3-P 2= ∴△m=g=1kg 8.解:-3.7℃ (提示:初状态时:P 1=P 0+mgsin60°/s ,T 1=268K ,末状态时:P 2=P 0+mg/s ,
T 2=,由11T P =22T P ,得T 2=12P P T 1=5
510035.1268
1004.1⨯⨯⨯K=,∴t==-3.7℃)
9.解.21cm (提示:设弹簧原长为l ,活塞截面积为S ,弹簧劲度系数为k ,由题意得
300302.10S P ⨯=400
36S
P •①,=P 0S+k ②,PS=P 0S+k ③,由①②③得l)
10.解:(1)B 中气体做等容变化,由查理定律得
'B B P P ='
B B
T T ,求得压强为时气体的温度T B ′=450K
A 中气体做等压变化,由于隔板导热,A 、
B 中气体温度相等,A 中气体温度也为450K ,对A 中气体有
A A V V '=A A T T ',V A ′=A A T T 'V A =A
B T T '
V A =,活塞距离缸底的高度为. (2)当A 中气体压强为,活塞将顶在卡环处对A 中气体有
A A A T V P =〃
〃
〃A A A T V P ,得T A ″=
A
A A A V P V P 〃
〃T A =750K ,则B 中气体温度也为750K. 11.解:(1)假设水银柱不动,由查理定律得
11T P =22T P =T P △△ ∴△P=1
1T P △T 显然在△T 、T 1相同情况下,初始压强P 1越大,升高相同温度时,压强的增量越大,而初始状态时,
P A <P B ,所以△P A <△P B ,则A 中水银上升,水银面高度差增大
(2)设-23℃时,B 中气体压强为P B ,对A 中理想气体有
A A A T L P ='
'
'A A A T L P ,即
25062)40(⨯-B P =300
62
)40'(⨯-B P ①
对B 中气体有
250B P =300
'
B P ② 由①②得P B =140cmHg。