《药品不良反应事件报告表》填写与上报
- 格式:ppt
- 大小:359.00 KB
- 文档页数:12

药品不良反应事件报告表填写示例示例文章篇一:哎呀呀,这“药品不良反应事件报告表填写示例”,刚开始我还真不太懂呢!不过听老师一讲,好像也没那么难。
就说上次吧,老师在课堂上给我们讲这个,大家都一脸懵。
“这是啥呀?”“怎么填呀?”教室里充满了这样的疑问声。
老师先给我们展示了一张报告表,哇,上面好多格子好多字!老师笑着说:“同学们,别害怕,咱们一步一步来。
”先看这姓名栏,这不就跟咱们写作业写名字一样嘛,得写清楚谁用了药出了问题。
再看年龄,这可得准确,小宝宝和大人用药反应能一样吗?然后是药品名称,这可不能写错,不然医生怎么知道是哪种药出了状况。
就好像我们认错了同学,那不是闹笑话啦?用药的剂量也重要得很,多了少了都可能有影响。
这就好比我们吃饭,吃多了撑得慌,吃少了又饿肚子。
还有用药时间,啥时候用的药得记清楚,这就像我们记住哪天过生日一样重要。
症状描述这一块,可得仔细说清楚。
是头疼?还是肚子疼?是痒痒?还是晕乎乎?要像给好朋友讲故事一样,把所有的不舒服都讲明白。
再看看过敏史,有没有对啥药过敏,这可关系到以后用药安不安全。
填这报告表就像是给药品做一次“体检”,每个细节都不能马虎。
要是填错了,医生不就找不到问题的关键啦?我觉得呀,认真填写这报告表太重要啦!它能帮助医生更好地了解情况,让病人更快地好起来。
大家说是不是呀?示例文章篇二:哎呀呀,说起这药品不良反应事件报告表,这可真是个重要的东西呢!就拿我上次生病来说吧,医生给我开了一堆药。
我乖乖地吃了,结果呢,身上居然起了好多小红疹子,痒痒得不行。
这可把我和爸爸妈妈急坏啦!你们想想,药品本来是用来治病的,可要是出现了不好的反应,那得多让人担心呀!这时候,填写药品不良反应事件报告表就变得超级重要啦。
比如说,报告表上会问你吃的是啥药,这就像警察叔叔查案,得先知道“嫌疑犯”是谁。
然后还会问你啥时候吃的,吃了多少,这就好比了解“犯罪”的时间和“作案”的程度。
还有啊,它会让你说一说身体出现了啥不舒服的情况。

药品不良反应上报流程及上报时限一、药品不良反应上报流程1. 发现药品不良反应在临床用药过程中,医务人员应密切观察患者对药品的反应。
一旦发现患者出现异常表现,并确认为药品不良反应,应立即进行记录和调查。
2. 填写药品不良反应报告表医务人员需根据调查结果,详细填写《药品不良反应/事件报告表》。
报告表主要包括以下内容:患者的个人信息、药品使用情况、不良反应表现、不良反应的程度和处理措施等。
3. 上交药品不良反应报告表填写完毕的药品不良反应报告表应上交至药剂科。
药剂科负责对报告表进行审核、整理和归档。
同时,保留输液器和药液样本,送药剂科封存。
4. 药剂科上报至相关部门药剂科将药品不良反应报告表上传至国家药品不良反应监测系统。
此外,还需将报告表上报至当地药品监督管理部门和医疗机构。
5. 分析和处理药品不良反应药品监督管理部门、医疗机构和生产企业根据药品不良反应报告表,对不良反应进行分析和处理。
必要时,采取措施通知患者、收回药品、限制药品使用等。
6. 随访和信息更新医务人员需对药品不良反应患者进行随访,了解患者的康复情况,并及时更新药品不良反应信息。
二、药品不良反应上报时限1. 个例药品不良反应:(1)新的、严重的药品不良反应:发现后15日内上报;(2)一般药品不良反应:发现后30日内上报;(3)死亡病例:立即上报;(4)有随访信息:及时上报。
2. 群体药品不良反应:(1)发现后立即上报;(2)医疗机构应于24小时内填写《药品不良反应/事件报告表》,并上报至当地药品监督管理部门和医疗机构;(3)生产企业应于24小时内上报至国家药品不良反应监测系统,并于48小时内填写《药品不良反应/事件报告表》,并上报至当地药品监督管理部门和医疗机构。
3. 医疗器械不良事件:(1)发现后立即上报;(2)医疗机构应于24小时内填写《医疗器械不良事件报告表》,并上报至当地药品监督管理部门和医疗机构;(3)生产企业应于24小时内上报至国家医疗器械不良事件监测系统,并于48小时内填写《医疗器械不良事件报告表》,并上报至当地药品监督管理部门和医疗机构。

《药品不良反应/事件报告表》可大致分为报告基本情况、患者基本情况、使用药品情况、ADR过程描述、关联性评价、报告人报告单位信息六部分。
1.报告基本情况首次报告□跟踪报告□编码:是电子上报后自动形成的每份报告的唯一编码。
报告类型:新的□严重□一般□(1)严重的药品不良反应:①导致死亡危及生命②致癌、致畸、致出生缺陷③导致显著的或者永久的人体伤残或者器官功能损伤④导致住院时间时间延长(2)新的药品不良反应:指药品说明书中未载明的不良反应或者说明书中已有描述,但不良反应发生的性质、程度、后果获准频率与说明书描述不一致或者严重,按照新的药品不良反应处理。
报告单位类别:医疗机构□√经营企业□生产企业□个人□其他□2.患者相关情况患者姓名:填写患者真实全名。
①当新生儿被发现有出生缺陷时,如果报告者认为这种出生缺陷可能与孕妇在妊娠期间服用药品有关时,患者是新生儿,并且将母亲使用的可能引起新生儿出现ADR的药品列在可以药品栏中;②如果孕妇在妊娠期间服用药品出现ADR没有影响到胎儿/新生儿,患者是母亲;如果ADR是胎儿死亡或自然流产,患者是母亲;③如果新生儿和母亲都发生ADR,应填写两张报告表,并且注明两张报告表的相关性。
出生日期/年龄:患者的出生年应填写4位数,如2004年。
如果患者的出生日期无法获得,应填写发生不良反应时的年龄(月龄/日龄)。
体重:注意以千克(公斤)为单位。
如果不知道准确的体重,请做一个最佳的估计。
联系方式:最好填写患者的联系电话或者移动电话。
如果填写患者的通信地址,请附上邮政编码。
原患疾病:患者所患的所有疾病。
若同时患有几种疾病,尽量完整填写所有疾病,建议首先填写与怀疑药品的使用相关的疾病。
疾病诊断应填写标准全称,如急性淋巴细胞白血病,不能写ALL。
既往药品不良反应/事件情况:包括药物过敏史:如选择“有”,应具体说明。
家族药品不良反应/事件:根据实际情况正确选择,如选择“有”,应具体说明。
相关重要信息:此栏的过敏史是指药物过敏史之外的其他过敏经历,如花粉过敏、牛奶过敏、花生过敏等;药物过敏史应在“既往药品不良反应/事件”一栏说明。
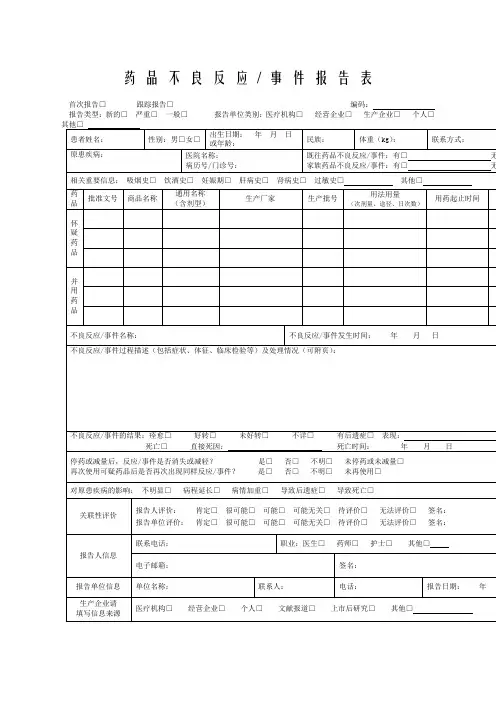
药品不良反应/ 事件报告表首次报告□跟踪报告□编码:报告类型:新的□严重□一般□报告单位类别:医疗机构□经营企业□生产企业□个人□药品不良反应/ 事件报告表示例首次报告□跟踪报告□编码:1.《药品不良反应/事件报告表》应填写真实事件,报表所列患者信息及怀疑药品信息项目必须真实、完整、准确。
2.《药品不良反应/事件报告表》填写字迹要清晰,其中选择项画“√”,叙述项应准确、简明,不得有缺漏项。
3. 新的□严重□一般□(1)新的药品不良反应:是指药品说明书中未载明的不良反应。
说明书中已有描述,但不良反应发生的性质、程度、后果或者频率与说明书描述不一致或者更严重的,按照新的药品不良反应处理。
根据不良反应/事件损害的严重程度,不良反应/事件可能是新的严重的,也可能是新的一般的。
(2)严重药品不良反应,是指因使用药品引起以下损害情形之一的反应:1) 导致死亡;2)危及生命;3)致癌、致畸、致出生缺陷;4)导致显著的或者永久的人体伤残或者器官功能的损伤;5)导致住院或者住院时间延长;6)导致其他重要医学事件,如不进行治疗可能出现上述所列情况的。
(3)一般:指新的、严重的药品不良反应以外的所有不良反应。
4. 单位名称:必须填写单位的完整全称,如日照市人民医院。
5. 部门:应填写科室的标准全称,如:消化内科、普外三科等。
6. 电话:填写报告部门(即科室)的电话。
7. 报告日期:指上交不良反应/事件报告的时间。
新的或严重的药品不良反应/事件应于发现之日起15日内报告,其中死亡病例须立即报告,其他药品不良反应应30日内报告。
有随访信息的,应当及时报告。
8. 患者姓名:填写患者真实全名。
9. 体重:以千克为单位。
如果不知道准确体重,请做一个最佳的估计。
10. 联系方式:最好填写患者的联系电话,也可填写患者的通信地址。
11. 家族药品不良反应/事件及既往药品不良反应/事件情况:请选择正确选项。
如果选择“有”,则在报告的空白处清晰叙述。

如何填写、评价和上报药品不良反应报告一、病例报告表填写要求(1)填报内容应真实、完整、准确。
(2)钢笔书写,填写内容、签署意见、签名等字迹清楚,选择项画“√”。
(3)每一个不良反应病例填写一张报告表。
(4)个人报告建议由专业人员(医生、药师等)填写。
(5)尽可能详细地填写报告表中所要求的项目。
有些内容无法获得时,须填写“不详”。
(6)对于报告表中的描述性内容,如果报告表提供的空间不够,可另附A4纸说明。
(7)报告单位名称须用全称。
(8)电话、报告日期、患者姓名、性别、出生日期、民族、体重、联系方式等应明确。
(9)家族药品不良反应/事件和既往药品不良反应/事件情况应仔细询问并填写清楚。
(10)不良反应/事件名称应填写不良反应中最主要、最明显的症状,并选取参考《WHO药品不良反应术语集》。
(11)不良反应/事件过程描述及处理情况:不良反应/事件的开始时间和变化过程要用具体时间,不良反应/事件的表现填写时要尽可能明确、具体,如为过敏型皮疹,要填写皮疹的类型、性质、部位、面积大小等;与可疑不良反应/事件有关的辅助检查结果要尽可能明确填写,并填写与不良反应/事件发生相关的病史。
(12)药品情况:填写报告人认为可能与不良反应/事件发生有关的药品,填写包括药品的商品名和通用名,尤其是通用名。
(13)说明用药情况:用法用量、用药起止时间、用药原因、并用药品等。
(14)不良反应/事件结果:注意鉴别原患疾病的后果和不良反应/事件结果。
二、药品不良反应的关联性评价依据不良反应/事件分析的五条标准,评价并记录结果,具体掌握如下:(1)肯定:用药及反应发生时间顺序合理;停药反应停止,或迅速减轻或好转(根据机体免疫状态某些ADR反应可出现在停药数天以后);再次使用,反应再现,并可能明显加重(即激发试验阳性);同时有文献资料佐证;并已除外原患疾病等其它混杂因素影响。
(2)很可能:无重复用药史,余同“肯定”,或虽然有合并用药,但基本可排除合并用药导致反应发生的可能性。

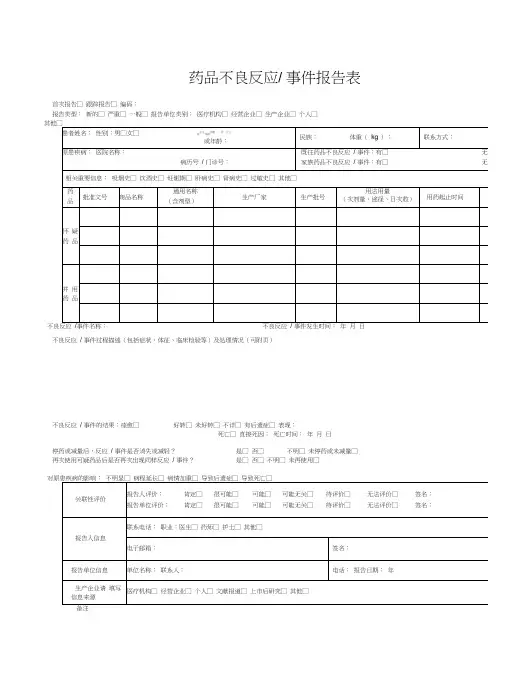
药品不良反应/ 事件报告表首次报告□ 跟踪报告□ 编码:报告类型:新的□ 严重□ 一般□ 报告单位类别:医疗机构□ 经营企业□ 生产企业□ 个人□不良反应事件名称:不良反应事件发生时间:年月日不良反应/ 事件过程描述(包括症状、体征、临床检验等)及处理情况(可附页)不良反应/ 事件的结果:痊愈□好转□ 未好转□ 不详□ 有后遗症□ 表现:死亡□ 直接死因:死亡时间:年月日停药或减量后,反应/ 事件是否消失或减轻?是□ 否□不明□ 未停药或未减量□再次使用可疑药品后是否再次出现同样反应/ 事件?是□ 否□ 不明□ 未再使用□电子邮箱: 签名:×××药 品 不 良 反 应 / 事 件 报 告 表示例不良反应 / 事件过程描述(包括症状、体征、临床检验等)及处理情况(可附页) 一般格式为:患者因×××疾病于×××月×××日(必要时应详细到×××时分)以×××途径给予×××药品,×××剂量,用药×× ×时间出现×××反应(反应描述须明确、具体) ,×××时间后给予是否停药及×××处理(包括以×××途径给予×××药品及×××剂 和其他处理措施) ,处理后×××时间患者转归情况。
对原患疾病的影响: 不明显□ 病程延长□ 病情加重□ 导致后遗症□ 导致死亡□报告人评价: 肯定□ 很可能□ 可能□ 可能无关□ 待评价□ 无法评价□ 签名:××× 报告单位评价:肯定□很可能□可能□可能无关□待评价□无法评价□签名:×××报告人信息患者姓名:×××性别:男□女□出生日期: 年 月 日 或年龄: ××民族:××体重( kg ):××联系方式:××××××原患疾病:指患者此次入 诊的主要疾病(如果有多 疾病可以补充在相关重要 是备注里面),不能写字院或就 种慢性信息或 母缩写。

药品不良反应报告表填写示例及填写说明 SANY标准化小组 #QS8QHH-HHGX8Q8-GNHHJ8-HHMHGN#药品不良反应 / 事件报告表首次报告□跟踪报告□编码:报告类型:新的□严重□一般□报告单位类别:医疗机构□经营企业□生产企业□个人药品不良反应 / 事件报告表示例首次报告□跟踪报告□编码:1.《药品不良反应/事件报告表》应填写真实事件,报表所列患者信息及怀疑药品信息项目必须真实、完整、准确。
2.《药品不良反应/事件报告表》填写字迹要清晰,其中选择项画“√”,叙述项应准确、简明,不得有缺漏项。
3. 新的□严重□一般□(1)新的药品不良反应:是指药品说明书中未载明的不良反应。
说明书中已有描述,但不良反应发生的性质、程度、后果或者频率与说明书描述不一致或者更严重的,按照新的药品不良反应处理。
根据不良反应/事件损害的严重程度,不良反应/事件可能是新的严重的,也可能是新的一般的。
(2)严重药品不良反应,是指因使用药品引起以下损害情形之一的反应:1) 导致死亡;2)危及生命;3)致癌、致畸、致出生缺陷;4)导致显着的或者永久的人体伤残或者器官功能的损伤;5)导致住院或者住院时间延长;6)导致其他重要医学事件,如不进行治疗可能出现上述所列情况的。
(3)一般:指新的、严重的药品不良反应以外的所有不良反应。
4. 单位名称:必须填写单位的完整全称,如日照市人民医院。
5. 部门:应填写科室的标准全称,如:消化内科、普外三科等。
6. 电话:填写报告部门(即科室)的电话。
7. 报告日期:指上交不良反应/事件报告的时间。
新的或严重的药品不良反应/事件应于发现之日起15日内报告,其中死亡病例须立即报告,其他药品不良反应应30日内报告。
有随访信息的,应当及时报告。
8. 患者姓名:填写患者真实全名。
9. 体重:以千克为单位。
如果不知道准确体重,请做一个最佳的估计。
10. 联系方式:最好填写患者的联系电话,也可填写患者的通信地址。

药品不良反应上报途径和注意事项药品不良反应(Adverse Drug Reaction, ADR)的上报是确保公众用药安全的重要环节。
以下是关于的详细内容,包括上报流程、具体步骤、注意事项及相关法律法规,旨在为您提供丰富、全面的信息。
一、药品不良反应上报途径1. 医疗机构上报医疗机构是药品不良反应监测的前沿阵地,以下是医疗机构上报不良反应的途径:临床药师上报:临床药师在临床工作中发现药品不良反应时,应立即填写《药品不良反应报告表》,并及时报告给医院的药品不良反应监测机构。
医师上报:医师在诊疗过程中发现药品不良反应,应告知患者并记录在病历中,同时填写《药品不良反应报告表》。
护士上报:护士在护理过程中发现药品不良反应,应及时通知医师和临床药师,并协助填写《药品不良反应报告表》。
2. 药品生产企业和经营企业上报药品生产企业和经营企业在生产、销售、使用过程中发现药品不良反应,应按照以下途径上报:主动监测:企业应建立药品不良反应监测制度,对上市药品进行主动监测,发现不良反应及时上报。
被动监测:企业通过医疗机构、患者等渠道收集药品不良反应信息,并上报。
3. 患者上报患者在使用药品过程中发生不良反应,可以通过以下途径上报:医疗机构:患者可以直接向医疗机构报告药品不良反应,由医疗机构进行上报。
药品不良反应监测中心:患者可以拨打当地药品不良反应监测中心的电话进行报告。
网络平台:部分地区的药品不良反应监测中心提供了在线上报的平台,患者可以通过网络进行上报。
二、药品不良反应上报流程及具体步骤1. 填写《药品不良反应报告表》《药品不良反应报告表》是上报药品不良反应的重要文件,应包含以下内容:患者信息:包括患者姓名、性别、年龄、体重、联系方式等。
药品信息:包括药品名称、规格、批号、生产厂家、使用剂量、使用频率等。
不良反应信息:包括不良反应的发生时间、表现、程度、治疗措施等。
报告人信息:包括报告人姓名、职业、联系方式等。
2. 提交报告医疗机构:将《药品不良反应报告表》提交给医院的药品不良反应监测机构。

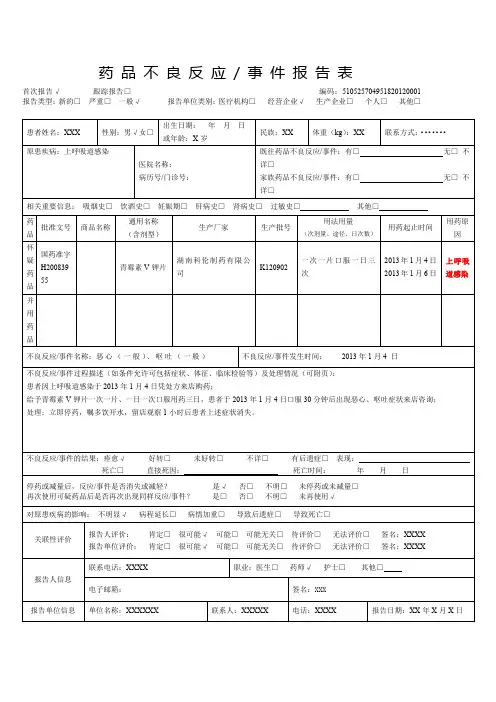
《药品不良反应/事件报告表》填写说明(一)、填写注意事项:(1)、药品不良反应/事件报告是在特定时间的某个具体的患者、具体的生产企业、使用某个批次的药品而出现的,《药品不良反应/事件报告表》的中的患者、药品名称、时间等填写内容应真实、完整、准确。
(2)、《药品不良反应/事件报告表》是药品安全性监测工作的重要档案资料,手工报表需要长期保存,因此务必用钢笔书写,填写内容、签署意见(包括有关人员的签字)字迹要清楚,不得用报告表中未规定的符号、代号、不通用的缩写形式和花体式签名。
其中选择项画“ⅴ”,叙述项应准确、完整、简明,不得有缺漏项。
(3)、每一个病人填写一张报告表。
(4)、尽可能详细地填写报告表中所要求的项目。
有些内容无法获得时,填写“不详”。
(5)、对于报告表中的描述性内容,如果报告表提供的空间不够,可另附A4纸说明。
并将“附件”写在一张纸的顶部,所有的附件应按顺序标明页码,附件中必须指出继续描述的项目名称。
(6)、如果报告的是补充报告,请填写与原始报告相同的编号,并在报告左上方注明“补充报告”,与原始报告重复的部分可不必再填写。
补充报告也可不填写报告表,只需要对补充部分附纸说明即可。
(二)、填写详细要求1、新的□ 、严重□ 一般□(1)、新的药品不良反应是指药品说明书中未载明的不良反应。
根据不良反应/事件损害的严重程度,不良反应/事件可能是新的严重的;也可能是新的一般。
(2)、药品严重不良反应是指因服药引起以下损害情形之一的反应:⑴引起死亡;⑵致癌、致畸、致出生缺陷⑶对生命有危险并能够导致人体永久的或显著的伤残;⑷对器官功能产生永久损伤;⑸导致住院或住院时间延长。
(3)、一般:新的、严重的药品不良反应以外的所有不良反应。
2、医疗机构□ 、生产企业经营企业□ 个人□选择药品不良反应/事件报告表的填报单位的类型:(1)、医疗卫生机构:指从事预防、诊断、治疗疾病活动并使用药品的医疗机构、疾病控制机构、保健机构、计划生育服务机构等。
药品不良反应与药害事件上报的流程药品不良反应(Adverse Drug Reaction, ADR)与药害事件的上报是确保药品安全、提高药品质量的重要环节。
以下是一份详细的药品不良反应与药害事件上报流程,内容丰富,旨在为相关工作人员提供具体指导。
一、药品不良反应上报流程1. 药品不良反应监测(1)医疗机构应建立药品不良反应监测制度,明确监测范围、内容和方法。
(2)医疗机构应配备专门的药品不良反应监测人员,负责收集、整理、报告药品不良反应信息。
(3)医疗机构应定期对医务人员进行药品不良反应知识培训,提高医务人员对药品不良反应的识别和报告能力。
2. 药品不良反应信息的收集(1)医务人员在诊疗过程中,应密切关注患者病情,发现可能与用药有关的不良反应,及时记录并报告。
(2)医疗机构应设立药品不良反应报告箱,鼓励患者及家属主动报告不良反应。
(3)医疗机构应建立药品不良反应信息管理系统,对收集到的信息进行整理、分析。
3. 药品不良反应报告(1)医务人员发现药品不良反应后,应填写《药品不良反应报告表》,内容包括患者基本情况、不良反应发生时间、临床表现、用药情况等。
(2)医疗机构药品不良反应监测人员对《药品不良反应报告表》进行审核,确保信息真实、准确、完整。
(3)医疗机构将审核后的《药品不良反应报告表》报送至所在地药品不良反应监测中心。
4. 药品不良反应评估(1)药品不良反应监测中心对收集到的药品不良反应信息进行评估,分析不良反应与药品的关系。
(2)对于严重、罕见或新的不良反应,药品不良反应监测中心应立即报告国家药品监督管理局。
(3)药品不良反应监测中心定期发布药品不良反应监测报告,为药品监管提供依据。
二、药害事件上报流程1. 药害事件的识别(1)医疗机构应建立药害事件监测制度,明确监测范围、内容和方法。
(2)医疗机构应设立药害事件报告箱,鼓励医务人员、患者及家属主动报告药害事件。
(3)医疗机构应定期对医务人员进行药害事件知识培训,提高识别和报告能力。
药店药品不良反应报告表填写范文英文回答:Adverse Drug Reaction Report Form.Name: [Your Name]Date: [Date of Report]Drug Name: [Name of Drug]Dosage: [Dosage of Drug]Frequency: [Frequency of Drug Administration]Description of Adverse Reaction:I am writing to report an adverse reaction that I experienced while taking the medication mentioned above. I started taking this drug two weeks ago to treat myallergies. However, after a few days of taking it, I began to experience severe dizziness and nausea. These symptoms persisted for several days and greatly affected my daily activities. I had to stop taking the medication immediately due to the intensity of the side effects.Impact on Daily Life:The adverse reaction I experienced had a significant impact on my daily life. I was unable to go to work for a few days as I was unable to drive or concentrate due to the dizziness. Additionally, the nausea made it difficult for me to eat or perform any physical activities. It was a challenging time for me as I had to rely on others for support and assistance.Actions Taken:As soon as I noticed the adverse reaction, I contacted my healthcare provider and informed them about my symptoms. They advised me to discontinue the medication and scheduled an appointment for further evaluation. I also filled outthis adverse drug reaction report form to ensure that my experience is documented and can contribute to the overall safety monitoring of this medication.Suggestions for Improvement:In order to prevent such adverse reactions in the future, I suggest that the pharmacy and healthcare providers provide more detailed information about the potential side effects of the medication. This would enable patients to make informed decisions and be aware of the possible risks associated with the drug. Additionally, it would be beneficial to have a helpline or support system in place for patients who experience adverse reactions, providing them with guidance and assistance during such situations.中文回答:药品不良反应报告表。
规范《药品不良反应/事件报告表》填报规范《药品不良反应/事件报告表》填报为进一步规范我省药品不良反应病例报告的书写,加强报告质量控制,保证报告的规范性、完整性和真实性,不断提高药品不良反应信息利用度。
现将《药品不良反应/事件报告表》规范化填报提出以下要求:一、基本要求国家中心在数据库中利用检索统计的方法对数据加以整理、分析和利用。
要求报表填写人员保证基础数据的精准,避免错误出现,才能使国家中心检索的宏观数据准确。
1、内容应客观真实、完整准确,避免错别字、缺漏项的出现;2、避免使用报告表中未规定的符号、代号和不通用的缩写形;3、每一个病人填写一张报告表;4、尽可能详细地填写报告表中所要求的项目。
有些内容确实无法获得时,可填写“不详”;5、省中心对不规范的电子报表采用在线直接退回,并提示报表中存在的问题,而上报机构收到退回的电子报表要认真对待,及时完善报表内容;二、适用对象:医疗卫生机构、药品生产企业、经营企业、监测机构及个人填报。
注意:用户注册时请注意填写正确的用户类别,注册时监测机构属于默认个人用户,只要在选择时勾选“个人”用户类别,即默认为监测机构。
三、退回报表中存在的比较集中的问题:1、报告单位填写:报告单位为上报报表的单位全称。
填写报告单位名称应统一、规范,务必做到经核实准确无误、一字不差,不可使用不规范简称,已在网上注册的填报单位必须与网报医院注册名称一致。
否则,可能造成检索时找不到单位或数量漏检的情况。
主要存在问题例如:“XX市第一人民医院”,如果简称“XX市第一医院”或“XX市一院”,系统会认为这是三家医疗机构,在检索统计时,按照所输入的名称分别统计报表数量。
2、部门、电话填写不良反应发生的科别,如内科、外科等;电话应填写相应的科室电话。
要求:各级监测机构集中填报表时,部门应填写不良反应发生的医院全称加上科别,如“XX 市第一人民医院内科”,电话填写相应的科室电话,并注意填写区号,无相应科室电话可填医院电话,保证报表的可追溯性。