最新九年级化学化学计算题常见题型及答题技巧及练习题(含答案)
- 格式:doc
- 大小:237.00 KB
- 文档页数:8

(化学)初三化学化学计算题常见题型及答题技巧及练习题(含答案)含解析一、中考化学计算题1.实验室欲测定一瓶标签破损的稀硫酸中溶质的质量分数,现取10g稀硫酸样品,将5%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化情况如图所示。
分析并计算:(1)a点溶液中含有的离子是_____。
(2)当pH=7时,消耗氢氧化钠溶液中NaOH质量为_____g。
(3)计算稀H2SO4中溶质的质量分数。
_____(4)计算恰好完全反应时所得溶液的溶质质量分数。
_____【答案】Na+、H+、SO42- 0.8 稀H2SO4的溶质质量分数是9.8%;恰好完全反应时所得溶液的溶质质量分数是5.5%。
【解析】【详解】(1)由图示可知,在a点时溶液的pH小于7,说明加入的NaOH完全反应,有剩余的硫酸,所以,溶液中含有的离子为:Na+、H+、SO42-;(2)由图示可知,在溶液的pH等于7,消耗的NaOH溶液的质量为16g,溶质的质量为:16g×5%=0.8g;(3)10g稀硫酸样品含有H2SO4的质量为x,生成的硫酸钠的质量为y2NaOH+H SO=Na SO+2H O2424280981420.8g x y解得:x=0.98g y=1.42g稀H2SO4的溶质质量分数为:×100%=9.8%;(4)恰好完全反应时所得溶液的溶质质量分数:×100%≈5.5%。
2.若要生产含杂质4%的生铁100t,需要含氧化铁60%的赤铁矿石的质量是多少________?(要求写出计算过程,计算结果保留小数点后1位)【答案】228.6t【解析】试题分析:含杂质物质的计算要把混合物的质量转化为纯物质的质量,即纯物质质量=含杂质物质质量×纯度,再把纯物质的质量带入化学方程式计算。
最后再把计算出的纯物质质量转换为含杂质物质的质量。
[解]设:需要向炼铁高炉中投入这种铁矿石的质量为xFe2O3+ 3CO2Fe + 3CO2160 11260%x (1-4%)×100 t=x=" 228.6" t答:需要向炼铁高炉中投入这种铁矿石的质量为228.6t。

初三化学化学计算题解题技巧及经典题型及练习题(含答案)及解析一、中考化学计算题1.取某碳酸钠样品放入烧杯中,加入95.8g 水充分溶解,再向其中加入稀硫酸,反应放出气体的总质量与所加入稀硫酸的质量关系曲线如下图所示,请根据题意解答问题:(1)当加入196g 稀硫酸时,放出气体的质量为___________g 。
(2)计算加入的稀硫酸溶液溶质的质量分数为____________。
(3)试通过计算求出加入98g 稀硫酸(即A 点)时烧杯中溶液溶质的质量分数。
(写出计算过程)_____________ 【答案】4.4 10% 7.1% 【解析】 【分析】 【详解】(1)从题中图像可知,当加入稀硫酸98g 时,生成的气体质量达到最大值4.4g ,此时碳酸钠和稀硫酸完全反应,因此继续加入稀硫酸至196g ,气体质量不会增加,因此反应中放出气体的质量为4.4g ;(2)因为加入稀硫酸98g 时,生成的气体质量达到最大值4.4g ,所以此时碳酸钠和稀硫酸完全反应。
设加入的98g 稀硫酸中溶质硫酸的质量为x ,恰好反应时生成的硫酸钠质量为y ,参加反应的碳酸钠的质量为z 。
23242422Na CO Na SO +H SO =++1069814244zxyH C gO O 4.4↑98x =44 4.4g解得x=9.8g稀硫酸中溶质的质量分数为:9.8g100%=10%98g⨯ 142y=44 4.4g解得y=14.2g106z=44 4.4g解得z=10.6g(3)加入98g稀硫酸溶液时的溶液为碳酸钠和稀硫酸恰好完全反应时的溶液,溶液中溶质的质量分数为:14.2g100%=7.1% 10.6g+95.8g+98g-4.4g答:稀硫酸的溶质质量分数为10%;A点时烧杯中溶液的溶质质量分数为7.1%。
2.某同学向一定质量的石灰石中加入7.3%的稀盐酸来制取二氧化碳,测得反应过程中溶液的pH与加入的稀盐酸的关系如图1所示。

【化学】九年级化学化学计算题及其解题技巧及练习题(含答案)一、中考化学计算题1.向13.6g碳酸钠和氯化钠的固体混合物滴加稀盐酸,所加稀盐酸质量与生成气体质量的关系如图所示。
计算:(1)固体混合物中碳酸钠的质量。
(2)该稀盐酸中溶质的质量分数。
(3)恰好完全反应时所得的溶液中溶质的质量分数。
(计算结果精确至0.1%)【答案】(1)10.6克(2)10%(3)17.9%【解析】试题分析:设固体混合物中Na2CO3的质量为x,稀盐酸中溶质的质量为y,反应生成NaCl 的质量为z。
Na2CO3+ 2HCl ="=" 2NaCl + H2O + CO2↑106 2×36.5 2×58.5 44x y z 4.4g得x=10.6克稀盐酸中溶质的质量分数为:恰好完全反应时所得的溶液溶质质量分数为:考点:根据化学方程式的计算物质的质量分数2.20g含杂质(杂质不溶于水,也不溶于酸)的锌样品,与一定质量的稀硫酸恰好完全反应,所得溶液质量为80.5g,同时生成氢气0.4g。
试计算:(1)样品中锌的质量分数是_____;(2)完全反应后生成溶液中溶质的质量分数是_____;(3)所用稀硫酸的质量分数是_____(计算结果保留到0.01%)。
【答案】65% 40% 28.87%【解析】【分析】样品中的锌能与稀硫酸反应生成硫酸锌和氢气。
【详解】设样品中锌的质量为x;生成的硫酸锌的质量为y;硫酸中溶质的质量为z;2442Zn+H SO=ZnSO+H65981612x z y0.4g↑65981612===x z y0.4gx=13gy=32.2gz=19.6g(1)样品中锌的质量分数为13g×100%=65% 20g(2)完全反应后生成溶液中溶质的质量分数为32.2g×100%=40% 80.5g(3)所用稀硫酸的质量分数为19.6g×100%28.87% 80.5g+0.4g-13g≈答:样品中锌的质量分数为65%,完全反应后生成溶液中溶质的质量分数为40%,所用稀硫酸的质量分数为28.87%。

九年级化学化学计算题解题技巧及经典题型及练习题(含答案)一、中考化学计算题1.下图所示为实验室中常见的气体制备、干燥、收集和性质实验的部分仪器。
试根据题目要求,回答下列问题:⑴请写出能用装置A制备的一种气体的化学反应方程式_____,该气体可选用装置_____来收集(填装置序号),其选择依据是_____。
⑵小颖同学欲用干燥..、纯净..的一氧化碳气体还原某氧化铜样品(杂质只有铜),并测定其纯度。
(查阅资料)将草酸(H2C2O4)晶体与浓硫酸混合加热,会产生一氧化碳等气体,其反应原理为:H2C2O4浓硫酸CO↑+CO2↑+H2O。
①若小颖同学选用草酸来制取CO,其发生装置她应选择_____(填装置序号)。
(定量实验)②小颖同学先用电子秤称取了1.00g氧化铜样品,放入装置C中的玻璃管内并组装好所有相关仪器,再将草酸分解得到的气体产物按照以下仪器的连接顺序进行实验:混合气体→D→C→E→H,最后,通过测量反应前后装置E的质量变化进行计算。
(已知:CO+CuO ΔCu+CO2)实验过程中,在装置C的大玻璃管内可观察到的现象是_____。
③请你分析上述实验方案存在的不足之处及.对应的改进方法_____。
④实验改进后,小颖同学对实验所得的正确数据进行分析处理(设所发生的反应均完全进行):通过测定,当装置C中的氧化铜全部被还原后,装置E的质量增加了0.33g,则该样品中氧化铜的质量分数为_____(结果精确至0.1%)。
⑤小黄同学提出了异议,他认为若②中实验方案不加以改进,也能正确测算出该样品中氧化铜的纯度,他的计算依据或方法为:_____。
【答案】CaCO3 + 2HCl == CaCl2 + H2O + CO2↑ F 二氧化碳密度比空气大 B 黑色固体变成红色应该装置D前连接装置一个装置E,吸收混合气体中的二氧化碳 60.0% 根据H2C2O4浓硫酸CO↑+CO2↑+H2O,生成的一氧化碳和二氧化碳的分子个数比为1:1的关系,装置E增加的质量的一半就是氧化铜和一氧化碳反应生成的二氧化碳的质量,再根据步骤④的计算方法计算出氧化铜的质量即可 【解析】 【分析】 【详解】⑴装置A 为固液不加热型,可用于实验室制取二氧化碳,化学反应方程式为:CaCO 3 + 2HCl = CaCl 2 + H 2O + CO 2↑;该气体可选用装置F 来收集,选择依据是二氧化碳密度比空气大。

(化学)九年级化学化学计算题解题技巧分析及练习题(含答案)一、中考化学计算题1.兴趣小组的同学为了测定某铜锌合金中锌的质量分数,小明同学利用该合金与稀硫酸反应,进行了三次实验,所得相关的实验数据记录如下(实验中的误差忽略不计)①上表数据分折,第_____次中的锌与稀硫酸中的硫酸恰好完全反应 ②试计算该铜锌合金中锌的质量分数为_____③恰好完全反应后所得溶液中溶质的质量分数____(保留0.1%) 【答案】二 52% 28.6% 【解析】 【分析】锌和稀硫酸反应生成硫酸锌和氢气。
【详解】①从上表数据分析,25g 合金需要酸的质量是100g ,100g 酸需要合金的质量是25g ,故第二次恰好完全反应。
生成氢气的质量为25g+100g 124.6g 0.4g ﹣= 设锌的质量为x ,生成硫酸锌的质量为y2442Zn H SO ZnSO +=+65H 16x12y 0.4g↑651612==x y 0.4gx 13gy 32.2g==②该铜锌合金中锌的质量分数为10130%g25g52%⨯=。
③恰好完全反应后所得溶液中溶质的质量分数为:32.2g124.6g-(25g-100%13g)28.6%⨯=答:上表数据分折,第二次中的锌与稀硫酸中的硫酸恰好完全反应,试计算该铜锌合金中锌的质量分数为52%,恰好完全反应后所得溶液中溶质的质量分数28.6%。
【点睛】=100% 溶质质量溶质质量分数溶液质量2.某石化厂有一种石油产品含有质量分数为4.9%的残余硫酸,过去他们都是用NaOH 溶液来清洗这些硫酸。
请计算:(1)若要清洗1000kg 的这种石油产品,需要______kg 的NaOH 。
(2)该石化厂进行了技术改造,采用Ca (OH )2中和这些残余硫酸。
每处理1000kg 这种产品,可以节约多少经费?已知工业级的NaOH 和Ca (OH )2的最新市场批发价如下表: 试剂 Ca (OH )2 NaOH 价格(元/kg )1.006.00(3)请画出用氢氧化钠和氢氧化钙处理1000kg 该石油产品时,残余硫酸溶质的质量变化曲线;氢氧化钠用虚线表示,氢氧化钙用实线表示。

最新九年级化学化学计算题答题技巧及练习题(含答案)一、中考化学计算题1.某化学兴趣小组的同学在实验室配制溶质质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数。
下图表示用该氢氧化钠溶液与10g某稀盐酸发生反应时溶液温度的变化情况。
试计算稀盐酸中溶质的质量分数。
【答案】14.6%【解析】试题分析:由于中和反应放热,故随着反应的进行,溶液的温度逐渐升高,直至反应恰好完全,溶液温度达到最高,故根据图示可判断,当加入氢氧化钠那溶液的质量为20g时,反应恰好完全解:分析图知与10g稀盐酸恰好完全反应的氢氧化钠质量为:20g×8%=1.6g设稀盐酸中溶质的质量为xNaOH+HCl=NaCl+H2O40 36.51.6g x40:1.6g=36.5:xx=1.46g稀盐酸中溶质的质量分数为:1.46g/10g=14.6%答:稀盐酸中溶质的质量分数为14.6%考点:根据化学方程式计算2.为测定某样品中锌的质量分数,取10g此样品,分五次向其中加入稀硫酸使之充分反应(假设锌的样品中杂质不与稀硫酸反应,且不溶于水),每次加入的稀硫酸质量及测定剩余固体的质量,记录数据如下表:第一次第二次第三次第四次第五次加入稀硫酸的质量/g1010101010剩余固体质量/g8.4 6.8 5.2 3.6 3.6请认真分析表中的数据,回答下列问题:(1)表示样品与稀硫酸恰好完全反应的是上表中第________次操作;(2)计算样品中锌的质量分数;(3)计算实验中所用稀硫酸的溶质质量分数。
【答案】(1)4(2)锌的质量分数(3)设恰好完全反应时消耗硫酸的质量为x【解析】本题考查的是实验数据处理的探究和根据化学反应方程式的计算。
(1)根据金属活动性,锌在活动性顺序中处于H之前,能与稀硫酸反应,而锌的样品中杂质不与稀硫酸反应,且不溶于水。
由记录数据表可知:第五次加入10g稀硫酸时,剩余固体质量不变仍为3.6g,说明混合物中的锌在第四次加酸后就已完全反应,剩余固体为不与硫酸反应的杂质。

【化学】九年级化学化学计算题解题技巧分析及练习题(含答案)含解析一、中考化学计算题1.向13.6g碳酸钠和氯化钠的固体混合物滴加稀盐酸,所加稀盐酸质量与生成气体质量的关系如图所示。
计算:(1)固体混合物中碳酸钠的质量。
(2)该稀盐酸中溶质的质量分数。
(3)恰好完全反应时所得的溶液中溶质的质量分数。
(计算结果精确至0.1%)【答案】(1)10.6克(2)10%(3)17.9%【解析】试题分析:设固体混合物中Na2CO3的质量为x,稀盐酸中溶质的质量为y,反应生成NaCl 的质量为z。
Na2CO3+ 2HCl ="=" 2NaCl + H2O + CO2↑106 2×36.5 2×58.5 44x y z 4.4g得x=10.6克稀盐酸中溶质的质量分数为:恰好完全反应时所得的溶液溶质质量分数为:考点:根据化学方程式的计算物质的质量分数2.某校化学兴趣小组为了测定某一碳酸钠样品中碳酸钠的质量分数,进行如下实验,取13.25g碳酸钠样品(杂质既不溶于酸也不溶于水)放入烧杯中,加入95.8g水使其完全溶解,再向其中加入稀盐酸,测得反应放出气体的总质量与所加入稀盐酸的质量关系曲线如图所示,请回答:(1)当加入212g稀盐酸时,放出气体的质量为_____g。
(2)碳酸钠样品中碳酸钠的质量分数为多少?_____(写出计算过程)(3)加入106g稀盐酸(即A点)时烧杯中溶液的溶质质量分数为多少?_____(写出计算过程)【答案】4.4g 80% 5.6%【解析】【分析】【详解】(1)根据图像,可以看出当加入106g稀盐酸的时候,反应就结束,产生气体质量为4.4g,所以当加入212g稀盐酸时,放出气体的质量仍然为4.4g(2)发生反应:Na2CO3+2HCl=2NaCl+H2O+CO2↑,根据方程式中碳酸钠与二氧化碳的质量关系可算出碳酸钠的质量,进而可以计算碳酸钠样品中碳酸钠的质量分数,反应后得到的是NaCl溶液,所以也可根据方程式中NaCl与二氧化碳的质量关系,求出溶液中溶质的质量解:设碳酸钠的质量为x,生成的NaCl质量为y。

九年级化学化学计算题常见题型及答题技巧及练习题(含答案)一、中考化学计算题1.将含有NaCl杂质的某烧碱样品10 g完全溶于90 g水中,再向所得溶液中慢慢滴入溶质质量分数为7.3%的稀盐酸。
在实验过程中,溶液的pH与滴入稀盐酸的质量关系如图所示。
(1)求10 g该样品中氢氧化钠的质量。
(2)求a点时,溶液中溶质的质量分数(计算结果精确到0.1%)。
【答案】(1)8 g (2)6.9%【解析】当恰好完全反应时消耗的盐酸溶液的质量为100g,对应的HCl的质量为100g×7.3%=7.3g设氢氧化钠的质量为x,生成的氯化钠的质量为yNaOH+HCl═NaCl+H2O40 36.5 58.5x 7.3g y==x=8gy=11.7ga点时,溶液中溶质的质量分数为×100%≈6.9%答:(1)l0g该样品中氢氧化钠的质量为8g.(2)a点时,溶液中溶质的质量分数约为6.9%2.我国化工专家侯德榜的“侯氏制碱法”为世界制碱工业做出了突出的贡献,工业上用侯氏制碱法制得的纯碱中含有一定量的氯化钠杂质。
现称取只含氯化钠杂质的纯碱样品11g,全部溶解在50g水中,当加入稀盐酸64.4g时,恰好完全反应,所得溶液的质量为121g。
试求:(1)该纯碱样品的纯度_________________。
(2)所得溶液中溶质的质量分数_________。
【答案】96.4% l0%【解析】【分析】纯碱中碳酸钠与稀盐酸反应放出二氧化碳,根据质量守恒定律,利用反应前后物质总质量差即反应放出二氧化碳的质量;根据反应的化学方程式,计算出纯碱中碳酸钠的质量和反应后溶液中溶质氯化钠的质量。
【详解】反应放出的CO2的质量为:64.4g+50g+11g-121g=4.4g设参加反应的Na2CO3质量为x,生成NaCl的质量为yNa2CO3+2HCl=2NaCl+H2O+CO2↑106 117 44x y 4.4g10611744==x y 4.4g解之得 x=10.6g,y=11.7g(1)碳酸钠纯度=10.6g100%11g≈96.4%;(2)纯碱样品中NaCl的质量=11g-10.6g=0.4g反应后溶液中NaCl的质量为=11.7g+0.4g=12.1g反应后溶液中NaCl的质量分数=12.1g121g×100%=10%答:(1)该纯碱样品的纯度约为96.4%;(2)所得溶液中溶质的质量分数为10%。
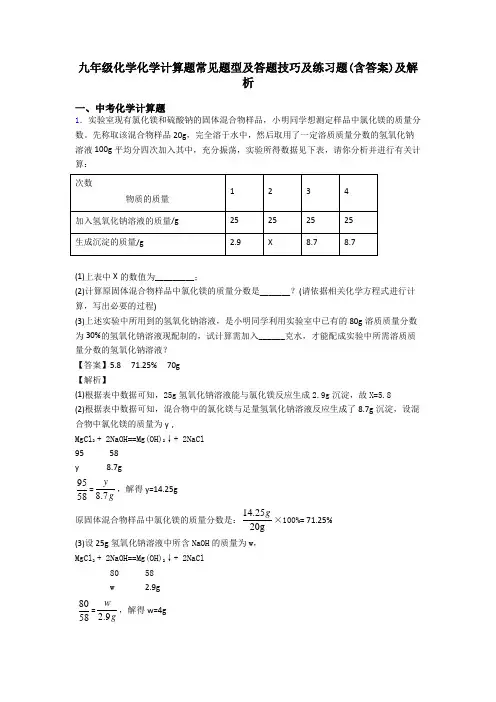
九年级化学化学计算题常见题型及答题技巧及练习题(含答案)及解析一、中考化学计算题1.实验室现有氯化镁和硫酸钠的固体混合物样品,小明同学想测定样品中氯化镁的质量分数。
先称取该混合物样品20g,完全溶于水中,然后取用了一定溶质质量分数的氢氧化钠溶液100g平均分四次加入其中,充分振荡,实验所得数据见下表,请你分析并进行有关计算:(1)上表中X的数值为_________;(2)计算原固体混合物样品中氯化镁的质量分数是_______?(请依据相关化学方程式进行计算,写出必要的过程)(3)上述实验中所用到的氢氧化钠溶液,是小明同学利用实验室中已有的80g溶质质量分数为30%的氢氧化钠溶液现配制的,试计算需加入______克水,才能配成实验中所需溶质质量分数的氢氧化钠溶液?【答案】5.8 71.25% 70g【解析】(1)根据表中数据可知,25g氢氧化钠溶液能与氯化镁反应生成2.9g沉淀,故X=5.8(2)根据表中数据可知,混合物中的氯化镁与足量氢氧化钠溶液反应生成了8.7g沉淀,设混合物中氯化镁的质量为y,MgCl2 + 2NaOH==Mg(OH)2↓+ 2NaCl95 58y 8.7g95 58=8.7yg,解得y=14.25g原固体混合物样品中氯化镁的质量分数是:14.2520gg×100%= 71.25%(3)设25g氢氧化钠溶液中所含NaOH的质量为w,MgCl2 + 2NaOH==Mg(OH)2↓+ 2NaCl80 58w 2.9g80 58=2.9wg,解得w=4g所用氢氧化钠溶液的溶质质量分数为:425gg×100%=16%稀释溶液前后,溶质的质量相等,设将80g溶质质量分数为30%的氢氧化钠溶液稀释为16%的溶液时,需要加水的质量是z,则80g×30%=(80g+z)×16%,解得z=70g点睛:根据化学方程式的计算,关键是找出相关物质的质量关系,利用反应中物质的质量比不变进行列比例式计算,易错点是,由质量比算数错误,所以这一步一定要仔细检查。
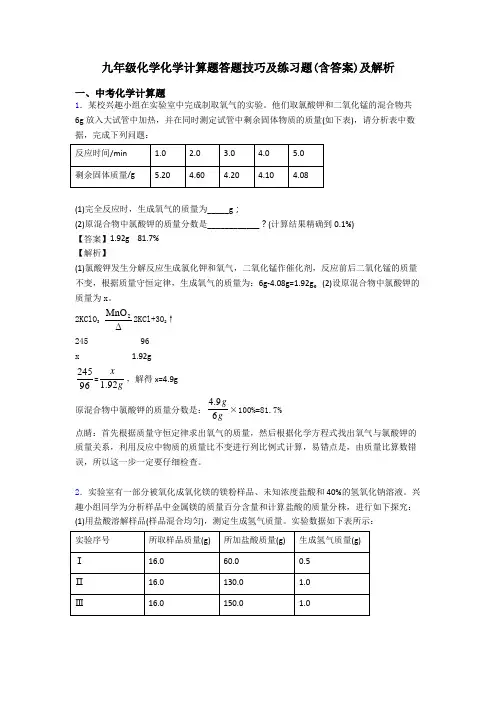
九年级化学化学计算题答题技巧及练习题(含答案)及解析一、中考化学计算题1.某校兴趣小组在实验室中完成制取氧气的实验。
他们取氯酸钾和二氧化锰的混合物共6g 放入大试管中加热,并在同时测定试管中剩余固体物质的质量(如下表),请分析表中数据,完成下列问题:(1)完全反应时,生成氧气的质量为_____g ;(2)原混合物中氯酸钾的质量分数是____________?(计算结果精确到0.1%) 【答案】1.92g 81.7% 【解析】(1)氯酸钾发生分解反应生成氯化钾和氧气,二氧化锰作催化剂,反应前后二氧化锰的质量不变,根据质量守恒定律,生成氧气的质量为:6g-4.08g=1.92g 。
(2)设原混合物中氯酸钾的质量为x 。
2KClO 32MnO Δ2KCl+3O 2↑ 245 96 x 1.92g24596=1.92x g,解得x=4.9g 原混合物中氯酸钾的质量分数是:4.96gg×100%=81.7%点睛:首先根据质量守恒定律求出氧气的质量,然后根据化学方程式找出氧气与氯酸钾的质量关系,利用反应中物质的质量比不变进行列比例式计算,易错点是,由质量比算数错误,所以这一步一定要仔细检查。
2.实验室有一部分被氧化成氧化镁的镁粉样品、未知浓度盐酸和40%的氢氧化钠溶液。
兴趣小组同学为分析样品中金属镁的质量百分含量和计算盐酸的质量分株,进行如下探究: (1)用盐酸溶解样品(样品混合均匀),测定生成氢气质量。
实验数据如下表所示:镁粉样品中金属镁的质量百分含量为_________________。
(2)向实验Ⅲ后的溶液中加入40%的氢氧化钠溶液,生成沉淀的质量随加入氢氧化钠溶液质量的变化关系如图所示。
计算盐酸的质量分数为_______________。
(写出计算过程)【答案】75% 36.5% 【解析】 【详解】(1)对比第Ⅱ、Ⅲ组中发现,对比第Ⅲ组中所加盐酸质量由130g 增加到150g 时,氢气的质量没有增加,说明第Ⅲ组中镁完全反应, 设样品中金属镁的质量为x ,22Mg+2HCl =MgCl +H 242x 1.0g 242=x 1.0g↑x=12.0g样品中金属镁的质量百分含量为:12.0g100%=75%16.0g⨯。

(化学)九年级化学化学计算题常见题型及答题技巧及练习题(含答案)含解析一、中考化学计算题1.为测定某H2SO4溶液的溶质质量分数,现取200g硫酸溶液置于烧杯中,不断加入一定质量分数的BaCl2溶液,反应过程中杯中溶液的质量与加入BaCl2溶液的质量关系如图所示。
请回答:(1)反应生成沉淀的质量为_____g;在Q点时溶液中的离子为_____(用符号)。
(2)在反应过程中,杯中溶液的pH_____(填“变大”、“不变”或“变小”)。
(3)原硫酸溶液的溶质质量分数是多少_____?【答案】23.3 H+、Cl﹣、Ba2+变大 4.9%【解析】【详解】(1)由图中信息可知,P点时氯化钡和硫酸恰好完全反应,反应前后的质量差即为反应生成沉淀硫酸钡的质量,则生成的硫酸钡的质量是200g+100g﹣276.7g=23.3g,故填23.3;Q点的氯化钡溶液过量,溶液中的溶质为盐酸和氯化钡,在Q点时溶液中的离子为H+、Cl ﹣、Ba2+,故填H+、Cl﹣、Ba2+;(2)反应的过程中硫酸不断被消耗,生成盐酸,随氯化钡溶液的加入,溶剂增加,溶液的酸性不断变弱,所以pH会不断变大,故填变大;(3)设氯化钡质量为x。
2244BaCl+H SO=BaSO+2HCl98233x23.3g98233=x23.3gx=9.8g原硫酸溶液的溶质质量分数为:9.8g200g×100%=4.9%答:硫酸溶液的溶质质量分数为4.9%。
2.小明称取用侯氏制碱法制得的纯碱样品(杂质仅为氯化钠)12.4g,加入到100g溶质质量分数为7.3%的稀盐酸中,恰好完全反应。
求所得溶液的溶质质量分数为__________。
【答案】12.5%【解析】 【详解】由题意得:100g 溶质质量分数为7.3%的稀盐酸中氯化钠的质量为100g ×7.3%=7.3g 。
设参加反应的Na 2CO 3质量为x ,生成的NaCl 的质量为y ,生成二氧化碳的质量为z 。
【化学】九年级化学化学计算题常见题型及答题技巧及练习题(含答案)一、中考化学计算题1.若要生产含杂质4%的生铁100t,需要含氧化铁60%的赤铁矿石的质量是多少________?(要求写出计算过程,计算结果保留小数点后1位)【答案】228.6t【解析】试题分析:含杂质物质的计算要把混合物的质量转化为纯物质的质量,即纯物质质量=含杂质物质质量×纯度,再把纯物质的质量带入化学方程式计算。
最后再把计算出的纯物质质量转换为含杂质物质的质量。
[解]设:需要向炼铁高炉中投入这种铁矿石的质量为xFe2O3+ 3CO2Fe + 3CO2160 11260%x (1-4%)×100 t=x=" 228.6" t答:需要向炼铁高炉中投入这种铁矿石的质量为228.6t。
考点:含杂质的物质利用化学方程式的计算2.阿司匹林(分子式为C9H8O4)是一种常用解热镇痛药,用于治疗感冒、发烧、头痛等疾病。
某阿司匹林肠溶片说明书的部分内容如图所示。
(1)阿斯匹林的相对分子质量是_____,其中氢、氧元素的质量比是_____。
(2)阿斯匹林中碳元素的质量分数_____;25mg阿斯匹林中含碳元素的质量_____;(3)治疗不稳定性心绞痛时,病人每天服用阿斯匹林肠溶片的最大量是_____片。
【答案】180 1:8 60% 15mg 12【解析】(1)根据相对分子质量为构成分子的各原子的相对原子质量之和、化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答;(2)根据化合物中元素的质量分数=⨯相对原子质量原子个数相对分子质量×100%,化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答;(3)不稳定性心绞痛时,每天阿斯匹林的剂量为75~300mg,据此进行分析解答。
解:(1)阿斯匹林的相对分子质量为12×9+1×8+16×4=180;其中氢、氧元素的质量比为(1×8):(16×4)=1:8。
(化学)初三化学化学计算题常见题型及答题技巧及练习题(含答案)含解析一、中考化学计算题1.为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品10g,向其中逐滴加入9.8%的稀硫酸至刚好不再产生气体为止。
反应过程中生成的气体与所用硫酸溶液的质量关系如图所示。
试计算:(1)样品中铜的质量分数;(2)反应所消耗的硫酸溶液质量;(3)反应后所得溶液质量。
【答案】(1)67.5%;(2)50g;(3)53.15g【解析】根据锌与硫酸反应的化学方程式,由图中最多生成的氢气质量0.10g,可以计算出:(1)参加反应的锌的质量,进而计算出样品中铜的质量分数;(2)参加反应的硫酸的质量,进而计算出硫酸溶液的质量;(3)生成硫酸锌的质量,进而计算出所得硫酸锌溶液的溶质质量分数。
解:设样品中铜的质量分数为x,消耗硫酸溶液的质量为y 。
Zn + H2SO4 = ZnSO4 + H2↑65 98 210g(1-x) y×9.8% 0.10g(1)652=101-x0.10gg()⨯,x=67.5%(2)982=9.800.10yg⨯,y=50g(3)所得溶液的质量为:50g+10g×(1-67.5%)-0.10g=53.15g答:(1)样品中铜的质量分数为67.5%;(2)消耗硫酸溶液的质量为50g;(3)所得溶液的溶质质量分数为53.15g。
2.将碳酸钠与氯化钠的固体混合物14.4g与一定质量的盐酸恰好完全反应生成4.4g二氧化碳,反应后所得溶液质量为60g。
求:⑴所得溶液中氯化钠的质量;⑵反应前盐酸中溶质的质量分数。
【答案】(1)15.5g;(2)14.6%【解析】【详解】设所得反应生成氯化钠的质量为x,样品中碳酸钠的质量为y,反应前盐酸中溶质的质量为z。
x=11.7g y=10.6g z=7.3g(1)所得溶液中氯化钠的质量11.7g+14.4g-10.6g=15.5g。
(2)反应前盐酸溶液的质量为:60g-14.4g+4.4g=50g,所以,反应前盐酸中溶质的质量分数为。
初三化学化学计算题常见题型及答题技巧及练习题(含答案)一、中考化学计算题1.BaCl 2是一种重金属盐,其水溶液具有很强的毒性。
若误服了BaCl 2溶液可立即服用MgSO 4溶液解毒。
为测定某BaCl 2溶液的溶质质量分数,现取100克BaCl 2溶液,不断加入MgSO 4溶液,反应过程中溶液总质量与加入MgSO 4溶液的质量关系如图所示,请回答:(1)P 点时溶液中的溶质名称是_________________; (2)反应生成沉淀的最大质量为_________________克;(3)试计算原溶液中BaCl 2溶液的溶质质量分数为_________________。
【答案】MgCl 2 23.3g 20.8% 【解析】 【分析】 【详解】(1)当硫酸镁溶液的质量加到100g 时,溶液总质量出现拐点,此后随着硫酸镁溶液的增加,溶液总质量增加,不再产生新的变化。
故P 点时硫酸镁溶液与氯化钡溶液恰好完全反应生成硫酸钡沉淀和氯化镁。
因此P 点时溶液中的溶质名称是氯化镁; (2)由图可知,反应生成沉淀的最大质量为100g+100g-176.7g=23.3g ; (3)设原BaCl 2溶液的溶质质量分数为x2442BaCl +MgSO =BaSO +MgCl 208233100g x23.3g↓⨯ 208233=100g x 23.3g⨯x=20.8%答:原BaCl 2溶液的溶质质量分数为20.8%。
2.我国化工专家侯德榜发明了侯氏制碱法,为世界制碱工业作出了突出贡献。
(1)主产品Na 2CO 3的俗名是_____,副产品氯化铵中阳离子符号为_____。
(2)在实际生产中,产品Na 2CO 3中常混有少量的NaCl ,现有样品11.0g ,将其放入干净的烧杯中,向烧杯中逐滴加入溶质质量分数为7.3%的稀盐酸,反应后烧杯中物质的质量与滴入稀盐酸的质量关系如图所示。
①图中A点表示_____,B点的溶质为_____。
【化学】九年级化学化学计算题答题技巧及练习题(含答案)含解析一、中考化学计算题1.取CaCl2和CaCO3的混合物12.5g于烧杯中,向其中滴加一定溶质质量分数的稀盐酸,请加稀盐酸的质量与产生气体质量的关系如图所示。
求:(1)混合物CaCO3中的质量为_______;(2)稀盐酸中的溶质质量分数为________;(3)恰好完全反应时,所得不饱和溶液中溶质的质量分数为________?(写出计算过程,计算结果精确到0.1%)【答案】10g7.3%12.6%【解析】试题分析:盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,由图可知:二氧化碳的质量为4.4g设碳酸钙的质量为x,稀盐酸中的溶质质量为z,生成氯化钙的质量为y。
CaCO3+2HCl=CaCl2+H2O+CO2↑100 73 111 44x z y 4.4gx=10g z=7.3g y=11.1g(1)混合物CaCO3中的质量为10g;(2)稀盐酸中的溶质质量分数为100%=7.3%;(3)恰好完全反应时,所得不饱和溶液中溶质的质量分数=100%≈12.6%。
考点:根据化学反应方程式的计算;有关溶质质量分数的简单计算2.现有l00g 8%的NaOH溶液,通过计算回答下列有关问题:(1)若用该溶液吸收CO2,最多可以生成Na2CO3多少克?____(写出详细计算过程)(2)当NaOH全部转化成为Na2CO3后,Na2CO3还会继续与CO2、H2O发生反应:Na2CO3+CO2+H2O=2NaHCO3,直至Na2CO3完全反应完。
请在如图画出利用l00g8%的NaOH 溶液吸收CO2与生成NaHCO3的曲线。
____(3)现有三种溶液:①100g8%NaOH溶液、②100g8%NaOH溶液吸收CO2转化为Na2CO3溶液、③100g8%NaOH溶液吸收过量CO2转化为NaHCO3溶液,分别用相同质量分数的硫酸与上述三种溶液恰好完全反应,需要的硫酸的质量_____(选填“相等”或“不相等”),原因是_____。
(化学)九年级化学化学计算题常见题型及答题技巧及练习题(含答案)一、中考化学计算题1.氧化亚铜(Cu 2O )可用于生产船底防污漆,防止海生物对船舶设备的污损。
现将Cu 2O 和Cu 的固体混合物20g 放入烧杯中,加入质量分数为24.5%的稀硫酸50g ,恰好完全反应。
已知:Cu 2O+H 2SO 4═CuSO 4+Cu+H 2O .计算:(1)所加稀硫酸中溶质的质量为_____g 。
(2)原混合物中Cu 2O 与Cu 的质量比_____(写出计算过程,结果用最简整数比表示) (3)在图中画出向20g Cu 2O 和Cu 的固体混合物中逐滴加入24.5%的稀硫酸至过量,铜的质量变化曲线_____。
【答案】12.25 9: 1 。
【解析】【分析】根据加入的硫酸中溶质的质量和对应的化学方程式求算氧化亚铜的质量,进而求算对应的比值以及画图。
【详解】(1)所加稀硫酸中溶质的质量为24.5%×50g =12.25g ;故填:12.25(2)设原混合物中Cu 2O 的质量为x ,生成的铜的质量为y 。
224421449864x 12.Cu O+H SO CuSO +C 2u +H 5O g y═ 1449864==x 12.25g y解得:x =18 g ;y =8g ; 原混合物中Cu 2O 与Cu 的质量比为18 g :(20 g ﹣18 g )=9:1;故填:9:1(3)没加入硫酸时,铜的质量为2g ,加入到50g 稀硫酸时铜的质量为2g+8g =10g 。
如下图所示;故填:【点睛】根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整。
2.取24g氢氧化钠和碳酸钠的固体混合物,加136g水完全溶解后,再缓慢加入石灰乳(氢氧化钙和水的混合物)至恰好完全反应,过滤得到4g沉淀和10%的氢氧化钠溶液.试计算反应中应加入石灰乳的质量是______________?【答案】73.6g【解析】【详解】设:24g样品中碳酸钠的质量为x,生成的氢氧化钠的质量为yCa(OH)2 + Na2CO3=CaCO3 + 2NaOH106 100 80x 4g yx= 4.24 g y = 3.2 g .得到的10%NaOH溶液的质量为(24 g – 4.24 g + 3.2 g) ÷10% = 229.6 g加入石灰乳的质量为 229.6 g + 4 g - 136 g -24 g = 73.6 g答:应加入石灰乳的质量是73.6 g。
最新九年级化学化学计算题常见题型及答题技巧及练习题(含答案)一、中考化学计算题1.某化学兴趣小组为了测定某黄铜(铜、锌合金)样品中锌的质量分数,取10克样品放入烧杯中,再取60克稀硫酸分六次加入烧杯中,均充分反应,实验数据如下:第一次第二次第三次第四次第五次第六次101010101010加入稀硫酸的质量(g)剩余固体的质量(g)9.358.78.057.4 6.75 6.75(1)黄铜样品中锌的质量分数为多少?(写出计算步骤,下同)(2)所用稀硫酸的质量分数为多少?【答案】(1)32.5%;(2)9.8%【解析】质量分数的一种常用的计算方法是分别计算出目的物质的质量和样品的总质量,然后求比值。
第(2)问中的化学反应方程式以及计算是关键。
(1)10g样品反应完全后,剩下6.75g为铜的质量,所以锌的质量为所以样品中锌的质量分数为(2)设在第二次加入稀硫酸后,参加反应硫酸的质量为x,据表中数据知,参加反应的锌的质量为根据反应方程式65 980.65g x有,解得所用稀硫酸的质量分数为2.为测定某一样品中含杂质的含量,并配制一定溶质质量分数的氯化镁溶液。
进行如下实验:把100g的稀盐酸加入到20g含杂质的MgCO3和MgCl2的样品粉末中(杂质即不溶于水,也不和盐酸反应),完全反应后得到中性溶液,其操作过程如图。
回答下列问题:(1)写出发生反应的化学方程___;(2)求解混合物中发生反应物质的质量(X)的比例式为___; (3)样品中杂质的含量为___; (4)所得溶液中溶质的质量分数为___;(5)用36.5%的浓盐酸配制100g 上述稀盐酸时,需要此浓盐酸的质量为___。
【答案】MgCO 3+2HCl ═MgCl 2+H 2O+CO 2↑ 84x =44 4.4g10.5%; 9.5% 20g 【解析】 【分析】碳酸镁和盐酸反应生成氯化镁和水以及二氧化碳。
【详解】根据质量守恒定律可得,生成的二氧化碳的质量为20g+100g 115.6g 4.4g ﹣= 设碳酸镁的质量为X ,HCl 的质量为y ,生成的氯化镁的质量为z3222MgCO 2HCl MgCl H O +=++CO 847395 44xgyz4.4↑84739544===x y z 4.4gx 8.4gy 7.3g z 9.5g=== 样品中杂质的含量为2.1g100%=10.5%20g⨯ 所得溶液中溶质的质量分数为20g-2.1g-8.4g+9.5g100%=9.5%20g-2.1g+100g-4.4g+86.5g⨯用36.5%的浓盐酸配制100g 上述稀盐酸时,需要此浓盐酸的质量为7.3g=20g 36.5%3.某混合溶液中含有硫酸和盐酸,取该混合溶液20g 于烧杯中,不断滴加溶质质量分数为17.1%的氢氧化钡溶液,反应过程中烧杯中产生沉淀的质量、溶液pH 的变化如图所示(BaCl 2溶液呈中性)。
求:(1)完全反应后生成沉淀的质量;_____(精确到0.01g ,下同)(此步写出计算过程) (2)20g 混合溶液中HCl 的质量为_____g 。
【答案】4.66g 2.92 【解析】 【分析】(1)该混合酸中只有硫酸与氢氧化钡反应产生沉淀,且由图可知,当两者恰好反应完时,消耗氢氧化钡溶液质量为20g ,据此原理进行解答;(2)当pH=7时,硫酸和盐酸被反应完了,此时滴加的氢氧化钡溶液质量为消耗两种酸所用溶液质量,据此原理进行解答 【详解】(1)解:设生成沉淀的质量为xH 2SO 4+Ba(OH)2=H 2O+BaSO 4↓ 171 233 20g ⅹ17.1% x17123320g 17.1%x=⨯x=4.66g答:生成沉淀的质量为4.66g(2)解:设20g 混合溶液中HCl 的质量为y 2HCl+Ba(OH)2=BaCl 2+H 2O 73 171y ( 60g-20g)ⅹ17.1%73171y 40g 17.1%=⨯ y=2.92g答:20g 混合溶液中HCl 的质量为2.92g 【点睛】该题为图像计算,解题关键是分清那种酸和氢氧化钡反应产生沉淀,pH=7时两种酸都消耗完。
4.将碳酸钠与氯化钠的固体混合物14.4g 与一定质量的盐酸恰好完全反应生成4.4g 二氧化碳,反应后所得溶液质量为60g 。
求:⑴所得溶液中氯化钠的质量;⑵反应前盐酸中溶质的质量分数。
【答案】(1)15.5g;(2)14.6%【解析】【详解】设所得反应生成氯化钠的质量为x,样品中碳酸钠的质量为y,反应前盐酸中溶质的质量为z。
x=11.7g y=10.6g z=7.3g(1)所得溶液中氯化钠的质量11.7g+14.4g-10.6g=15.5g。
(2)反应前盐酸溶液的质量为:60g-14.4g+4.4g=50g,所以,反应前盐酸中溶质的质量分数为。
5.在我国青海湖地区有一种说法,冬天捞碱,夏天晒盐。
这里的碱是指Na2CO3,盐是指NaCl。
人们从盐湖中捞得的碱会含有少量的NaCl。
某研究性学习小组称取含NaCl的Na2CO3固体25.0g,将其配制成溶液,再向其中逐滴加入足量的溶质质量分数为7.3%的稀盐酸,使气体完全放出,共收集到8.8gCO2气体。
试计算:(1)原固体中Na2CO3的质量分数________。
(2)反应中消耗盐酸的总质量______。
【答案】(1)84.8%.(2)200g.【解析】解:(1)设碳酸钠的质量为x,盐酸溶液中溶质的质量为yNa2CO3+2HCl=2NaCl+H2O+CO2↑106 73 44x y 8.8gx=21.2g,y=14.6g所以原固体中碳酸钠的质量分数为 ×100% =84.8%(2)反应中消耗盐酸的总质量为: =200g答:(1)原固体中Na2CO3的质量分数为84.8%;(2)反应中消耗盐酸总质量为200g。
6.实验室有化学实验考试后留下混有少量食盐的小苏打( NaHCO3)样品。
现称取样品10克,加入某溶质质量分数的稀盐酸90克,至充分反应不再有气泡产生为止,称得剩余溶液质量为96.04克。
求:(1)生成气体的质量;(2)样品中 NaHCO3的质量分数。
【答案】3.96g;75.6%。
【解析】【详解】(1):根据质量守恒:反应前后质量相等,故生成二氧化碳的质量为10+90-96.04=3.96g;(2):碳酸氢钠与稀盐酸反应方程式为:NaHCO3+HCl=NaCl+H2O+CO2根据差值法可知:每由84g碳酸氢钠反应,就会生成44g二氧化碳,现在已知生成3.96g二氧化碳,故有3.96/44*84=7.56g反应,故质量分数为7.56/10*100%=75.6%。
【点睛】依据质量守恒,分清楚反应物、生成物,集合化学方程式,利用差值法计算产物或者生成物,还要熟练掌握方程式书写。
7.请根据如图所示的实验过程和提供的数据(步骤②产生的气体全部逸出),完成下列问题:(1)该反应产生的CO2气体质量为 g。
(2)计算反应后所得溶液中溶质质量分数(写出计算过程)【答案】(1)4.4(2)11.7%【解析】试题分析:根据质量守恒定律可以知道:生成二氧化碳的质量为:22.3g+100g+82.1g﹣200.0g=4.4g,设碳酸钠的质量为x,生成氯化钠的质量为y,Na2CO3+2HCl═2NaCl+H2O+CO2↑,106 117 44x y 4.4g列比例式得:106:x=117:y=44:4.4克,解得:x=10.6g,y=11.7g,反应后所得溶液中溶质氯化钠的质量分数为:(22.3克-10.6克+11.7克)/200.0克×100%=11.7%,考点:根据化学反应方程式的计算;溶质质量分数的简单计算8.用Ba(OH)2溶液测定某种氮肥中(NH4)2SO4的质量分数(杂质溶于水,但不参加反应)。
实验如下:称取该氮肥20g加水完全溶解,向该溶液中不断滴入Ba(OH)2溶液,生成气体及沉淀质量与加入Ba(OH)2溶液的质量关系如下所示:实验次序123滴入Ba(OH)2溶液的质量/g204060生成气体的质量/g0.85m2.55试分析并计算:[已知:(NH4)2SO4+Ba(OH)2=BaSO4↓+2H2O+2NH3↑](1)表格中m的值为 g。
(2)实验所用氢氧化钡溶液中溶质的质量分数。
(3)该氮肥中(NH4)2SO4的质量分数。
(计算结果精确至0.1%)【答案】(1)1.70;(2)2.1%;(3)6.6%【解析】试题分析:(1)根据表中信息可知,20gBa(OH)2溶液与硫酸铵反应,生成氨气0.85g,到60gBa(OH)2溶液与硫酸铵反应,生成氨气2.55g,说明每20gBa(OH)2溶液与硫酸铵反应,能生成氨气0.85g,40gBa(OH)2溶液与硫酸铵反应,能生成氨气1.70g,故m的值为1.7g;设所用氢氧化钡的质量为x,(NH4)2SO4的质量为y,硫酸钡沉淀的质量为2.33g (NH4)2SO4+Ba(OH)2=BaSO4↓+2H2O+2NH3↑132 171 233y x 2.33g132:233=y:2.33g 171:233=x:2.33gy=1.32g x=1.71g(2)实验所用氢氧化钡溶液中溶质的质量分数1.71g/80g×100%=2.1%(3)该氮肥中(NH4)2SO4的质量分数1.32g/20g×100%=6.6%考点:根据化学方程式的计算、有关溶液的计算9.欲测定某石灰石样品中碳酸钙的质量分数,甲、乙两位同学分别设计了如下两个实验方案:(已知碳酸钙在900℃左右可分解生成氧化钙和二氧化碳,化学方程式为:CaCO3CaO+CO2↑;石灰石样品中的杂质受热不分解,且不与酸反应)方案一:①称取石灰石样品质量8g;②用酒精灯加热样品,直至质量不再改变;③将固体残余物放在干燥的器皿中冷却后称得质量6.9g;④计算.方案二:①称取石灰石样品质量8g;②加入质量分数为7.3%的盐酸100g,使碳酸钙完全反应;③向反应后的溶液中加入含溶质3.2g的氢氧化钠溶液,恰好中和多余的盐酸;④计算.请回答下列有关问题:(1)经过讨论,他们认为上述方案中,切实可行的是方案二.不选用方案一的原因是:.(2)求方案二样品中碳酸钙的质量分数.【答案】(1)用酒精灯难以让碳酸钙完全分解.(2)75%.【解析】(1)由题意可知,第一个方案中用酒精灯加热,温度达不到石灰石分解的高温要求,方案二中碳酸钙可以和盐酸发生反应.所以,上述方案中可行的是方案二.(2)解:设与氢氧化钠反应的HCl质量为x.HCl+NaOH=NaCl+H2O36.5 40x 3.2g则,解得x=2.92g.则与碳酸钙反应的稀盐酸为100g×7.3%﹣2.92g=4.38g.设与4.38gHCl反应的碳酸钙的质量为y.CaCO3+2HCl=CaCl2+CO2↑+H2O100 73y 4.38g则,解得y=6g.故样品中碳酸钙的质量分数为=75%.【点评】本题主要考查了碳酸钙的性质及化学方程式的计算,会根据碳酸钙的性质分析判断方案的可行性.10.烧碱是一种重要的化工原料,用碳酸钠溶液与熟石灰发生反应,之后将生成物进行一系列处理得到固体烧碱,同学们在实验室制取少量烧碱固体.实验过程中向200g碳酸钠溶液中不断加入澄清石灰水,所加澄清石灰水的质量与生成沉淀的质量关系如图所示.请回答下列问题.(1)a点时反应混合液中的阳离子主要是(填化学式);(2)通过计算回答,此碳酸钠溶液中溶质的质量分数是多少?【答案】Na+;5.3%.【解析】(1)a点为反应的过程中,此时碳酸钠没有完全反应,而碳酸钠和氢氧化钙反应生成了氢氧化钠和碳酸钙,所以此时溶液中的溶质是碳酸钠和氢氧化钠,所以溶液含有的阳离子主要是钠离子;故填:Na+;(2)由图中可以知道生成沉淀的质量为10g设碳酸钠的质量为xNa2CO3+Ca(OH)2═CaCO3↓+2NaOH106 100x 10g解得:x=10.6g碳酸钠溶液中溶质的质量分数为:×100%=5.3%答:碳酸钠溶液中溶质的质量分数为5.3%.【点评】在对反应图象中曲线进行分析时,曲线的折点的意味着曲线所表示的反应在此时恰好完全反应,解答时要理清反应指所发生的反应,并正确的书写化学方程式.。