苯的化学性质
- 格式:ppt
- 大小:692.00 KB
- 文档页数:5


苯的性质及应用分子式:C6H6物理性质苯的沸点为80.1℃,熔点为5.51℃,在常温下是一种无色、味甜、有芳香气味的透明液体,易挥发。
苯比水密度低,密度为0.88g/ml,但其分子质量比水重。
苯难溶于水,易溶于有机溶剂,苯也是一种良好的有机溶剂。
化学性质苯参加的化学反应大致有3种:一种是其他基团和苯环上的氢原子之间发生的取代反应;一种是发生在碳原子之间的共价键上的加成反应;一种是苯环的断裂。
一、取代反应1、卤代反应苯的卤代反应的通式可以写成:PhH+X2——→PhX+HX反应过程中,卤素分子在苯和催化剂的共同作用下异裂,X+进攻苯环,X-与催化剂结合。
以溴为例,将液溴与苯混合,溴溶于苯中,形成红褐色液体,不发生反应,当加入铁屑后,在生成的三溴化铁的催化作用下,溴与苯发生反应,混合物呈微沸状,反应放热有红棕色的溴蒸汽产生,冷凝后的气体遇空气出现白雾(HBr)。
反应后的混合物倒入冷水中,有红褐色油状液团(溶有溴)沉于水底,用稀碱液(如NaOH溶液)洗涤后生成可溶性盐(NaBr 和NaBrO),溴苯比水重且分层,在用干燥剂除水,最后蒸馏得无色液体溴苯。
注意:实验过程中,跟瓶口垂直的玻璃管起导气和冷凝的作用、导管不能伸入水中,因为HBr 极易溶于水,发生倒吸。
2、硝化反应向浓硝酸中加入浓硫酸,待温度为50到60摄氏度时,再加入苯,反应生成硝基苯。
其中,浓硫酸既做催化剂。
PhH+HO-NO2-----H2SO4(浓)△---→PhNO2+H2O硝化反应是一个强烈的放热反应,若加入苯太快,温度急剧上升,而得到副产物,而且温度过高,苯容易挥发。
3、磺化反应用浓硫酸或者发烟硫酸在较高温度下可以将苯磺化成苯磺酸。
PhH+HO-SO3H------△→PhSO3H+H2O苯环上引入一个磺酸基后反应能力下降,不易进一步磺化,需要更高的温度才能引入第二、第三个磺酸基。
这说明硝基、磺酸基都是钝化基团,即妨碍再次亲电取代进行的基团。



苯的化学反应方程式苯是一种常见的有机化合物,化学式为C6H6。
它具有六个碳原子和六个氢原子,呈环状结构。
苯的化学性质非常活泼,可以发生多种反应。
下面将介绍苯的几种常见反应,并给出相应的化学反应方程式。
1. 加成反应:苯可以和一些化学物质进行加成反应,即在环状结构上加入新的官能团。
例如,苯可以和氯气发生加成反应,生成氯代苯。
反应方程式如下:C6H6 + Cl2 → C6H5Cl + HCl这个反应是通过苯的芳烃环上一个氢原子被氯原子取代,生成氯代苯。
这是一种重要的化学反应,可以用于苯的取代反应。
2. 卤素代替反应:苯在加热条件下,可以和卤素发生取代反应。
例如,苯可以和溴发生反应,生成溴代苯。
反应方程式如下:C6H6 + Br2 → C6H5Br + HBr这个反应是通过苯的芳烃环上一个氢原子被溴原子取代,生成溴代苯。
类似地,苯也可以和氯、碘等发生类似的取代反应。
3. 烷基化反应:苯可以和卤代烷烃发生烷基化反应,生成烷基苯。
反应通常在强酸存在下进行。
例如,苯可以和氯甲烷发生反应,生成甲基苯。
反应方程式如下:C6H6 + CH3Cl → C6H5CH3 + HCl这个反应是通过苯的芳烃环上一个氢原子被甲基基团取代,生成甲基苯。
这种反应在有机合成中有广泛应用。
4. 氢化反应:苯可以和氢气在适当的催化剂存在下发生氢化反应,生成环己烷。
反应方程式如下:C6H6 + 3H2 → C6H12这个反应是苯环上的双键被氢气加成,生成饱和的环己烷。
这种反应在工业上用于苯的加氢脱芳烃。
5. 硝化反应:苯可以和浓硝酸反应,生成硝基苯。
反应方程式如下:C6H6 + HNO3 → C6H5NO2 + H2O这个反应是通过苯的芳烃环上一个氢原子被硝基取代,生成硝基苯。
硝化反应是制备苯胺等有机化合物的重要步骤。
以上是苯的几种常见反应,其中加成反应、取代反应、烷基化反应、氢化反应和硝化反应是苯的重要反应。
这些反应不仅可以用于苯的化学合成,还可以用于制备苯衍生物,进一步扩展苯的化学应用领域。


苯【知识要点】一、苯的物理性质1.苯的组成:苯是由C、H 两种元素组成的,苯的分子式是C6H6。
注意不要将苯写作“笨”。
2.苯的结构:(1)碳碳键:苯分子中不存在碳碳单键,也不存在碳碳双键,其碳碳键是介于碳碳单键和碳碳双键之间的一种独特的化学键。
(2)结构简式:(3)空间构型:苯分子中,所有C、H原子都处在同一个平面上。
图5-24三、苯的化学性质1.苯的取代反应(1)该反应是放热反应,不需加热反应自发进行。
(2)反应中起催化作用的是FeBr3,实验时实际加入的是Fe。
2Fe+3Br22FeBr3(3)纯净的溴苯是无色的,密度比水大。
(4)生成的HBr可用AgNO3(aq)检验。
(1)反应物及催化剂混合时,不可先将苯(或硝酸)加到浓H2SO4中,以防产生大量的热使液体飞溅。
(2)反应温度必须控制在55℃~60℃,以防止副反应发生,控制温度的方法是水浴加热。
图5-25(3)硝基苯的主要物理性质苯与H2的加成反应3、分子中没有C C双键,不能使溴水和酸性KMnO4(aq)褪色。
四、苯的主要用途【典型例题】例题1苯分子实际上不具有碳碳单键和碳碳双键的交替结构,可以作为证据的事实有①苯的间位二元取代物只有一种。
②苯的邻位二元取代物只有一种。
③苯不能使酸性KMnO4溶液褪色。
④苯能在一定条件下与氢气反应生成环己烷。
⑤苯在FeBr3存在的条件下同液溴发生取代反应。
A.①③④B.③④⑤C.②③⑤D.①③⑤例题2苯乙烯是一种重要的有机化工原料,其结构简式为,它一般不可能具有的性质是A.易溶于水,不易溶于有机溶剂B.在空气中燃烧产生黑烟C.它能使溴的四氯化碳溶液褪色,也能使酸性高锰酸钾溶液褪色D.能发生加成反应,在一定条件下可与4倍物质的量的氢气加成例题3苯与乙烯相比较,下列叙述正确的是()A.都可以与溴发生取代反应B.都容易发生加成反应C.乙烯易发生加成反应,苯不能发生加成反应D.乙烯易被酸性KMnO4氧化,而苯不能例题4下列化学式只表示一种物质的是()A、C6H12B、C4H8C、CH2Cl2D、P例题5将下列各种液体分别与溴水混合并振荡。
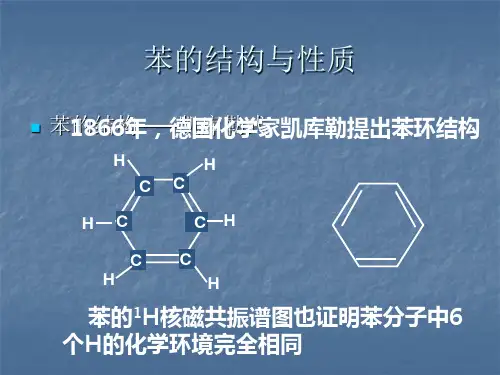
苯的结构和性质一、苯的性质物理性质苯是一种无色有特殊气味的液体,密度比水小,不溶于水,是一种常用的有机溶剂。
二、苯的分子结构(1)苯不与溴的四氯化碳溶液、酸性高锰酸钾溶液反应,说明苯分子中没有与乙烯类似的碳碳双键。
(2)研究表明:①苯分子为平面正六边形结构。
②分子中6个碳原子和6个氢原子共平面。
③6个碳碳键完全相同,是一种介于碳碳单键和碳碳双键之间的独特的键。
三、结构决定性质(1)苯不能使溴的四氯化碳溶液褪色,但能使溴水褪色,这是因为苯能将溴从溴水中萃取出来。
(2)苯的凯库勒式为,不能认为苯分子是单双键交替结构,苯分子中6个碳碳键完全相同。
(3)苯分子中的碳碳键是介于碳碳单键和碳碳双键之间的独特的键,故苯兼有烯烃的加成反应和烷烃的取代反应的特征,且比烯烃的加成反应和烷烃的取代反应困难。
(4)苯易发生取代反应,能发生加成反应,难被氧化(燃烧除外),其化学性质不同于烷烃和烯烃。
1.苯的结构简式可用来表示,下列关于苯的叙述中正确的是( )A.苯分子中处于对位的两个碳原子及与它们相连的两个氢原子,不可能在同一条直线上B.苯中含有碳碳双键,所以苯属于烯烃C.苯分子中的6个碳碳键可以分成两类不同的化学键D.苯分子中既不含有碳碳双键,也不含有碳碳单键答案 D解析苯分子处于对位的两个碳原子及与它们相连的两个氢原子,这四个原子共直线;苯分子中不含有碳碳双键,苯不属于烯烃;苯分子中的6个碳碳键完全相同,是一种介于碳碳单键和碳碳双键之间的独特的键。
故选D。
2.下列物质的所有原子,不可能处于同一平面上的是( )A.CH3CH==CH2 B.CH2==CH2 C. D.答案A解析乙烯和苯都属于平面形结构,所有原子都处于同一平面内,而甲烷分子是正四面体结构,故可以得出甲基中的原子不可能处于同一平面内,A项含有甲基,所有原子不可能共面,C项可以看作是乙烯中的一个氢原子被苯环取代,推知C项中物质的所有原子可能处于同一平面内。
3.在①丙烯②氯乙烯③苯④甲苯四种有机化合物中,分子内所有原子均在同一平面内的是( )A.①②B.②③C.③④D.②④答案B解析在①丙烯CH2==CH—CH3和④甲苯C6H5—CH3中,—CH3是空间立体结构(与甲烷类似),这四个原子不在同一平面上;②氯乙烯和乙烯相同,是六原子共面结构;③苯是十二个原子共面结构。
引言概述:在上一篇文章中,我们已经介绍了苯的基本化学性质,包括其结构、物理性质和一些常见的反应。
在这篇文章中,我们将继续探讨苯的化学性质,重点关注苯的取代反应、加成反应、氧化反应、还原反应和重排反应。
通过对苯的这些化学性质的深入了解,可以更好地理解苯及其衍生物的化学行为。
正文内容:一、苯的取代反应1.亲电芳香取代反应卤代烷的取代反应:亲电卤素与苯反应取代的苯基卤代烷。
酰基化反应:酰基化试剂与苯反应酰基取代的苯基化合物。
磺酰化反应:磺酰化试剂与苯反应磺酰基取代的苯基化合物。
2.自由基取代反应自由基取代反应:自由基取代剂与苯反应自由基取代的苯基化合物,常见的反应有氯代烷与苯反应形成取代的苯基氯代烷。
3.亲核芳香取代反应氨基化反应:胺类试剂与苯反应苯胺或取代的苯基胺。
羟基化反应:羟基化试剂与苯反应酚或取代的苯基酚。
二、苯的加成反应1.加成反应加成反应:双键试剂与苯反应,加成产物。
常见的反应有苯与亚乙炔反应二苯乙烯。
2.共轭加成反应共轭加成反应:含有亲电试剂的体系与苯反应,共轭加成产物。
常见的反应有苯与硝酸反应亚硝基苯。
三、苯的氧化反应1.氧化反应碱性高锰酸钾氧化:苯在碱性高锰酸钾溶液中氧化苯酚。
雷诺氧化:苯在雷诺试剂的存在下,氧化成苯酚。
2.高温氧化高温氧化:苯在高温下氧化苯酸。
四、苯的还原反应1.加氢还原加氢还原:苯与氢气在催化剂的作用下进行反应环己烷。
2.还原反应还原反应:苯的芳香性被破坏,饱和的烷基化合物。
五、苯的重排反应1.缩合重排缩合重排:苯环内两个不相邻的碳原子间形成一个新的碳碳键。
2.羟基迁移重排羟基迁移重排:苯环上的羟基原子迁移到相邻的碳原子上。
总结:通过对苯的化学性质的探讨,我们可以发现苯是一种非常重要的化合物,具有丰富的化学反应性和反应途径。
苯的取代反应、加成反应、氧化反应、还原反应和重排反应使得苯能够形成多种结构复杂的衍生物。
了解苯的化学性质,有助于我们更好地理解和应用苯及其衍生物在有机化学领域的广泛应用。
一、教学目标1. 理解苯的结构特点和化学键的特殊性。
2. 掌握苯的物理性质和化学性质,包括反应类型和条件。
3. 能够运用苯的性质进行简单的有机合成反应。
4. 培养学生分析问题和解决问题的能力。
二、教学重难点重点:苯的化学键特性、苯的化学性质及反应类型。
难点:苯的化学性质在有机合成中的应用。
三、教学方法1. 讲授法:讲解苯的基本概念、结构特点和化学性质。
2. 案例分析法:通过实际案例讲解苯的化学性质及其在有机合成中的应用。
3. 讨论法:引导学生分组讨论苯的性质,并总结归纳。
四、教学过程【导入】1. 展示橘子皮使气球爆破的动图,引发学生对芳香烃的兴趣。
2. 提问:气球爆破的原因是什么?芳香烃在生活中的应用有哪些?【讲解】1. 苯的基本概念- 苯是一种含有苯环的碳氢化合物。
- 苯的分子式为C6H6,分子中碳原子和氢原子以共价键相连。
2. 苯的结构特点- 苯的碳原子以sp2杂化形成平面正六边形结构。
- 苯分子中碳原子间形成特殊的化学键——芳香键,具有共轭π电子系统。
3. 苯的物理性质- 苯是无色、有特殊香味的液体。
- 苯的密度小于水,不溶于水,易溶于有机溶剂。
4. 苯的化学性质- 苯的化学性质主要表现为取代反应和加成反应。
- 取代反应:苯在催化剂的作用下,可发生硝化、卤代、磺化等反应。
- 加成反应:苯在高温、高压、催化剂的作用下,可发生氢化、卤化等反应。
5. 苯在有机合成中的应用- 通过苯的取代反应和加成反应,可以合成多种有机化合物。
【案例分析】1. 以苯的硝化反应为例,讲解苯的取代反应。
2. 以苯的氢化反应为例,讲解苯的加成反应。
【讨论】1. 引导学生分组讨论苯的性质及其在有机合成中的应用。
2. 总结归纳苯的性质,并让学生举例说明。
【总结】1. 强调苯的化学键特性、物理性质和化学性质。
2. 总结苯在有机合成中的应用。
五、作业与拓展1. 完成课后习题,巩固所学知识。
2. 查阅资料,了解苯在工业和生活中的应用。
第2课时 苯的结构和性质[学习目标定位] 1.会写苯的分子式、结构式、结构简式。
2.知道苯分子中的碳碳键是一种介于碳碳单键与碳碳双键之间的独特的键。
3.知道苯能够发生氧化反应、加成反应、取代反应,并会写相应的化学方程式。
4.了解苯的来源及用途。
一、苯的分子结构1.苯是一种重要的化工原料,其分子式为C 6H 6,远没有达到饱和。
根据下列实验,总结苯的某些性质。
2.德国化学家凯库勒在苯分子结构的确定中做出了重要贡献,他分析了大量实验事实之后,提出了苯的分子结构为,我们称其为凯库勒式并一直沿用到现在。
(1)你认为这种结构符合实验事实吗?说出你的理由。
答案 不符合实验事实,因为苯不能与溴水发生加成反应使溴水褪色,也不能被酸性KMnO 4溶液氧化,说明它没有典型的碳碳双键。
(2)查阅资料,写出苯分子结构的另一种表达方式,并用文字归纳苯分子的空间结构和化学键的特征。
答案 ,苯分子为平面正六边形结构,6个碳碳键完全相同,是介于碳碳单键和碳碳双键之间的独特的化学键。
(3)由苯分子的空间结构可以推测六个碳碳键之间的夹角大小关系是什么?两个碳氢键的夹角又是多少?答案 六个碳碳键之间的夹角相等,都是120°,两个碳氢键的夹角也是120 °。
归纳总结 1.苯的组成与结构2.苯的结构特点(1)苯分子为平面正六边形结构。
(2)分子中6个碳原子和6个氢原子共平面。
(3)6个碳碳键完全相同,是一种介于碳碳单键和碳碳双键之间的特殊化学键。
1.能说明苯分子的平面正六边形结构中,碳碳键不是单、双键交替排布,而是6个碳原子之间的键完全相同的事实是( )A.苯的一氯取代物()只有1种B.苯的邻位二氯取代物()只有1种C.苯的间位二氯取代物()只有1种D.苯的对位二氯取代物()只有1种答案 B解析 苯分子结构中无论是单、双键交替出现,还是6个碳原子之间的键完全相同,苯的一取代物都只有一种结构,间位二取代物、对位二取代物也都只有一种结构,因此A 、C 、D 项不能用以说明苯环不存在单、双键交替结构;B 项,苯分子结构中若单、双键交替出现,则苯的邻位二取代物有两种结构,因此B 项可以说明苯分子不存在单、双键交替结构。