[推荐学习]2019年高考化学一轮复习酸碱中和滴定曲线大全专题05物质的量分数曲线练习
- 格式:doc
- 大小:2.54 MB
- 文档页数:23

人教部编版高中化学酸碱中和滴定曲线知识点总结在历年高考命题中,通过图象考查弱电解质电离平衡、pH与起始浓度的关系、有关混合溶液pH的计算、离子浓度的大小比较、盐类水解、守恒关系的应用以及沉淀溶解平衡等知识的题目是必考题,具有一定难度和区分度。
酸碱中和滴定曲线类试题是近几年高考的热点和难点,试题通常以酸碱滴定过程为基础,涉及电解质水溶液中离子浓度的等量关系、大小关系以及水的电离程度等知识和规律,综合性强,难度较大。
一、解题方法:1.要仔细分析所给图象,确定图象各点的成分和溶液酸碱性,充分挖掘图象信息中的隐含条件,如图示中的最高点、最低点、交汇点、突变点都是提供解题信息的关键点。
2.用守恒法、不等式(先主次、后大小)等方法解决问题。
(1)三大守恒:①电荷守恒,②物料守恒,③质子守恒。
(2)一个不等式:主要微粒>次要微粒。
①强酸、强碱、大多数盐(含水解和不水解)溶液主要以电离产生的离子形式存在于溶液中。
②弱酸、弱碱主要以弱电解质的分子形式存在于溶液中。
③可水解的盐溶液中可水解的离子的水解程度极小、弱电解质分子的电离程度极小。
④强碱弱酸的酸式盐溶液,需要讨论酸式酸根水解和电离程度的相对大小。
3.对于混合溶液的离子平衡图象题,解题思维必须触及:混合溶液有无反应、反应物是否过量、电离与水解何者强、溶液体积变化有无影响定性分析或定量计算等。
若不发生反应的混合溶液,则同时考虑电离和水解。
若恰好完全反应的混合溶液,生成的是酸或碱则考虑电离,生成的是盐则考虑水解。
若反应物过量,则根据过量程度考虑电离或水解。
若有定量计算,则要考虑混合溶液的体积变化。
4.一定要理解透坐标用对数表示的含义。
结合平衡移动原理确定变化量到底是增大了还是减小了。
5.选择题中的曲线图通常有以下几种:(1)弱电解质的电离平衡图象。
该类试题中,图象中一般会同时涉及强电解质和弱电解质。
(2)酸碱混合液的pH与离子浓度大小之间的关系图象。
(3)沉淀溶解平衡图象。
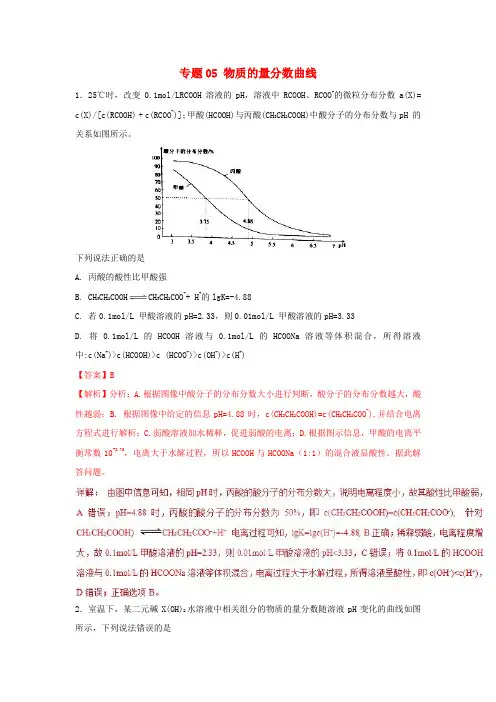
专题05 物质的量分数曲线1.25℃时,改变0.1mol/LRCOOH溶液的pH,溶液中RCOOH、RCOO-的微粒分布分数a(X)= c(X)/[c(RCOOH) + c(RCOO-)];甲酸(HCOOH)与丙酸(CH3CH2COOH)中酸分子的分布分数与pH 的关系如图所示。
下列说法正确的是A. 丙酸的酸性比甲酸强B. CH3CH2COOH CH3CH2COO-+ H+的lgK=-4.88C. 若0.1mol/L 甲酸溶液的pH=2.33,则0.01mol/L 甲酸溶液的pH=3.33D. 将0.1mol/L 的HCOOH溶液与0.1mol/L 的HCOONa溶液等体积混合,所得溶液中:c(Na+)>c(HCOOH)>c (HCOO-)>c(OH-)>c(H+)【答案】B【解析】分析:A.根据图像中酸分子的分布分数大小进行判断,酸分子的分布分数越大,酸性越弱;B. 根据图像中给定的信息pH=4.88时,c(CH3CH2COOH)=c(CH3CH2COO-),并结合电离方程式进行解析;C.弱酸溶液加水稀释,促进弱酸的电离;D.根据图示信息,甲酸的电离平衡常数10-3.75,电离大于水解过程,所以HCOOH与HCOONa(1:1)的混合液显酸性。
据此解答问题。
2.室温下,某二元碱X(OH)2水溶液中相关组分的物质的量分数随溶液pH变化的曲线如图所示,下列说法错误的是A. K b2的数量级为10-8B. X(OH)NO3水溶液显碱性C. 等物质的量的X(NO3)2和X(OH)NO3混合溶液中c(X2+)>c[X(OH)+]D. 在X(OH)NO3水溶液中,c[X(OH)2]+c(OH-)= c(X2+)+ c(H+)【答案】C【解析】分析:本题是一道图形比较熟悉的题目,不过题目将一般使用的二元酸变为了二元碱,所以在分析图示时要随时注意考查的是多元碱的分步电离。
详解:A.选取图中左侧的交点数据,此时,pH=6.2,c[X(OH)+]=c(X2+),所以K b2=,选项A正确。

强碱滴定二元弱酸曲线-2019 高考复习专题——酸碱中和滴定曲线大全- 1- 1(其1.常温下,向 20 mL 0.2 mol L · H 2A 溶液中滴加0.2 mol L· NaOH 溶液。
有关微粒物质的量变化如下图中Ⅰ代表H 2A ,Ⅱ代表 HA -,Ⅲ代表 A 2- ) 。
根据图示判断,下列说法正确的是()A. H 2A 在水中的电离方程式是:H2A===H ++ HA -、HA -H ++ A 2-B.等体积等浓度的 NaOH 溶液与 H 2A 溶液混合后溶液显碱性C. 当 V(NaOH) = 20 mL 时,溶液中存在以下关系:+2--c(H )+ c(H 2A) = c(A)+ c(OH )D. 当 V(NaOH) =30mL 时,溶液中各粒子浓度的大小顺序为:c(Na +)>c(HA -)>c(A 2- )>c(H+ )>c(OH - )【答案】 C2.已知: pK a= -lgK a,25℃时, H 2SO3的 pK a1=1.85,pK a2=7.19。
常温下,用0.1mol/LNaOH 溶液滴定 20mL 0. 1mol/L H SO溶液的滴定曲线如图所示。
下列说法不正确的是A. A 点所得溶液中:V o等于 lOmLB. B 点所得溶液中:C. C 点所得溶液中:D. D 点所得溶液中水解平衡常数【答案】 A【解析】分析: A .A 点溶液中 pH=1.85 ,则溶液中 c( H+)=10 -1.85mol/L ,结合亚硫酸的电离平衡常数分析;B . B 点加入 NaOH 溶液的体积为 20mL,此时反应恰好产生 NaHSO3,根据溶液中电荷守恒分析;C.根据亚硫酸的电离平衡常数结合电荷守恒分析;D . D 点为加入NaOH 溶液 40mL ,此时溶液中恰好生成亚硫酸钠,根据水解常数与电离常数的关系计算。
详解: A . A点溶液中 pH=1.85 ,则溶液中 c ( H+) =10-1.85mol/L , H 2SO3的一级电离平衡常数为K a1=c(H + )c(HSO 3- )/c(H 2SO3)=10 -1.85 mol/L ,所以 c( H +)=K a1,表明溶液中 c( NaHSO 3)=c( H2 SO3),若恰好是 10mLNaOH ,由于此时溶液显酸性,则所得溶液中c(H 2SO3)< c(NaHSO 3),因此所加 NaOH 体积需< 10mL,才能使溶液中c(NaHSO 3)=c ( H2SO3),即 V 0< 10mL , A 错误;B . B 点加入 NaOH 溶液的体积为20mL ,此时反应恰好产生NaHSO 3,为第一个滴定终点,溶液中存在电荷守恒, c( Na+)+c ( H+) =c(HSO 3-)+2c( SO32-)+c( OH -), B 正确;C.H2SO3的二级电离平衡常数为K a2=c(H + )c( SO32-)/c(HSO 3- )=10 -7.19mol/L , C 点溶液的 pH=7.19 ,即溶液中 c( H +)=10-7.19 mol/L ,则 c(H +)=K a2,表明溶液中 c( SO32-)=c(HSO 3- ),溶液中存在电荷守恒, c( Na+)+c( H +) =c(HSO 3- )+2c( SO32-) +c( OH -),溶液显碱性,则溶液中c(Na+)> 3c(HSO 3- ), C 正确;D . D 点为加入 NaOH 溶液 40mL ,此时溶液中恰好生成亚硫酸钠,为第二个滴定终点,此时亚硫酸钠水解使溶液显碱性,则 K h1= K w /K a2= 10- 14- 7.19= 10-6.81, D 正确。



专题五化学实验1.下列玻璃仪器的洗涤方法涉及氧化还原反应的是A.附有银镜的试管用稀硝酸清洗B.附有油脂的烧杯用热纯碱溶液清洗C.附有苯酚的试管用热的烧碱溶液清洗D.附有氢氧化铁的试管用盐酸清洗【答案】A【解析】【详解】A.银单质与稀硝酸反应生成硝酸银、一氧化氮、水,属于氧化还原反应,故A正确;B.附有油脂的烧杯用热纯碱溶液清洗,属于油脂水解,属于非氧化还原反应,故B错误;C.附有苯酚的试管用热的烧碱溶液清洗,苯酚和烧碱反应生成苯酚钠和水,属于非氧化还原反应,故C错误;D. 附有氢氧化铁的试管用盐酸清洗,是酸碱中和反应,属于非氧化还原反应,故D错误。
答案选A。
【点睛】本题结合用化学方法进行玻璃仪器的洗涤考查氧化还原反应的判断,明确氧化还原反应的判断方法是解题的关键,要注意用化学方法洗涤玻璃仪器的化学原理。
2.下列有关实验操作的叙述合理的是A.用pH试纸测定溶液pH时,不需要预先润湿B.蒸馏实验中,忘记加沸石,应立即趁热加入沸石C.要量取15.80mL溴水,须使用棕色的碱式滴定管D.用酸性KMnO4溶液检验FeCl3溶液中混有的Fe2+【答案】A【解析】【详解】A项、测定溶液pH时,若先润湿将会导致所测溶液浓度减少,结果不准确,故A正确;B项、蒸馏实验中,忘记加沸石,需要先冷却后再加入沸石,以防剧烈的暴沸,故B错误;C项、溴水具有强氧化性,应该用酸式滴定管量取,故C错误;D项、由于Cl-能被酸性高锰酸钾溶液氧化,所以不能用酸性高锰酸钾溶液检验FeCl3溶液中的Fe2+,故D错误。
故选A。
【点睛】本题考查了化学实验操作,熟练掌握操作的注意事项,明白操作的原理是解答关键,注意用PH试纸检验溶液的PH值时不能用蒸馏水润湿,但用石蕊试纸检验气体时要用蒸馏水润湿。
3.下列选项中,利用相关实验器材(规格和数量不限)能够完成相应实验的是A.A B.B C.C D.D【答案】D【解析】【详解】A、配制100mL1.00mol /L NaCl溶液,需要天平(带砝码)、100mL容量瓶、烧杯、胶头滴管、玻璃棒,缺少玻璃棒不能完成相应实验,选项A错误;B、中和反应反应热的测定,需要烧杯、环形玻璃搅拌棒、碎泡沫塑料、硬纸板、温度计,缺少温度计不能完成相应实验,选项B错误;C、实验测定酸碱滴定曲线,需要酸/碱式滴定管、滴定管夹、烧杯、锥形瓶、铁架台、pH计,缺少pH计不能完成相应实验,选项C错误;D、钾在空气中燃烧实验,需要三脚架、酒精灯、坩埚、坩埚钳、镊子、泥三角,符合实验所需要仪器选用,选项D正确。
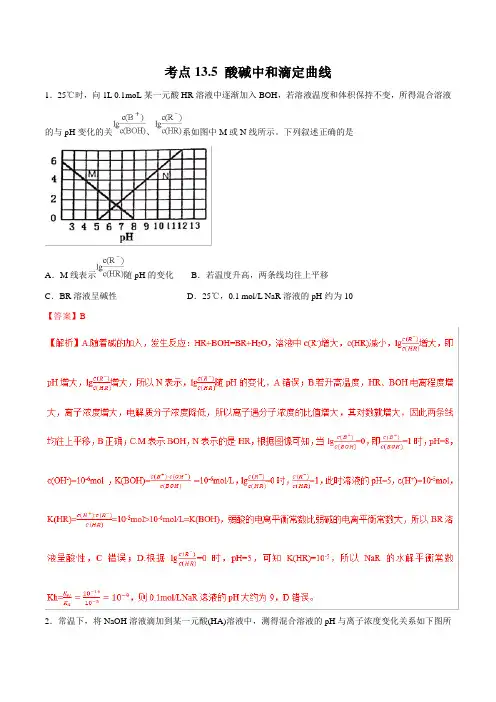
考点13.5 酸碱中和滴定曲线1.25℃时,向1L 0.1moL某一元酸HR溶液中逐渐加入BOH,若溶液温度和体积保持不变,所得混合溶液的与pH变化的关、系如图中M或N线所示。
下列叙述正确的是A.M线表示随pH的变化B.若温度升高,两条线均往上平移C.BR溶液呈碱性D.25℃,0.1 mol/L NaR溶液的pH约为10【答案】B2.常温下,将NaOH溶液滴加到某一元酸(HA)溶液中,测得混合溶液的pH与离子浓度变化关系如下图所示[已知:]。
下列叙述不正确...的是A.K a(HA) = 10-4.76B.滴加NaOH溶液过程中,保持不变C.m点所示溶液中:c(H+) = c(HA)+c(OH-)-c(Na+)D.n点所示溶液中可能:c((Na+) = c(A-)+c(HA)【答案】D3.25℃时,向20mL 0.1 mol·L -1二元弱酸H2A 溶液中逐滴加入0.1 mol·L -1NaOH 溶液,混合溶液中H2A、HA-、A2-的物质的量分数随pH 的变化如图所示(混合时不考虑体积变化)。
下列叙述正确的是A.H2A 溶液中存在微粒浓度关系:2c(A2-) + c(HA- )+ c(OH-) = c(H2A) + c(H+)B.N 点pH=4.2 时,c(A2-) = c(HA-),A2-水解程度与HA-电离程度相等C.0.1 mol·L-1H2A 溶液与0.1 mol·L-1NaOH 溶液混合后,溶液中HA- 物质的量分数位于曲线 b 的最大值D.滴加氢氧化钠的体积为10mL时,c(A2-) + c(HA-) + c(H2A)+ c(Na+) = 0.1 mol·L-1【答案】D4.25℃时,向某Na2CO3溶液中加入稀盐酸,溶液中含碳微粒的物质的量分数(φ)随溶液pH变化的部分情况如图所示。
下列说法中正确的是A.pH=7时,c(Na+)=(Cl-)+c(HCO3-)+2c(CO32-)B.pH=8时,c(Na+)=c(C1-)C.pH=12时,c(Na+ )>c(OH-)>c(CO32-)>c(HCO3-)>c(H+)D.25℃时,CO32-+H2O HCO3-+OH-的水解平衡常数K h=10-10mol·L-1【答案】A【解析】A、由电荷守恒:c(Na+)+c(H+)=(OH-)+Cl-)+c(HCO3-)+2c(CO32-), pH=7时,c(H+)=(OH-),c(Na+)=(Cl-)+c(HCO3-)+2c(CO32-),故A正确;B、pH=8时溶液为碳酸氢钠和氯化钠,溶液中c(Cl-)<c(Na+),故B错误;C、pH=12时,溶液为Na2CO3溶液,先电离,然后碳酸根离子水解生成碳酸氢根离子和氢氧根离子,碳酸氢根离子水解生成碳酸和氢氧根离子,c(Na+ )>c(CO32-)>c(OH-)>c(HCO3-)>c(H+),故C错误;D、CO32-的水解常数Kh=c(HCO3-)c(OH-)/c(CO32-),当溶液中c(HCO3-):c(CO32-)=1:1时,图象可知PH=10,c(H+)=10-10mol·L-1,由Kw可知c(OH-)=10-4mol·L-1,则Kh=c(HCO3-)c(OH-)/c(CO32-)=c(OH-)=10-4mol·L-1,故D错误。

2019年秋高三化学复习强化练习题——酸碱中和滴定曲线分析(word版,解析)2019年年年年年年年年年年年年——年年年年年年年年年年一、单选题(本大题共30小题,共30.0分)1.在常温下,向100mL0.01mol/LHA溶液中逐滴加入0.02mol/LMOH溶液,混合溶液的pH变化情况如图中所示曲线(体积变化忽略不计)。
下列叙述正确的是()A. MA溶液的pH>7B. K点时加水稀释溶液,c(H+)减小C. 在N点,c(A−)=c(M+)+c(MOH)D. 在K点,c(M+)>c(A−)>c(OH−)>c(H+)2.298K时,在20.0mL0.10mol⋅L−1氨水中滴入0.10mol⋅L−1的盐酸,溶液的pH与所加盐酸的体积关系如图所示。
已知0.10mol⋅L−1氨水的电离度为1.32%,下列有关叙述正确的是()A. 该滴定过程应该选择酚酞作为指示剂B. M点对应的盐酸体积为20.0mLC. M点处的溶液中c(NH4+)=c(Cl-)=c(H+)=c(OH-)D. N点处的溶液中pH<123.25℃时,用浓度为0.01mol·L−1的HA溶液滴定20mL浓度为0.01mol·L−1的NaOH溶液,滴定曲线如图所示。
下列说法错误的是()A.应选用酚酞作指示剂B. M点溶液中存在:c(Na+)>c(A−)C. Ka(HA)≈2×10−8D. N点溶液中存在:c(OH−)−c(H+)=c(HA)4.常温下,用0.1000mol⋅L−1的盐酸滴定20.00mL0.1000mol⋅L−1的Na2A溶液,溶液的pH与所加盐酸体积的变化关系如图所示。
下列叙述错误的是()A. 常温下,K a2(H2A)的数量级为10−11B. c点溶液中:c(Na+)=2c(A2−)+c (HA−)+c(Cl−)1/ 22C. 水的电离程度:a>b>d>cD. a点溶液中:c(Na+)>c(A2−)>c(OH−)>c(HA−)5.25℃时,向20.00mL的NaOH溶液中逐滴加入某浓度的CH3COOH溶液。

滴定曲线考点深度剖析【解题思路分析】滴定曲线分析的方法(1)分析步骤:首先看纵坐标,搞清楚是酸加入碱中,还是碱加入酸中;其次看起点,起点可以看出酸性或碱性的强弱,这在判断滴定终点时至关重要;再次找滴定终点和pH=7的中性点,判断滴定终点的酸碱性,然后确定中性点(pH=7)的位置;最后分析其他的特殊点(如滴定一半点,过量一半点等),分析酸、碱过量情况。
(2)滴定过程中的定量关系:①电荷守恒关系在任何时候均存在;②物料守恒可以根据加入酸的物质的量和加入碱的物质的量进行确定,但不一定为等量关系。
【考点深度剖析】一、中和滴定的实验操作1.原理(1)酸碱恰好中和是指酸与碱按化学方程式中化学计量数关系恰好完全反应生成正盐。
利用中和反应,用已知浓度的酸(或碱)来测定未知浓度的碱(或酸)的实验方法称为酸碱中和滴定。
(2)在酸碱中和滴定过程中,开始时由于被滴定的酸(或碱)浓度较大,滴入少量的碱(或酸)对其pH的影响不大。
当滴定接近终点(pH=7)时,很少量(一滴,约0.04 mL)的碱(或酸)就会引起溶液pH突变(如图所示)。
[注意] 酸碱恰好中和时溶液不一定呈中性,最终溶液的酸碱性取决于生成盐的性质,强酸强碱盐的溶液呈中性,强碱弱酸盐的溶液呈碱性,强酸弱碱盐的溶液呈酸性。
2.酸碱中和滴定的关键(1)准确测定参加反应的酸、碱溶液的体积。
(2)选取适当指示剂,准确判断滴定终点。
3.实验用品(1)仪器酸式滴定管(如图A)、碱式滴定管(如图B)、锥形瓶、滴定管夹等。
(2)试剂标准液、待测液、指示剂、蒸馏水。
[注意] ①滴定管的精确度为0.01 mL。
②酸性、氧化性的试剂一般用酸式滴定管,因为酸性和氧化性物质易腐蚀橡胶管。
③碱性的试剂一般用碱式滴定管,因为碱性物质易腐蚀玻璃,致使活塞无法打开。
④常用酸碱指示剂及变色范围4.中和滴定实验操作(以酚酞作指示剂,用盐酸滴定氢氧化钠溶液)(1)滴定前的准备(2)滴定(3)终点判断等到滴入最后一滴标准液,溶液由红色变为无色,且在半分钟内不恢复原来的颜色,视为滴定终点并记录标准液的体积。
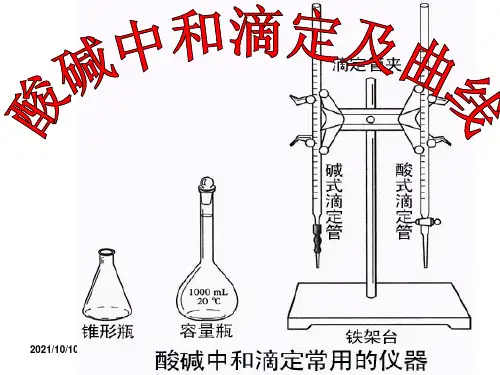
1.在常温下,用0.1000 mol/L的盐酸滴定25 mL 0.100 mol/Lna2CO3溶液,所得滴定曲线如下图所示。
下列相关微粒浓度间的关系不正确的是A. a点: c(CO32-) >c(Cl-)> c(HCO3-)B. b点: c(Na+)+c(H+)= c(Cl-)+ c(HCO3-)+2c(CO32-)+c(OH-)C. c点: c(OH-)+ c(CO32-)= c(H+) +c(H2CO3)D. d点: c(Cl-)= c(Na+)2.H2RO3是一种二元酸,常温下用1L1mol·L-1 Na2RO3溶液吸收RO2气体,溶液的pH随RO2气体的物质的量的变化如图所示。
下列说法正确的是A. a点溶液中2c(Na+)=3c(RO32-)B. 向b点溶液中加水可使溶液的pH由6.2升高到7.4C. 常温下,NaHRO3溶液中c(HRO3-)>c(RO32-)>c(H2RO3)D. 当吸收RO2的溶液呈中性时,c(Na+)=c(RO32-)+c(HRO3-)3.常温时,配制一组c(Na2CO3)+c(NaHCO3)=0.100 mol·L-1的混合溶液,溶液中c(CO32-)、c(HCO3-)与pH的关系如图所示。
下列说法中错误的是(己知:CO32-+H2O HCO3-+OH- K=2×10-4,1g5=0.7)A. a 点的溶液中:c(HCO 3-)> c(H 2CO 3)+c(CO 32-)B. b 点横坐标数值大约为10.3C. c 点的溶液中:c(Na +)<2c(CO 32-)十c(HCO 3-)D. 溶液中水的电离程度:a<b<c4.25℃时,向Na 2CO 3溶液中滴入盐酸,混合溶液的pH 与离子浓度变化的关系如图所示。
己知:lgX=lg()2-3-3CO (HCO c c )或lg()-323HCO (H CO c c ),下列叙述正确的是A. 曲线m 表示pH 与()-323HCO (H CO c c )的变化关系 B. 当溶液呈中性时,c (Na +)= ()-3HCO c +2()2-3CO cC. Ka 1(H 2CO 3)=1.0×10-6.4D. 25℃时,CO 32-+H 2O-3HCO +OH -的平衡常数为1.0×10-7.6 5.常温下,用0. 1000 mol·L -1的盐酸滴定20.00 mL 未知浓度的Na 2CO 3溶液,溶液的pH 与所加盐酸的体积关系如图所示(饱和H 2CO 3溶液pH=5.6)。
专题09 强碱滴定三元酸曲线1.砷(As)是一些工厂和矿山废水中的污染元素。
常温下,H3AsO4水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与加NaOH溶液调节pH的关系如图所示(已知:p K a=-lg K a),下列说法错误的是A. Na2HAsO4溶液显碱性B. H3AsO4溶液p K a2为2.2C. m点对应溶液中由水电离出的c(OH-)为10-2.5mol·L-1D. n点对应溶液中离子浓度关系为:c(Na+)>c(HAsO42-)=c(H2AsO4-)>c(H+)=c(OH-)【答案】B【解析】分析:A.根据Na2HAsO4溶液pH大于7判断;B.根据H3AsO4的电离平衡常数计算;C.m点对应溶液为HAsO42-和AsO43-的混合溶液,溶液显碱性,说明是盐的水解的原因;D.n点对应溶液pH=7,溶液呈中性,据此解答。
详解:A.根据图象分析可知,HAsO42-溶液pH大于7,溶液显碱性,A正确;B.H3AsO4的K a2=,pH=7时c(HAsO42-)=c(H2AsO4-),K a2=c(H+)=10-7,pK a2=7,B错误;C.m点对应溶液为HAsO42-和AsO43-的混合溶液,溶液显碱性,盐类水解促进水的电离,m点溶液的pH=11.5,则对应溶液中由水电离出的c(OH-)为10-2.5mol·L-1,C正确;D.n点对应溶液pH=7,溶液中c(Na+)>c(HAsO42-)=c(H2AsO4-)>c(H+)=c(OH-),D正确;答案选B。
2.25℃时,向10mL0.1mol·L-1H3AsO4水溶液滴加0.1 mol·L-1NaOH溶液,含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如下图,下列说法错误的是A. H3AsO4H2AsO4-+H+的电离常数为10-2.2B. b点所处溶液中:c(Na+)=3c(H2AsO4-)+3c(AsO43-)C. 水的电离程度:a>b>cD. HAsO4-的水解程度大于电离程度【答案】C3.亚砷酸(H3AsO3)可用于治疗白血病,在溶液中存在多种微粒形态。
专题05 物质的量分数曲线1.25℃时,改变0.1mol/LRCOOH溶液的pH,溶液中RCOOH、RCOO-的微粒分布分数a(X)= c(X)/[c(RCOOH) + c(RCOO-)];甲酸(HCOOH)与丙酸(CH3CH2COOH)中酸分子的分布分数与pH 的关系如图所示。
下列说法正确的是A. 丙酸的酸性比甲酸强B. CH3CH2COOH CH3CH2COO-+ H+的lgK=-4.88C. 若0.1mol/L 甲酸溶液的pH=2.33,则0.01mol/L 甲酸溶液的pH=3.33D. 将0.1mol/L 的HCOOH溶液与0.1mol/L 的HCOONa溶液等体积混合,所得溶液中:c(Na+)>c(HCOOH)>c (HCOO-)>c(OH-)>c(H+)【答案】B【解析】分析:A.根据图像中酸分子的分布分数大小进行判断,酸分子的分布分数越大,酸性越弱;B. 根据图像中给定的信息pH=4.88时,c(CH3CH2COOH)=c(CH3CH2COO-),并结合电离方程式进行解析;C.弱酸溶液加水稀释,促进弱酸的电离;D.根据图示信息,甲酸的电离平衡常数10-3.75,电离大于水解过程,所以HCOOH与HCOONa(1:1)的混合液显酸性。
据此解答问题。
2.室温下,某二元碱X(OH)2水溶液中相关组分的物质的量分数随溶液pH变化的曲线如图所示,下列说法错误的是A. K b2的数量级为10-8B. X(OH)NO3水溶液显碱性C. 等物质的量的X(NO3)2和X(OH)NO3混合溶液中c(X2+)>c[X(OH)+]D. 在X(OH)NO3水溶液中,c[X(OH)2]+c(OH-)= c(X2+)+ c(H+)【答案】C【解析】分析:本题是一道图形比较熟悉的题目,不过题目将一般使用的二元酸变为了二元碱,所以在分析图示时要随时注意考查的是多元碱的分步电离。
详解:A.选取图中左侧的交点数据,此时,pH=6.2,c[X(OH)+]=c(X2+),所以K b2=,选项A正确。
专题05 物质的量分数曲线1.25℃时,改变0.1mol/LRCOOH溶液的pH,溶液中RCOOH、RCOO-的微粒分布分数a(X)= c(X)/[c(RCOOH) + c(RCOO-)];甲酸(HCOOH)与丙酸(CH3CH2COOH)中酸分子的分布分数与pH 的关系如图所示。
下列说法正确的是A. 丙酸的酸性比甲酸强B. CH3CH2COOH CH3CH2COO-+ H+的lgK=-4.88C. 若0.1mol/L 甲酸溶液的pH=2.33,则0.01mol/L 甲酸溶液的pH=3.33D. 将0.1mol/L 的HCOOH溶液与0.1mol/L 的HCOONa溶液等体积混合,所得溶液中:c(Na+)>c(HCOOH)>c (HCOO-)>c(OH-)>c(H+)【答案】B【解析】分析:A.根据图像中酸分子的分布分数大小进行判断,酸分子的分布分数越大,酸性越弱;B. 根据图像中给定的信息pH=4.88时,c(CH3CH2COOH)=c(CH3CH2COO-),并结合电离方程式进行解析;C.弱酸溶液加水稀释,促进弱酸的电离;D.根据图示信息,甲酸的电离平衡常数10-3.75,电离大于水解过程,所以HCOOH与HCOONa(1:1)的混合液显酸性。
据此解答问题。
2.室温下,某二元碱X(OH)2水溶液中相关组分的物质的量分数随溶液pH变化的曲线如图所示,下列说法错误的是A. K b2的数量级为10-8B. X(OH)NO3水溶液显碱性C. 等物质的量的X(NO3)2和X(OH)NO3混合溶液中c(X2+)>c[X(OH)+]D. 在X(OH)NO3水溶液中,c[X(OH)2]+c(OH-)= c(X2+)+ c(H+)【答案】C【解析】分析:本题是一道图形比较熟悉的题目,不过题目将一般使用的二元酸变为了二元碱,所以在分析图示时要随时注意考查的是多元碱的分步电离。
详解:A.选取图中左侧的交点数据,此时,pH=6.2,c[X(OH)+]=c(X2+),所以K b2=,选项A正确。
B.X(OH)NO3水溶液中X的主要存在形式为X(OH)+,由图示X(OH)+占主导位置时,pH为7到8之间,溶液显碱性,选项B正确。
C.等物质的量的X(NO3)2和X(OH)NO3混合溶液中c(X2+)和c[X(OH)+]近似相等,根据图示此时溶液的pH约为6,所以溶液显酸性X2+的水解占主导,所以此时c(X2+)<c[X(OH)+],选项C错误。
D.在X(OH)NO3水溶液中,有电荷守恒:c(NO3-)+c(OH-)=2c(X2+)+c(H+)+c[X(OH)]+,物料守恒:c(NO3-)=c(X2+)+c[X(OH)2]+c[X(OH)]+,将物料守恒带入电荷守恒,将硝酸根离子的浓度消去,得到该溶液的质子守恒式为:c[X(OH)2]+c(OH-)=c(X2+)+c(H+)。
3.25℃时,在“H2A―HA-―A2-”的水溶液体系中,H2A、HA-和A2-三者中各自所占的物质的量分数(α)随溶液pH变化的关系如图所示。
下列说法正确的是A. 在含H2A、HA-和A2-的溶液中,加入少量NaOH固体,α(HA-)一定增大B. 将等物质的量的NaHA和Na2A混合物溶于水,所得的溶液中α(HA-)=α(A2-)C. NaHA溶液中,HA-的水解能力小于HA-的电离能力D. 在含H2A、HA-和A2-的溶液中,若c(H2A)+2c(A2-)+c(OH-)=c(H+),则α(H2A)和α(HA -)一定相等【答案】C【解析】A.根据图像,在含H2A、HA-和A2- 的溶液中,加入少量NaOH固体,溶液的酸性减弱,α(HA-)可能增大,可能减小,与原溶液的成分有关,故A错误;B. 根据图像,将等物质的量的NaHA和Na2A混合物溶于水时,溶液的pH在4~5之间,溶液显酸性,以HA-电离为主,所得的溶液中α(HA-)<α(A2-),故B错误;C.NaHA溶液显酸性,以电离为主,可知其电离程度大于其水解程度,故C正确;D. 在含H2A、HA-和A2-的溶液中,根据电荷守恒,有2c(A2-)+c(OH-)+c(HA-)=c(H+)+ c(Na+),因为c(H2A)+2c(A2-)+c(OH-)=c(H+),则2c(A2-)+c(OH-)+c(HA-)=c(H+)+ c(Na+)=c(H2A)+2c(A2-)+c(OH-)+ c(Na+),因此c(HA-)=c(H2A) + c(Na+),故D错误;故选C。
4.常温下,HA为一元弱酸。
已知溶液中HA、A-的物质的量分数δ随溶液pH变化的曲线如右图所示。
向10mL0.1mol/LHA溶液中,滴加0.1mol/LNaOH溶液x mL。
下列不正确的是A. 常温下,HA的电离平衡常数K a=10-9B. x=0时,1<pH<7C. x=5时,C(A-)=c(HA)D. x=10时,c(A-)+c(HA)=c(Na+)=0.05mol/L【答案】C【解析】A. 当pH值为9时,溶液中c(H+)=1×10-9mol/L,由c(HA)= c(A-)得,K a=10-9,A 正确;B. HA为弱酸,当不添加NaOH时,溶液呈酸性,且不完全电离,c(H+)<0.1mol/L,B 正确;C. 当x=5时,不能将电离出的H+完全中和,溶液呈酸性,C(A-)与c(HA)不相等,C 错误;D. x=10时,溶液体积为20mL,则此时c(A-)+c(HA)==0.05mol/L,c(Na+)=0.05mol/L,D正确。
故选择C。
5.已知常温下,K a1(H2CO3)=4.3×10-7, K a2(H2CO3)=5.6×10-11。
某二元酸H2R及其钠盐的溶液中,H2R、HR-、R2-三者的物质的量分数随溶液pH变化关系如图所示,下列叙述错误的是()A. 在pH=4.3的溶液中:3c(R2-)=c(Na+)+c(H+)-c(OH-)B. 等体积、等浓度的NaOH溶液与H2R溶液混合后,此溶液中水的电离程度比纯水小C. 等浓度的NaOH溶液与H2R溶液按体积比1∶2混合,溶液的pH=1.3D. 向Na2CO3溶液中加入少量H2R溶液,发生反应:2CO32-+H2R=2HCO3-+R2-【答案】C6.常温下,现有0.1mol· L-1NH4HCO3溶液,pH=7.8。
已知含氮(或含碳)各微粒的分布分数(平衡时,各微粒浓度占总微粒浓度之和的分数)与pH 的关系如图所示。
下列说法正确的是A. 当pH=9时,溶液中存在下列关系:c(NH4+)>c(HCO3-)>c(NH3·H2O)>c( CO32-)B. NH4HCO3溶液中存在下列关系:<1C. 向pH=6.5的上述溶液中逐滴滴加氢氧化钠溶液时,NH4+和HCO3-浓度逐渐减小D. 分析可知,常温下水解平衡常数K h(HCO3-)的数量级为10-7【答案】B【解析】分析:A项,由NH3·H2O的分布分数的变化分析NH4+的分布分数的变化,再结合图像判断当pH=9时,溶液中各离子浓度大小;B项,根据碳酸氢铵溶液pH=7.8,判断NH4+与HCO3-的大小关系,结合物料守恒解决该项;C项,结合图像判断滴入氢氧化钠溶液后NH4+和HCO3-浓度变化;D项,利用图像中的特殊点(如pH=6.5时)对应的离子浓度,计算水解平衡常数K h(HCO3-)。
7.25℃时,向20mL 0.1mol/L HAuCl4溶液中滴加0.1mol/LNaOH 溶液,滴定曲线如图1,含氯微粒的物质的量分数(δ) 随pH变化关系如图2,则下列说法不正确的是A. 在c点溶液中: c(Na+)=c(AuCl4-)B. a 点对应溶液pH 约为5C. 25℃时,HAuCl4的电离常数为1×10-3D. d点时,溶液中离子浓度大小关系为: c(Na+)>c(AuCl4-)>c(OH-) >c(H+)【答案】C【解析】c点溶液中,pH=7,c(OH-)=c(H+),根据电荷守恒可知:c(Na+)=c(AuCl4-),A正确;根据Ka= c(H+)×c(AuCl4-)/c(HAuCl4)=10-3×10-3/(0.1-10-3)≈10-5,由于a点时,c(AuCl4-)= c(HAuCl4),所以c(H+)≈10-5mol/L, pH≈5,B正确;0.1mol/LHAuCl4溶液pH=3,根据HAuCl4=H++ AuCl4-可知,该反应的电离常数为Ka=c(H+)×c(AuCl4-)/c(HAuCl4)= 10-3×10-3/(0.1-10-3)=10-5,C错误;d点时,溶液溶质为NaAuCl4,溶液显碱性,所以溶液中离子浓度大小关系为:c(Na+)>c(AuCl4-)>c(OH-)>c(H+),D正确;正确选项C。
8.常温下向100mL0.2mol/L的氨水中逐滴加入0.2mol/L的盐酸,所得溶液中NH4+和NH3·H2O 的物质的量分数φ与加入盐酸的体积V及混合液pH变化的关系如图所示,下列说法正确的是A. 表示NH3·H2O物质的量分数变化的曲线是BB. pH=9.26时的溶液中,NH3·H2O的电离程度小于NH4+的水解程度C. 常温下,NH3·H2O的电离常数为1.8×10-5mol/L (已知lg1.8=0.26)D. 当加入盐酸体积为50mL时,溶液中c(NH4+)-c(NH3·H2O)=2×(10-5+10-9)mol/L【答案】C【解析】NH3·H2O与HCl能够发生反应: NH3·H2O+HCl=NH4Cl+H2O,随着HCl的滴入,NH3·H2O 浓度逐渐减小,NH4+的浓度逐渐增大,所以曲线B表示的是NH4+,不是NH3·H2O的物质的量分数,A选项错误;pH=9.26时,溶液呈碱性,说明NH3·H2O的电离程度大于NH4+离子的水解程度,B选项错误;NH3·H2O NH4++ OH-,K=[C(NH4+)×C(OH-)]/C(NH3·H2O),根据图示得:当PH=9.26时,溶液中NH3·H2O和NH4+的物质的量分数相同,即浓度相同,所以K=C(OH-)=Kw/C(H+)=1×10-14/10-9.26=10-4.74=1.8×10-5,C选项正确;当加入盐酸体积为50mL时,C(Cl-)=1/15mol·L-1,C(NH3·H2O)+C(NH4+)=2/15 mol•L-1,所以有:2C(Cl-)= C(NH3·H2O)+C(NH4+),根据电荷守恒:2C(H+)+2C(NH4+) =2C(Cl-)+2C(OH-),所以c(NH4+)-c(NH3·H2O)=2×(10-5-10-9)mol/L,D选项错误,正确答案是C。