2019化学竞赛—结构化学—晶体结构与对称性
- 格式:ppt
- 大小:5.62 MB
- 文档页数:118

郴州市二中高一化奥班辅导资料——晶体结构(2008-05-28)【涉及概念和内容】根据《化学课程标准》和中学化学教材以及《物质结构与性质》选修教材,晶体结构涉及的内容包括:(1)基本概念:周期性有序排列、晶胞及晶胞类型、晶胞中粒子数的计算、配位数、空隙、堆积方式、晶格能、并置碓砌;(2)堆积方式:面心立方、六方、体心立方和简单立方堆积;(3)晶体种类和性质:金属晶体、离子晶体、分子晶体、原子晶体,自范性、各向异性、金属晶体的导电导热和延展性、X-射线衍射。
这些内容看似零碎,实际上它们有着密切的内在联系,了解和建立它们的关系,对于晶体结构的教与学,深刻理解晶体结构和性质,掌握核心、突出重点都是很重要的。
它们的联系可以用下面的结构表示,其中堆积类型是联系晶体基本概念、基本结构与不同晶体类型的结构和性质的桥梁。
面心立方最密堆积(A1)最密堆积六方最密堆积(A3)体心立方密堆积(A2)简单立方堆积金刚石型堆积(四面体堆积)(A4)一、晶体的结构1、晶体的概念晶体是质点(原子、分子、离子)在空间有规律周期性地重复排列,是具有规则的多面体固体物质。
2自范性:在一定条件下晶体能自动地呈现具有一定对称性的多面体的外形(晶体的形貌)。
非晶体不能呈现多面体的外形。
晶态石英的谱图非晶态石英的谱图3、晶体的点阵结构概念:在晶体内部原子或分子周期性地排列的每个重复单位的相同位置上定一个点,这些点按一定周期性规律排列在空间,这些点构成一个点阵。
点阵是一组无限的点,连结其中任意两点可得一矢量,将各个点阵按此矢量平移能使它复原。
点阵中每个点都具有完全相同的周围环境。
晶体结构= 点阵+ 结构基元结构基元:在晶体的点阵结构中每个点阵所代表的具体内容,包括原子或分子的种类和数量及其在空间按一定方式排列的结构。
(1)直线点阵(2)平面点阵(3)晶胞(晶胞是人为划定的,为平行六面体)空间点阵必可选择3个不相平行的连结相邻两个点阵点的单位矢量a,b,c,它们将点阵划分成并置的平行六面体单位,称为点阵单位。


全国化学竞赛初赛讲义——晶体结构晶体结构是化学竞赛中的重要内容之一、晶体是指由具有有序排列的原子,分子或离子组成的固态物质,具有规则的几何形状。
晶体结构的了解对于理解物质的性质和反应机理非常重要。
下面是晶体结构的讲义。
一、晶体结构的基本概念晶体的结构由最小的重复单元所组成,这个最小重复单元称为晶胞。
晶体结构中的重复单元之间的关系是平移关系,即晶胞通过平移操作得到整个晶体。
晶体结构可以分为离子晶体结构、共价晶体结构和金属晶体结构三种。
离子晶体由阳离子和阴离子组成,通常具有高熔点和硬度,如NaCl、CaF2等。
共价晶体由原子通过共价键相连形成,通常具有高熔点和硬度,如钻石、石墨等。
金属晶体由金属离子通过金属键相连形成,通常具有良好的导电性和延展性,如Cu、Al等。
二、晶体结构的表示方法1.点阵表示法:用数学点阵表示晶体中原子的相对位置关系。
有三种常见的点阵表示方法:简单立方点阵、面心立方点阵和体心立方点阵。
(1)简单立方点阵:晶胞内只含一个原子,每个原子都在晶体的角落上。
(2)面心立方点阵:晶胞内含有4个原子,每个原子都在晶体的角落和晶胞的中心。
(3)体心立方点阵:晶胞内含有2个原子,其中一个原子在晶体的角落上,另一个原子在晶胞的中心。
2.坐标表示法:用坐标系表示晶体中原子的位置。
在二维平面上,可以使用直角坐标系或斜坐标系表示晶体中原子的位置。
直角坐标系中,原子的位置可以用x和y两个坐标表示;斜坐标系中,原子的位置可以用a和b两个坐标表示。
在三维空间中,晶体中原子的位置通常用直角坐标系表示,即通过x、y和z三个坐标来确定原子的位置。
三、晶体的常见缺陷与晶体的生长晶体中常见的缺陷有点缺陷、线缺陷和面缺陷。
1.点缺陷:晶体中原子在其位置上发生的缺失、置换、插入或附加等现象。
(1)缺失缺陷:晶体中缺少一个原子。
(2)置换缺陷:晶体中一个原子被其他原子所替代。
(3)插入缺陷:晶体中多了一个原子。
(4)附加缺陷:晶体中多了一个原子,同时缺少一个原子。

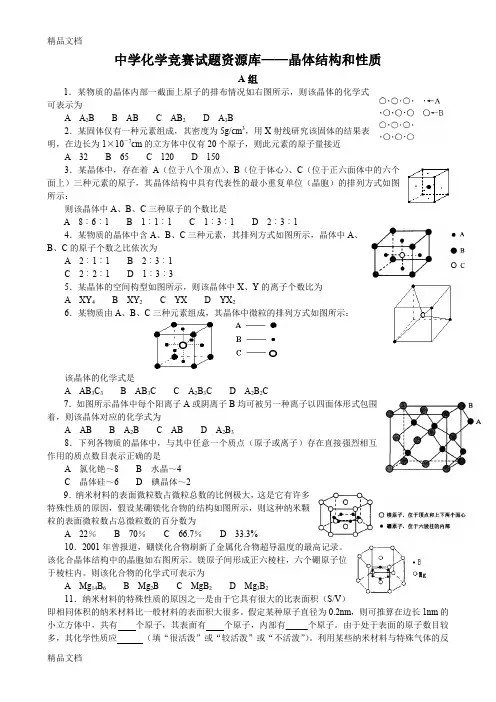
中学化学竞赛试题资源库——晶体结构和性质A组1.某物质的晶体内部一截面上原子的排布情况如右图所示,则该晶体的化学式可表示为A A2B B ABC AB2D A3B2.某固体仅有一种元素组成,其密度为5g/cm3,用X射线研究该固体的结果表明,在边长为1×10-7cm的立方体中仅有20个原子,则此元素的原子量接近A 32B 65C 120D 1503.某晶体中,存在着A(位于八个顶点)、B(位于体心)、C(位于正六面体中的六个面上)三种元素的原子,其晶体结构中具有代表性的最小重复单位(晶胞)的排列方式如图所示:则该晶体中A、B、C三种原子的个数比是A 8︰6︰1B 1︰1︰1C 1︰3︰1D 2︰3︰14.某物质的晶体中含A、B、C三种元素,其排列方式如图所示,晶体中A、B、C的原子个数之比依次为A 2︰1︰1B 2︰3︰1C 2︰2︰1D 1︰3︰35.某晶体的空间构型如图所示,则该晶体中X、Y的离子个数比为A XY4B XY2C YXD YX26.某物质由A、B、C三种元素组成,其晶体中微粒的排列方式如图所示:该晶体的化学式是A AB3C3B AB3C C A2B3CD A2B2C7.如图所示晶体中每个阳离子A或阴离子B均可被另一种离子以四面体形式包围着,则该晶体对应的化学式为A AB B A2BC ABD A2B38.下列各物质的晶体中,与其中任意一个质点(原子或离子)存在直接强烈相互作用的质点数目表示正确的是A 氯化铯~8B 水晶~4C 晶体硅~6D 碘晶体~29.纳米材料的表面微粒数占微粒总数的比例极大,这是它有许多特殊性质的原因,假设某硼镁化合物的结构如图所示,则这种纳米颗粒的表面微粒数占总微粒数的百分数为A 22%B 70%C 66.7%D 33.3%10.2001年曾报道,硼镁化合物刷新了金属化合物超导温度的最高记录。
该化合晶体结构中的晶胞如右图所示。
镁原子间形成正六棱柱,六个硼原子位于棱柱内。

2019化学竞赛—晶体结构出题模式及知识点分析—湖南师范⼤学化学院黄宏新152pdf晶体结构出题模式及知识点分析湖南师范⼤学化学院黄宏新第⼀节点阵理论,布拉维格⼦及平移法的应⽤⼀. 晶体的定义: 微粒在空间作周期性分布.周期: ⼀个重复单位内的内容例画出如下图形的周期结构基元: ⼀个周期中的组成.点阵点: 将⼀个周期压缩成⼀个⼏何点, 表⽰它的⼏何位置.点阵: 由点阵点组成的图形.晶体结构=点阵+结构基元格⼦: 由相邻点阵点组成素向量, 由素向量组成格⼦.晶胞: 格⼦范围内的组成.晶胞=格⼦+结构基元结构基元=晶胞组成/晶胞周期数平移法五个⽤法: 1 画出晶胞; 2 判断点阵形式; 3 判断是否是晶胞; 4判断原⼦的位置; 5 判断原⼦的晶体环境⼆. ⼀维点阵及⼀维晶体例例三. 平⾯点阵1. 正当格⼦: 1对称性⾼, 2 点阵点少2. 平⾯点阵的四种对称类型和五种点阵形式(1) 正⽅格⼦晶胞参数平移法应⽤1:在已知图形中画晶胞(三步骤)1)在图形中选⼀个原⼦(最好是个数少的那种原⼦),然后在邻近找相同的原⼦,连接,假设为向量a,整个图形沿a 平移,如果图形重合,则向量a找成功;2)同法找到向量b;3)以a,b 为邻边作平⾏四边形。
例 1 (中国化学会2003年全国⾼中学⽣化学竞赛试题第6题12分)2003年3⽉⽇本筑波材料科学国家实验室⼀个研究⼩组发现⾸例带结晶⽔的晶体在5K下呈现超导性。
据报道,该晶体的化学式为Na0.35CoO2 ? 1.3H2O,具有……-CoO2-H2O-Na-H2O-……层状结构;在以“CoO2”为最简式表⽰的⼆维结构中,钴原⼦和氧原⼦呈周期性排列,钴原⼦被4个氧原⼦包围,Co-O键等长。
代表氧原⼦,以代表钴原⼦,画出CoO2层的结构,⽤粗线画出两种⼆维晶胞。
使⽤平移法的第⼀个⽤法,有:求出结构基元 (公式:结构基元=晶胞组成/晶胞周期数)(2) 六⽅格⼦例 2 ⽯墨的晶胞: 使⽤平移法的第⼀个⽤法,可以画出晶胞; 求出结构基元例 3⽂献中常⽤下图表达六⽅晶体氟磷灰⽯的晶体结构:该图是c轴投影图,位于图中⼼的球是氟,⼤球是钙,四⾯体是磷酸根(氧原⼦未画出)。

高中化学竞赛经典讲义——晶体结构晶体结构是高中化学竞赛中一个非常重要的知识点。
晶体是由一定数量的离子、分子或原子按照一定的几何排列方式所组成的固体,其最具有代表性的性质就是具有规则的几何形状。
晶体结构的了解对于理解晶体的性质、结构与合成具有重要意义。
晶体结构的揭示是通过实验技术以及理论研究来实现的。
其中最重要的实验手段是X射线衍射。
当X射线穿过晶体时,会产生衍射现象,出现一系列亮斑,这些亮斑的位置和强度依赖于晶体结构。
通过对衍射图像的解析,可以确定晶胞参数,揭示出晶体内部的几何排列。
理论上,可以使用动力学理论计算晶体的结构,得出一系列理论結构参数。
实验与理论的比较可以验证理论的正确性,并进一步完善理论模型。
晶体结构是有一定规律的,可以分为离子晶体和共价晶体两种类型。
离子晶体是由正离子和负离子通过离子键结合而成的晶体。
离子晶体的结构稳定,离子之间的排列有一定的规则。
若正离子与负离子的离子半径比较接近,离子晶体的结构会较紧密,例如氯化钠、氟化钙等。
若离子半径比差异较大,离子晶体的结构则会较为散松,例如氧化银、氧化铅等。
共价晶体是由原子通过共价键结合而成的晶体。
共价晶体的原子之间的键长和键角与几何排列有密切关系。
晶体结构可以通过晶胞参数来描述。
晶胞是晶体的最小重复单元,其正六面体的两边长度为a,与该边垂直的四棱面间的夹角为90°,而与该边相邻的两棱面间的夹角为120°。
晶胞参数a、b、c分别代表了晶体沿三个坐标轴方向的长度,而α、β、γ代表了晶体坐标轴之间的夹角。
晶体结构的描述还需要引入晶体结构中的间隙。
间隙是晶胞中没有原子、离子或分子占据的空隙,可以是正交的,也可以是六角形的。
晶胞中间隙的存在对于许多晶体性质有着重要影响,例如导电性、光学性质等。
为了更好的理解晶体结构,可以引入晶体结构分类的一些基本概念。
首先是晶格点的概念,晶格点是描述晶体排列的重要参考点。
晶格参数是晶体中两个晶格点之间的最短距离,而晶格的基元则是指两个相邻晶格点之间的最短距离。


化学竞赛——晶体结构化学竞赛,晶体结构晶体结构是化学竞赛中的一个重要知识点,它涉及到晶体的组成、结构、性质等方面。
下面我将详细介绍晶体结构的相关知识。
晶体是由原子、离子或分子按照一定的几何规律排列而形成的具有固定形状和结构的物质。
晶体的结构可以分为晶格和晶胞两个层面。
晶格是指晶体中的原子、离子或分子的排列方式。
晶格可以分为三种类型:点阵、空间点阵和布拉维格子。
点阵是指晶体中原子、离子或分子的周期性排列形式,可以分为平面点阵、体心点阵、面心点阵等。
空间点阵是三维空间中具有平移对称性的点的集合,它可以由平面点阵通过添加一个垂直于平面的平移矢量得到。
布拉维格子是指空间中按照一定的几何规律分布的点,它由空间点阵通过移动原点所得到。
晶胞是晶体中一个最小的、具有完整晶体结构的单位。
晶胞可以分为简单晶胞、面心立方晶胞、体心立方晶胞等。
简单晶胞是指由一个或多个原子组成,没有原子在晶体内的重合部分的晶胞。
面心立方晶胞是指在体心立方晶胞的基础上,在每个体心加入了一个原子的晶胞。
体心立方晶胞是指在每个面心和一个体心分别加入一个原子的晶胞。
晶体结构可以通过X射线衍射、电子衍射等实验手段进行研究。
通过这些实验可以确定晶体中原子、离子或分子的位置和排列方式,从而揭示晶体的结构和性质。
晶体结构还可以用来解释化学反应的发生过程。
例如,固态反应与气态反应相比,通常速度较慢。
原因是固态反应需要克服晶体结构的稳定性,使反应物分子能够进入晶体内部,而气态反应则不受晶体结构的限制。
除了晶体结构,晶体中还存在一些缺陷,如点缺陷、线缺陷和面缺陷。
点缺陷是晶体中原子或离子位置的缺陷,如空位、空隙等。
线缺陷是晶体中原子或离子位置的缺陷,如缺陷线、螺旋线等。
面缺陷是晶体中晶面的缺陷,如晶界、孪晶等。
总之,晶体结构是化学竞赛中的一个重要知识点。
它涉及到晶体的组成、结构、性质等方面,对于理解物质的性质和变化过程具有重要意义。
同时,晶体结构的研究也为合成新材料、开发新技术提供了重要的理论基础。


五、晶 体 结 构1. 因为立方晶系中,六个面都是等价的,若有底心立方晶胞存在,则必有面心立方晶胞存在,故立方晶系中不存在底心立方晶胞。
不带电荷的分子或原子(金属)之间的相互作用力小,若原子(非金属)以共价键连接,简单立方中的两个原子之间距离又太大,不利于共价键形成,所以不带电荷的分子或原子往往采取六方或立方最紧密堆积或立方体心密堆积结构。
由于六方最紧密堆积结构与立方紧密堆积的空间利用率相同,所以它们具有相同的密度。
在这两种紧密堆积中,原子的配位数为12。
2. Cu 为面心立方晶体,1个晶胞中Cu 原子个数=8×(18) + 6×(12)= 4(1)(2) =1.119 Å 3. ∵Fe 原子半径是相同的,在α型中,Fe3A 2M N a ααρ=g ,在γ型中, Fe γ3A γ4M N a ρ=g 在α型中,43r a α=,∴43a rα=;在γ型中,42r a γ=,∴22a r γ=∴Fe 3A (43)N rαρ=g ,Fe γ3A (22)N r ρ=g∴ 33γ(22)360.918682(43)r r αρρ===4. (1)(2) 原子堆积系数(100)=2222(4141)0.78544(22)r a r ππ⨯+=== 原子堆积系数(110)=22(414212)0.5554242r a π⨯+⨯== 原子堆积系数(111)= 22(316312)30.90696(12)(2)sin60r a ππ⨯+⨯==⨯o 23A 324A 463.548.936,8.97110(3.165)10m N V N ρ-⨯===⨯⨯⨯ 解得=Cu 42,24r a r a =∴=5. (1 ) MgO 与MnO 的d M —O 相差很大,这说明O 2–围成的正八面体空隙小,而Mg 2+、Mn 2+的半径差别大,导致d MnO >d MgO ;而S 2–和Se 2–半径大,围成的正八面体空隙既大于 ,又大于 ,所以d MgS ~d MnS ,d MgSe =d MnSe ,相当于Mg 2+和Mn 2+在S 2–和Se 2–围成的正八面体空隙中“扰动”。
第五章晶体结构§5-1晶体的点阵理论1. 晶体的结构特征人们对晶体的印象往往和晶莹剔透联系在一起。
公元一世纪的古罗马作家普林尼在《博物志》中,将石英定义为“冰的化石”,并用希腊语中“冰”这个词来称呼晶体。
我国至迟在公元十世纪,就发现了天然的透明晶体经日光照射以后也会出现五色光,因而把这种天然透明晶体叫做"五光石"。
其实,并非所有的晶体都是晶莹剔透的,例如,石墨就是一种不透明的晶体。
日常生活中接触到的食盐、糖、洗涤用碱、金属、岩石、砂子、水泥等都主要由晶体组成,这些物质中的的晶粒大小不一,如,食盐中的晶粒大小以毫米计,金属中的晶粒大小以微米计。
晶体有着广泛的应用。
从日常电器到科学仪器,很多部件都是由各种天然或人工晶体而成,如,石英钟、晶体管,电视机屏幕上的荧光粉,激光器中的宝石,计算机中的磁芯等等。
晶体具有按一定几何规律排列的内部结构,即,晶体由原子(离子、原子团或离子团)近似无限地、在三维空间周期性地呈重复排列而成。
这种结构上的长程有序,是晶体与气体、液体以及非晶态固体的本质区别。
晶体的内部结构称为晶体结构。
晶体的周期性结构,使得晶体具有一些共同的性质:(1) 均匀性晶体中原子周期排布的周期很小,宏观观察分辨不出微观的不连续性,因而,晶体内部各部分的宏观性质(如化学组成、密度)是相同的。
(2) 各向异性在晶体的周期性结构中,不同方向上原子的排列情况不同,使得不同方向上的物理性质呈现差异。
如,电导率、热膨胀系数、折光率、机械强度等。
(3) 自发形成多面体外形无论是天然矿物晶体还是人工合成晶体,在一定的生长条件下,可以形成多面体外形,这是晶体结构的宏观表现之一。
晶体也可以不具有多面体外形,大多数天然和合成固体是多晶体,它们是由许多取向混乱、尺寸不一、形状不规则的小晶体或晶粒的集合。
(4) 具有确定的熔点各个周期内部的原子的排列方式和结合力相同,到达熔点时,各个周期都处于吸热溶化过程,从而使得温度不变。
全国化学竞赛初赛讲义——晶体结构汕头市潮阳第一中学 谢新民 xxmmy@【初赛要求】晶胞。
原子坐标。
晶格能。
晶胞中原子数或分子数的计算及化学式的关系。
分子晶体、原子晶体、离子晶体和金属晶体。
配位数。
晶体的堆积与填隙模型。
常见的晶体结构类型,如NaCl 、CsCl 、闪锌矿(ZnS )、萤石(CaF 2)、金刚石、石墨、硒、冰、干冰、尿素、金红石、钙钛矿、钾、镁、铜等。
点阵的基本概念。
1.晶胞晶体的外表特征是有一定的、整齐的、有规则的凸多面体外形。
晶体的这种外形是晶体中的原子在微观空间里呈周期性整齐排列的结果,为了表达晶体的微观结构,可以从晶体的微观空间中取出一个基本单位,这种基本单位通常是一个平行六面体(如果只研究二维平面则取平行四边形),称为晶胞。
晶胞是晶体微观结构的代表物,这就决定了:一个晶胞的上下左右前后都有与之完全无隙且并置的形状与内容完全相同的晶胞,或者说整个晶体就是晶胞按一定方式并置而成的。
晶胞是晶体中最小的结构单元,但不是最基本的实体,最基本的实体可以看成是原子、分子、离子或原子团。
简而言之,晶胞是晶体中最小的结构单元,它是一个平行六面体,它按一定方式并置就可以得到整个晶体。
晶胞的最基本特征:【问题与思考】下图中的氯化钠晶胞和金刚石晶胞是分别指实线的小立方体还是虚线的大立方体?【分析与归纳】作为晶胞最基本的特征就是顶角、棱、面之间的无差别性,或者说从一个晶胞平移到另一个晶胞,不会察觉是否平移过了。
因此上图中的实线小立方体不是氯化钠晶胞和金刚石的晶胞,因为它们的顶角不同,图中的虚线大立方体才是。
晶胞有两个基本要素:一是晶胞的大小和形状,二是晶胞的内容(晶胞中有哪些微粒以及它们在晶胞中的分布位置)。
晶胞的大小和形状可用晶胞参数来描述。
晶胞的边长a 、b 、c 及它们之间的夹角α、β、γ就规定了晶胞的大小和形状,这些总称晶胞参数(符号定义如下图所示)。
顶角(8个):每个顶角为8个晶胞共用,8个顶角无任何差别。
全国化学竞赛初赛讲义——晶体结构一、晶体结构的概念和基本特点1.晶体结构的定义:晶体是由重复排列的原胞构成的固体。
2.晶体结构的基本特点:(1)有序性:晶体具有一定的有序性,原子、离子或分子排列有规律。
(2)三维性:晶体结构在三个维度上都有周期性重复性。
(3)稳定性:晶体结构对外界条件的变化具有较高的稳定性。
二、晶体结构的描述和表示方法1.晶胞:晶胞是由原胞重复平移所得到的一个最小重复单元,可以完全描述晶体的结构。
2.原胞:原胞是晶体中重复出现的、具有最简单结构的单元。
3.晶体参数:晶体参数包括晶胞的长度和夹角,用来描述晶体的形状和结构特征。
4.晶格:晶格是由原胞构成的、具有无限重复的空间点阵。
晶格可以用晶面和晶轴来表示。
三、晶体的结构类型和晶系分类1.结构类型:晶体的结构类型有离子晶体、共价晶体、金属晶体和分子晶体等。
2.晶系:晶系是根据晶格的对称性将晶体分为不同的类型。
晶系包括立方系、四方系、单斜系、正交系、斜方系、菱方系和三斜系。
四、晶体的基本结构单元1.离子晶体的基本结构单元是离子。
(1)离子晶体的特点:离子晶体由正、负离子通过电荷吸引力相互结合而成。
(2)离子晶体的类型:离子晶体包括简单离子晶体和复式离子晶体。
2.共价晶体的基本结构单元是原子。
(1)共价晶体的特点:共价晶体由共享电子键结合而成,键强较大。
(2)共价晶体的类型:共价晶体包括晶体分子、网络共价晶体和金刚石型晶体。
3.金属晶体的基本结构单元是金属离子。
(1)金属晶体的特点:金属晶体由金属阳离子和自由移动的电子云组成。
(2)金属晶体的类型:金属晶体包括简单金属晶体和合金。
4.分子晶体的基本结构单元是分子。
(1)分子晶体的特点:分子晶体由分子之间的相互作用力相互结合而成。
(2)分子晶体的类型:分子晶体包括极性分子晶体和非极性分子晶体。
五、晶体的性质与应用1.晶体的性质:晶体具有各向异性、光学性、热学性、电学性等特点。
2.晶体的应用:(1)光学应用:晶体在光学领域有着广泛的应用,如光学仪器、激光技术等。