雷诺嗪杂质总结分享
- 格式:pdf
- 大小:112.62 KB
- 文档页数:1

执业药师笔记吩嚷嗪类药物吩嘎嗓类药物结构:抗精神病药,具有硫氮杂]S母核。
鉴别:紫外分光光度法。
氧化反应。
盐酸氯丙嗪鉴别:加硝酸显红色,渐变淡黄色。
盐酸异丙嗪鉴别:加硫酸,显樱桃红色,放置,色渐变深。
加硝酸生成红色沉淀,加热,沉淀溶解,变为橙黄色。
CI-的反应。
加硝酸使成酸性后,加硝酸银试液,即生成白色凝乳状沉淀,分离,沉淀加氨试液即溶解,再加硝酸,沉淀复出现O加等量二氧化猛,混匀,加硫酸湿润,缓缓加热,发生的氮气能使湿润的碘化钾淀粉试纸显蓝色。
含量测定:非水溶液滴定法。
吩嚷嗪类药物母核上缸原子的碱性极弱,不能被滴定,侧链上脂氨基碱性较强,可以用非水溶液滴定法滴定。
一般用冰醋酸或醋肝为溶剂,用高氯酸滴定液滴定,由于为盐酸盐,所以滴定前应加入一定量醋酸汞试液,使生成难离解的氯气化汞,将盐酸盐转化为醋酸盐,再进行滴定。
盐酸异丙嗓用冰醋酸作溶剂,每1ml的高氯酸滴定液(O.1mol/L)相当于32.09mg的C17H20N2S.HCI.盐酸氯丙嗓采用醋酥作溶剂,橙黄IV作指示剂,用高氯酸滴定液滴定。
紫外分光光度法。
本类药物的制剂(如片剂、注射剂)由于辅料有干扰,不能采用非水溶液滴定法滴定,所有一般用紫外分光光度法测定含量。
两个药物的注射剂均加有维生素C作用抗氧化剂,维生素C在243nm处有最大吸收,若在249nm处测定药物含量,则维生素C有干扰。
所以盐酸氯丙嗪和盐酸异丙嗪注射液分别在第三个吸收峰,即306nm和299nm的波长处测定,虽然吸收系数略低,但避开了抗氨化剂维生素C的干扰肾上腺素类药物肾上腺素类药物的结构特点:本类药物具煌氨基侧链,显弱酸性,游离碱溶于有机溶剂,其盐可溶于水;分子中具有邻苯二酚(或苯酚)结构的药物可与重金属离子络合呈色,露置空气中或遇光易筑化,色渐变深,在碱性溶液中更易变色;多数药物分子中有手性碳原子,具有光学活性;苯环上的取代基也各具特性均可供分析用。
有紫外及红外吸收特性。

地氯雷他定杂质汇总1.水分含量:地氯雷他定的水分含量是一种重要的杂质参数。
高水分含量可能会对地氯雷他定的稳定性和质量造成不良影响。
因此,药品生产过程中需要严格控制水分含量。
2.有机杂质:地氯雷他定药物生产过程中可能会残留一些有机杂质。
这些有机杂质可能是由原料、溶剂、反应中产生的副产物等引起的。
常见的有机杂质包括醛、酮、酸、酯等。
这些有机杂质的含量应符合药典或相应法规的规定。
3.金属杂质:地氯雷他定药物中可能存在一定量的金属杂质。
这些金属杂质可以通过原料、溶剂、反应器材等引入。
常见的金属杂质有铁、镍、铜、锌等。
这些杂质的含量应符合药典或相应法规的规定,以保证药物的质量和安全性。
4.不纯物:地氯雷他定药物可能会存在一些不纯物,如杂质、过程废弃物等。
这些不纯物可能会对地氯雷他定药物的质量和安全性产生不良影响。
因此,在药品生产过程中需要对不纯物进行有效的控制和去除。
5.外物:地氯雷他定药物在包装和运输过程中可能会受到外来杂质的污染,如灰尘、微生物等。
这些外物可能会对地氯雷他定药物的质量和安全性产生不良影响。
因此,在包装和运输过程中需要采取相应的措施来保护药物的纯度和无菌性。
综上所述,地氯雷他定药物在生产和使用过程中可能会存在多种杂质,包括水分、有机杂质、金属杂质、不纯物和外物等。
这些杂质对地氯雷他定药物的质量和安全性都有一定的影响。
因此,在药品生产过程中需要严格控制这些杂质的含量,并采取相应的措施来减少杂质的污染。
这样才能保证地氯雷他定药物的质量和安全性,确保患者的用药效果和用药安全。
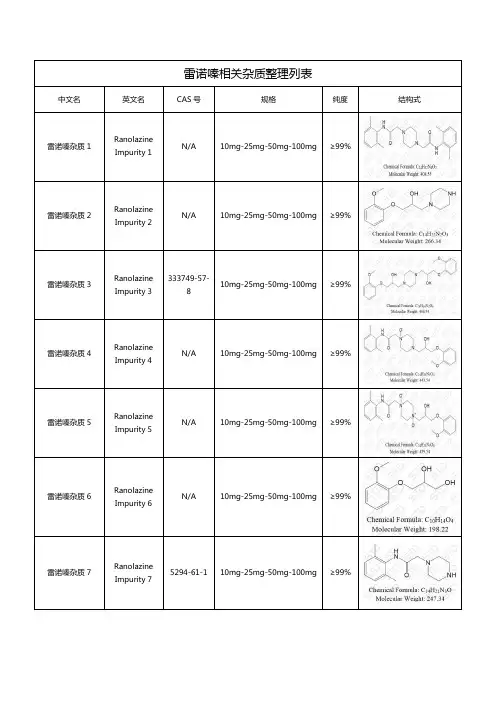
雷诺嗪相关杂质整理列表中文名英文名CAS号规格纯度结构式雷诺嗪杂质1 RanolazineImpurity 1N/A 10mg-25mg-50mg-100mg ≥99%雷诺嗪杂质2 RanolazineImpurity 2N/A 10mg-25mg-50mg-100mg ≥99%雷诺嗪杂质3 RanolazineImpurity 3333749-57-810mg-25mg-50mg-100mg ≥99%雷诺嗪杂质4 RanolazineImpurity 4N/A 10mg-25mg-50mg-100mg ≥99%雷诺嗪杂质5 RanolazineImpurity 5N/A 10mg-25mg-50mg-100mg ≥99%雷诺嗪杂质6 RanolazineImpurity 6N/A 10mg-25mg-50mg-100mg ≥99%雷诺嗪杂质7 RanolazineImpurity 75294-61-1 10mg-25mg-50mg-100mg ≥99%湖北扬信医药科技有限公司经营上万种杂质对照品(优势供应硫酸羟氯喹杂质、硝苯地平杂质、沙丁胺醇杂质、达格列净杂质、厄贝沙坦杂质、阿莫西林克拉维酸钾杂质、利伐沙班杂质、阿托伐他汀钙杂质、西格列汀杂质、利格列汀杂质、、舒更葡糖钠杂质、普乐沙福杂质、紫杉醇杂质、卡前列素杂质、替罗非班杂质、特地唑胺杂质、阿哌沙班杂质、泮托拉唑杂质、叶酸杂质、艾地骨化醇杂质、他克莫司杂质、氯雷他定杂质、尼可地尔杂质等),并代理销售中检所、STD、LGC、TLC、EP、USP、TRC等多个品牌产品,提供上万种标准品对照品,真诚为您服务。
雷诺嗪杂质8 RanolazineImpurity 8N/A 10mg-25mg-50mg-100mg ≥99%雷诺嗪杂质9 RanolazineImpurity 9N/A 10mg-25mg-50mg-100mg ≥99%雷诺嗪杂质优势供应————10mg-25mg-50mg-100mg ≥99%雷诺嗪杂质10 RanolazineImpurity 10N/A 10mg-25mg-50mg-100mg ≥99%雷诺嗪杂质11 RanolazineImpurity 111393717-45-710mg-25mg-50mg-100mg ≥99%雷诺嗪杂质12 RanolazineImpurity 121393717-46-810mg-25mg-50mg-100mg ≥99%。
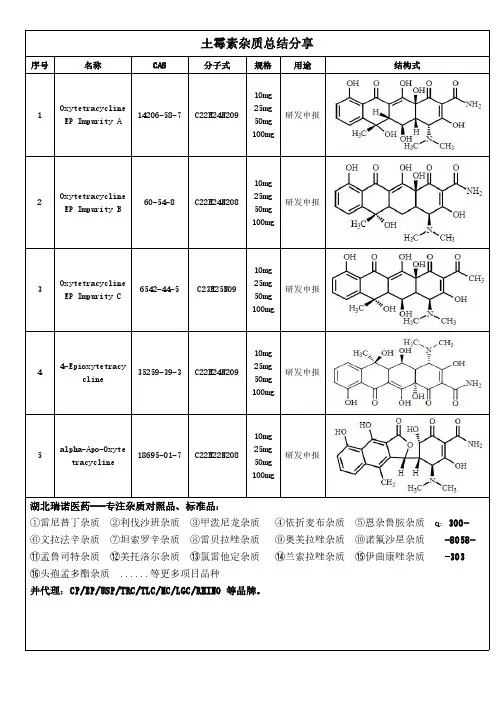

雷诺嗪有关物质及其含量的HPLC快速测定作者:傅收于斐王华栋吴拥军来源:《中国当代医药》2009年第06期[摘要]目的:建立雷诺嗪有关物质及其含量的HPLC测定方法。
方法:以YMC—Pack ODS-A C18 (4.6 mm×l50.O mm,5μm)为色谱柱;流动相为0.05 mol/L磷酸二氢钾缓冲溶液(含0.2%的三乙胺)—乙腈(48:52);流速为1.0 ml/min;进样量为10 μl;检测波长为215 nm。
结果:在0.06-150μg/ml浓度范围内呈良好的线性关系,相关系数1=0.999 9,日内精密度RSD为0.61%,日间精密度RSD为1.40%(n=6);平均回收率为100.5%,RSD为1.3%(n=9)。
结论:本文所建立的方法,简便、重现性好、准确度高,可适用于雷诺嗪及其有关物质的含量测定。
[关键词]雷诺嗪;高效液相色谱法;含量测定;有关物质[中图分类号1 R927,2[文献标识码]A[文章编号]1674-4721(2009)03(b)-012-02心绞痛是冠心病中常见的一类心血管疾病,用于治疗心绞痛的传统药物副作用较大,尤其是对心脏的损害,因此,人们一直致力于寻找更有效、副作用少的新药和新的治疗途径来改善心肌缺血。
一种晚钠离子电流选择性阻滞剂雷诺嗪于2006年由Roche公司在美国正式上市。
它是唯一的不引起心率、血压改变的抗心绞痛药,与其他抗心绞痛药联合应用,也不产生相加作用。
从而避免心脏功能进一步受损害,能提高心绞痛患者的生活质量,具有很好的应用前景。
目前雷诺嗪的测定方法有非水滴定法、紫外分光光度法和高效液相色谱法:《中华人民共和国药典》2005年版也没有雷诺嗪的相关记载。
本文采用反相高效液相色谱法,尝试了不同的色谱分离条件,建立了雷诺嗪及其有关物质含量测定方法,并对方法的专属性和重现性等进行了考察。
1实验仪器与药品1.1仪器Agilent HP1100高效液相色谱仪,G1311A四元梯度洗脱泵(在线脱气);G1316A恒温柱温箱;G1315ADAD检测器;Chemstation色谱工作站。