高中化学新课程总复习(课堂PPT)
- 格式:ppt
- 大小:348.00 KB
- 文档页数:13


高三化学总复习知识点归纳ppt一、化学基础知识回顾1. 元素与化合物元素:由相同类型的原子组成,无法通过化学方法分解为其他物质。
化合物:由多种不同类型的原子以一定比例组成,可以通过化学方法分解为更简单的物质。
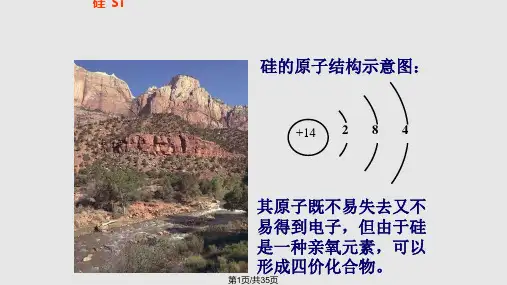
2. 原子结构原子由电子、质子和中子组成。
电子:负电荷,围绕原子核运动。
质子:正电荷,位于原子核内。
中子:无电荷,位于原子核内。
3. 元素周期表元素周期表是按照原子序数排列的,其中元素周期数代表了原子的能级,元素周期表上方的编号为原子序数。
同一周期的元素具有相似的化学性质,同一族的元素具有相似的电子结构和性质。
4. 化学键化学键是原子之间形成的相互连接的力。
离子键:形成于金属和非金属元素之间,其中金属元素失去电子成正离子,非金属元素获得电子成负离子。
共价键:形成于非金属元素之间,原子通过共享电子来达到稳定的电子结构。
5. 配位化合物配位化合物是由一个中心金属离子与周围配位体(通常是非金属离子或分子)形成的化合物。
配位化合物的性质受中心金属离子和配体的种类、数量和配位方式影响。
二、化学反应与化学方程式1. 反应类型- 合成反应:两个或多个物质结合形成一个新的化合物。
- 分解反应:一个化合物分解为两个或多个简单物质。
- 单一置换反应:一种元素或离子取代另一种化合物中的元素或离子。
- 双置换反应:两种化合物中的离子互相交换。
2. 化学方程式的表示方法化学方程式用符号和化学式表示,包括反应物、生成物和反应条件。
反应物在化学方程式的左侧,生成物在化学方程式的右侧,用箭头(→)表示反应方向。
三、物质的量与摩尔1. 原子量与相对分子质量原子量:元素的相对原子质量,以碳-12的质量为准。
相对分子质量:化合物中各种原子的相对原子质量之和。
2. 摩尔与摩尔质量摩尔:物质的量的单位,用符号“mol”表示。
摩尔质量:1摩尔物质的质量,单位是克/mol。
3. 摩尔与化学方程式的关系化学方程式中的系数表示物质的物质的摩尔比,可以用来推算反应物和生成物的摩尔比。