上海市各区2018届中考化学二模试题分类汇编 电解质溶液试题(有答案)最新
- 格式:doc
- 大小:209.00 KB
- 文档页数:9
热化学【2018年上海长宁区二模】7. 下列变化会放出热量的是()A.碘升华 B.冰融化 C.氢氧化钠溶于水 D.氯化铵溶于水【答案】C【2018年上海长宁区二模】12. 下列表示吸热反应的图像是()【答案】A【2018年上海长宁区二模】14.下列关于钢铁发生吸氧腐蚀的分析正确的是()A.吸氧腐蚀是吸热反应 B.铁作原电池正极C.正极电极反应为:2H2O+O2+4e→4OH-D. 原电池负极反应为:Fe-3e→Fe3+ 【答案】C【2018年上海杨浦区二模】10. 下列反应中的能量变化与图示一致的()A. 盐酸和NaOH溶液混合是B. CH4在空气中燃烧C. Al与Fe2O3反应D. 电解水得到H2和O2【答案】D【2018年上海闵行区二模】11.关于硝酸铵说法正确的是()A.属于共价化合物 B.溶于水放热 C.受热易分解 D.属于有机氮肥【答案】C【2018年上海闵行区二模】20.恒容密闭容器中发生反应:SiO 2(s)+4HF(g)SiF4(g)+2H2O(g)+148.9 kJ。
叙述错误的是()A.反应物的总能量高于生成物的总能量B.若生成2mol液态水,则放出的热量大于148.9 kJC.当v正(HF)=2v逆(H2O)时,反应达到平衡状态D.平衡后放出的热量随加入SiO2量的增加而增大【答案】D【2018年上海奉贤区二模】16.已知2SO2(g)+O2(g) 2SO3(g)+Q kJ·mol-1(Q>0)。
下列说法正确的是()A.相同条件下,2molSO2(g)和1molO2(g)所具有的能量小于2molSO3(g)所具有的能量B.将2molSO2(g)和1molO2(g)充分反应可放出的热量为Q kJC.增大压强或升高温度,该平衡都向逆反应方向移动D.若充分反应后放热Q kJ,则此过程中有2molSO2(g)被氧化【答案】D【2018年上海奉贤区二模】17.下图是2SO3(g) ⇌ 2SO2(g) + O2(g) 的能量变化图,据图得出的相关叙述正确的是()A.2SO3(g) ⇌ 2SO2(g) + O2(g) + (a-b) kJB.1mol SO2的能量比1mol SO3的能量高C.若有2mol SO3充分反应,吸收(a-b) kJ热量D.该化学反应过程中的能量变化既有吸热又有放热【答案】D【2018年上海青浦区二模】6.下列变化过程中Q>0的是()A.CH3COOH CH3COO-+ H+ + QB. CaCO3(s)→ CaO(s)+ CO2(g)+ QC.S2- + H 2O HS- + OH- + QD.S(g)→S(l)+ Q【答案】D【2018年上海青浦区二模】9.下列试剂或方法肯定不能鉴别氯化钠和氯化铵固体的是() A.观察颜色 B.加热 C.加水 D.加紫色石蕊试液【答案】A【2018年上海普陀区二模】15、反应2A(g)+B(g)2C(g)的能量变化如图所示,下列说法错误的是()A. 加入催化剂,X点位置不变B. 加入催化剂,G的大小不变C. 该反应为放热反应D. 反应热为E与G的和【答案】D【2018年上海浦东新区二模】5.化学反应中的能量变化符合右图所示的是()A. 甲烷燃烧B. 碳酸钙高温分解C. 电石与水反应D. 酸碱中和【答案】B【2018年上海静安区二模】6. 下列过程的热效应属于吸热的是()A. 碘蒸气的凝华B.化学反应中化学键的形成C. 铝热反应D. 氯化铵的水解【答案】D【2018年上海静安区二模】17.已知C2H2 (g) + 52O2 (g) → 2CO2 (g) + H2O (g)+1256 kJ,下列说法正确的是()A.1 份乙炔完全燃烧可放热1256 kJ B.反应中乙炔做还原剂、被还原C.乙炔完全燃烧时,生成2 mol液态水,所放热量小于2512 kJD.若有10 mol电子发生转移,则需消耗2.5 mol O2【答案】D【2018年上海金山区二模】7.下列过程能实现化学能转化为热能的是()A.光合作用B.木炭燃烧C.风力发电D.电解饱和食盐水【答案】B【2018年上海嘉定区二模】10.合成氨反应过程中的能量变化如图所示,下列说法正确的是()A.反应体系中加入催化剂,会改变反应的热效应B.反应物的总能量低于生成物的总能量C.该反应的热化学方程式为 3H2(g)+N2(g)2NH3(g)+Q(Q>0)D.该反应是吸热反应【答案】C【2018年上海宝山区二模】8.下列固体溶于水时吸热的是()A. 氯化铵B.氢氧化钠C. 氧化钙D. 过氧化钠【答案】A【2018年上海宝山区二模】10.已知1mol氢气和氧气完全燃烧生成水蒸气放出241.8千焦热量,下列热化学方程式正确的是()A. 2H2(g)+O2(g)→2H2O(g)+241.8kJB. H2(g)+1/2O2(g)→H2O(s)+241.8 kJC. H2(g)+1/2O2(g)→H2O(g)-241.8D. H2O(g)→H2(g)+1/2O2(g)-241.8 kJ kJ【答案】D【2018年上海徐汇区二模】8.分析右面的能量变化示意图,下列热化学方程式正确的是()A.2A(g) + B(g) → 2C(g) - Q B.2A(g) + B(g) → 2C(g) + Q C.2A + B → 2C + Q D.2C → 2A + B - Q【答案】B。

燃烧与灭火【2018年上海宝山区一模】30.X 是一种常用能源,X 完全燃烧的化学方程式:X+3O 2−−−→点燃2CO 2+3H 2O ,则X 的化学式为( ) A. C 2H 6 B. C 2H 6OC. C 2H 4OD. C 2H 4O 2【答案】 B【2018年上海宝山区一模】40.下列做法错误的是( )A. 进入废气矿井,火把照明B. 油锅着火,盖锅盖灭火C. 电器着火,用水浇灭D. 架空柴火,火烧得更旺 【答案】 C【2018年上海奉贤区一模】44. 将燃着的蜡烛放在如右图1所示的密闭容器中,同时用氧气传感器测出密闭容器中氧气含量的变化如右图2所示,下列说法正确的是( )A. 蜡烛燃烧前瓶内只有氧气B. 蜡烛熄灭是因为瓶内没有氧气C. 蜡烛熄灭后瓶内只剩二氧化碳气体D. 氧气浓度小于一定值时,蜡烛无法燃烧【答案】 D【2018年上海奉贤区一模节选】47. 在人们担心化石能源将被耗尽时,科学家发现海底埋藏着大量可燃烧的“冰”---“可燃冰”,可燃冰外观像冰。
主要含有甲烷水合物,还含少量二氧化碳等物质。
2017年5月,我国在南海成功试采可燃冰,它将推动世界能源利用格局的改变。
④甲烷(4CH )中氢元素为+1价,碳元素为______价,甲烷充分燃烧的化学方程式_________。
⑤从环境保护的角度考虑,下列燃料中最理想的是____________。
(填字母序号) A. 甲烷 B. 煤 C. 氢气 D. 汽油【答案】④-4;CH 4+2O 2−−−→点燃CO 2+2H 2O ⑤C 【2018年上海闵行区一模节选】③水在化学实验中的作用不可小觑。
A. 电解水B. 硫燃烧C. 铁丝燃烧D. 燃烧条件探究E. 保存白磷 IV. D 可以探究可燃物燃烧的条件是_______________________________ V. 上述实验中,水用来隔绝空气的是______________(填字母序号)。

2017学年第二学期徐汇区学习能力诊断卷初三理化试卷化学部分2018.4相对原子质量:H-1 C-12 N-14 O-16 S-32 Cl-35.5Na-23 Mg-24 Al-27 K-39 Ca-40 Fe-56 Cu-64 Zn-65六、选择题(共20分)27.生活中常见的物质变化,属于化学变化的是A.冰融化成水 B.玻璃破碎 C.铁制品生锈 D.酒精挥发28.光变色防伪油墨中含有MgF2,MgF2中F的化合价为A.+2B. +1C. -1D.-229.厨房中常用的物种中,不属于有机物的是A.食盐 B.甲烷 C.蔗糖 D.淀粉30.物质的化学式书写正确的是A.氯化铝-AlCl B.硝酸钠-NaNO3 C.氢氧化铜-CuOH D.氧化镁-OMg31.下列符号中只表示微观意义的是A.H2B.FeC.COD.3H2O32.规范的实验操作时实验成功的必要条件。
下列实验操作中,正确的是A. 给液体加热B. 滴加试剂C. 读取液体体积D. 移走蒸发皿33.保护环境,节约资源。
下列做法正确的是A.将工厂废液直接排入江河B.将煤脱硫处理后再燃烧C.自来水价格便宜,可以尽情使用D.废旧电池掩埋在土壤中34.测定溶液的酸碱性强弱应选用的是A.酚酞试液B. pH试纸C.石蕊试液D.蓝色石蕊试纸35.关于溶液的叙述正确的是A.溶液中各部分的性质不同B.凡是均一稳定的液体都是溶液C.饱和溶液一定是浓溶液D.医用生理盐水是溶液高温Si+2CO ↑,该反应的基本类型是36.生产单质硅的过程中有一个重要反应:SiO2+2C −−−→A.化合反应B. 分解反应C.置换反应D.复分解反应37.物质的性质决定其用途,有关物质的性质与用途对应正确的是A.氢氧化钠固体能吸水,可用来干燥CO 2气体B.利用氧气的可燃性做火箭燃料C.盐酸可用于焊接金属前除去金属表面的锈D.氦气的化学性质稳定,可用作霓虹灯 38.右图是某个化学反应前后的微观模拟图,、表示不同元素的原子,下列叙述正确的是A.反应物a 、b 是由原子构成的,生成物c 是由分子构成的B.该反应的基本反应类型为置换反应C.该反应中的生成物一定属于氧化反应D.该化学反应中,反应物和生成物a 、b 、c 的微粒个数之比为1:3:2 39.能正确反映我国早在西汉发现,宋初应用的湿法炼铜反应原理的是A.2CuO+C −−−→高温2Cu+CO ↑B.Hg+CuCl 2→Cu+ HgCl 2 C.2Fe+3CuSO 4→3Cu+Fe 2(SO 4)3D. Fe+CuSO 4→Cu+FeSO 440.木炭在耐高温的容器中(内含足量空气),密封加热,下列各图中,能正确表示容器中所盛的气体总质量变化的是41.对有关实验现象的描述正确的是 A. 氯化铁溶液中滴加氢氧化钠溶液,黄色溶液变成红褐色溶液 B. 硫在氧气中燃烧发出明亮的黄色火焰 C. 打开浓盐酸的瓶盖,瓶口出现大量白雾D. 镁条在氧气中燃烧,火星四射,生成黑色固体物质42.在硝酸银和硝酸铜的混合溶液中,加入一定量的铁粉,充分反应后,有少量金属析出,过滤后,向滤液中滴加稀盐酸,有白色沉淀析出,则析出的少量金属是A.铜B.银C.铁和铜D.铜和银 43.与碳酸钠、硫酸钠、硝酸镁三种溶液都能发生反应,且都有白色沉淀生成的是A.氯化钡溶液B.氢氧化钾溶液C.氯化钙溶液D.氢氧化钡溶液 44.对物质的量的理解正确的是A.物质的量就是6.02⨯1023个微粒的集合体,单位是molB.1molO 3和1.5molO 2含有相同数目的氧原子C.物质的量就是物质所含微粒的数量D.任何物质的摩尔质量就是它的相对原子质量或相对分子质量45.图1是甲、乙两种物质的溶解度曲线。

电解质溶液【2018年上海长宁二模】10. 对于常温下1升pH=1的硝酸溶液,下列叙述正确的是( ) A.该溶液lmL 稀释至100mL 后,pH 等于3B.向该溶液中加入含0.1mol 氢氧化钡的溶液恰好完全中和C.该溶液中硝酸电离出的c(H+)等于水电离出的c(H+)D.该溶液中硝酸电离出的c(H+)是水电离出的c(H+)的100倍 【答案】A【2018年上海杨浦区二模】20. 25℃,有两种盐的稀溶液,分别是a mol/L NaX 溶液和b mol/L NaY 溶液,下列判断错误的是( )A. 若a b >,测得(X )(Y )c c --=,则溶液中的(HX)(HY)c c >B. 若a b >,测得(HX)(HY)c c >,则溶液中的(X )(Y )c c --=C. 若a b =,且pH(NaX)pH(NaY)>,则酸性:HX HY <D. 若a b =,并测得(X )(Y )(HY)a c c c --==+,则HX 是强酸,HY 是弱酸 【答案】B【2018年上海杨浦区二模节选】28. Na 2SO 3和NaHSO 3混合溶液的pH 随Na 2SO 3和NaHSO 3比例的不同而不同,数据如下:表中第________组(填写序号)数据,可判断NaHSO 3溶液显_______性(填“酸”或“碱”)。
29. NaHSO 3既能和强酸反应也能和强碱溶液反应。
用平衡移动原理说明NaHSO 3能和强碱溶液反应的原因:_________________________________________________________。
【答案】28. ③;酸29. NaHSO 3溶液中HSO 3-发生电离:HSO 3-H ++SO 3-,电离出的H +与强碱溶液中的OH -发生反应,其浓度降低,平衡正向移动,使反应能持续进行。
【2018年上海闵行区二模】17.室温时,0.1 mol/L某酸HA溶液的pH=3。

定量实验【2018年上海市长宁区二模】15. 配制250 mL 0.100 mol/L的氯化钠溶液,操作错误的是()【答案】C【2018年上海市长宁区二模节选】(三)(本题共15分)无水MgBr2可广泛用于有机反应催化剂、污水处理剂等。
实验室可用镁屑与液溴为原料,采用下图装置制备无水MgBr2,请回答:33.为测定产品的纯度,可用EDTA(简写为Y4-)标准溶液滴定,反应的离子方程式:Mg2++ Y4-====Mg Y2-①滴定前润洗滴定管的操作方法是。
②测定前,先称取0.2500g无水MgBr2产品,溶解后,用0.0500 mol/L的EDTA标准溶液滴定至终点,消耗EDTA标准溶液26.50 mL,则测得无水MgBr2产品的纯度是____________(以质量分数表示)。
【答案】33.(每空2分,共4分)①从滴定管上口加入少量标准液,倾斜着转动滴定管,使液体润湿内壁,然后从下部放出,重复2-3次②97.5%【2018年上海市闵行区二模】(三) (本题共15分)小苏打是一种常用的食品添加剂。
31.精制食盐是制备小苏打的原料之一。
粗盐中含有少量Ca 2+、Mg 2+、SO 42-,粗盐精制的 步骤顺序是:溶解→ → → → (填字母编号)。
a .加盐酸调pH b .加Ba(OH)2溶液 c .加Na 2CO 3溶液 d .过滤 32.NH 3、CO 2先后通入饱和食盐水中,反应的离子方程式________________。
33.侯氏制碱法中,母液的处理方法是通入氨气,再加入细小食盐颗粒,最后冷却析出的副产品是_______;简述通氨气的作用____________________________________。
33. 称取2.640 g 小苏打样品(含少量NaCl),配置成250 mL 溶液,准确取出20.00 mL溶液于锥形瓶中,滴加_______作指示剂,滴定时消耗0.1000 mol/L 盐酸的体积为20.67 mL 。
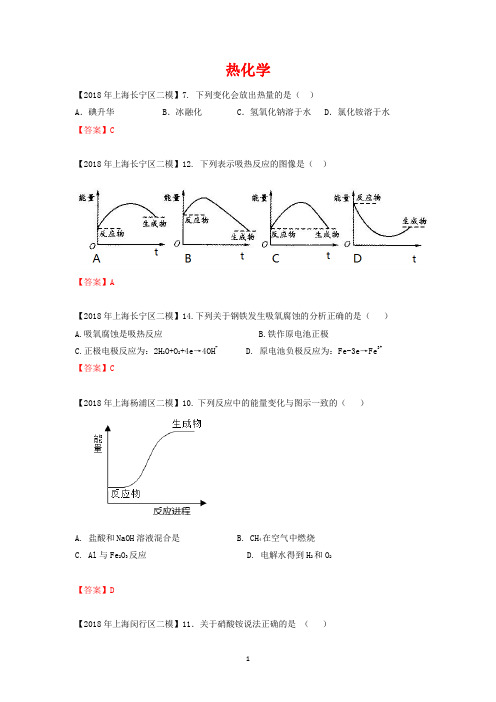
热化学【2018年上海长宁区二模】7. 下列变化会放出热量的是()A.碘升华 B.冰融化 C.氢氧化钠溶于水 D.氯化铵溶于水【答案】C【2018年上海长宁区二模】12. 下列表示吸热反应的图像是()【答案】A【2018年上海长宁区二模】14.下列关于钢铁发生吸氧腐蚀的分析正确的是()A.吸氧腐蚀是吸热反应 B.铁作原电池正极C.正极电极反应为:2H2O+O2+4e→4OH-D. 原电池负极反应为:Fe-3e→Fe3+ 【答案】C【2018年上海杨浦区二模】10. 下列反应中的能量变化与图示一致的()A. 盐酸和NaOH溶液混合是B. CH4在空气中燃烧C. Al与Fe2O3反应D. 电解水得到H2和O2【答案】D【2018年上海闵行区二模】11.关于硝酸铵说法正确的是()A.属于共价化合物 B.溶于水放热 C.受热易分解 D.属于有机氮肥【答案】C【2018年上海闵行区二模】20.恒容密闭容器中发生反应:SiO 2(s)+4HF(g)SiF4(g)+2H2O(g)+148.9 kJ。
叙述错误的是()A.反应物的总能量高于生成物的总能量B.若生成2mol液态水,则放出的热量大于148.9 kJC.当v正(HF)=2v逆(H2O)时,反应达到平衡状态D.平衡后放出的热量随加入SiO2量的增加而增大【答案】D【2018年上海奉贤区二模】16.已知2SO2(g)+O2(g) 2SO3(g)+Q kJ·mol-1(Q>0)。
下列说法正确的是()A.相同条件下,2molSO2(g)和1molO2(g)所具有的能量小于2molSO3(g)所具有的能量B.将2molSO2(g)和1molO2(g)充分反应可放出的热量为Q kJC.增大压强或升高温度,该平衡都向逆反应方向移动D.若充分反应后放热Q kJ,则此过程中有2molSO2(g)被氧化【答案】D【2018年上海奉贤区二模】17.下图是2SO3(g) ⇌ 2SO2(g) + O2(g) 的能量变化图,据图得出的相关叙述正确的是()A.2SO3(g) ⇌ 2SO2(g) + O2(g) + (a-b) kJB.1mol SO2的能量比1mol SO3的能量高C.若有2mol SO3充分反应,吸收(a-b) kJ热量D.该化学反应过程中的能量变化既有吸热又有放热【答案】D【2018年上海青浦区二模】6.下列变化过程中Q>0的是()A.CH3COOH CH3COO-+ H+ + QB. CaCO3(s)→ CaO(s)+ CO2(g)+ QC.S2- + H 2O HS- + OH- + QD.S(g)→S(l)+ Q【答案】D【2018年上海青浦区二模】9.下列试剂或方法肯定不能鉴别氯化钠和氯化铵固体的是() A.观察颜色 B.加热 C.加水 D.加紫色石蕊试液【答案】A【2018年上海普陀区二模】15、反应2A(g)+B(g)2C(g)的能量变化如图所示,下列说法错误的是()A. 加入催化剂,X点位置不变B. 加入催化剂,G的大小不变C. 该反应为放热反应D. 反应热为E与G的和【答案】D【2018年上海浦东新区二模】5.化学反应中的能量变化符合右图所示的是()A. 甲烷燃烧B. 碳酸钙高温分解C. 电石与水反应D. 酸碱中和【答案】B【2018年上海静安区二模】6. 下列过程的热效应属于吸热的是()A. 碘蒸气的凝华B.化学反应中化学键的形成C. 铝热反应D. 氯化铵的水解【答案】D【2018年上海静安区二模】17.已知C2H2 (g) + 52O2 (g) → 2CO2 (g) + H2O (g)+1256 kJ,下列说法正确的是()A.1 份乙炔完全燃烧可放热1256 kJ B.反应中乙炔做还原剂、被还原C.乙炔完全燃烧时,生成2 mol液态水,所放热量小于2512 kJD.若有10 mol电子发生转移,则需消耗2.5 mol O2【答案】D【2018年上海金山区二模】7.下列过程能实现化学能转化为热能的是()A.光合作用B.木炭燃烧C.风力发电D.电解饱和食盐水【答案】B【2018年上海嘉定区二模】10.合成氨反应过程中的能量变化如图所示,下列说法正确的是()A.反应体系中加入催化剂,会改变反应的热效应B.反应物的总能量低于生成物的总能量C.该反应的热化学方程式为 3H 2(g)+N2(g)2NH3(g)+Q(Q>0)D.该反应是吸热反应【答案】C【2018年上海宝山区二模】8.下列固体溶于水时吸热的是()A. 氯化铵B.氢氧化钠C. 氧化钙D. 过氧化钠【答案】A【2018年上海宝山区二模】10.已知1mol氢气和氧气完全燃烧生成水蒸气放出241.8千焦热量,下列热化学方程式正确的是()A. 2H2(g)+O2(g)→2H2O(g)+241.8kJB. H2(g)+1/2O2(g)→H2O(s)+241.8 kJC. H2(g)+1/2O2(g)→H2O(g)-241.8 kJD. H2O(g)→H2(g)+1/2O2(g)-241.8 kJ 【答案】D【2018年上海徐汇区二模】8.分析右面的能量变化示意图,下列热化学方程式正确的是()A.2A(g) + B(g) → 2C(g) - Q B.2A(g) + B(g) → 2C(g) + Q C.2A + B → 2C + Q D.2C → 2A + B - Q【答案】B。
热化学【2018年上海长宁区二模】7. 下列变化会放出热量的是()A.碘升华 B.冰融化 C.氢氧化钠溶于水 D.氯化铵溶于水【答案】C【2018年上海长宁区二模】12. 下列表示吸热反应的图像是()【答案】A【2018年上海长宁区二模】14.下列关于钢铁发生吸氧腐蚀的分析正确的是()A.吸氧腐蚀是吸热反应 B.铁作原电池正极C.正极电极反应为:2H2O+O2+4e→4OH-D. 原电池负极反应为:Fe-3e→Fe3+ 【答案】C【2018年上海杨浦区二模】10. 下列反应中的能量变化与图示一致的()A. 盐酸和NaOH溶液混合是B. CH4在空气中燃烧C. Al与Fe2O3反应D. 电解水得到H2和O2【答案】D【2018年上海闵行区二模】11.关于硝酸铵说法正确的是()A.属于共价化合物 B.溶于水放热 C.受热易分解 D.属于有机氮肥【答案】C【2018年上海闵行区二模】20.恒容密闭容器中发生反应:SiO 2(s)+4HF(g)SiF4(g)+2H2O(g)+148.9 kJ。
叙述错误的是()A.反应物的总能量高于生成物的总能量B.若生成2mol液态水,则放出的热量大于148.9 kJC.当v正(HF)=2v逆(H2O)时,反应达到平衡状态D.平衡后放出的热量随加入SiO2量的增加而增大【答案】D【2018年上海奉贤区二模】16.已知2SO2(g)+O2(g) 2SO3(g)+Q kJ·mol-1(Q>0)。
下列说法正确的是()A.相同条件下,2molSO2(g)和1molO2(g)所具有的能量小于2molSO3(g)所具有的能量B.将2molSO2(g)和1molO2(g)充分反应可放出的热量为Q kJC.增大压强或升高温度,该平衡都向逆反应方向移动D.若充分反应后放热Q kJ,则此过程中有2molSO2(g)被氧化【答案】D【2018年上海奉贤区二模】17.下图是2SO3(g) ⇌ 2SO2(g) + O2(g) 的能量变化图,据图得出的相关叙述正确的是()A.2SO3(g) ⇌ 2SO2(g) + O2(g) + (a-b) kJB.1mol SO2的能量比1mol SO3的能量高C.若有2mol SO3充分反应,吸收(a-b) kJ热量D.该化学反应过程中的能量变化既有吸热又有放热【答案】D【2018年上海青浦区二模】6.下列变化过程中Q>0的是()A.CH 3COOH CH3COO-+ H+ + QB. CaCO3(s)→ CaO(s)+ CO2(g)+ QC.S2- + H 2O HS- + OH- + QD.S(g)→S(l)+ Q【答案】D【2018年上海青浦区二模】9.下列试剂或方法肯定不能鉴别氯化钠和氯化铵固体的是() A.观察颜色 B.加热 C.加水 D.加紫色石蕊试液【答案】A【2018年上海普陀区二模】15、反应2A(g)+B(g)2C(g)的能量变化如图所示,下列说法错误的是()A. 加入催化剂,X点位置不变B. 加入催化剂,G的大小不变C. 该反应为放热反应D. 反应热为E与G的和【答案】D【2018年上海浦东新区二模】5.化学反应中的能量变化符合右图所示的是()A. 甲烷燃烧B. 碳酸钙高温分解C. 电石与水反应D. 酸碱中和【答案】B【2018年上海静安区二模】6. 下列过程的热效应属于吸热的是()A. 碘蒸气的凝华B.化学反应中化学键的形成C. 铝热反应D. 氯化铵的水解【答案】D【2018年上海静安区二模】17.已知C2H2 (g) + 52O2 (g) → 2CO2 (g) + H2O (g)+1256 kJ,下列说法正确的是()A.1 份乙炔完全燃烧可放热1256 kJB.反应中乙炔做还原剂、被还原C.乙炔完全燃烧时,生成2 mol液态水,所放热量小于2512 kJD.若有10 mol电子发生转移,则需消耗2.5 mol O2【答案】D【2018年上海金山区二模】7.下列过程能实现化学能转化为热能的是()A.光合作用B.木炭燃烧C.风力发电D.电解饱和食盐水【答案】B【2018年上海嘉定区二模】10.合成氨反应过程中的能量变化如图所示,下列说法正确的是()A.反应体系中加入催化剂,会改变反应的热效应B.反应物的总能量低于生成物的总能量C.该反应的热化学方程式为 3H 2(g)+N2(g)2NH3(g)+Q(Q>0)D.该反应是吸热反应【答案】C【2018年上海宝山区二模】8.下列固体溶于水时吸热的是()A. 氯化铵B.氢氧化钠C. 氧化钙D. 过氧化钠【答案】A【2018年上海宝山区二模】10.已知1mol氢气和氧气完全燃烧生成水蒸气放出241.8千焦热量,下列热化学方程式正确的是()A. 2H2(g)+O2(g)→2H2O(g)+241.8kJB. H2(g)+1/2O2(g)→H2O(s)+241.8 kJC. H2(g)+1/2O2(g)→H2O(g)-241.8 kJD. H2O(g)→H2(g)+1/2O2(g)-241.8 kJ 【答案】D【2018年上海徐汇区二模】8.分析右面的能量变化示意图,下列热化学方程式正确的是()A.2A(g) + B(g) → 2C(g) - Q B.2A(g) + B(g) → 2C(g) + QC.2A + B → 2C + Q D.2C → 2A + B - Q【答案】B。
定量实验【2018年上海市长宁区二模】15. 配制250 mL 0.100 mol/L的氯化钠溶液,操作错误的是()【答案】C【2018年上海市长宁区二模节选】(三)(本题共15分)无水MgBr2可广泛用于有机反应催化剂、污水处理剂等。
实验室可用镁屑与液溴为原料,采用下图装置制备无水MgBr2,请回答:33.为测定产品的纯度,可用EDTA(简写为Y4-)标准溶液滴定,反应的离子方程式:Mg2++ Y4-====Mg Y2-①滴定前润洗滴定管的操作方法是。
②测定前,先称取0.2500g无水MgBr2产品,溶解后,用0.0500 mol/L的EDTA标准溶液滴定至终点,消耗EDTA标准溶液26.50 mL,则测得无水MgBr2产品的纯度是____________(以质量分数表示)。
【答案】33.(每空2分,共4分)①从滴定管上口加入少量标准液,倾斜着转动滴定管,使液体润湿内壁,然后从下部放出,重复2-3次②97.5%【2018年上海市闵行区二模】(三) (本题共15分)小苏打是一种常用的食品添加剂。
31.精制食盐是制备小苏打的原料之一。
粗盐中含有少量Ca2+、Mg2+、SO42-,粗盐精制的步骤顺序是:溶解→→→→ (填字母编号)。
a.加盐酸调pH b.加Ba(OH)2溶液 c.加Na2CO3溶液 d.过滤32.NH3、CO2先后通入饱和食盐水中,反应的离子方程式________________。
33.侯氏制碱法中,母液的处理方法是通入氨气,再加入细小食盐颗粒,最后冷却析出的副产品是_______;简述通氨气的作用____________________________________。
33.称取2.640 g小苏打样品(含少量NaCl),配置成250 mL溶液,准确取出20.00 mL溶液于锥形瓶中,滴加_______作指示剂,滴定时消耗0.1000 mol/L盐酸的体积为20.67 mL。
则该样品中碳酸氢钠的质量分数为(保留两位小数)。
定量实验【2018年上海市长宁区二模】15. 配制250 mL 0.100 mol/L的氯化钠溶液,操作错误的是()【答案】C【2018年上海市长宁区二模节选】(三)(本题共15分)无水MgBr2可广泛用于有机反应催化剂、污水处理剂等。
实验室可用镁屑与液溴为原料,采用下图装置制备无水MgBr2,请回答:33.为测定产品的纯度,可用EDTA(简写为Y4-)标准溶液滴定,反应的离子方程式:Mg2++ Y4-====Mg Y2-①滴定前润洗滴定管的操作方法是。
②测定前,先称取0.2500g无水MgBr2产品,溶解后,用0.0500 mol/L的EDTA标准溶液滴定至终点,消耗EDTA标准溶液26.50 mL,则测得无水MgBr2产品的纯度是____________(以质量分数表示)。
【答案】33.(每空2分,共4分)①从滴定管上口加入少量标准液,倾斜着转动滴定管,使液体润湿内壁,然后从下部放出,重复2-3次②97.5%【2018年上海市闵行区二模】(三) (本题共15分)小苏打是一种常用的食品添加剂。
31.精制食盐是制备小苏打的原料之一。
粗盐中含有少量Ca2+、Mg2+、SO42-,粗盐精制的步骤顺序是:溶解→→→→ (填字母编号)。
a.加盐酸调pH b.加Ba(OH)2溶液 c.加Na2CO3溶液 d.过滤32.NH3、CO2先后通入饱和食盐水中,反应的离子方程式________________。
33.侯氏制碱法中,母液的处理方法是通入氨气,再加入细小食盐颗粒,最后冷却析出的副产品是_______;简述通氨气的作用____________________________________。
33.称取2.640 g小苏打样品(含少量NaCl),配置成250 mL溶液,准确取出20.00 mL溶液于锥形瓶中,滴加_______作指示剂,滴定时消耗0.1000 mol/L盐酸的体积为20.67 mL。
则该样品中碳酸氢钠的质量分数为(保留两位小数)。
热化学【2018年上海长宁区二模】7. 下列变化会放出热量的是()A.碘升华 B.冰融化 C.氢氧化钠溶于水 D.氯化铵溶于水【答案】C【2018年上海长宁区二模】12. 下列表示吸热反应的图像是()【答案】A【2018年上海长宁区二模】14.下列关于钢铁发生吸氧腐蚀的分析正确的是()A.吸氧腐蚀是吸热反应B.铁作原电池正极C.正极电极反应为:2H2O+O2+4e→4OH-D. 原电池负极反应为:Fe-3e→Fe3+【答案】C【2018年上海杨浦区二模】10. 下列反应中的能量变化与图示一致的()A. 盐酸和NaOH溶液混合是B. CH4在空气中燃烧C. Al与Fe2O3反应D. 电解水得到H2和O2【答案】D【2018年上海闵行区二模】11.关于硝酸铵说法正确的是()A.属于共价化合物 B.溶于水放热 C.受热易分解 D.属于有机氮肥【答案】C【2018年上海闵行区二模】20.恒容密闭容器中发生反应:SiO 2(s)+4HF(g)SiF4(g)+2H2O(g)+148.9 kJ。
叙述错误的是()A.反应物的总能量高于生成物的总能量B.若生成2mol液态水,则放出的热量大于148.9 kJC.当v正(HF)=2v逆(H2O)时,反应达到平衡状态D.平衡后放出的热量随加入SiO2量的增加而增大【答案】D【2018年上海奉贤区二模】16.已知2SO2(g)+O2(g) 2SO3(g)+Q kJ·mol-1(Q>0)。
下列说法正确的是()A.相同条件下,2molSO2(g)和1molO2(g)所具有的能量小于2molSO3(g)所具有的能量B.将2molSO2(g)和1molO2(g)充分反应可放出的热量为Q kJC.增大压强或升高温度,该平衡都向逆反应方向移动D.若充分反应后放热Q kJ,则此过程中有2molSO2(g)被氧化【答案】D【2018年上海奉贤区二模】17.下图是2SO3(g) ⇌ 2SO2(g) + O2(g) 的能量变化图,据图得出的相关叙述正确的是()A.2SO3(g) ⇌ 2SO2(g) + O2(g) + (a-b) kJB.1mol SO2的能量比1mol SO3的能量高C.若有2mol SO3充分反应,吸收(a-b) kJ热量D.该化学反应过程中的能量变化既有吸热又有放热【答案】D【2018年上海青浦区二模】6.下列变化过程中Q>0的是()A.CH 3COOH CH3COO-+ H+ + QB. CaCO3(s)→ CaO(s)+ CO2(g)+ QC.S2- + H 2O HS- + OH- + QD.S(g)→S(l)+ Q【答案】D【2018年上海青浦区二模】9.下列试剂或方法肯定不能鉴别氯化钠和氯化铵固体的是()A.观察颜色 B.加热 C.加水 D.加紫色石蕊试液【答案】A【2018年上海普陀区二模】15、反应2A(g)+B(g)2C(g)的能量变化如图所示,下列说法错误的是()A. 加入催化剂,X点位置不变B. 加入催化剂,G的大小不变C. 该反应为放热反应D. 反应热为E与G的和【答案】D【2018年上海浦东新区二模】5.化学反应中的能量变化符合右图所示的是()A. 甲烷燃烧B. 碳酸钙高温分解C. 电石与水反应D. 酸碱中和【答案】B【2018年上海静安区二模】6. 下列过程的热效应属于吸热的是()A. 碘蒸气的凝华B.化学反应中化学键的形成C. 铝热反应D. 氯化铵的水解【答案】DO2 (g) → 2CO2 (g) 【2018年上海静安区二模】17.已知C2H2 (g) + 52+ H2O (g)+1256 kJ,下列说法正确的是()A.1 份乙炔完全燃烧可放热1256 kJB.反应中乙炔做还原剂、被还原C.乙炔完全燃烧时,生成2 mol液态水,所放热量小于2512 kJ D.若有10 mol电子发生转移,则需消耗2.5 mol O2【答案】D【2018年上海金山区二模】7.下列过程能实现化学能转化为热能的是()A.光合作用B.木炭燃烧C.风力发电D.电解饱和食盐水【答案】B【2018年上海嘉定区二模】10.合成氨反应过程中的能量变化如图所示,下列说法正确的是()A.反应体系中加入催化剂,会改变反应的热效应B.反应物的总能量低于生成物的总能量C.该反应的热化学方程式为 3H2(g)+N2(g)2NH3(g)+Q(Q>0) D.该反应是吸热反应【答案】C【2018年上海宝山区二模】8.下列固体溶于水时吸热的是()A. 氯化铵B.氢氧化钠C. 氧化钙D. 过氧化钠【答案】A【2018年上海宝山区二模】10.已知1mol氢气和氧气完全燃烧生成水蒸气放出241.8千焦热量,下列热化学方程式正确的是()A. 2H2(g)+O2(g)→2H2O(g)+241.8kJB. H2(g)+1/2O2(g)→H2O(s)+241.8 kJC. H2(g)+1/2O2(g)→H2O(g)-241.8 kJD. H2O(g)→H2(g)+1/2O2(g)-241.8 kJ【答案】D【2018年上海徐汇区二模】8.分析右面的能量变化示意图,下列热化学方程式正确的是()A.2A(g) + B(g) → 2C(g) - Q B.2A(g) + B(g) → 2C(g) + QC.2A + B → 2C + Q D.2C → 2A + B - Q【答案】B。
电解质溶液【2018年上海长宁二模】10. 对于常温下1升pH=1的硝酸溶液,下列叙述正确的是( ) A.该溶液lmL 稀释至100mL 后,pH 等于3B.向该溶液中加入含0.1mol 氢氧化钡的溶液恰好完全中和C.该溶液中硝酸电离出的c(H+)等于水电离出的c(H+)D.该溶液中硝酸电离出的c(H+)是水电离出的c(H+)的100倍 【答案】A【2018年上海杨浦区二模】20. 25℃,有两种盐的稀溶液,分别是a mol/L NaX 溶液和b mol/L NaY 溶液,下列判断错误的是( )A. 若a b >,测得(X )(Y )c c --=,则溶液中的(HX)(HY)c c >B. 若a b >,测得(HX)(HY)c c >,则溶液中的(X )(Y )c c --=C. 若a b =,且pH(NaX)pH(NaY)>,则酸性:HX HY <D. 若a b =,并测得(X )(Y )(HY)a c c c --==+,则HX 是强酸,HY 是弱酸 【答案】B【2018年上海杨浦区二模节选】28. Na 2SO 3和NaHSO 3混合溶液的pH 随Na 2SO 3和NaHSO 3比例的不同而不同,数据如下:表中第________组(填写序号)数据,可判断NaHSO 3溶液显_______性(填“酸”或“碱”)。
29. NaHSO 3既能和强酸反应也能和强碱溶液反应。
用平衡移动原理说明NaHSO 3能和强碱溶液反应的原因:_________________________________________________________。
【答案】28. ③;酸29. NaHSO 3溶液中HSO 3-发生电离:HSO 3-H ++SO 3-,电离出的H +与强碱溶液中的OH -发生反应,其浓度降低,平衡正向移动,使反应能持续进行。
【2018年上海闵行区二模】17.室温时,0.1 mol/L某酸HA溶液的pH=3。
关于该溶液叙述正确的是()A.溶质的电离方程式为HA→H+ + A- B.升高温度,溶液的pH增大C.若加入少量NaA固体,则c(A-)降低 D.该溶液稀释10倍后,pH < 4【答案】D【2018年上海闵行区二模节选】联氨(N2H4)具有较强的还原性。
工业上用过量氨气和NaClO 溶液来制备。
28.制取NaClO所用的原料是_________、_________。
解释氨气过量的原因_____________________________________________。
常温下,向10mL pH=2的盐酸中滴加等浓度氨水。
加入氨水的体积(V)与溶液pH的关系如右图所示。
29.a点溶液中由水电离产生的c(H+) 10-7mol/L (填>、<或=);用平衡移动原理解释b点溶液呈酸性的原因___________。
30.比较c点溶液中所有离子浓度大小关系是。
【答案】28.(3分) Cl2、NaOH(2分);防止N2H4被NaClO氧化。
(1分)29.(4分) <(2分);NH4+水解结合水电离出的OH-,使水的电离平衡H2O H++OH-向正方向移动,溶液中c(H+)>c(OH-),所以溶液呈酸性。
30.(2分)c(NH4+)=c(Cl-)>c(H+)=c(OH-)【2018年上海奉贤区二模】3.下列物质属于强电解质的是()A. 硫酸钡B.盐酸C. 乙醇D.三氧化硫【答案】A【2018年上海奉贤区二模】11.对滴有酚酞试液的溶液中,下列操作溶液颜色会变深的是()A.AlCl3溶液中再溶入AlCl3 B.CH3COONa溶液加热C.氨水中加入少量NH4Cl固体 D.醋酸溶液加热【答案】B【2018年上海奉贤区二模节选】28.氨水是一种很好的氮肥,常温下测定0.1mol/L 氨水溶液,其PH 值小于13,其原因是_____________________________(用电离方程式解释);常见 氮肥种类有_____________________________(列举两个)。
29. 硝酸铵易溶于水,其水溶液呈 ________(填“酸性”、“碱性”、或“中性”),原 因是_______________________________(用离子方程式表示)。
【答案】28. NH 3·H 2O NH 4++ OH -铵态氮肥、硝态氮肥、有机氮肥(任意两个即可) 29. 酸性 NH 4++H 2O NH 3·H 2O+H +【2018年上海崇明区二模】18.物质的量浓度均为0.1mol/L 的盐酸和醋酸溶液,下列说法正确的是( )A .两溶液加入等质量的锌粉,产生氢气的速率相同B .两溶液中氢氧根离子浓度均为13110-⨯mol/LC .加入醋酸钠固体,二者的pH 均增大D .与氢氧化钠反应至中性时,二者消耗氢氧化钠的质量相同 【答案】C【2018年上海崇明区二模】(二)(本题共15分)NH 4Al(SO 4)2是常见的焙烤食品添加剂;NH 4HSO 4在医药、电子工业中用途广泛。
请回答下列问题:25.相同条件下,10.1mol L -⋅ NH 4Al(SO 4)2中4(NH )c + (填“等于”“大于”或“小于”)10.1mol L -⋅ NH 4HSO 4中4(NH )c +。
10.1mol L -⋅ NH 4Al(SO 4)2溶液的pH 随温度变化的曲线如图甲所示:26.图甲中符合10.1mol L -⋅ NH 4Al(SO 4)2的pH 随温度变化的曲线是 (填字母)。
27.向100mL 10.1mol L -⋅ NH 4Al(SO 4)2溶液中滴入90ml 10.5mol L -⋅ NaOH 溶液,产生白色沉 淀 克。
28.写出NH 4HSO 4溶液中滴加足量NaOH 溶液的化学方程式 ; 25℃时,向100mL 10.1mol L -⋅ NH 4HSO 4溶液中滴加10.1mol L -⋅ NaOH 溶液,得到的溶液pH 与NaOH 溶液体积的关系曲线如图乙所示。
29.试分析图乙中a 、b 、c 、d 四个点,水的电离程度最大的是 。
【答案】(二)(本题共15分) 25.小于 (3分) 26.A (3分) 27.0.39g (3分)28.NH 4HSO 4+NaOH → NH 3·H 2O+Na 2SO 4+H 2O(3分) 29.a (3分);【2018年上海青浦区二模】5.下列物质溶于水时会破坏水的电离平衡,且属于电解质的是( )A .氯气B .二氧化碳C .氯化钾D .醋酸钠 【答案】D【2018年上海青浦区二模】17.常温下,若HA 溶液和NaOH 溶液混合后pH=7,下列说法错误的是 ( )A .反应后HA 溶液可能有剩余B .HA 溶液和NaOH 溶液的体积可能相等C .溶液中c(Na +)>c( A —)D .HA 溶液的c (H +)和NaOH 溶液的c (OH -)可能不相等 【答案】C【2018年上海青浦区二模】20.在0.1 mol/L Na 2CO 3溶液中,微粒间浓度关系正确的是( ) A .[Na +] + [H +]=[OH —] + [HCO 3—] + [CO 32—]B .[Na +]>[CO 32—]>[HCO 3—]>[OH —]C .[Na +]=2[CO 32—] + 2[HCO 3—] + 2[H 2CO 3]D .[Na +]>[HCO 3—]>[CO 32—]>[OH —] 【答案】C【2018年上海青浦区二模节选】(二)本题共14分 海洋是资源的宝库,含有丰富的化学元素。
30.同温同浓度的Na 2CO 3溶液、NaHCO 3溶液,PH 大小顺序为 ˃ 。
NaHCO 3溶液中滴入少量氢氧化钠溶液,溶液中c(CO 32-) (填变大或变小), 请用平衡理论解释发生这种变化的原因 。
【答案】Na 2CO 3>NaHCO 3(2分);增大(2分),HCO 3—H ++ CO 32—,滴入氢氧化钠, OH —结合H +生成水,导致电离平衡正向移动,[CO 32—]增大。
(2分)【2018年上海普陀区二模】16、将浓度和体枳均相同的一元酸HA 与NaOH 溶液混合,下列说法一定错误的是( ) A. c(H +)=c(OH -) B. c(A -)=c(Na +) C. c(A -)>c(Na +)D. c(H +)<c(OH -)【答案】C【2018年上海浦东新区二模】12.有关水的表述正确的是( ) A. 电子式为H [:O:H]+-⋅⋅⋅⋅B. 是直线型分子C. 是非电解质D. 可以作氧化剂【答案】D【2018年上海浦东新区二模】13.能证明乙酸是弱酸的是( ) A. 乙酸钠溶液pH > 7B. 乙酸溶液能导电C. 乙酸溶液能使石蕊变红D. 乙酸溶液易挥发【答案】A【2018年上海浦东新区二模】23.KSCN 水溶液呈中性,则硫氰酸(HSCN )的电离方程式为__________________________________;硫氰化铵(NH 4SCN )溶液中各种离子浓度由大到小的顺序是_______________。
【答案】23.HSCN → H ++SCN-; c(SCN -)>c(NH 4+)>c(H +)>c(OH -)【2018年上海静安区二模】13.将下列物质溶于水,能促进水的电离的是A.NaHSO4 B.Na2CO3 C.SO2 D.NaOH【答案】B【2018年上海静安区二模】23. 消除NH3对水体污染的重要方法是在一定条件下向水体中加入适量NaOH,这样能使NH3的脱除率增大,试用平衡移动原理解释其原因______________________________。
为实现CO2减排,合成氨工厂采用苯菲尔法脱碳。
该方法是用碳酸钾溶液为吸收剂捕集混合气中的CO2得到富液,再高温加热富液使之分解释放出CO2 ,正常情况下再生的二氧化碳气体体积分数可达98.5%以上。
24. 某研究小组用200mL 1.5mol/L K2CO3溶液吸收了3.36L 的CO2(标准状况)形成富液,碳酸钾溶液吸收CO2的离子反应方程式为,该富液中的溶质是(填化学式),各离子的浓度关系正确的是。
a.c(K+) + c(H+) = 2c(CO32-) +c(HCO3-) +c(OH-)b.3c(K+)=4 c(CO32-)+4 c(HCO3-)+4c(H2CO3)c.c(K+)>c(OH-)>c(HCO3-)>c(CO32-)>c(H+)【答案】23.氨气在水中存在如下平衡:NH3+H2O NH3•H2O NH4++OH﹣,当加入NaOH后,c (OH﹣)浓度增大,平衡逆向移动,故有利于氨的脱除。