专题8-硅元素
- 格式:doc
- 大小:40.00 KB
- 文档页数:2

硅及其化合物【考向分析】硅及其化合物在高考的考点一是以新材料、新技术为背景考查C、Si及其重要化合物的性质及应用;二是以硅、硅酸的制备为载体,考查实验探究能力,Si和SiO2在现代科技中的用途常已成为高考选择题考查的热点。
【要点讲解】要点1. 硅和二氧化硅1.硅(1)自然界存在形式:硅在地壳中的含量仅次于氧,全部以化合态存在。
主要单质有:晶体硅和无定性硅两大类。
(2)物理性质:晶体硅为原子晶体,灰黑色、有金属光泽、硬度大而脆、熔沸点高。
导电性介于导体和绝缘体之间,是常用的半导体材料。
(3)化学性质:常温下化学性质不活泼,只能跟F2、HF和NaOH溶液反应,在高温条件下,单质硅能与O2和Cl2等非金属单质反应。
(4)用途:太阳能电池、计算机芯片、半导体材料、制作特种钢及合金等。
(5)制备:自然界中无游离态的硅,工业上,用C在高温下还原SiO2可制得粗硅,有关反应的化学方程式: SiO2+2C 高温Si(粗)+2CO↑,Si(粗)+2Cl2高温SiCl4,SiCl4+2H2高温Si(纯)+4HCl温馨提示:①硅主要用于半导体材料(如集成电路的芯片),另外还用于制作特种纲及合金。
②非金属单质一般为非导体(如硫),但Si却为半导体。
③C、Si同属IVA族,还原性是Si大于C,而C却能将Si从SiO2中还原出来(条件是高温),原因是产物CO气体迅速从反应体系中逸出。
④非金属单质一般不跟非氧化性酸作用,而Si却能与HF发生反应。
2.二氧化硅(SiO2)(1)SiO2的空间结构:SiO2晶体是立体网状结构。
在SiO2晶体里,每个Si周围结合四个O,同时每个O与两个Si相结合,在SiO2晶体中原子个数比为1∶2,因此用“SiO2”这个式子表示二氧化硅晶体的组成。
SiO2直接由原子构成不存在单个SiO2分子。
(2)物理性质:熔点高,硬度大,不溶于水。
(3)化学性质:SiO2常温下化学性质很不活泼,不与水、酸反应(氢氟酸除外),能与强碱溶液、氢氟酸反应,高温条件下可以与碱性氧化物反应。

专题八元素化合物知识的复习第八课时硅及其化合物【课堂目标】熟练掌握各种含硅物质的性质及用途【回顾准备】【基础梳理】活动一:含硅物质的存在、用途及结构硅在自然界中的存在方式: (游离态、化合态)1.单质硅的用途:①②。
1molSi含Si-Si键的数目。
2.二氧化硅的用途:。
1molSiO2含Si-O键的数目。
3.硅胶的用途:。
4.硅酸钠的用途:。
硅酸钠的水溶液俗名:。
辨析①晶体硅具有半导体性质,可用于生产光导纤维( )②SiO2既能与HF反应,又能与NaOH反应,属于两性氧化物( )③高纯硅及其氧化物在太阳能电池及信息高速传输中有重要应用( )④二氧化硅是制造太阳能电池板的主要材料( )⑤氢氟酸具有强酸性,用氢氟酸蚀刻玻璃( )⑥SiC的硬度很大,可用作砂纸、砂轮的磨料( )⑦硅酸钠溶液可用来生产防火剂和黏合剂( )⑧硅酸盐化学性质稳定,可用作光导纤维的材料( )⑨60g二氧化硅中Si-O键个数为2N A个( )⑩二氧化硅的分子式为:SiO2( )活动二:硅、二氧化硅、硅酸、硅酸钠的化学性质1.硅硅燃烧放出的热量多,且燃烧产物对环境污染程度低,容易有效控制,可做“未来石油”。
2.二氧化硅①碱性溶液的保存不能用塞,原因(离子方程式):。
②与C在高温下反应的化学方程式。
3.硅酸钠①硅酸钠溶液在空气中变质的方程式:。
离子方程式:。
证明酸性:>。
②硅酸钠溶液与盐酸反应的方程式:。
③传统硅酸盐产品:、、。
【课堂训练】1.设N A为阿伏加德罗常数的值。
下列叙述正确的是A.12g金刚石中,含C-C键的数目为4N AB.12g石墨中,含C-C键的数目为2N AC.28g单质硅中,含Si-Si键的数目为2N AD.60g二氧化硅中,含Si-O键的数目为2N A2.常温下,下列各组离子在指定溶液中可以大量共存的是A.使pH试纸变红的溶液:K+、Na+、Cl-、SiO32-B.加酚酞变红的溶液:K+、Na+、Cl-、SiO32-C.加入Al粉后反应产生H2的溶液中:NH4+、Na+、SiO32-、HCO3-D.c(OH-)/c(H+)=1×1014的溶液:Ca2+、Na+、SiO32-、NO3-3.下列叙述正确的是A.玻璃试剂瓶被烧碱溶液腐蚀:SiO2+2Na++2OH-=Na2SiO3↓+H2OB.二氧化硅不与任何酸反应,可用石英制造耐酸容器C.硅胶可用作实验室和袋装食品、瓶装药品等的干燥剂D.硅的燃烧产物粉尘不会造成污染4.下列叙述不正确的是A.碳单质具有还原性,高温不能将二氧化硅还原为硅B.用激光笔照射水玻璃溶液,有丁达尔现象,SiO32-水解生成硅酸胶体C.高纯度的硅单质广泛用于制作光导纤维,光导纤维遇强碱会“断路”。

高中化学硅的教案化学教案一、概述在高中化学教学中,硅是一个非常重要的元素。
硅在自然界中广泛存在,同时在工业生产、农业生产以及日常生活中也起着重要作用。
本教案将从硅的性质、结构、用途等方面进行系统的介绍和讲解,帮助学生更好地理解硅的特点及其在现实生活中的应用。
二、硅的基本性质1. 硅的基本性质硅是元素周期表中的第14号元素,其化学符号为Si,原子序数为14,原子量为28.09。
硅是一种非金属元素,具有典型的金属非金属特性。
硅具有四个价电子,可以形成SiO4四面体结构,因此硅具有广泛的共价键化合物。
2. 硅的物理性质硅是一种灰色晶体,硬度较高。
硅具有较好的导电性,常用于制造半导体材料。
硅的熔点为1414摄氏度,沸点为3265摄氏度。
三、硅的结构1. 硅的晶体结构硅主要存在于石英和硅铁矿中,其晶体结构为六方密堆积结构。
硅原子通过共价键结合在一起,形成硅氧四面体单元,依次堆积形成石英或其他硅化合物的晶体结构。
2. 硅的分子结构硅元素通常以多聚体的形式存在,如硅酸盐、硅烷等。
硅的共价键结构使其具有较强的稳定性和耐高温性,常用于制备耐高温材料。
四、硅的应用1. 半导体材料硅是最重要的半导体材料之一,被广泛应用于电子工业中。
硅晶体可以形成n型或p型半导体,通过掺杂和控制形成p-n结,构成二极管、晶体管、集成电路等电子元件。
2. 硅橡胶硅橡胶是一种优良的橡胶材料,具有优异的耐高温、耐寒性能。
硅橡胶被广泛用于密封材料、绝缘材料等领域。
3. 硅油硅油是一种绝缘性能很好的润滑剂,常用于机械设备的润滑和绝缘保护。
五、实验教学为了帮助学生更好地理解硅的性质和结构,可以设计一些简单的实验,如硅的氧化反应、硅纳米颗粒的制备等实验,让学生通过实践感受硅的化学特性。
六、教学反馈在教学过程中,可以结合课堂讨论、思维导图、实验报告等形式,对学生的学习效果进行及时的评估和反馈,帮助学生及时弥补不足,提高学习效果。
以上就是对高中化学硅的教案设计,希望通过本教案的讲解和实践,能够使学生对硅这一重要元素有更深入的了解,激发学生学习化学的兴趣,为将来的学习和工作打下坚实基础。

无机非金属材料的主角——硅专题训练及答案一、选择题(本题包括8小题,每题6分,共48分)1.大多数物质的俗名是根据其特殊的物理性质或用途得来的。
下列物质的俗名与化学式或用途不相符的一组是( )【解析】选A。
石英主要用于生产玻璃和光导纤维等,晶体硅才用于制作集成电路。
【加固训练】下列关于硅及其化合物的叙述错误的是( )A.硅是良好的半导体材料,二氧化硅可用于制造光导纤维B.二氧化硅能与石灰石反应:SiO2+CaCO3CaSiO3+CO2↑C.可以用焦炭还原二氧化硅生产硅:SiO2+2C Si+2CO↑D.水泥的主要成分是Na2SiO3、CaSiO3和SiO2【解析】选D。
水泥的主要成分是硅酸二钙、硅酸三钙和铝酸三钙,普通玻璃的主要成分是Na2SiO3、CaSiO3和SiO2,D错误。
2.气凝胶是一种世界上最轻的固体,也被称为“固态烟”,非常坚固耐用,它可以承受相当于自身重量几千倍的压力,最高能承受1 400摄氏度的高温,绝热性能十分优越,其主要成分是二氧化硅等。
下列说法正确的是( )A.Si→SiO2→H2SiO3可以通过一步反应实现B.可以用陶瓷坩埚熔融烧碱C.二氧化硅溶于氢氧化钠溶液又溶于氢氟酸,所以二氧化硅是两性氧化物D.气凝胶与豆浆具有相似的性质【解析】选D。
二氧化硅不与水反应,A错误;陶瓷坩埚的成分中含二氧化硅,与烧碱反应,B错误;二氧化硅是酸性氧化物,C错误;气凝胶与豆浆都属于胶体,具有相似的性质,D正确。
【加固训练】硅是构成无机非金属材料的一种主要元素,下列有关硅的化合物的叙述错误的是( )A.氮化硅陶瓷是一种新型无机非金属材料,其化学式为Si3N4B.碳化硅(SiC)的硬度大,熔点高,可用于制作砂纸、砂轮的磨料C.祖母绿的主要成分为Be3Al2Si6O18,用氧化物形式表示为3BeO·Al2O3·6SiO2D.二氧化硅为立体网状结构,其晶体中硅原子和硅氧单键的个数之比为1∶2【解析】选D。
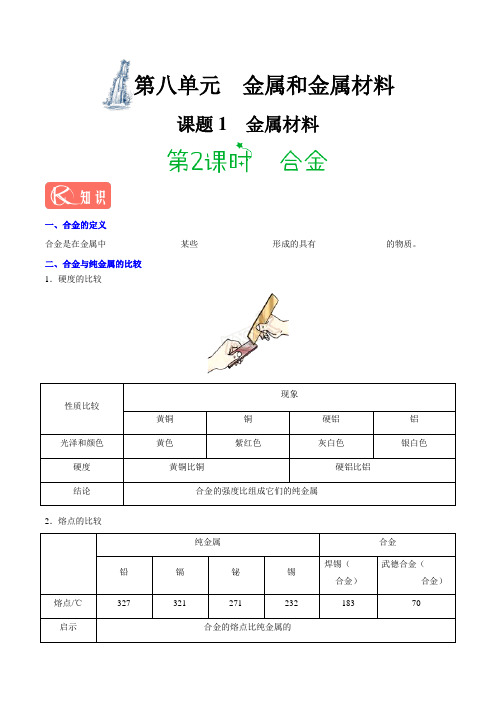
第八单元金属和金属材料课题1 金属材料一、合金的定义合金是在金属中________________ 某些________________形成的具有________________的物质。
二、合金与纯金属的比较1.硬度的比较性质比较现象黄铜铜硬铝铝光泽和颜色黄色紫红色灰白色银白色硬度黄铜比铜_________ 硬铝比铝_________结论合金的强度比组成它们的纯金属_______________2.熔点的比较纯金属合金铅镉铋锡焊锡(_____合金)武德合金(______________合金)熔点/℃327 321 271 232 183 70 启示合金的熔点比纯金属的_____________三、合金的优良性能1.机械加工与_______________更好。
2.比组成它们的纯金属_______________更大,_______________更低。
3.合金的优良性能可满足人们许多特殊的需求,从而比纯金属应用更广泛。
四、常见的合金1.生铁和钢生铁钢含碳量含碳量在______________之间的铁合金含碳量在______________之间的铁合金其他元素_______________,以及少量的硫和磷不锈钢中含有______________等机械性能纯铁较软,生铁硬而脆,无韧性较硬,有良好的________________,机械性能好2.钛和钛合金(1)性能:熔点高、__________、可塑性好、易加工、机械性能好、_______________非常好。
(2)用途:人造骨骼、__________、__________、___________、船舶、_____________、通信设备。
【答案】一、加热熔合金属或非金属金属特征二、1.硬硬硬2.锡铅铅、铋、锡、镉低三、1.抗腐蚀性能2.强度和硬度熔点四、1.2%~4.3%0.03%~2%硅、锰铬、镍延展性和弹性2.(1)密度小抗腐蚀性能(2)火箭导弹航天飞机化工合金的特征1.组成合金是一种金属中熔合了其他金属或非金属形成的,因此合金中最少含有一种金属,且属于混合物。

硅有关练习题硅(化学符号:Si)是地壳中含量最丰富的非金属元素之一,它在现代工业和科技领域有着广泛的应用。
以下是一些与硅相关的练习题,帮助读者加深对硅及其应用的理解。
一、选择题1. 下列元素中,属于硅的同族元素的是:A) 氮B) 塑料C) 硒D) 硫2. 下列关于硅的说法中,错误的是:A) 硅是地壳中含量最丰富的元素之一B) 硅是一种非金属元素C) 硅在电子行业中常用于制作半导体器件D) 硅是一种有毒物质,使用时需注意安全措施3. 硅的原子序数是:A) 12B) 14C) 16D) 184. 下列哪个是硅最常见的氧化物?A) 二氧化硅B) 一氧化硅C) 氢氧化硅D) 碳酸硅5. 硅是地壳中常见的主要矿石,以下哪个矿石是硅的重要来源?A) 磷矿石B) 铁矿石C) 钴矿石D) 石英矿石二、填空题1. 硅的原子结构中有 __ 个中子, __ 个质子, __ 个电子。
2. 硅在室温下为 __ 状固体。
3. 硅的密度约为 __ 克/立方厘米。
4. 硅是 __ 最重要的原料之一。
5. 硅的晶体结构属于 __ 结构。
三、简答题1. 简要描述硅在电子行业中的应用。
2. 解释硅的半导体特性以及其在电子元器件中的作用。
3. 说明硅的导电性质与金属的导电性质之间的差异。
4. 举例说明硅的高熔点和抗腐蚀性对其工业应用的重要性。
四、应用题1. 某电子公司需要制造一批硅晶片,已知每片硅晶片的质量为10克,按照客户的需求,需要制造1000万片硅晶片。
请计算出这批硅晶片的总质量。
2. 硅是光伏电池的重要组成部分之一。
某光伏电站每天需要产生10000千瓦时的电能,假设每块硅光伏电池板每天平均发电8小时,每块电池板可产生100瓦的电能。
请计算这个光伏电站需要多少块硅光伏电池板?3. 硅是玻璃制造的重要原料之一。
某玻璃厂生产一批玻璃需要用到1000千克的石英砂,已知石英砂的成分主要为二氧化硅(SiO2),其质量分数为0.95。
请计算这批玻璃需要多少千克的硅?以上是与硅有关的练习题,通过解答这些问题,读者可以加深对硅及其应用领域的了解,并对相关概念进行巩固。
专题八氯、硅及其化合物考纲展示考情汇总备考指导1.理解常见非金属元素单质及其重要化合物的主要性质。
2.了解常见非金属元素单质及其重要化合物的应用。
3.了解常见非金属元素单质及其重要化合物对环境质量的影响。
2020年7月:142019年6月:24,34,382019年1月:8,16,20,352018年6月:12,13,25,322018年1月:452017年:25,422016年:15,19,34,40,41硅及其化合物主要集中在其用途和无机非金属材料种类,注意区分Si、SiO2的用途。
氯及其化合物重点了解氯水成分及其表现的性质。
硅及其化合物的性质1.单质硅(Si)(1)物理性质:有金属光泽的灰黑色固体,熔点高,硬度大。
(2)化学性质①常温下化学性质不活泼,只能跟F2、HF和NaOH溶液反应。
Si+2F2===SiF4;Si+4HF===SiF4↑+2H2↑;Si+2NaOH+H2O===Na2SiO3+2H2↑。
②在高温条件下,单质硅能与O 2、Cl 2等非金属单质反应。
Si +O 2=====高温SiO 2,Si +2Cl 2=====高温SiCl 4。
(3)用途:太阳能电池、计算机芯片以及半导体材料等。
(4)硅的制备:工业上,用C 在高温下还原SiO 2可制得粗硅。
2.SiO 2(1)物理性质:熔点高,硬度大,不溶于水。
(2)化学性质:SiO 2常温下化学性质很不活泼 ,不与水、酸反应(氢氟酸除外),能与强碱溶液、氢氟酸反应,高温条件下可以与碱性氧化物反应:①与强碱反应:SiO 2+2NaOH===Na 2SiO 3+H 2O(生成的硅酸钠具有粘性,所以存放NaOH 溶液和Na 2SiO 3溶液的试剂瓶不能用磨口玻璃塞,避免Na 2SiO 3将瓶塞和试剂瓶粘住,打不开,应用橡胶塞)。
②与氢氟酸反应(SiO 2的特性):SiO 2+4HF===SiF 4↑+2H 2O(利用此反应,氢氟酸能用于雕刻玻璃,氢氟酸不能用玻璃试剂瓶存放,应该用塑料瓶)。
元素及其化合物[考纲要求] 1.理解并能应用常见金属的活动顺序。
2.了解常见金属(如Na、Al、Fe、Cu等)及其重要化合物的主要性质和重要应用。
3.了解常见非金属(如H、C、N、O、S、Si、Cl等)及其重要化合物的主要性质和重要应用。
4.认识化学在海水、金属矿物等自然资源综合利用和实现物质间转化等方面的实际应用。
5.了解金属材料在生产和生活中的重要应用。
认识常见无机物在生产中的应用和对生态环境的影响。
考点一元素化合物基础知识及简单应用(一)钠及其化合物钠是“极其活泼”金属的代表,学习钠的性质可类比知道第ⅠA族、第ⅡA族活泼金属的一般性质,复习时应从以下几个方面掌握:1.(2021学年学科教研组复习备考编写)树立物质转化思想(1)理清知识主线Na→Na2O→Na2O2→NaOH→Na2CO3→NaHCO3(2)形成网络构建2.重要反应规范书写用方程式回答下列问题(1)实验室怎样处理钠屑?2CH3CH2OH+2Na―→2CH3CH2ONa+H2↑。
(2)写出Na与CuSO4溶液反应的离子方程式。
2Na+2H2O+Cu2+===Cu(OH)2↓+H2↑+2Na+。
(3)怎样将Na2CO3溶液转化为NaOH溶液(用化学方程式表示)。
Na2CO3+Ca(OH)2===CaCO3↓+2NaOH。
(4)向NaOH、Na2CO3、NaHCO3溶液中逐滴加入盐酸,发生反应的离子方程式。
OH-+H+===H2O;CO2-3+H+===HCO-3;HCO-3+H+===H2O+CO2↑。
(5)怎样除去CO2中的SO2气体(用离子方程式表示)。
SO2+2HCO-3===2CO2↑+SO2-3+H2O。
(6)怎样除去Na2CO3溶液中的NaHCO3(用离子方程式表示)。
HCO-3+OH-===CO2-3+H2O。
(7)怎样除去NaHCO3溶液中的Na2CO3(用离子方程式表示)。
CO2-3+H2O+CO2===2HCO-3。
专题八物质的组成与分类考点一元素考向1元素及元素含量1.有机物一定含有的元素是()A.碳B.氧C.氢D.氯2.地壳中含量最多的元素是()A.S iB.F eC.OD.A l3.地壳中,含量最多的金属元素与含量最多的非金属元素组成的化合物属于()A.酸B.碱C.盐D.氧化物4.下列科学家中,发现了元素周期律并编制了元素周期表的是()A.拉瓦锡B.门捷列夫C.道尔顿D.阿伏加德罗考向2元素周期表5.下图为元素周期表的一部分(X元素信息不全)㊂下列说法正确的是()A.碳的化学性质活泼B.X表示N2C.氧原子的质子数是8D.三种元素原子的核外电子数相同6.如图是钠元素在元素周期表中的信息和钠原子结构示意图㊂下列说法错误的是()A.钠的原子序数为11B.钠原子核外有3个电子层C.钠的相对原子质量为22.989D.化学反应中,钠原子易得电子7.下列说法正确的是()A.空气中氮气的体积分数为21%B.人体中含量最多的元素是氢元素C.海洋中含量最多的非金属元素是氧元素5758D.地壳中含量最多的金属元素是硅元素8.下列结构示意图表示元素周期表中同一纵行的原子的是()A.②④B .②③C .①③ D.①④考向3微粒结构示意图与元素周期表综合题9.核电荷数为1~18的元素的原子结构示意图等信息如下,请回答下列问题㊂(1)2017年5月9日,中国科学院等单位联合发布了115号元素的中文名为 镆 ,此元素原子的核电荷数为,核外电子数为 ㊂(2)在第三周期中,随着原子序数的递增,元素原子核外电子排布的变化规侓是 ㊂(3)利用上表中给出的元素,写出含有氮元素的常见单质㊁氧化物㊁酸㊁碱㊁盐的化学式各一个,并标出所写化学式中氮元素的化合价:单质 ㊁氧化物 ㊁酸 ㊁碱 ㊁盐 ㊂(4)以钠和氯为例,简述结构与性质的关系㊂ ㊂(5)国产C 919大型客机上使用了大量的铝合金㊂工业上用电解氧化铝(A l 2O 3)得到铝和氧气,试计算电解102t 氧化铝最多能生成铝的质量是多少?(写出计算过程)10.在宏观㊁微观和符号之间建立联系是化学学科的特点㊂(1)物质的组成及构成关系如下图所示,图中①表示的是 ,②表示的是㊂(2)下列说法正确的是 (填字母)㊂A.氯化氢是由氢㊁氯两种元素组成的B .氯化氢是由氢气和氯气混合而成的C .氯化氢是由一个氢原子和一个氯原子构成的(3)下图是氧㊁硫㊁氯三种元素的原子结构示意图㊂O SC l①氯原子的结构示意图中x的数值是㊂②氧和硫两种元素的化学性质具有相似性的原因是它们原子的相同㊂③氧和氯两种元素最本质的区别是它们原子中的不同㊂11.原子序数为1~18的元素的原子结构示意图等信息如下,请认真分析并回答下列问题㊂(1)原子序数为12的元素位于元素周期表中第周期,它属于(填 金属 或 非金属 )元素㊂(2)在化学反应中,原子序数为16的元素的原子容易(填 得到 或 失去 )电子,所形成的粒子的符号是㊂(3)根据氟原子和氯原子的结构示意图分析,由于氟原子和氯原子的相同,所以氟元素与氯元素的化学性质相似㊂(4)同周期元素,从左到右,各元素原子随原子序数的增加,最外层电子数依次㊂12.下表是元素周期表的一部分㊂原子序数为10的元素名称为;氟原子的核外电子数为;等质量的氧气和氟气中,所含原子数较少的是㊂8 O9 F10 N e氧氟16.0019.0020.1813.下面是元素周期表中某一周期元素的原子结构示意图:元素名称锂铍硼碳氮氧氟氖元素符号L i B e B C N O F N e59原子结构(1)硼原子结构示意图中的X= ;(2)镁原子的结构示意图为,上图中与其化学性质相似的元素是;(3)图中元素从左至右排列所遵循的规律是(任写一条);(4)根据图示信息,确定1个一氧化碳分子中所含电子总数为㊂14.核电荷数为1~18的元素的原子结构示意图等信息如下,回答下列问题:(1)在第三周期中,各原子结构的共同之处是;该周期中,各原子核外电子排布的变化规律是㊂(2)在第三周期中,元素类型的变化情况是:从左到右由元素过渡到元素,并以稀有气体元素结尾㊂(3)写出核外电子排布与氖原子相同的阳离子和阴离子符号各一个:阳离子,阴离子㊂(4)写出含有氮元素的常见氧化物㊁酸㊁碱㊁盐的化学式各一个:物质的类别氧化物酸碱盐物质的化学式考点二物质的分类1.下列物质中,属于纯净物的是()A.氧气B.糖水C.食醋D.大理石2.氮气在物质分类中属于()A.单质B.化合物C.氧化物D.混合物3.分类是化学学习和研究的重要方法之一,下列分类中不正确的是()6061A.纯净物:氧气㊁干冰㊁水银B .肥料:二氧化碳㊁硫酸铵㊁硝酸钾C .单质:金刚石㊁铁粉㊁黄铜D.盐:氯化钠㊁硝酸钠㊁碳酸钙4.下列四种物质符合下图所示关系的是()A.石墨B .干冰C .沥青 D.陶瓷5.下列物质中属于混合物的是( )A.河水B .氯酸钾C .三氧化硫 D.五氧化二磷6.下列选项中的物质所属类别错误的是( )选项物质类别A 空气㊁石油㊁干冰混合物B 氮气㊁水银㊁金刚石单质C 糖类㊁油脂㊁蛋白质营养物质D甲烷㊁乙醇㊁塑料有机物7.分类 可以使人们有序地研究物质,以下分类正确的是( )A.合金:生铁㊁锰钢㊁青铜B .碱:纯碱㊁烧碱㊁消石灰C .盐:氯化银㊁氯化钠㊁氯化氢D.合成材料:塑料㊁合成纤维㊁铝合金8.在化学反应6C O 2+6H 2O 光照叶绿素 C 6H 12O 6+6O 2中没有涉及的物质类别是( )A.单质B .氧化物C .盐 D.有机化合物9.下列各图中Ә和ʻ分别表示两种不同元素的原子,其中表示混合物的是( )10.下列物质:①空气㊁②硫酸㊁③氧气㊁④硝酸钠㊁⑤水㊁⑥氢氧化钠㊁⑦天然气㊁⑧生铁㊁⑨碳酸钙,对其分类完全正确的一组是( )A.混合物:①⑥⑦⑧B .酸:②④C .氧化物:③⑤D.盐:④⑨11.下列属于氧化物的是( )62A.O 2B .S O 2C .K C l D.N a OH12.下图是氢气和氧气发生反应的微观模拟图,请回答下列问题:(1)在B 图中将相关粒子图形补充完整;(2)A 图所示物质属于(填物质分类),从微观角度说明理由是 ;(3)画出比氧元素多一个周期少一个族的元素的原子结构示意图 ㊂13.请从A 或B 两题中任选1个作答,若两题均作答,按A 计分㊂A B洗衣凝珠 是由一层薄膜包裹洗衣液制成的新型洗涤产品㊂该薄膜的主要成分是可溶于水的聚乙烯醇(P V A )塑料㊂(1)P V A 塑料属于(填 合金 或 有机合成材料 )㊂(2)醋酸(C H 3C O OH )是合成P V A 的原料之一㊂醋酸中碳元素的质量分数为40%,其计算式为纳米材料具有特殊的性质和功能㊂纳米四氧化三铁具有类似人工模拟酶的催化性能㊂(1)四氧化三铁属于 (填 无机物 或 有机物 )㊂(2)纳米四氧化三铁能将过氧化氢催化分解为水和氧气,该反应的化学方程式为14.如图所示,用 表示A 原子, Ә 表示B 原子, ʻ 表示C 原子,在点燃条件下,每四个甲分子能与三个乙分子反应,生成两个丙分子和六个丁分子㊂从微观角度回答下列问题:(1)在丙中将相关粒子图形补充完整;(2)丁物质属于化合物的原因是 ㊂15.请用线段连接有对应关系的两行间的点(每个点只能连接1次)㊂考点二 化学式考向1化学式的书写1.以下对于物质的俗称㊁化学式㊁分类和用途的说法,其中不完全正确的一组是( )63选项俗称化学式分类用途A 干冰C O2氧化物人工降雨B 酒精C 2H 5OH 有机物消毒C 水银H g金属单质水银温度计D苏打N a H C O 3盐治疗胃酸过多2.生物体中含有多种氨基酸,下列有关甘氨酸的叙述正确的是( )A.甘氨酸是有机高分子化合物B .甘氨酸中碳原子与氢原子的个数比为24ʒ5C .甘氨酸是由碳㊁氢㊁氧㊁氮四种原子构成的D.一个甘氨酸分子中含有10个原子3.氨气的化学式是( )A.N 2B .N H 3C .H N 3 D.N H 44.吸烟有害健康,香烟燃烧产生的烟气中含有尼古丁(化学式为C 10H 14N 2)㊂下列相关说法正确的是( )A.尼古丁分子中含有氮分子B .尼古丁的相对分子质量为162gC .尼古丁分子中碳㊁氢原子个数比为5ʒ7D.尼古丁由碳㊁氢㊁氧三种元素组成5.P L A 是一种新型可降解塑料,以乳酸(C 3H 6O 3)为主要原料聚合而成,下列有关乳酸的说法错误的是( )A.乳酸是由碳㊁氢㊁氧三种元素组成B .乳酸分子中含有12个原子C .乳酸的相对分子质量是90D.乳酸中氧元素的质量分数最大6.烈性炸药T N T (化学式为C 7H 5N 3O 6)广泛用于开矿㊁修路㊁兴修水利等,下列关于T N T 的说法错误的是( )A.T N T 是一种有机物B .T N T 爆炸后会产生二氧化硫C .T N T 由四种元素组成D.每个T N T分子含有21个原子7.某同学制作的试剂标签如下,其中化学式书写不正确的是()8.在化学符号①N O2 ②2C O ③C a2+ ④H2O2 ⑤2OH-⑥Z n+2S O4中,关于数字 2 的意义,下列说法错误的是()A.表示分子个数的是②B.表示离子所带电荷数的是③⑤C.表示化合价数值的是⑥D.表示一个分子中所含某种原子个数的是①④9.南昌汉代海昏侯墓出土的文物中,保存完好的玉器非常罕见㊂对玉石主要成分(化学式为N a A l S i2O6)的描述正确的是()A.含有3个氧分子B.相对分子质量为94C.钠元素的质量分数为13.4%D.钠元素与铝元素的质量比为23ʒ2710.下列化学用语的书写或理解正确的是()A.氦气:H e2B.钙离子:C a+2C.3个氢分子:3H2D.2个氮原子:N2考向2化学式的意义及相关计算11.如图是某物质的分子模型,下列关于该物质说法正确的是()A.属于有机物B.化学式为N H3C.氮元素和氢元素的质量比为3ʒ1D.氢元素的质量分数=117ˑ100%=5.9%12.液化石油气是经加压后压缩到钢瓶中的,瓶内压强是大气压强的7~8倍㊂液化石油气的主要成分是丙烷㊁丁烷㊁丙烯和丁烯等㊂下列有关丁烷的叙述正确的是()64A.丁烷中碳㊁氢元素的个数比为2ʒ5B.丁烷分子中氢元素的质量分数最大C.丁烷是由碳㊁氢原子构成的有机物D.在通常状况下,丁烷是气体13. 珍爱生命,远离毒品 ㊂冰毒是一种毒品,其主要成分为甲基苯丙胺(化学式为C10H15N)㊂有关甲基苯丙胺的说法正确的是()A.属于混合物B.属于有机物C.一个分子中原子总数为25D.燃烧只生成二氧化碳和水14.某功能饮料含牛磺酸(C2H7N O3S),下列关于牛磺酸的说法正确的是()A.共含有14种元素B.分子中O㊁S元素的质量比为3ʒ2C.相对分子质量为125gD.含有臭氧(O3)分子15.在横线(1)(2)(3)处用化学用语填空:(1);(2);(3)㊂16.食盐是维持人体正常生理活动必不可少的物质㊂低钠盐能预防高血压,碘盐能补充人体所需碘元素,工业用盐使用不当易使人中毒㊂(1)氯化钠中质量分数较大的是(填名称)元素㊂(2)硫酸镁可以改变钠盐的 口味 ,硫酸镁的化学式为㊂(3)碘盐中加了碘酸钾(K I O3),则K I O3中碘元素的化合价为㊂(4)工业用盐含N a N O2,N a N O2的名称为(填序号)㊂A.磷酸钠B.硝酸钠C.亚硝酸钠17.尿素[C O(N H2)2]是氮肥中最主要的一种,其含氮量高,在土壤中不残留任何有害物质,长期施用没有不良影响㊂计算:(1)C O(N H2)2中共含有(写数字)种元素;(2)C O(N H2)2的相对分子质量是;(3)若C O(N H2)2中含有3g氮元素,则该C O(N H2)2的质量为g(计算结果精确到0.1)㊂6518.中国科学家屠呦呦因发现和研制了青蒿素(C15H22O5)而荣获诺贝尔生理学或医学奖,受到世界的高度关注㊂青蒿素是一种用于治疗疟疾的药物,据此信息回答:(1)青蒿素中各元素的质量比为㊂(2)青蒿素中氧元素的质量分数是㊂(3)青蒿素的研制成功,体现了化学在提高人类生活质量方面的重要作用是㊂19.(1)掌握化学用语是学习化学的关键,请用化学用语填空:①氩元素;②氯酸钾中的阳离子;③氯化铝;④2个五氧化二磷分子㊂(2) F e2+ 中数字 2 表示的意义是㊂20.写出符合下列要求的物质(或主要成分)的化学式:(1)相对分子质量最小的氧化物;(2)铅蓄电池中含有的酸;(3)会造成温室效应的单质;(4)可以治疗胃酸过多的一种盐;(5)一种钾肥㊂21.新药帕拉米韦注射液可用于治疗H7N9禽流感,其说明书中部分内容如图所示㊂(1)帕拉米韦由种元素组成,其中氢㊁氮的原子个数比是㊂(2)帕拉米韦属于(填 有机物 或 无机物 )㊂(3)帕拉米韦中氧元素的质量分数是(精确到0.1%)㊂(4)成人禽流感患者,每天应注射帕拉米韦支㊂考点三化合价考向1化合价的计算1.中药砒霜的主要成分为三氧化二砷(A s2O3),可用于治疗肿瘤㊂其中砷元素的化合价为()A.-3B.+3C.-2D.+22.2017年5月18日,我国成为了世界上第一个连续海上开采可燃冰时间最长的国家,可燃冰的主要成分是甲烷水合物,C H4中碳元素的化合价是()A.-4B.-1C.+1D.+23.硫代硫酸钠,又名大苏打,化学式为N a2S2O3,其中S元素的化合价是()66A.+2B.+4C.+6D.-24.正确使用和理解化学用语是重要的学科素养㊂下列说法正确的是()A.H2O㊁H2C O3中均含有氢分子B.K C l O3㊁K C l中氯元素的化合价不相同C.N a+㊁M g2+㊁A l3+原子核内质子数均为10D.㊁㊁表示的粒子都是阴离子5.亚硝酸钠(N a N O2)是一种有毒的工业用盐,N a N O2中氮元素的化合价是()A.-3B.+3C.+4D.+56.三氧化二铬(C r2O3)可用作油漆颜料,C r2O3中C r的化合价是()A.-3B.-2C.+2D.+37.锂电池是新型的高能电池,质量轻㊁电容量大,颇受手机㊁电脑等用户的青睐㊂某种锂电池的总反应可表示为L i+M n O2 L i M n O2㊂以下说法错误的是()A.该反应中L i的化合价发生了变化B.M n O2中锰元素的化合价为+4价C.L i M n O2属于氧化物D.该反应属于化合反应8.钴(C o)的化合物在锂电池中有很好的应用㊂L i C o O2(钴酸锂)在酸性介质中有强氧化性,其化学方程式为:2L i C o O2+H2O2+3H2S O4 L i2S O4+2C o S O4+4H2O+O2ʏ,已知锂与钠有相似的化学性质,且反应中只有钴和氧元素的化合价发生了改变㊂则下列说法正确的是()A.该反应是复分解反应B.该反应中钴的化合价由+3价变为+2价C.该反应中氧的化合价降低D.钴酸根离子是C o O2-2考向2化学用语9.(1)用化学用语填空㊂①碳元素;②3个钾原子;③4个氮分子;④钠离子;⑤氢气;⑥标出氧化钙中钙元素的化合价㊂(2)①3C u2+中表示离子个数的数字是;6768②S O 2中2 表示 ㊂10.成语是我国的文化瑰宝,请用恰当的化学用语表示下列成语相关内容中带点的字:(1)如胶似漆:胶中含有碳㊁氢㊁钙等元素,写出其中一种非金属的元素符号 ;(2)争风吃醋:醋溶液中含有氢离子 ;(3)大浪淘沙:沙的主要成分二氧化硅的化学式 ;(4)信口雌黄:雌黄即三硫化二砷(化学式为A s 2S 3),三硫化二砷中砷元素的化合价为+3价 ㊂11.家中常备的 84消毒液 的有效成分是次氯酸钠(N a C l O )㊂试计算:(1)次氯酸钠中钠㊁氯㊁氧元素的质量比为 ;(2)次氯酸钠中氯元素的化合价为 ㊂12.根据右图中标签上的信息填空:(1)写出物质的化学式 ㊂(2)写出物质中阴离子的符号 ㊂(3)标出物质中钙元素的化合价 ㊂(4)列举物质的一种用途 ㊂13.金属钠与氯气在一定条件下可以发生化学反应㊂该反应的化学方程式:2N a +C l 2点燃 2N a C l ㊂根据所给信息,请回答下列问题:(1)当钠与氯气反应时,每个氯原子 成为氯离子㊂(2)从氯气变为氯化钠时,氯元素化合价的具体变化为:( )ң( )㊂(3)氯化钠溶液能导电,是因为氯化钠溶于水形成了大量自由移动的 (填微粒符号)㊂14.江西龙虎山因特有的丹霞地貌被誉为 中国红石公园 ,其红色砂砾岩由石灰岩㊁氢氧化铁㊁石膏等成分组成㊂请用恰当的化学用语表示下列带点部分:(1)石灰岩中含有的钙元素 ;(2)石膏主要成分硫酸钙中含有的阴离子;(3)岩石呈红色是含氢氧化铁所致,氢氧化铁中铁元素显+3价㊂69。
专题8硅元素
1.硅在周期表中的位置是周期族,其原子结构示意图为
2.SiO2的物理性质:色____体,____溶于水。
3.SiO2与氢氟酸反应(此反应可用于解释) SiO2与氧化钙反应
SiO2与氢氧化钠反应(此反应可用于解释) 4.硅酸是一种很的酸,溶解度很____。
硅酸浓度较大时,则合成软而透明的、________状的硅酸______。
硅酸的制备原理:
5.最简单的硅酸盐是:,可溶于水,其水溶液俗称为,是制备硅胶和等的原料。
练习:
1.(07夏季)下列有关物质用途的说法中,不正确
...的是
A . 明矾可用作净水剂 B. 铁制容器可用于盛放稀硫酸
C. 二氧化硅可用于制作光导纤维
D. 苯酚的水溶液具有杀菌消毒性能
2.(08夏季)硅单质及其化合物在材料领域中一直扮演着主要角色。
下列叙述中,不正确
...的是A.石英可用来制作工艺品
B.硅单质可用来制造太阳能电池
C.硅单质是制造玻璃的主要原料
D.二氧化硅是制造光导纤维的材料
3.(08春季)下列有关物质用途的说法中,不正确
...的是
A.硅可用作半导体材料
B.二氧化硫可用于漂白纸浆等
C.铝制容器可用于盛放稀硫酸
D. 过氧化钠可用作呼吸面具中氧气的来源
4.(10夏季)下列有关物质用途的说法中,不正确
...的是
A.硅可用作半导体材料 B.铜或铝可用于制造电缆
C.工业上在常温常压下用氮气和氢气直接合成氨 D.过氧化钠可作为呼吸面具或潜水艇中氧气的来源
5.(10春季)下列说法正确的是
A.工业上常用电解法冶炼单质铁
B.晶体硅可用于制造光导纤维
C.氯气可以用于制造漂白粉
D.甲烷的产量可以用来衡量一个国家石油化工发展水平
6.(11夏季)下列关于SiO2性质的说法中,不正确
...的是
A.能与水反应B.能与氢氟酸反应
C.能与氧化钙反应D.能与氢氧化钠溶液反应
7.(11春季)下列元素中,原子半径最小的是
A.Si B.P C.S D.Cl
8.下列有关物质用途的说法中,正确的是
①Cl2可用于制造漂白粉②Si可用于制造半导体材料③SiO2可用于制造光导纤维A.只有①②B.只有②③C.只有①③D.都正确9.(07春季).(3分)工业上可用碳在高温下还原二氧化硅的方法制取少量粗硅:
SiO2 + 2C 高温
Si + 2CO↑。
在该反应中,作为氧化剂的物质是(填化学式),作为
还原剂的物质是(填化学式);若反应中生成了1 mol Si,则需消耗mol SiO2。
10. 有下列物品或设备:①陶瓷餐具②砖瓦③水泥路桥④门窗玻璃⑤水晶镜片⑥石英钟表
⑦玛瑙手镯⑧硅太阳能电池⑨石英光导纤维⑩计算机芯片
(1)用到硅单质的是_______________________________________________
(2)所用材料为SiO2或要用到SiO2的是______________________________
(3)所用材料为硅酸盐的是_________________________________________。