钠的还原性和用途
- 格式:doc
- 大小:11.60 KB
- 文档页数:3

钠的高中化学知识点总结钠是一种极为重要的化学元素,它是周期表中的一种碱金属,属于第一族元素。
它的化学符号为Na,原子序数为11,电子构型为[Ne]3s1。
钠是一种非常活泼的金属,它在常温常压下是一种银白色的固体,具有良好的导电性和导热性,是现代工业中的重要原材料之一。
下面就来总结一下钠的高中化学知识点。
一、钠的物理性质钠的密度是0.97g/cm3,熔点为97.8℃,沸点为893℃。
钠在常温下呈固态,是一种非常软的金属。
二、钠的化学性质1.钠的反应性钠是一种非常活泼的金属,在空气中容易发生氧化反应。
钠可以和氧气、水蒸气、氯气等各种化合物反应,其中最典型的反应是和水反应,生成氢气和氢氧化钠:2Na(s)+ 2H2O(l)→2NaOH(aq)+ H2(g)2.钠的还原性钠在化学反应中通常是还原剂。
它可以与氧、硫、卤素等其他元素发生反应,将它们还原成更高价态的化合物。
3.钠的酸碱性钠的氧化物是一种碱性氧化物,它可以与酸反应,产生盐和水,如:Na2O(s)+ H2SO4(aq)→ Na2SO4(aq)+ H2O(l)4.钠在生活中的应用由于钠是一种非常活泼的金属,因此它在生活中的应用非常广泛。
晒盐、泡糖、洗衣粉、汽车制动器等都含有钠元素。
此外,在冶金和化工行业中,钠也是非常重要的原材料之一。
三、钠的化合物1.氧化钠(Na2O)氧化钠是钠的一种氧化物,它是一种白色固体,具有极强的碱性。
氧化钠可以和水反应生成氢氧化钠:Na2O(s)+ H2O(l)→ 2NaOH(aq)2.氢氧化钠(NaOH)氢氧化钠是钠的一种氢氧化物,它是一种白色固体,具有极强的碱性。
氢氧化钠可以和酸反应,形成盐和水,如:NaOH(aq)+ HCl(aq)→ NaCl(aq)+ H2O(l)3.碳酸钠(Na2CO3)碳酸钠是钠的一种碳酸盐,它是一种白色固体,具有极强的碱性。
碳酸钠可以和酸反应,形成盐和二氧化碳,如:Na2CO3(s)+ 2HCl(aq)→ 2NaCl(aq)+ CO2(g)+ H2O (l)四、钠的安全注意事项1.钠是一种非常活泼的金属,具有极强的还原性,平时使用时必须格外小心。

金属钠用途2篇金属钠用途(上)金属钠,化学符号Na,是一种常见的碱金属元素。
它具有低熔点、高导电性、良好的塑性和较强的还原性,因此在很多领域都有着广泛的应用。
本文将介绍金属钠的两个主要用途。
第一,金属钠在化学工业中的应用。
金属钠作为还原剂可以广泛应用于化学合成反应中。
例如,钠与水反应生成氢气和氢氧化钠,常用于废水处理、制取氢气等过程中。
此外,钠在其他化学反应中也起到重要作用。
比如,金属钠可以用于制备有机化合物中的那些活泼低价反应物,如烷基溴化物、酯类和芳香化合物等,用于重要的合成反应,如Finkelstein反应、Williamson合成等。
第二,金属钠在冶金工业中的应用。
钠可以与很多金属形成合金,这些合金具有一些特殊的性质。
例如,钠与铅、锌等金属形成的合金具有低熔点和良好的流动性,被广泛应用于钎焊、涂铝和熔莱等工艺中。
此外,钠还可以与一些高活性金属如锂、钾等形成合金,来改善这些金属的性能。
例如,钠-锂合金广泛应用于电池领域,可以提高电池的放电容量和循环寿命。
金属钠还有许多其他的应用领域,例如在玻璃工业中用于去除气泡、制取氧化钠等;在电化学工业中用作电解质;在农业上用于土壤改良等。
总的来说,金属钠作为一种常见的化学元素,在各个领域都有重要的用途。
金属钠用途(下)金属钠是一种常见的碱金属元素,具有许多独特的化学特性,因此在各个领域都有广泛的应用。
除了化工和冶金行业之外,金属钠还在食品添加剂和医药领域中发挥着重要作用。
首先,金属钠在食品添加剂中的应用。
钠在人体中具有重要的生理功能,是维持生命活动所必须的元素之一。
因此,钠离我们的生活非常近,我们平常所吃的食物中可能有所添加的钠成分。
比如,钠盐(食盐)是我们食物中不可或缺的调味品,用于提鲜和改善口味。
此外,钠还用作食品加工过程中的抗氧化剂、pH调节剂和防腐剂等。
其次,金属钠在医药领域的应用。
钠离子在人体中起着重要的生理作用。
钠离子与钾离子在人体内外细胞液中的浓度差异维持了细胞内外电位差,对神经传导、肌肉收缩和体液平衡等都起到了重要作用。

钠和氯化钠的区别及应用钠和氯化钠是化学中常见的物质,它们在性质和应用方面有着明显的区别。
本文将探讨钠和氯化钠的区别,并介绍它们在实际应用中的用途。
一、钠的特性和应用钠是一种具有金属光泽的银白色固体,在常温下具有较强的活泼性。
它属于碱金属元素,处于周期表第一组,原子序数为11,化学符号为Na。
钠在自然界中主要以氯化钠的形式存在于海水、盐湖和地下矿床中。
钠的主要特性及应用如下:1. 高反应活性: 钠是周期表中最活泼的金属元素之一,与水反应时能够剧烈放热,并产生氢气。
这种高反应活性使钠广泛用于制备金属合金和有机合成反应中。
2. 强还原性: 钠具有较强的还原能力,可以和许多非金属元素直接发生反应。
因此,在冶金和化工领域中,钠常被用作还原剂,例如在高温下用于炼制金属和合成有机物。
3. 玻璃工业: 钠离子对玻璃的透明度和抗热性具有重要影响。
钠在玻璃制造中被广泛应用,用于调节玻璃的物理特性,例如使玻璃更耐高温和耐腐蚀。
4. 医药领域: 钠是人体细胞内外的一种重要离子,它参与调节细胞内外的液体平衡,维持神经和肌肉功能的正常运作。
因此,钠离子是医药领域中一种常用的重要药物配方和生理盐水的成分。
二、氯化钠的特性和应用氯化钠是由钠离子(Na+)和氯离子(Cl-)组成的化合物。
它是一种白色晶体固体,在自然界中广泛存在于海水、盐湖和地下盐矿中。
氯化钠的主要特点及应用如下:1. 食盐: 氯化钠是人类饮食中最常见的食盐来源,被广泛应用于调味和食品加工中。
氯化钠还被添加到许多加工食品和罐头食品中,以延长其保质期和增加口感。
2. 医疗用途: 氯化钠溶液被广泛应用于医疗领域,如生理盐水用于注射、眼药水、漱口水、鼻用溶液等。
这是因为氯化钠具有生理盐水溶液相似的渗透压,能够与人体组织充分兼容。
3. 工业应用: 氯化钠在工业领域具有多种应用,例如用于制备氯气和钠金属。
另外,氯化钠还用作染料和纤维工业中的盐酸、硫酸和烟酸的原料。
4. 水处理剂: 氯化钠在水处理中被广泛用作软化水、消毒和除垢剂。


金属钠的主要用途
金属钠是一种非常活泼的金属,在化学反应中往往具有很强的还
原性和反应性。
因此,在工业上,金属钠的主要用途是作为还原剂和
反应剂来使用。
下面,就我们来看看金属钠在不同行业的主要应用。
1. 有机合成工业:金属钠可用于许多有机合成反应,如羧酸盐
的还原、卤代烃的烷基化、脱氢反应等。
此外,金属钠还广泛用作有
机合成中的强还原剂,例如,可以将硝基化合物和草酸盐转化为氨、
烷基和芳香族化合物。
2. 制取有机化学品:金属钠在合成有机化学品中也有广泛的应用,如制取苯乙烯、甲基丙烯酸、丙烯酸、乙烯基酮等。
此外,金属
钠还用作染料、橡胶、药品、香料等有机化学品的生产原料。
3. 金属材料工业:金属钠能与氧气、氮气、碳、硫等元素反应
生成不同的金属化合物,这些金属化合物具有很高的物理和化学性质,在金属材料工业中具有广泛的应用,如用于钢铁、铜、铝、锌等金属
的冶炼、烧结和脱氧等。
4. 化肥农药工业:金属钠是合成某些高附加值农药的重要原料
之一。
例如,金属钠可以用来合成防治茶叶黑夜盗、稻瘟、葡萄霜霉病、白菜黑腐病等的农药;同时,金属钠也可以用来制造各种化肥,
如镁肥、钾肥等。
总之,金属钠在各个行业的应用范围非常广泛,同时,由于其活
泼性比较大,所以在使用过程中必须要注意使用方法,防止安全事故
的发生。

单质钠的知识点总结1. 物理性质单质钠是一种银白色的金属,在常温下呈固态,具有良好的延展性和可塑性。
钠的熔点为97.72°C,沸点为883°C,密度为0.97g/cm³。
钠是一种较活泼的金属,易与空气和水反应,生成氢氧化钠和氢气。
2. 化学性质钠是一种典型的碱性金属,具有较强的还原性。
它与氧、氮、硫等非金属元素反应,生成相应的氧化物、氮化物和硫化物。
此外,钠还与许多无机化合物发生反应,如与酸类、氯化物、硫酸盐等反应生成相应的盐类。
3. 表面处理钠具有良好的表面处理性能,可以通过轧制、冷拔、挤压、锻造等方式加工成各种形状的产品。
另外,钠还可以进行电解抛光、阳极氧化等表面处理,使其表面光亮、光滑、耐腐蚀。
4. 金属合金钠可以与铅、铝、铜、锌等金属形成多种合金,这些合金具有较好的力学性能、电导率和耐腐蚀性能。
钠铅合金具有低熔点和良好的润湿性,常用于电子焊接和密封领域。
5. 化工用途钠是许多化工产品的重要原料,如氢氧化钠、氯化钠、碳酸钠等。
这些化工产品广泛应用于玻璃、皂业、造纸、制药、冶金等领域,对于人们的日常生活有着重要的影响。
6. 金属钠的应用金属钠在冶金、电池、合成橡胶、制备有机化合物等方面有着广泛的应用。
在择优的储能系统中,钠-硫电池系统因其低成本、高能量密度和对不同规模的储能需求具有优越性,被认为是充分利用钠资源的重要手段。
7. 健康影响钠是人体必需的微量元素之一,参与调节体内的电解质平衡和细胞功能。
但是,过量摄入钠会导致高血压、心脏病、中风等疾病,因此建议人们适量摄入食盐和高钠食物,并注重平衡膳食。
以上是关于单质钠的一些知识点总结,希望能帮助您更好地了解这种重要的金属元素。
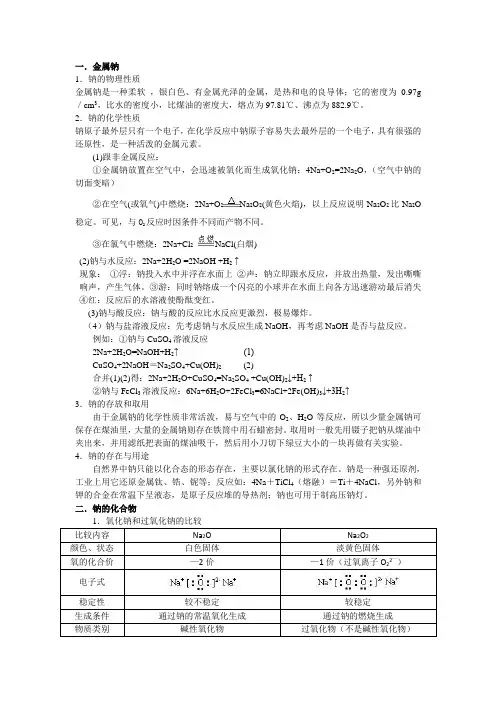
一.金属钠1.钠的物理性质金属钠是一种柔软,银白色、有金属光泽的金属,是热和电的良导体;它的密度为0.97g /cm3,比水的密度小,比煤油的密度大,熔点为97.81℃、沸点为882.9℃。
2.钠的化学性质钠原子最外层只有一个电子,在化学反应中钠原子容易失去最外层的一个电子,具有很强的还原性,是一种活泼的金属元素。
(1)跟非金属反应:①金属钠放置在空气中,会迅速被氧化而生成氧化钠:4Na+O2=2Na2O,(空气中钠的切面变暗)②在空气(或氧气)中燃烧:2Na+O2Na2O2(黄色火焰),以上反应说明Na2O2比Na2O 稳定。
可见,与O2反应时因条件不同而产物不同。
③在氯气中燃烧:2Na+Cl2NaCl(白烟)(2)钠与水反应:2Na+2H2O =2NaOH +H2↑现象:①浮:钠投入水中并浮在水面上②声:钠立即跟水反应,并放出热量,发出嘶嘶响声,产生气体。
③游:同时钠熔成一个闪亮的小球并在水面上向各方迅速游动最后消失④红:反应后的水溶液使酚酞变红。
(3)钠与酸反应:钠与酸的反应比水反应更激烈,极易爆炸。
(4)钠与盐溶液反应:先考虑钠与水反应生成NaOH,再考虑NaOH是否与盐反应。
例如:①钠与CuSO4溶液反应2Na+2H2O=NaOH+H2↑ (1)CuSO4+2NaOH=Na2SO4+Cu(OH)2(2)合并(1)(2)得:2Na+2H2O+CuSO4=Na2SO4 +Cu(OH)2↓+H2↑②钠与FeCl3溶液反应:6Na+6H2O+2FeCl3=6NaCl+2Fe(OH)3↓+3H2↑3.钠的存放和取用由于金属钠的化学性质非常活泼,易与空气中的O2、H2O等反应,所以少量金属钠可保存在煤油里,大量的金属钠则存在铁筒中用石蜡密封。
取用时一般先用镊子把钠从煤油中夹出来,并用滤纸把表面的煤油吸干,然后用小刀切下绿豆大小的一块再做有关实验。
4.钠的存在与用途自然界中钠只能以化合态的形态存在,主要以氯化钠的形式存在。

一.金属钠1.钠的物理性质2.钠的化学性质钠原子最外层只有一个电子,在化学反应中钠原子容易失去最外层的一个电子,具有很强的还原性,是一种活泼的金属元素。
(1)跟非金属单质(如与O2 ,Cl2反应)反应:(2)钠与水反应现象:离子方程式:-----------------------------------------------------------------------------------(3)钠与酸反应:钠与酸的反应比水反应更激烈,极易爆炸。
(4)钠与盐溶液反应:先考虑钠与水反应生成NaOH,再考虑NaOH 是否与盐反应。
例如:①钠与CuSO4溶液反应钠与硫酸铜反应的离子方程式:--------------------------------------------------------②钠与FeCl3溶液反应:---------------------------------------------------------------------3.钠的制取保存及用途:(1)制取:(2)保存:密封保存,通常保存在煤油或石蜡油中。
4.钠的存在与用途自然界中钠只能以化合态的形态存在,主要以氯化钠的形式存在。
钠是一种强还原剂,工业上用它还原金属钛、锆、铌等;反应如:4Na+TiCl4(熔融)=Ti+4NaCl,另外钠和钾的合金在常温下呈液态,是原子反应堆的导热剂;钠也可用于制高压钠灯。
5.钠的化合物(1).氧化钠和过氧化钠的比较(2).碳酸钠与碳酸氢钠溶解度比较:热稳定性稳定易失水、风化受热易分解:----------------------------------------色态白色粉末无色晶体H+NaOH不反应HCO3-+OH—=CO32-+H2O用途用于玻璃、肥皂、造纸、纺织等工业,洗涤发酵剂、灭火器,医疗上用于治胃酸过多转化6.有关钠及其化合物的几个问题(1).金属钠露置在空气中的变化过程:银白色金属钠(2).Na2CO3与盐酸的互滴反应a.向盐酸里逐渐滴加入Na2CO3溶液(开始时酸过量)开始就有气体放出;b向Na2CO3溶液里逐滴加入盐酸(开始时酸不足)开始无气体产生:HCl+Na2CO3=NaCl+NaHCO3(无气泡)HCl+NaHCO3=NaCl+CO2↑+H2O可见不同的滴加顺序产生不同的现象,利用这种现象不用其他试剂就可鉴别Na2CO3溶液和盐酸。

钠的主要性质及其应用1.钠的物理性质(1)颜色:银白色,有金属光泽。
(2)密度:ρ(H 2O)>ρ(Na)>ρ(煤油)。
(3)熔点:低于100 ℃。
(4)硬度:质地柔软,可以用小刀切割。
2.从钠原子的结构认识钠的化学性质——还原性(1)与非金属单质(如O 2、Cl 2)的反应O 2⎩⎪⎨⎪⎧常温:4Na +O 2===2Na 2O点燃:2Na +O 2=====△Na 2O 2Cl 2:2Na +Cl 2=====点燃2NaCl(2)与水反应离子方程式:2Na +2H 2O===2Na ++2OH -+H 2↑。
要点提取钠与滴有酚酞的水反应的现象及解释(3)与盐酸反应离子方程式:2Na +2H +===2Na ++H 2↑。
特别提醒(1)钠的取用方法:用镊子夹取一小块钠,用滤纸吸干表面的煤油,在玻璃片上用小刀切取黄豆大小的钠,剩余的钠放回原试剂瓶。
(2)钠失火的处理:沙土盖灭,不能用水或泡沫灭火器灭火。
3.钠的制取及保存(1)制取:化学方程式为:2NaCl(熔融)=====电解2Na +Cl 2↑。
(2)保存:密封保存,通常保存在石蜡油或煤油中。
4.钠的用途(1)制取Na 2O 2等化合物。
(2)钠、钾合金(液态)可用于原子反应堆的导热剂。
(3)用作电光源,制作高压钠灯。
(4)冶炼某些金属金属钠具有强的还原性,熔融状态下可以用于制取金属,如:4Na +TiCl 4=====熔融4NaCl +Ti 。
【互动思考】1.取一小块金属钠,放在燃烧匙里加热,下列实验现象描述正确的是________(填序号)。
①金属钠先熔化 ②在空气中燃烧,放出黄色火花 ③燃烧后得白色固体 ④燃烧时火焰为黄色 ⑤燃烧后生成浅黄色固体物质答案 ①④⑤2.金属钠露置在空气中会发生一系列变化:银白色金属钠――→O 2(生成 )表面变暗 ――→H 2O (生成 )出现白色固体 ――→H 2O (NaOH )表面变稀――→CO 2(生成Na 2CO 3·10H 2O )白色块状物质 ――→风化(生成 )白色粉末状物质答案 Na 2O NaOH 溶液 Na 2CO 33.将一小块金属钠分别投入盛a 水、b 乙醇、c 稀H 2SO 4的三个小烧杯中,反应速率由快到慢的顺序为_____________________________________________________________________ ___。

金属钠用途金属钠是一种常见的金属元素,具有广泛的应用领域。
本文将从多个角度介绍金属钠的用途。
一、化学反应剂金属钠是一种极活泼的金属元素,能够与氧气、水和许多非金属元素发生剧烈反应。
由于其极强的还原性,金属钠常被用作化学反应剂。
例如,在有机合成反应中,金属钠可以用来去除醛、酮等化合物中的羰基,从而合成相应的醇。
此外,金属钠还可以与醇反应生成烷基钠,用于合成烷烃化合物。
二、合金制备金属钠具有良好的可塑性和导电性,因此常被用于制备合金。
与铝、铅、锡等金属元素合金化后,可以增加材料的强度、硬度和耐腐蚀性。
此外,由于金属钠的低熔点和良好的润湿性,它还常被用作铝合金的焊接剂,能够提高焊缝的质量。
三、储能材料金属钠是一种重要的储能材料。
钠离子电池是一种高能量密度的二次电池,其中的正极材料通常采用金属钠或钠化合物。
金属钠的电极反应具有较高的反应活性和电化学稳定性,能够实现高能量密度的储能效果。
钠离子电池在电动汽车、太阳能储能等领域具有广阔的应用前景。
四、玻璃制备金属钠在玻璃工业中也有重要的应用。
钠化合物是玻璃的主要成分之一,可以降低玻璃的熔点和粘度,提高玻璃的透明度和抗热冲击性。
金属钠通常与硅酸盐等玻璃成分一起熔融,用于制备各种类型的玻璃,如平板玻璃、玻璃纤维等。
五、制备有机化合物金属钠在有机合成中的应用也非常广泛。
金属钠可以与卤代烃反应,生成相应的有机钠化合物。
有机钠化合物是许多有机合成反应的重要中间体,可以用于合成醇、酮、醛等有机化合物。
此外,金属钠还可以与醇反应生成烷基钠,用于碳-碳键的形成,从而实现复杂有机分子的合成。
六、防腐剂金属钠在金属表面处理中用作防腐剂。
金属钠可以与金属表面的氧气和水反应,形成氧化钠和氢氧化钠,从而形成一层保护膜,防止金属表面进一步氧化和腐蚀。
这种防腐效果在航空、船舶等领域有着广泛的应用。
金属钠具有许多重要的应用领域,包括化学反应剂、合金制备、储能材料、玻璃制备、有机化合物合成和防腐剂等。

钠及其化合物知识点总结钠是第11个元素,属于金属元素。
在化学反应中,钠常被用作还原剂,因为它对氧化物具有强烈的还原性。
钠是一种非常活泼的金属,它可以在接触空气时产生火花并起火,因此必须以特殊的方式储存和处理。
钠的物理特性:钠是一种银白色的金属,具有非常低的密度,因此它可以漂浮在水上。
它的熔点为97.8°C,沸点为882°C,密度为0.97克/毫升。
钠的化学特性:钠具有非常高的反应性,它能够与许多元素和化合物反应,生成各种类型的化合物。
钠和氧气反应时,会产生白色的氧化钠(Na2O)。
钠还可以与水反应,生成氢氧化钠(NaOH)和氢气(H2)。
当钠和氯气反应时,会生成白色的氯化钠(NaCl)。
氢氧化钠:氢氧化钠(NaOH)是一种强碱性化合物,是钠最常见的化合物之一。
它可以通过将钠金属直接与水反应得到。
氢氧化钠在工业上用于生产肥皂、卫生纸和清洁剂等。
氯化钠:氯化钠(NaCl)也被称为食盐,是钠最常见的化合物之一。
氯化钠在食品中被广泛使用,也用于制药、化工和水处理等领域。
碱性火箭燃料:钠也可以被用作火箭燃料的成分之一,其中钠与液氧混合在一起。
这种混合物的燃烧产生了非常高的温度和火焰速度,可以使火箭运行更有效率。
钠的危害:钠在人体内必须以适量的方式摄入,过量的摄入会对健康造成危害,包括增加血压、心脏病、肥胖和骨质疏松等疾病。
总之,钠是一种非常活泼的金属,它具有强烈的还原性和反应性,可以与许多元素和化合物反应生成多种类型的化合物。
它的化合物包括氢氧化钠、氯化钠等,在工业生产和日常生活中都具有重要的应用价值。
同时,过量的摄入会对人体健康造成危害,应注意控制摄入量。
除了以上介绍的氯化钠和氢氧化钠,钠还有一些常见的化合物,如硫酸钠、磷酸钠、碳酸钠等,它们在工业生产、医药和日常生活中都有重要的用途。
硫酸钠:硫酸钠(Na2SO4)是一种无色无臭的结晶体,它是一种重要的工业化学品,用于制造玻璃、纸张、墨水、清洁剂等。
高中化学-钠及其化合物的性质最全知识点总结1、知识点1:钠原子结构从钠的原子核外电子排布看,其最外电子层上只有一个电子,因此,极易将这一电子失去,而达到稳定结构,形成+1价的钠阳离子(Na+)。
即金属钠的原子结构决定了其性质的活泼。
因其易失电子被氧化,故金属钠是还原剂。
2、知识点2:钠的物理性质钠是银白色金属,质软(可用刀切割),密度小(0.97g/cm3),熔点低,是电和热的良导体。
3、知识点3:钠的化学性质由于钠原子最外层只有一个电子,在化学反应中容易失去最外层的一个电子变为钠离子:Na-e-→Na+所以钠的化学性质极活泼,具有强还原性,是强还原剂,具有金属的典型性质。
(1)与非金属反应A、与氧气的反应常温下能与空气中的氧气化合,表面变暗。
4Na+O2=2Na2O 在空气或氧气中燃烧,发出黄色火焰,生成淡黄色固体。
2Na+O2Na2O2B、与硫反应2Na+S=Na2S(研磨易爆炸)C、与氯气反应2Na+Cl22NaCl(发出黄色火焰,产生白烟)(2)与水反应钠与水反应的实验现象及现象解释如下:注:钠与水反应在钠的周围有白雾生成,此白雾是氢气燃烧产生的水蒸气。
钠与水反应的化学方程式为: 2Na+2H2O=2NaOH+H2↑该反应的实质是钠原子与水电离出的H+发生氧化还原反应,其离子方程式为: 2Na+2H2O=2Na++2OH-+H2↑注:钠与水反应的现象可概括为“浮、熔、游、响、红”,并结合钠的性质进行记忆。
(3)与酸反应钠与酸反应比与水反应更加激烈,极易爆炸。
钠与盐酸反应 2Na+2HCl=2NaCl+H2↑钠与稀硫酸反应 2Na+H2SO4 =Na2SO4 +H2↑钠与酸溶液反应的实质是:钠与酸电离出来的H+直接反应,而不是钠先与水反应,生成的氢氧化钠再和酸溶液反应。
因为钠与水反应时,得电子的是水电离的H+,而酸中H+浓度大于水中H+的浓度。
(4)与盐的反应与熔融盐的反应4Na+TiCl4(熔融)==Ti+4NaCl与盐溶液反应将钠加到盐溶液中,首先是钠与水反应,若生成的氢氧化钠与盐能发生复分解反应,生成难溶物或弱电解质等,则氢氧化钠和盐再反应;否则钠只与水反应。
钠金属知识点总结钠是一种常见的化学元素,它是第11号元素,化学符号为Na,原子序数为11。
钠是一种易熔、易氧化的金属,在自然界中以碳酸盐和氯化钠的形式广泛存在。
钠金属在工业生产和实验室应用中具有广泛的用途,本文将对钠金属的性质、用途以及相关的知识点进行总结。
一、钠金属的性质1. 外观和物理性质钠金属是一种银白色的块状金属,在常温下具有良好的延展性和可塑性。
钠的熔点为97.80°C,沸点为893.0°C,密度为0.971 g/cm³。
钠金属具有较低的硬度和熔点,因此易于加工和熔炼。
2. 化学性质钠金属具有较强的还原性,在空气中会迅速氧化生成氧化钠。
由于钠的还原性较强,因此在水中会剧烈反应并放出氢气,产生氢氧化钠。
此外,钠金属还与酸类物质发生反应,生成相应的盐类化合物。
3. 放射性由于钠金属中存在稳定的钠-23同位素,并且钠的原子核中的中子数比质子数稍多,因此钠金属是一种轻微的放射性物质。
然而,钠的放射性活性很低,对人体健康的影响极小。
二、钠金属的用途1. 工业生产钠金属在工业生产中有着重要的应用价值,主要用于制备金属钠化合物,如氢氧化钠、碳酸钠等。
这些化合物广泛应用于玻璃工业、皂液生产、纺织工业和冶金工业等领域。
2. 实验室应用钠金属在实验室中也有着重要的应用价值,例如用于合成有机化合物、催化剂制备、金属表面处理等方面。
此外,钠金属还可用于研究放射性同位素的性质和研究核反应等领域。
3. 其他用途钠金属还可用于制备钠灯、蓄电池、合金制备等领域。
由于钠金属具有较强的还原性和导热性,因此在一些特殊的工业领域具有重要的应用价值。
三、钠金属的安全问题1. 存储和运输由于钠金属具有强烈的还原性和与水反应产生氢气的特性,因此在存储和运输过程中应注意避免与水和潮湿空气接触。
此外,钠金属还应存放在干燥的环境中,并采取防火防爆措施。
2. 使用注意事项在使用钠金属时,应戴上防护眼镜和手套等个人防护装备,以避免钠金属造成的化学灼伤。
钠的性质与应用一、金属钠的物理性质二、从钠原子的原子结构认识钠的化学性质——还原性 1、主要化学性质(1)与非金属单质反应⎩⎨⎧O 2⎩⎨⎧常温:4Na +O 2===2Na 2O 点燃:2Na +O 2=====点燃Na 2O 2Cl 2:2Na +Cl 2=====点燃2NaCl(2)与水反应:2Na +2H 2O===2NaOH +H 2↑;(3)与酸(如盐酸)反应:2Na +2HCl===2NaCl +H 2↑; (4)与乙醇反应:2Na +2C 2H 5OH ―→2C 2H 5ONa +H 2↑;(5)与盐溶液(如硫酸铜溶液)反应:2Na +CuSO 4+2H 2O===Cu(OH)2↓+Na 2SO 4+H 2↑。
2、与滴加酚酞的水反应的现象及解释三、钠的制备原理、保存及用途 1、制备原理:2NaCl=====通电2Na +Cl 2↑。
2、保存方法实验室通常将少量钠保存在煤油中,目的是防止钠与空气中的O 2和水反应。
3、用途(1)制取钠的化合物;(2)冶炼特殊金属,如制钛:TiCl 4+4Na =====700~800 ℃Ti +4NaCl ; (3)钠钾合金常温下为液体,用于快中子反应堆作热交换剂;(4)高压钠灯发出的黄光射程远,透雾能力强,常用于道路和广场的照明。
4、金属钠与可溶性盐溶液反应的思维模板5、金属钠与溶液反应现象分析的思维模板(1)共性:因为钠与水的反应属于剧烈的置换反应,故钠与溶液反应有共同的现象产生。
①浮:钠浮在液面上;②熔:钠熔化成光亮的小球;③游:在液面上不停地游动直至反应完;④响:反应中不停地发出“嘶嘶”的响声。
(2)差异性:与酸及能形成弱碱的金属盐溶液反应时,由于溶液中H+浓度较大,反应比钠与水的反应剧烈,最后钠可能在液面上发生燃烧;与盐溶液反应时,还可能会生成沉淀四、钠的重要化合物1.氧化钠和过氧化钠的比较从元素化合价角度分析Na2O2的性质:(1)Na2O2的强氧化性4222 (3)遇CO2、H2O、H+,Na2O2发生自身的氧化还原反应。
化学钠归纳总结化学钠,化学符号为Na,原子序数为11,是一种常见的金属元素,属于碱金属族。
在自然界中,钠以盐的形式广泛存在,如食盐(氯化钠)和红花盐(亚硝酸钠)。
钠具有重要的工业和生物学应用,在化学领域中也有着广泛的研究和应用。
本文将对钠的性质、用途以及相关的化学反应进行归纳总结。
一、钠的性质钠是一种银白色的金属,具有良好的延展性和导电性。
在常温下,钠处于固态,但是由于其活泼的化学性质,钠很容易与空气中的氧气和水反应,产生氧化钠和氢气。
钠是一种相对软的金属,可以轻易被切割和压扁。
由于其活泼性,钠在储存和使用过程中需要注意防止与水和氧气接触。
二、钠的用途1. 钠在冶金和合金制备中广泛应用。
钠可以作为还原剂使用,将金属氧化物还原为金属。
此外,钠也可以与其他金属形成合金,提高金属的性能和特性。
2. 钠在化学工业中扮演着重要的角色。
例如,钠可以作为有机合成中的催化剂,加快化学反应速率。
此外,钠化合物如氯化钠、亚硝酸钠等也在生产化学品和制药领域中被广泛使用。
3. 钠在生物学中具有重要的作用。
人体内的神经细胞和肌肉细胞通过钠离子传递信号和实现肌肉收缩。
因此,钠离子是维持人体正常生理功能的重要离子之一。
食盐中的钠也是人体所需的重要营养元素。
三、钠的化学反应1. 钠与氧气反应生成氧化钠。
钠与氧气在加热条件下迅速发生反应,生成白色的氧化钠,并放出大量的热。
化学方程式如下:2Na + O2 → 2Na2O2. 钠与水反应生成氢气和氢氧化钠。
钠与水反应非常剧烈,产生氢气和氢氧化钠。
该反应会放出大量热量,甚至会引起水的剧烈沸腾和溅射,需要小心操作。
化学方程式如下:2Na + 2H2O → 2NaOH + H23. 钠与酸反应生成盐和氢气。
钠可以与酸反应,产生相应的盐和氢气。
具体的盐的类型取决于所用酸的种类。
例如,钠与盐酸反应生成氯化钠和氢气。
化学方程式如下:2Na + 2HCl → 2NaCl + H2总结:钠是一种具有重要应用价值的金属元素,具有良好的导电性和延展性。
考点一钠的性质及用途1.钠的物理性质银白色,有金属光泽的固体,质地柔软,熔点低(小于100 ℃),密度比水的小,但比煤油的大。
2.从钠原子的原子结构认识钠的化学性质——还原性Na――――――――→O2、Cl2、H2O、H+等失去e-Na+(1)与非金属单质(如O2、Cl2)的反应O2常温:4Na+O2===2Na2O=====△))Na2O2Cl2:2Na+Cl2点燃2NaCl(2)与水反应①离子方程式:2Na+2H2O===2Na++2OH-+H2↑。
②与滴加酚酞的水反应的现象及解释(3)与盐酸反应离子方程式:2Na+2H+===2Na++H2↑。
3.钠的制取及保存(1)制取:化学方程式为2NaCl(熔融)电解2Na+Cl2↑。
(2)保存:密封保存,通常保存在石蜡或煤油中。
4.钠的用途(1)钠钾合金(液态)可用于原子反应堆的导热剂。
(2)用作电光源,制作高压钠灯。
(3)冶炼某些金属金属钠具有强还原性,熔融状态下可以用于制取金属,如4Na+TiCl4熔融4NaCl+Ti。
例1、下列关于钠及其化合物的叙述正确的是____(填字母代号)。
①金属钠着火,可用水扑灭②钠是最活泼的金属③用瓷坩埚灼烧Na、Na2O、NaOH等④电解饱和食盐水可以制得金属钠⑤钠投入硫酸铜溶液中,先与水反应,不能置换出铜⑥将一小块钠放在石棉网上,用酒精灯加热后,剧烈燃烧,产生黄色火焰,生成氧化钠⑦比较水与乙醇中氢的活泼性的方法是分别将少量钠投入到盛有水和乙醇的烧杯中⑧钠在空气中燃烧可生成多种氧化物,23 g钠充分燃烧时转移电子数为N ANa2O Na2O2⑤过氧化钠的电子式:应生成Na2CO3和O2,反应中Na2O2既是氧化剂也是还原剂,②错误;Fe2+被Na2O2氧化成Fe3+,Fe2+数目减少,Fe3+数目增多,③错误;Na2O2与H2O反应生成NaOH和O2,NaOH与CuSO4反应生成Cu(OH)2和Na2SO4,两个方程式加和可得离子方程式,④正确;过氧化钠是离子化合物,电子式为,⑤错误;1 mol Na2O2中阳离子数目为2N A,阴离子数目为N A,离子数目为3N A,⑥错误;二氧化碳通过Na2O2粉末发生的反应为2Na2O2+2CO2====2Na2CO3+O2,固体由Na2O2变为Na2CO3,1mol Na2O2的质量为78g,1mol Na2CO3的质量为106g,反应后固体质量增加,⑦正确;Na2O是碱性氧化物,与盐酸反应生成NaCl和水,Na2O2盐酸反应生成NaCl、水和氧气,不是碱性氧化物,⑧错误;Na2O、Na2O2都易与空气中的H2O和CO2反应,都需密封保存,⑨错误;Na2O2放入氢氧化钠溶液中,会与溶液中的水反应,产生氧气,⑩错误。
钠与水反应还原剂钠是一种常见的金属元素,其化学性质非常活泼,具有很强的还原性。
钠与水反应的化学反应式为:2Na + 2H2O → 2NaOH + H2。
在这个反应中,钠原子失去一个电子,形成钠离子,并和水中的氢离子(H+)结合,生成氢气(H2)和氢氧化钠(NaOH)。
由于钠的还原性非常强,因此它可以被用作还原剂,用于许多化学反应中。
钠与水反应的过程非常剧烈,产生的氢气可以燃烧,产生明亮的火焰。
因此,在实验室中进行钠与水反应时,必须格外小心,避免产生危险。
在实验室中,通常使用小块的钠,将其放入一个装有水的玻璃容器中。
钠与水反应的速度非常快,因此要及时地将玻璃容器盖上,以防止氢气逸出。
钠与水反应的产物氢氧化钠是一种常见的碱性物质,具有强烈的腐蚀性。
因此,在实验室中进行钠与水反应时,必须小心处理产生的氢氧化钠溶液,以避免对环境和人体造成危害。
此外,钠与水反应的过程还会产生大量的热量,因此在实验室中进行反应时,必须注意控制温度,避免产生危险。
钠作为还原剂在化学反应中有着广泛的应用。
例如,在有机合成中,钠可以被用作还原剂,将羰基化合物还原成相应的醇。
此外,钠还可以被用作制备金属钠、钠酸、钠盐等化合物的原料。
在冶金工业中,钠也被广泛应用,用于提取金属、制备合金等。
钠与水反应的过程是一种非常重要的化学反应,具有广泛的应用价值。
但是,由于其反应过程剧烈、产物具有腐蚀性等特点,因此在实验室中进行反应时必须格外小心,避免产生危险。
同时,钠作为还原剂在化学反应中的应用也需要注意安全,避免产生危险。
只有在安全的条件下,才能充分发挥钠与水反应的应用价值。
钠的还原性和用途
钠是一种常见的金属元素,具有很强的还原性和广泛的用途。
在自然界中,钠主要以氯化钠(NaCl)的形式存在于海水和盐矿中。
下面我将详细介绍钠的还原性和用途。
首先,钠具有很强的还原性。
还原性是指金属元素易于失去电子的性质。
钠的还原性很强,其原子结构中的3s电子层只有一个电子,这导致钠原子容易失去这个电子以形成单正电荷的钠离子(Na+)。
因为钠原子中具有较低的电离能,所以钠很容易失去这个电子,而形成稳定的钠离子。
这种失去电子的能力使得钠具有很强的还原性能力,可以与许多物质发生反应,使其得到电子,从而还原成较低氧化态的状态。
当钠与其他元素或化合物反应时,钠的电子转移到其他物质中,使其他物质发生氧化反应。
此外,钠的还原性还表现为其能与水剧烈反应,生成氢气和氢氧化钠。
其次,钠具有广泛的用途。
由于钠的还原性和化学活性,使得钠在许多领域都有着重要用途。
1. 冶金工业:钠可以用于从锂、铅、锌、锡等金属的氧化物或氯化物中还原金属,制备精制的金属。
2. 食品工业:氢氧化钠(苛性钠)是一种重要的工业碱,它被广泛用于食品加工过程中的脱毛、脱皮和清洁。
3. 化学工业:钠作为原料和还原剂,被广泛用于制备许多化学品,如钠盐、有机合成、染料和涂料等。
4. 药品工业:钠离子在生物体内起着重要的作用,包括维持酸碱平衡和神经传导。
因此,钠离子在药品中广泛应用,如生理盐水、补充钠的口服补液等。
5. 玻璃工业:钠可以增加玻璃的折射率和熔点,使其透明度更高。
因此,钠化合物被广泛应用于玻璃制造中。
6. 石化工业:钠在石油加工中被用作催化剂,促使反应发生,提高石油转化效率。
7. 钠灯:钠灯是一种高强度放射光源,广泛用于室内和室外照明,如高速公路路灯和体育场照明等。
8. 核工业:钠在核工业中被用作冷却剂,其在快中子反应堆中的高热导率和低密度使其成为理想的冷却剂。
除了上述用途外,钠还被用于水处理、电池制造、金属加工、制浆造纸等领域。
然而,钠具有高度的活性,容易与氧气或水分子反应,在存储和使用过程中需要格外注意安全措施,避免产生火灾和爆炸等危险。
总结起来,钠是一种高度活性的金属元素,具有很强的还原性和广泛的用途。
钠的还原性使其能够与其他物质发生反应,从而在许多工业领域中得到应用。
然而,由于钠的活性和反应性,人们在存储和使用钠时需要格外小心,以防止事故的发生。