原子核式结构模型
- 格式:pptx
- 大小:9.58 MB
- 文档页数:11


原子核式结构模型
1 什么是原子核式结构模型
原子核式结构模型是指以原子核为中心,以其结构核素为外围组成的一种模型,是现代物理学提出的一种量子力学模型。
根据这种模型,原子核由质子和中子构成,其外围有质子、中子和费米子存在,使原子核具有特殊的结构。
2 原子核式结构模型的特点
1、核子的发明:今年是发现原子核的百年纪念,由爱因斯坦和玻尔在1905年提出核子模型,只有由正质子、负质子和中子组成。
2、结构特性:原子核由核子和核质子共同构成,核子质量极小,要比中子大2000倍以上,构成原子核的核质子的构成数量为其质量的比例,有的原子核还带有中性的费米子。
3、区别:原子核式结构模型与物理学里的分子模型完全不同,分子模型是以分子的中心的分子键为中心的,原子核式结构模型是以原子核的结构核素构成一个完整的模型。
3 原子核式结构模型的应用
原子核模型对物理学、化学、核物理学等多领域有重大影响,它可以解释原子中核子的形成、核素的变异等现象,为大规模原子核研究奠定了坚实的理论基础。
此外,它还可以用来解释原子构型的形成
以及其价态间的相互作用等,广泛应用于原子核反应和量子表现、原子与微粒子的测定等。

原子的核式结构模型20世纪20年代,科学家们开始采取一种叫做原子核式结构模型的概念,以研究原子的形态与特性。
自此以后,原子的核式结构模型的发展与改进一直是原子理论的中心所在。
原子核式结构模型源于二十世纪初丹麦物理学家斯提威尔预言的原子模型,以及由罗伯茨橹和法国物理学家卢克提出的确定原子结构的结构模型。
该模型假设原子是一个由原子核中心外围由电子组成的球形均匀结构。
原子核模型表明,电子存在于原子核周围以布朗电子球结构排列,形成了一个空间结构,这种空间结构是原子构型的基本动力。
因此,原子的结构在不同的元素中可以有不同的形态。
原子核模型同时提出了电子层次结构的概念,表明电子在原子核周围也按照层次结构排列。
在每一层次中,电子能限的数量也不同。
例如,一些元素有七个电子层次,而另一些元素可能只有三层电子层次。
同样,在不同的电子层次中,电子具有不同的能量。
随着进一步发展,原子核式结构模型也发展出一系列新的理论,包括量子电子理论、费米能级理论、空间结构理论、电子能级理论、电子轨道理论等。
量子电子理论可以解释原子的可见光谱线,费米能级理论可以解释原子核内电子的序列,而空间结构理论可以描述原子核内电子的周期性结构,电子能级理论可以解释复杂的元素结构,而电子轨道理论则可以解释电子结构中不同能级之间的转变。
原子核式结构模型改变了人们对原子结构的认知,也改变了物质特性的认识,特别是特定元素的化学性质等的理解。
它的发展也为物理学、化学等其他学科的发展作出了重大贡献,也极大地拓展了物理世界的认知范围。
总的来说,原子核式结构模型为研究原子的结构和性质奠定了基础,在今天仍然是原子理论研究的基础。
随着科学技术的发展,原子核式结构模型也发生了很大的变化,以更好地满足研究的需要。
因此,原子核式结构模型仍然是科学研究原子结构和性质的重要参考模型。
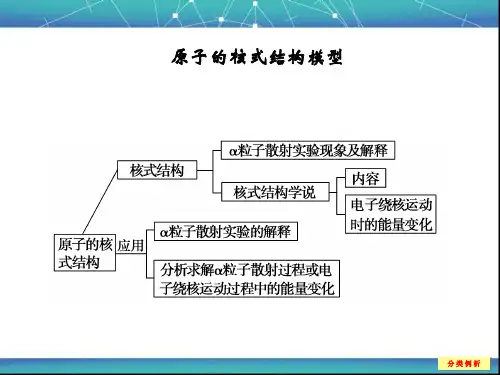


原子核式结构模型原子核式结构模型是一种描述原子内部结构的模型,它将原子的中心部分称为原子核,核外电子以云状分布在原子核周围。
该模型由英国的物理学家Rutherford于1911年提出,他通过一系列的金箔散射实验得出了这一结构模型。
在Rutherford的实验中,他使用了一个金箔和一个细小的放射性源,将放射性源发射出的α粒子射向金箔。
他观察到,射向金箔的大部分α粒子直接穿过金箔而没有发生任何偏转,但也有少数α粒子发生了较大角度的散射。
这个实验结果对于当时普遍认为原子是一个均匀分布的物质,或是由电子与正电荷均匀分布的"杏仁布丁模型"提出了挑战。
根据实验结果,Rutherford提出了原子核式结构模型:1.大部分的α粒子直接穿过金箔而没有发生偏转,说明原子内有一个非常小而且带有正电荷的核心,这个核心所占据的体积与整个原子相比非常小。
2.少数的α粒子发生了较大角度的散射,说明原子核带有正电荷,并且具有较高的密度。
3.原子核中带有正电荷,质量相对较大的粒子,这些粒子被称为质子。
4.原子核中可能还存在中性的、质量相对较大的粒子,这些粒子被称为中子。
这个假设后来得到了实验证实。
5.核外电子以一种云状的分布环绕在原子核周围,构成了原子的外部结构。
然而,原子核式结构模型仍然存在着一些问题和局限性。
例如,它无法解释电子如何在原子核附近运动,以及原子中质子和电子如何保持静止的平衡。
因此,在20世纪初,科学家们开始发展量子力学的理论来更加全面地描述原子内部结构。
总的来说,原子核式结构模型是一个革命性的模型,它的提出对原子结构的认识产生了重大影响。
虽然它的一个重要局限是无法解释质子和电子之间的平衡,但它为后来量子力学的发展奠定了基础,为我们更好地理解原子内部结构提供了关键性的启示。


原子的核式结构模型一、背景在深入研究原子的内部结构后,科学家们得出了一种关于原子构造的理论,即核式结构模型。
这个模型揭示了原子中心的秘密,为我们打开了理解物质世界的新视角。
二、核式结构模型的提出19世纪末,卢瑟福通过α粒子散射实验,发现原子中心有一个密集的原子核,其体积仅占据原子体积的几千分之一。
同时,他发现原子核周围环绕着电子,这些电子沿着轨道运动,就像行星围绕太阳运动一样。
这一发现,彻底改变了我们对原子的理解。
三、核式结构模型的内容核式结构模型的主要内容是:原子由一个位于中心的原子核和核外电子组成,电子在特定轨道上运动,并受到原子核的吸引。
原子核由质子和中子组成,其质量约占原子质量的99.9%,而电子的质量几乎可以忽略不计。
因此,原子的大部分体积是由原子核占据的。
四、核式结构模型的意义核式结构模型的提出,为我们理解原子的性质和行为提供了基础。
它解释了为什么原子在化学反应中会形成稳定的化合物,为什么元素之间会有不同的化学亲和力等等。
这一模型成为了现代化学的基础,为我们的科技发展提供了重要的理论基础。
五、结论总的来说,原子的核式结构模型是科学史上的一个重大突破,它为我们打开了理解物质世界的新视角。
然而,随着科技的发展,我们还需要更深入的研究和探索,以揭示原子内部的更多秘密。
让我们期待更多的科学发现,以更好地理解这个美丽的物质世界。
原子的核式结构模型一、背景在深入研究原子的内部结构后,科学家们得出了一种关于原子构造的理论,即核式结构模型。
这个模型揭示了原子中心的秘密,为我们打开了理解物质世界的新视角。
二、核式结构模型的提出19世纪末,卢瑟福通过α粒子散射实验,发现原子中心有一个密集的原子核,其体积仅占据原子体积的几千分之一。
同时,他发现原子核周围环绕着电子,这些电子沿着轨道运动,就像行星围绕太阳运动一样。
这一发现,彻底改变了我们对原子的理解。
三、核式结构模型的内容核式结构模型的主要内容是:原子由一个位于中心的原子核和核外电子组成,电子在特定轨道上运动,并受到原子核的吸引。



原子的核式结构模型核式结构模型最早由英国物理学家卢瑟福在1911年提出。
他的实验是在散射实验的基础上进行的,通过让高能α粒子正入射到金箔上观察散射的粒子轨迹,研究原子的内部结构。
核式结构模型的基本假设是原子由一个带正电荷的中心核和围绕核运动的电子组成。
核中包含质子和中子,质子带正电荷,中子不带电荷。
电子带负电荷,具有质量,绕核轨道运动。
根据核式结构模型,核中的质子和中子集中在原子的中心,形成原子核,质子和中子的数量决定了元素的原子序数和质量数。
围绕核的是电子云,电子云具有质量很小的特点,且电子数与质子数相等,以达到整个原子中的总正电荷等于总负电荷的平衡。
核式结构模型的主要特点有以下几点:1.原子核是原子的中心,质子和中子集中在这个中心,形成一个紧密结合的核。
质子带正电荷,中子不带电荷,所以核带正电荷。
原子核是非常小而密集的,但也是非常重要的,因为其中的质子和中子决定了元素的化学性质和质量数。
2.电子围绕着原子核,形成电子云。
电子云由负电荷的电子组成,它们被正电荷的核吸引,使得整个原子中的正电荷和负电荷保持平衡。
电子云的位置和运动状态是不确定的,只有在特定距离和特定能级上才能稳定地存在。
3.不同元素的原子核中质子和中子的数量不同,决定了元素的原子序数和质量数。
原子序数是指元素中的质子数,决定了其在元素周期表中的位置。
质量数是指一种元素中质子和中子的总数,决定了元素的相对原子质量。
核式结构模型的提出对后来的原子结构研究和理解有着重要的意义。
虽然核式结构模型无法解释电子云的具体结构和能级分布,也无法解释更微观的原子核内部结构和核反应的发生机制,但它奠定了原子结构领域的基础,并为后来量子力学的发展提供了重要的思路和依据。
总结起来,核式结构模型是描述原子内部结构的模型,认为原子由带正电荷的中心核和围绕核运动的电子组成。
质子和中子集中在核中,电子围绕着核形成电子云。
核式结构模型的提出为后来对原子结构的研究奠定了基础,也为量子力学的发展提供了启示。