烯烃的化学性质
- 格式:doc
- 大小:145.00 KB
- 文档页数:8

烯烃的化学性质烯烃是一类含有碳-碳双键的不饱和烃,具有一系列独特的化学性质。
它们在广泛的化学反应中扮演着重要的角色,包括聚合反应、加成反应、环化反应等。
了解烯烃的化学性质对于掌握它们的化学反应机理和应用具有重要意义。
第一部分烯烃的结构和基本性质烯烃的通式为CnH2n,其中n为整数。
它们通常用以下通式表示:R-CH=CH-R'其中R和R'代表烃基,它们可以相同或不同。
双键可以处于不同的位置,例如,丁烯可以具有以下两种结构:H2C=CH-CH2-CH3CH3-CH=CH-CH3烯烃与烷烃相比具有以下基本性质:1. 烯烃比烷烃更不稳定。
由于碳-碳双键中含有一个较弱的π键,烯烃比烷烃更容易发生化学反应。
然而,这种不稳定性也是烯烃广泛应用的原因之一。
2. 烯烃比烷烃的相对分子质量要小,这是由于没有饱和的碳-碳单键所带来的。
3. 烯烃的熔点和沸点通常较低,这使得它们易于挥发和处理。
4. 由于双键的存在,烯烃比烷烃更极性,从而更容易溶解在极性溶剂中。
然而,这也使得它们在空气中更易于氧化,从而稳定性较差。
第二部分烯烃的聚合反应烯烃聚合反应是一种重要的工业化学反应。
聚合反应是指将小分子单体通过共价键连接成高分子化合物的反应。
在烯烃聚合反应中,烯烃分子本身作为单体,通过引发剂或其他催化剂的作用,加入双键反应,形成高分子链。
聚合反应不仅在工业上应用广泛,也是生命体系中最基本的过程之一。
人体中的蛋白质、多糖和核酸等都是通过聚合反应形成的高分子化合物。
1. 自由基聚合反应烯烃自由基聚合是一种重要的聚合反应。
自由基聚合反应通常分为两个阶段:引发阶段和链延长阶段。
引发阶段由自由基引发剂引发。
自由基引发剂是一种可以在加热的条件下向双键直接断裂的化学物质。
断裂后,自由基会将一个氢原子从烯烃分子中夺取,从而生成新的自由基,继续进行反应。
链延长阶段是指自由基不断向分子添加,从而形成更长的链。
通常需要控制温度和催化剂添加速率以控制连锁反应的速率。

烯烃类知识点总结一、结构与命名烯烃的结构特点在于分子中存在一个或多个碳-碳双键。
烯烃分子可以是直链烯烃、支链烯烃、环烯烃或者芳香烯烃。
在直链烯烃中,碳-碳双键与链方向成直角,而在支链烯烃中,碳-碳双键与支链方向成直角。
环烯烃是由碳-碳双键连接而成的多环芳烃,而芳香烯烃则是指双键连接在芳香环上的化合物。
烯烃的命名符合一定的规则,以直链烯烃为例,按照IUPAC命名法的规定,将双键中的第一个碳原子所在的碳链称为主链,然后对其进行编号,以使双键取得最小的编号。
接着,需要根据碳-碳双键的位置添加前缀,如1-烯烃、2-烯烃等。
此外,对于支链或环状结构的烯烃,还需要考虑到支链或环状结构的位置以及命名顺序的问题。
二、性质1. 物理性质烯烃具有一些一般的碳氢化合物的物理性质,如挥发性、溶解性等。
其蒸气密度一般小于空气,在水中溶解度一般也较小。
2. 化学性质烯烃的化学性质主要与其碳-碳双键结构有关。
碳-碳双键具有较高的反应活性,在化学反应中往往会发生加成、氧化、还原等反应。
此外,烯烃还具有较强的亲电性和极性,因此能够与许多亲电试剂进行反应。
3. 烯烃的物理化学性质结合烯烃能够发生加成、氧化等反应,还具有比较强的亲电性与极性,因此具有很高的反应活性,往往能够参与许多重要的化学反应,如卤代反应、氧化反应等。
三、合成烯烃的合成方法较为多样,常见的合成方法包括以下几种。
1. 蒸汽裂解蒸汽裂解是一种重要的化学工业生产方法,它是通过将重质烃类化合物在高温下进行裂解,生成轻质的烯烃和烷烃。
在这一过程中,通常需要使用催化剂来调控裂解的反应条件。
2. 石油精制在石油精制过程中,可以通过对原油进行精制处理来分离出烯烃。
3. 化学合成烯烃还可以通过化学合成的方法来生产。
例如,可以通过醇的脱水反应或者氢化反应来合成烯烃。
四、应用烯烃在工业生产和科学研究中有着广泛的应用。
1. 燃料烯烃通常作为燃料使用,因其燃烧能力较强,在航空、汽车等领域有广泛的应用。




15周化学辅导(烯烃的结构特点、化学性质)一、烯烃的结构特点从乙烯的结构知,乙烯的两个C原子、四个氢原子在同一平面上,如果把乙烯中的四个氢原子换成甲基,由于CH2=CH2进行的是SP2杂化,所有原子在同一平面上,-CH3却进行的是SP3杂化,每个C原子处于小四面体的中心,C原子不在同一平面。
此物质中一定在同一平面的C原子有三个。
所以,在烯烃中只有C=C周围原来乙烯的六个原子的位置是一定在同一平面,这往往是考查点,再就是例1、描述分子结构的下列叙述中,正确的是:( )A、有6个碳原子可能都在同一条直线上B、7个碳原子有可能都在同一平面上C、有6个碳原子可能在同一平面上D、不可能有6个碳原子在同一平面上解析:乙烯的六个原子的位置是一定在同一平面,乙炔的四个原子在同一条直线上。
该结构中的后四个原子确实在一条直线上,但三个必定有键角接近与120°,所以A项不正确,而在中双键两边的碳原子共面,而叁键碳两边的碳原子共直线,所以这六个碳原子共面,而甲基的碳原子不能与它们共面.故本题选C.点拨:乙烯分子中所有原子都在同一平面内,键角为120°。
当乙烯分子中某氢原子被其他原子或原子团取代时,则代替该氢原子的原子一定在乙烯的平面内。
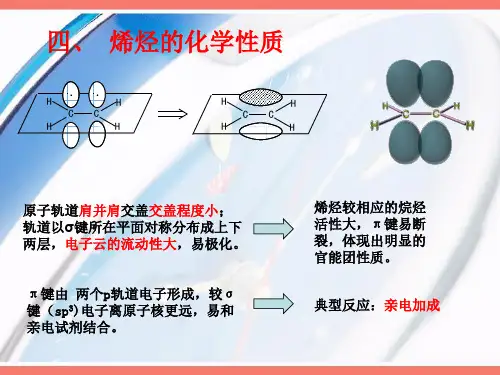
二、烯烃主要化学性质结构决定性质,由烯烃的结构可以得出含有碳碳双键,双键中的∏键容易断裂而发生加成反应,不稳定易被氧化。
1、加成反应①CH3-CH=CH2+ H2CH3-CH2-CH3②CH3-CH=CH2 + Br2 CH3-CHBr-CH2Br③CH3-CH=CH2+ HCl CH3-CHCl-CH3由反应②得出可使溴水或溴的四氯化碳溶液褪色,此反应可区别烷烃和烯烃。
同时还可以用来除杂.反应③符合马氏规则,注意方程式的书写。
例2、除去CH4气体中混有的少量乙烯,选用的最佳试剂是()A、NaOH溶液B、溴水C、浓H2SO4D、酸性KMnO4溶液解析:要除掉甲烷中的乙烯,可以运用两者的性质,即能除掉杂质,但又不能带入新的杂质,乙烯不与NaOH溶液和浓H2SO4反应,故排除A、C;可以与溴水反应,并且可以除掉乙烯,B正确;也能与酸性KMnO4溶液反应,但是反应后可生成CO2,有新的杂质生成。

烯烃的化学性质烯烃的化学性质很活泼,可以和很多试剂作用,主要发生在碳碳双键上,能起加成、氧化聚合等反应。
此外,由于双键的影响,与双键直接相连的碳原子(α-碳原子)上的氢(α-H)也可发生一些反应。
一.加成反应在反应中π键断开,双键上两个碳原子和其它原子团结合,形成两个σ-键的反应称为加成反应。
(一)催化加氢烯烃在催化剂作用下,低温低压既与氢加成生成烷烃。
(二)亲电加成在烯烃分子中,由于π电子具流动性,易被极化,因而烯烃具有供电子性能,易受到缺电子试剂(亲电试剂)的进攻而发生反应,这种由亲电试剂的作用而引起的加成反应称为亲电加成反应。
对电子具有亲和力的试剂叫做亲电试剂。
亲电试剂由于缺少电子,容易进攻反应物上带部分负电荷的位置,由这类亲电试剂进攻而发生发反应称为亲电反应。
亲电试剂通常为路易斯酸。
如:H+Br+、Cl+、H3O+、RC+=O、Cl2、Br2、I2、HCl、HBr、HOCl、H2SO4、F3C─COOH、BF3、AlCl3等烯烃的亲电加成反应历程烯烃的亲电加成反应历程可由实验证明实验说明:1.与溴的加成不是一步,而是分两步进行的。
因若是一步的话,则两个溴原子应同时加到双键上去,那么Cl–就不可能加进去,产物应仅为1,2-二溴乙烷,而不可能有1-氯-2-溴乙烷。
但实际产物中竟然有1-氯-2-溴乙烷,没有1,2-二氯乙烷。
因而可以肯定Cl–是在第二步才加上去的,没有参加第一步反应。
2.反应为亲电加成历程溴在接近碳碳双键时极化成,由于带微正电荷的溴原子较带微负电荷的溴原子更不稳定,所以,第一步反应是Brδ+首先进攻双键碳中带微负电荷的碳原子,形成溴鎓离子,第二步负离子从反面进攻溴鎓离子生成产物(反面进攻的证明见P142~144)。
第一步第二步在第一步反应时体系中有Na+、Brδ+,但Na+具饱和电子结构,有惰性,故第一步只有Brδ+参与反应,因而无1,2-二氯乙烷生成。
烯烃与各种酸加成时,第一步是H+ 加到双键碳上,生成碳正离子中间体,第二步再加上负性基团形成产物。

有关烯烃有关性质的总结13142125 李彤摘要:烯烃(alkene)是一类含有碳碳双键()的不饱和烃。
烯烃的代表物乙烯。
乙烯是石油化工基础的原料之一,乙烯产量的大小是衡量一个国家石油化工发展水平的重要标志。
烯烃是一个庞大的家族,因此有系统的命名方法。
大部分烯烃的化学反应都发生在双键上,主要有加成反应,取代反应以及氧化还原反应。
烯烃是重要的有机合成中间体,其化学性质值得人们深入的思考研究。
关键字:烯烃双键加成马氏规则一、烯烃的命名及结构1、烯烃的命名1)选主链:选择含双键最长的碳链为主链,命”某烯”。
2)编号码:近双键端开始编号,将双键位号写在母体名称前。
3)名支链:支链基团作为取代基。
注意:带有侧链的环状烯烃命名时,若只有一个不饱和碳上有侧链,该不饱和碳编号为1,若两个不饱和碳都有侧链,或都没有侧链,则碳原子编号顺序除双键所在位置号码最小外,还要同时以侧链位置号码的加和数最小为原则。
2、烯烃的结构烯烃与相应的烷烃在结构上的最大差别是分子中含有碳碳双键,因此要了解烯烃的结构就必须了解碳碳双键的形成。
乙烯是最简单的烯烃,其结构简式为H2C CH2。
当两个碳原子与四个氢原子形成乙烯分子时,在氢原子的影响下,两个碳原子均采取sp2杂化,所形成的的三个sp2杂化轨道在一个平面上,杂化轨道间的夹角为120°,有一个2p轨道未参与杂化,三个sp2杂化轨道和2p轨道中各有一个电子;而氢原子的1s轨道中有一个电子。
两个碳原子各用一个sp2杂化轨道沿键轴方向以“头碰头”方式重叠,形成一个C-Cσ键,每个碳原子又分别用两个sp2杂化轨道与两个氢原子的1s轨道以“头碰头”方式重叠,形成两C-Hσ键。
同时,两个碳原子的2p轨道又垂直于三个σ键所在的平面以“肩并肩”的方式重叠,形成一个C-Cπ键。
3、烯烃的异构和Z/E标记法1)烯烃的顺反异构相同基团处于双键的同侧叫顺式,反之为反式。
成顺反异构的充分条件:每个双键碳原子必须连接两个不同的原子或原子团。


烯烃的结构与性质乙烯是一种重要的化工原料,是合成橡胶,合成纤维,合成塑料的主要原料。
一直以来,乙烯的产量是衡量一个国家化学工业水平的标志。
在高中化学必修二中,我们重点学习了乙烯的性质,在选修《有机化学基础》中,我们将由乙烯扩展到烯烃。
烯烃的化学性质是一个重要的高中化学知识点。
1.基本理论1.1概述1.概念分子里含有碳碳双键的一类链烃,叫做烯烃。
2.通式:CnH2n(n≥2)说明:①烯烃的实验式相同,都为CH2,碳氢质量比为6:1,即含碳的质量分数都为85.7%,含氢的质量分数都为14.3%。
②烯烃与环烷烃的通式相同,但二者不是同系物。
当n≥3时,碳原子数相同的烯烃和环烷烃互为同分异构体。
3.物理性质一般随碳原子数的增加而呈现规律性的变化。
例如熔、沸点随碳原子数的增多而升高,液态时的密度随碳原子数的增多而增大。
2.性质应用2.1烯烃的官能团、通性和同分异构体1.官能团在烯烃分子里碳原子所结合的氢原子数少于饱和链烃里的氢原子数,烯烃分子中C=C双键里的一个键容易断裂,C=C双键里的这种碳原子还可以结合其他的原子或原子团,所以C=C双键是烯烃的官能团。
2.通性:烯烃的化学性质比较活泼,容易发生加成反应、氧化反应、加聚反应等。
①加成反应CH3-CH=CH2+Br2→CH3-CHBr-CH2Br(1,2-二溴丙烷)备注:烯烃和卤化氢,卤素单质,氢气和水等四类物质发生加成。
②氧化反应a.烯烃都能使酸性KMnO4溶液褪色b.燃烧通式为CnH2n+(3n/2)O2→nCO2+nH2O③加聚反应丙烯在一定条件下聚合的化学方程式为:nCH3CH=CH2→[CH(CH3)-CH2]n3.综合应用1.烯烃的臭氧氧化分解规律烯烃在经臭氧氧化后在Zn存在下水解,可发生如下反应:R1-CH=C(R3)-R2→R1-CHO+R2-CO-R3此反应称为臭氧分解。
其反应规律是:“C=C”双键断裂,碳原子上各形成一个“C=O”双键,若原“C=C”上有氢原子,则生成醛(或进一步氧化成羧酸),无氢原子则生成酮。
烷烃与烯烃的结构与性质烷烃和烯烃是有机化合物中的两类主要化合物。
它们的结构和性质有着显著的差异。
本文将对烷烃和烯烃的结构与性质进行详细的探讨。
1. 烷烃的结构与性质烷烃是由碳氢键连接而成的碳氢化合物。
其分子中只包含碳和氢原子。
烷烃分子中的碳原子通过共价键形成直线或环状结构。
烷烃的分子式一般表示为CnH2n+2,其中n为代表碳原子数的整数。
烷烃分子的结构呈现出碳原子的四面体构型。
碳原子与相邻的碳原子以及氢原子形成共价键,共享电子。
由于碳与氢原子的电负性相近,烷烃中的碳氢键呈非极性,不易被其他化合物攻击。
烷烃的物理性质取决于分子的大小和分子之间的作用力。
随着分子量的增大,烷烃的沸点和熔点也会增加。
烷烃物质多为无色气体或液体,随着分子量的增大,会逐渐转变为固体。
烷烃的化学性质相对较稳定。
由于烷烃分子中没有含有极性键,烷烃不易发生化学反应。
烷烃可以与氧气发生燃烧反应,生成二氧化碳和水。
烷烃也可以通过催化剂的作用参与加氢、氧化和卤代反应等。
2. 烯烃的结构与性质烯烃是由含有碳-碳双键的碳链组成的有机化合物。
其分子中存在至少一个碳-碳双键。
烯烃的通式通常表示为CnH2n,其中n为代表碳原子数的整数。
烯烃分子的碳链中有一个或多个碳-碳双键。
碳-碳双键的存在使得烯烃分子呈现出刚性和平面构型。
烯烃分子中的碳-碳双键可发生立体异构现象,即两个碳原子的取向可以是顺式或反式的。
烯烃的物理性质与烷烃相似,取决于分子的大小和分子之间的作用力。
由于烯烃分子具有双键的存在,使得其分子间作用力较烷烃分子间作用力要强,因此烯烃的沸点和熔点通常会高于相应分子量的烷烃。
烯烃的化学性质较为活泼。
由于烯烃分子中含有碳-碳双键,这些双键对外界的化学物质具有较高的反应活性。
烯烃可以与水发生加成反应,生成醇类产物。
烯烃还可参与加聚反应,生成高分子化合物。
3. 烷烃与烯烃的比较烷烃和烯烃的结构差异主要在于碳原子之间键的连接方式。
烷烃中的碳原子通过单键连接,而烯烃中的碳原子通过双键连接。
[烯烃的化学性质]烯烃的化学性质归纳3.1.4 烯烃的化学性质 Chemical Properties of Alkenes烯烃的化学性质和烷烃不同。
它的分子中存在碳碳双键,化学活泼性大,烯烃的大部分反应发生在碳碳双键上,所以碳碳双键是烯烃的官能团。
和双键碳原子直接相连的碳原子称为α-碳原子,α-碳原子上的α-氢也容易发生取代反应。
(1)加成反应。
烯烃的加成反应,实质上是碳碳双键的加成反应,也就是打断一个π键,两个一价原子或基团分别加到双键碳原子上,形成两个新的σ键,从而生成饱和化合物。
一般可表示为:Y Z象这种由一个不饱和化合物和另一个化合物或单质作用,生成一个加成产物的反应,称为加成反应。
烯烃能与一系列加成试剂发生加成反应,例如氢、卤素、卤化氢、次卤酸、硫酸、水等。
a. 加氢。
在催化剂铂、钯、镍等存在下,烯烃与氢气加成得到烷烃,这种反应称为催化氢化。
2 + H22HH它是一种还原反应。
从烯烃催化加氢生成烷烃的过程中可以看出,发生变化的不仅仅是π键,双键的两个碳原子的全部价键都发生了变化。
碳原子的杂化轨道由sp2转变为sp3,分子的构型也从烯烃的平面排布结构变成四面体结构。
所以,不要将复杂的化学变化简单地理解为一个价键的改变。
烯烃的催化氢化是一个放热反应。
一摩尔烯烃氢化时所放出的热量称为氢化热。
不同烯烃的氢化热是不同的。
根据氢化热的不同,可以分析不同烯烃的相对稳定性。
一般氢化热愈小,则烯烃愈稳定。
例如:CHCH3HHCH3+ H2+ H2CH3223-1CCH3223-1可见,(E)-2-丁烯比(Z)-2-丁烯稳定。
烯烃的加氢反应是定量进行的,一个双键吸收1摩尔氢,常常用它来测定烯烃的双键数。
b.加卤素。
烯烃容易与氯、溴加成,生成邻二卤代烷。
例如,将乙烯通入溴的四氯化碳溶液中,红棕色的溴很快褪色,生成无色的1,2-二溴乙烷。
CH2 = CH2 + Br222BrBr在实验室里常用此反应来检验烯烃。
烯烃的化学性质
烯烃是一类化合物,特征是含有一个或多个碳-碳双键。
根据不同的双键位置、数量
和取代基团的不同,烯烃具有不同的化学性质。
1. 加成反应
由于烯烃分子中含有碳-碳双键,易于发生加成反应。
常见的加成反应包括氢化、卤化、水化、羟基化等。
在这些反应中,双键断裂,原子或分子添加到原有的分子中,产生
新的化合物。
例如,在氢气存在下,烯烃可以被催化加氢,生成对应的烷烃。
在卤素存在
的条件下,烯烃可以发生卤素加成反应,生成卤代烃。
在水存在的条件下,烯烃可以被催
化水化,生成醇。
2. 氧化反应
烯烃分子中含有不饱和的双键,易于发生氧化反应。
常见的氧化反应包括氧化、双氧
水氧化、氧气氧化等。
在这些反应中,双键上的电子可以被氧化剂夺取,生成羰基化合物、羧酸等。
例如,烯烃可以被氧化剂强氧化,生成对应的酮、醛等。
3. 聚合反应
烯烃分子中的双键易于发生聚合反应。
聚合反应是一种将单体分子链接成高分子材料
的反应过程。
例如,乙烯可以通过聚合反应制得聚乙烯。
这种聚合反应需要催化剂的存
在。
4. 消除反应
消除反应是指烯烃分子中双键的两个碳原子之间的σ-键或官能团与双键的共有对称
轴的发生断裂,而生成一个新的双键,并同时放出一个小分子。
常见的消除反应包括脱氢
反应、脱醇反应、脱卤反应、脱水反应等。
5. 其他反应
烯烃还可以发生一些其他的反应,如复分解反应、还原反应、自由基加成反应等。
烯烃的化学性质烯烃的化学性质很活泼,可以和很多试剂作用,主要发生在碳碳双键上,能起加成、氧化聚合等反应。
此外,由于双键的影响,与双键直接相连的碳原子(α-碳原子)上的氢(α-H )也可发生一些反应。
一. 加成反应在反应中π键断开,双键上两个碳原子和其它原子团结合,形成两个σ-键的反应称为加成反应。
( 一) 催化加氢烯烃在催化剂作用下,低温低压既与氢加成生成烷烃。
( 二) 亲电加成在烯烃分子中,由于π电子具流动性,易被极化,因而烯烃具有供电子性能,易受到缺电子试剂(亲电试剂)的进攻而发生反应,这种由亲电试剂的作用而引起的加成反应称为亲电加成反应。
对电子具有亲和力的试剂叫做亲电试剂。
亲电试剂由于缺少电子,容易进攻反应物上带部分负电荷的位置,由这类亲电试剂进攻而发生发反应称为亲电反应。
亲电试剂通常为路易斯酸。
如: H +Br +、Cl +、H 3O +、RC +=O 、Cl 2、Br 2、I 2、HCl 、HBr 、HOCl 、H 2SO 4、F 3C ─COOH 、BF 3、AlCl 3等烯烃的亲电加成反应历程烯烃的亲电加成反应历程可由实验证明实验说明:1.与溴的加成不是一步,而是分两步进行的。
因若是一步的话,则两个溴原子应同时加到双键上去,那么Cl –就不可能加进去,产物应仅为1,2-二溴乙烷,而不可能有1-氯-2-溴乙烷。
但实际产物中竟然有1-氯-2-溴乙烷,没有1,2-二氯乙烷。
因而可以肯定Cl –是在第二步才加上去的,没有参加第一步反应。
2.反应为亲电加成历程RCH=CHR + H 2RCH 2CH 2RCH 2=CH 2Br 2(水溶液)CH 2-CH 2BrBrCH 2-CH 2CH 2-CH 2BrClClCl无Br Brδδ溴在接近碳碳双键时极化成 ,由于带微正电荷的溴原子较带微负电荷的溴原子更不稳定,所以,第一步反应是Br δ+首先进攻双键碳中带微负电荷的碳原子,形成溴鎓离子,第二步负离子从反面进攻溴鎓离子生成产物(反面进攻的证明见P 142~144)。
第一步第二步在第一步反应时体系中有Na +、Br δ+,但Na +具饱和电子结构,有惰性,故第一步只有Br δ+参与反应,因而无1,2-二氯乙烷生成。
烯烃与各种酸加成时,第一步是H + 加到双键碳上,生成碳正离子中间体,第二步再加上负性基团形成产物。
要明确两点:1)亲电加成反应历程有两种,都是分两步进行的,作为第一步都是形成带正电的中间体(一种是碳正离子,另一种是鎓离子)。
2)由于形成的中间体的结构不同,第二步加负性基团时,进攻的方向不一样,中间体为鎓离子时,负性基团只能从反面进攻,中间体为碳正离子时,正反两面都可以。
C CH HH HBr BrδδCC HH HBr Br BrCH CH BrCl( )( Cl )CH 2CH 2Br BrC CHC HC XC C HXCCENuδδ C CC C C C C C EEtNuE Nu Nu反面进攻反式加成产物顺式加成反式加成混合产物(第二步)(第一步)一般Br 2, I 2通过鎓离子历程,HX 等通过碳正离子历程。
1) 与HX 的加成CH 2=CH 2 + HX → CH 3CH 2-X (HX 等通过碳正离子历程) 1° HX 的反应活性HI > HBr > HCl > (HF 的加成无实用价值。
)2°不对称烯烃的加成产物遵守马氏规则(有一定的取向,即区位选择性)。
例如:上述两例说明不对称烯烃加HX 时有一定的取向,马尔可夫尼可夫总结了这个规律,我们把它称为马尔可夫尼可夫规则,简称马氏规则。
马氏规则 不对称烯烃与卤化氢等极性试剂进行加成时,试剂中带正电荷的部分E + 总是加到含氢较多的双键碳原子上,试剂中带负电荷的部分(Nu )总是加到含氢较少的双键碳原子上。
碳正离子的稳定性顺序为:3° 过氧化物效应当有过氧化物(如 H 2O 2, R-O-O-R 等)存在时,不对称烯烃与HBr 的加成产物不符合CH 3CH=CH 2 + HBr CH 3-CH-CH 3 + CH 3-CH 2-CH 2BrBrCH 3-C=CH 2 + HClCH 3-C-CH 3CH 3Cl80%20%100%(主)CH 3C CH 3HCH 3C CH 3CH 3CH 3C HHCH 3>>>叔仲伯(2°)(1°)(3°)马氏规则(反马氏取向)的现象称为过氧化物效应。
例如:(2)加卤素CH 2=CH 2 + Br 2CH 2BrCH 2Br将乙烯通入溴的四氯化碳溶液中,溴的颜色很快褪去,常用这个反应来检验烯烃。
(3)加硫酸(加水)烯烃能与浓硫酸反应,生成硫酸氢烷酯。
硫酸氢烷酯易溶于硫酸,用水稀释后水解生成醇。
工业上用这种方法合成醇,称为烯烃间接水合法。
CH 3CH=CH 2 + H 2SO 4 CH 3CH(OSO 3H)CH 3CH 3CH(OH)CH 3 + H 2SO 4 (4)加次卤酸烯烃与次卤酸加成,生成β– 卤代醇。
由于次卤酸不稳定,常用烯烃与卤素的水溶液反应。
如:CH 2=CH 2 + HOCl CH 2(OH)CH 2Cl5)与乙硼烷的加成(硼氢化反应)此反应是用末端烯烃来制取伯醇的好方法,其操作简单,副反应少,产率高。
在有机合成上具有重要的应用价值。
硼氢化反应是美国化学家布朗(Brown )与1957年发现的,由此布朗获得了1979年的诺贝尔化学奖。
二、氧化反应1.用KMnO 4或OsO 4氧化1) 用稀的碱性KmnO 4氧化,可将烯烃氧化成邻二醇。
CH 3-CH=CH 2 + HBrCH 3-CH 2-CH 2-Br过氧化物反马氏产物CCl 4Δ C=C+ 1 / 2 B 2H 6C C H BH 2RCH=CH 22KMnO 44H 2O3R-CH-CH 22MnO 2KOH3OH OH或中性反应中KMnO 4褪色,且有MnO 2沉淀生成。
故此反应可用来鉴定不饱合烃。
此反应生成的产物为顺式-1,2-二醇,可看成是特殊的顺式加成反应。
也可以用OsO 4代替KMnO 4进行反应,见P 61。
2)用酸性KMnO 4氧化在酸性条件下氧化,反应进行得更快,得到碳链断裂的氧化产物(低级酮或羧酸)。
反应的用途: 1鉴别烯烃, 2° 制备一定结构的有机酸和酮, 3° 推测原烯烃的结构。
2.臭氧化反应(用含有臭氧6~8%的氧气作氧化剂)将含有臭氧(6~8%)的氧气通入液态烯烃或烯烃的四氯化碳溶液,臭氧迅速 而定量地与烯烃作用,生成臭氧化物的反应,称为臭氧化反应。
为了防止生成的过氧化物继续氧化醛、酮,通常臭氧化物的水解是在加入还原剂(如Zn / H 2O )或催化氢化下进行。
例如:R-CH=CH 2KMnO H 2SO 4R-COOHCO 2 + H 2OC CHR''R R ′KMnO H 2SO 4C OR R ′R''-COOH羧酸酮羧酸C=CHR''R R'O 3C C R''H RR'2C OR R''O R''H 2O 2H2O臭氧化物粘糊状,易爆炸,不必分离,可直接在溶液中水解。
CH 3-C=CHCH 3CH 31) O 2) Zn/H 2OCOCH 3CH 3CH 3CHO丙酮乙醛烯烃臭氧化物的还原水解产物与烯烃结构的关系为: 烯烃结构 臭氧化还原水解产物 CH 2= HCHO (甲醛) RCH= RCHO (醛) R 2C= R 2C=O (酮)故可通过臭氧化物还原水解的产物来推测原烯烃的结构。
例如:臭氧化还原水解产物, CH 3COCH 3 OCHCH 2CHO HCHO,原烯烃的结构3.催化氧化某些烯烃在特定催化剂存在下能被氧化生成重要的化工原料:此类反应是特定反应,不能泛用。
例如,如要将其它烯烃氧化成环氧烷烃,则要用过氧酸来氧化。
四、聚合反应烯烃在少量引发剂或催化剂作用下,键断裂而互相加成,形成高分子化合物的 反应称为聚合反应。
例如,乙烯的聚合CH 3-C=CHCH 2CH=CH 23CH 3-C-CH 2CHCH 2CHOOCH 3CH 3CH 3CH 3CH=CH 2CH 3O CH 3-CH CH 2CH 3COOHn CH 2=CH 2少量引发剂150~250℃150~300Mpa[ CH 2-CH 2 ]n乙烯(单体)聚乙烯(高分子)高压法高压聚乙烯低压法低压聚乙烯TiCl 4 Al(C 2H 5)3聚乙烯是一个电绝缘性能好,耐酸碱,抗腐蚀,用途广的高分子材料(塑料)。
TiCl 4-Al(C 2H 5)3 称为齐格勒(Ziegler 德国人)、纳塔(Natta 意大利人)催化剂。
1959年齐格勒 纳塔利用此催化剂首次合成了立体定向高分子,人造天然橡胶。
为有机合成做出了具大的贡献。
为此,两人共享了1963年的诺贝尔化学奖。
五、α-H (烯丙氢)的卤代反应双键是烯烃的官能团,凡官能团的邻位统称为α位,α位(α碳)上连接的氢原子称为α- H (又称为烯丙氢)。
α- H 由于受C=C 的影响,αC-H 键离解能减弱。
.故α- H 比其它类型的氢易起反应。
其活性顺序为: α- H (烯丙氢)> 3°H > 2°H > 1°H > 乙烯H有α- H 的烯烃与氯或溴在高温下(500~600℃),发生α- H 原子被卤原子取代的反应而不是加成反应。
例如:10Mpa[ CH-CH 2 ]n TiCl 4 Al(C 2H 5)350℃nCH 3CH=CH 2CH 3聚丙烯CH 3-CH=CH 2 + Cl 2CH 2-CH=CH 2 + HCl ClCl 2+ HClCl卤代反应中α- H 的反应活性为:3°α- H > 2°α- H > 1°α- H 例如:高温下发生取代而不是加成的原因: 高温时反应为自由基取代历程。
Cl 22Cl •CH 3CH=CH 2 + Cl •HCl + •CH 2CH=CH 2•CH 2CH=CH 2 + Cl 2CL-CH 2CH=CH 2当烯烃在温度低于250℃时与氯反应,则主要是进行加成反应。
CH-CH=CH-CH 3CH 3Br 2(1mol)CH3C-CH=CH-CH 3CH 3CH 3CH-CH=CH-CH 2CH 3CH 3BrBr主要产物次要产物。