高一化学化学能与电能测试.doc
- 格式:pdf
- 大小:134.20 KB
- 文档页数:7

第二章化学反应与能量总结巩固与测试一、重点聚焦(1)化学反应中的能量变化,通常主要表现为热量变化——吸热或放热E1>E2新化学键的形成所释放的能量小于破坏旧化学键所吸收的能量,该反应就是吸热反应。
E1<E2新化学键的形成所释放的能量大于破坏旧化学键所吸收的能量,该反应就是放热反应。
(2)常见的放热反应和吸热反应:放热反应:①燃烧反应;②中和反应;③物质的缓慢氧化;④金属与水或酸反应;⑤部分化合反应。
吸热反应:①氢氧化钡晶体与氯化铵晶体:Ba(OH)2·8H2O+2NH4Cl==2NH3↑+BaCl2+10H2O;②大多数分解反应。
③CO2+C2CO ④C+H2O(g)CO+H2(3)中和热:酸和碱发生中和反应生成1mol水时所释放的热量称为中和热。
(2)原电池概念:借助于氧化还原反应将化学能转变为电能的装置。
(3)原电池的结构:(4)形成原电池的条件:①两种活泼性不同的金属(或金属与非金属单质)作电极②电极材料插入电解质溶液中③两极相连构成闭合回路④在电极上能自动发生氧化还原反应(5)原电池的表示方法总的来说,原电池中的化学反应是氧化还原反应。
①负极反应:由于负极是电子流出的电极,所以负极上发生的反应是氧化反应。
表示负极反应的式子叫做负极反应式。
铜、锌和稀H2SO4组成的原电池的负极反应式是:Zn-2e-==Zn2+(氧化反应)②正极反应:由于正极是电子流入的电极,所以正极上发生的反应是还原反应。
表示正极反应的式子叫做正极反应式。
铜、锌和稀H2SO4组成的原电池的正极反应式是:2H++2e-==H2↑(还原反应)(6)原电池的判断方法①据组成原电池的两极材料判断:一般活泼性较强的金属为负极,活泼性较弱的金属或能导电的非金属为正极。
②据电流方向或电子流动方向判断:电流是由正极流向负极,而电子流动方向是由负极流向正极。
③据原电池内部电解质溶液中离子的定向移动方向判断:在原电池的电解质溶液中,阳离子向正极移动,阴离子向负极移动。

2-第二节化学能与电能一、选择题1.(2011·河北南宫中学高一第二学期期中考试化学试题)下列各组中的能源均属于二次能源的是()A.电力、蒸汽B.电力、风力C.蒸汽、风力D.原煤、石油答案:A点拨:风力、原煤、石油均为一次能源,故只有A选项电力、蒸汽均属于二次能源。
2.(2011·山东苍山一中高一第二学期期中考试)下列有关原电池的说法中正确的是()A.原电池是把电能转化为化学能的装置B.原电池中电子流出的一极是负极,发生还原反应C.构成原电池两极必须是两种不同的金属D.原电池中的阳离子向正极移动答案:D点拨:原电池是把化学能转化为电能的装置,故A错。
原电池中电子流出的一极是负极,失去电子,发出氧化反应,故B错,构成原电池的两极一般是活动性较强的金属作负极,活动性较弱的金属或能导电的非金属为正极,故C错。
3.(2012·山东临沂高一下学期期中考试模拟试题)下图为铜锌原电池示意图,下列说法正确的是()A.锌片逐渐溶解B.烧杯中溶液逐渐呈蓝色C.电子由铜片通过导线流向锌片D.该装置能将电能转变为化学能答案:A点拨:在铜锌原电池中,锌是负极,铜是正极,电子从锌片流向铜片,负极的反应式为:Zn-2e-===Zn2+正极的反应式为2H++2e-===H2↑反应一段时间后,锌片逐渐溶解,溶液中H+浓度减小,该装置是化学能转化为电能,故正确答案为A。
4.(2011·山东沾化二中高一下学期学分认定测试)废电池处理不当不仅造成浪费,还会对环境造成严重污染,对人体健康也存在极大的危害。
有同学想变废为宝,他的以下想法你认为不正确的是() A.把锌皮取下洗净用于实验室制取氢气B.碳棒取下洗净用作电极C.把铜帽取下洗净回收利用D.电池内部填有氯化铵等化学物质,将废电池中的黑色糊状物直接作化肥用答案:D5.(2011·山东苍山一中高一第二学期期中考试)现在各类碱性电池已经占有了越来越多的市场份额,这类电池广泛地应用于各种小型用电器(如照相机、收音机等)中。

第六章 化学反应与能量 检测题一、单选题1.在体积为2L 的密闭容器中,充入22mol CO 和26mol H ,一定条件下发生反应:2232CO (g)3H (g)CH OH(g)H O(g)++,能说明上述反应达到平衡状态的是A .反应中2CO 与3CH OH 的物质的量浓度相等时B .V(CO 2)=V(H 2)C .单位时间内每消耗23molH ,同时生成21mol H OD .2CO 的体积分数在混合气体中保持不变2.一种新型燃料电池,一极通入空气,另一极通入丁烷(C 4H 10)气体,电解质是掺杂氧化钇(Y 2O 3)的氧化锆(ZrO 2)晶体,其在熔融状态下能传导O 2-。
已知电池的总反应是2C 4H 10+13O 2→8CO 2+10H 2O 。
下列说法不正确的是( )A .在熔融电解质中,O 2-向负极移动B .通入丁烷的一极是负极,电极反应为C 4H 10-26e -+13O 2-=4CO 2+5H 2OC .通入空气的一极是正极,电极反应为O 2+4e -=2O 2-D .通入丁烷的一极是正极,电极反应为C 4H 10+26e -+13O 2-=4CO 2+5H 2O3.乙苯在催化剂作用下在550~600℃时脱氢生成苯乙烯:+H 2下列说法不正确的是( )A .该反应既是一个消去反应,也可以认为是一个还原反应B .恒压下在进料中掺入大量高温水蒸气有利于提高苯乙烯的产量C .乙苯可由苯和乙烯反应得到,且该反应原子利用率能达到100%D .等质量的苯乙烯与苯燃烧时耗氧量相同4.CO 2(g)+3H 2(g)⇌CH 3OH(g)+H 2O(g)是CO 2综合利用的一种方法。
下列关于该反应的说法正确的是 A .升高温度能加快反应速率B .催化剂对反应速率无影响C .减小H 2浓度能加快反应速率D .达到化学平衡时,CO 2能100%转化为CH 3OH5.下列关于化学反应中能量变化的说法正确的是A .在常温下可以发生的反应一定是放热反应B.放热反应为“贮存”能量的过程,吸热反应为“释放”能量的过程C.断开化学键的过程是吸热过程D.化学反应中能量变化的大小与反应物的质量多少无关6.下列变化中有化学键的断裂的是A.HCl溶于水B.酒精的挥发C.干冰的升华D.裁剪布料7.下列化学反应属于吸热反应的是A.碘的升华B.氢氧化钙与氯化铵晶体混合C.镁与稀盐酸反应D.生石灰溶于水8.一定条件下存在反应:CO(g)+H2O(g)CO2(g)+H2(g),其正反应放热。

(人教版必修2)第二章化学反应与能量第二节化学能与电能(第1课时)【学习目标】1.通过实验探究、交流讨论,知道原电池概念及原电池工作原理、构成原电池的条件.2.通过对实验现象的讨论与分析,提高实验探究和总结归纳的能力,感受自主学习、合作学习的乐趣.在趣味原电池制作活动中,感受化学能转化为电能的奇妙和参与探究的喜悦。
3. 通过举例说明化学能与电能的转化关系及其应用,认识到化学能转化为电能的重要性,感悟化学学科的学习价值和社会价值。
【学习重点】原电池概念、原理、组成及应用.【温馨提示】建立宏观现象与反应本质间的联系可能是你学习的难点。
【自主学习】旧知回顾:1.氧化还原反应的特征:__反应前后有元素化合价变化_,氧化还原反应的本质:有电子转移_____,氧化剂在反应中得电子,还原剂在反应中失电子。
2.氧化还原反应中转移电子数=_____失电子总数___=___得电子总数_____新知预习:阅读教材P39—40,尝试回答下列问题:1.一次能源是指:直接从自然界取得的能源,流水、风、煤、石油、天然气、铀矿等,二次能源是指:一次能源经过加工,转换得到的能源电力等。
2.燃烧的本质是什么?火力发电中能量的转化方式是怎样的?火力发电又有哪些优点和缺点呢?情景导入:电能是现代社会中应用最广泛,使用最方便、污染最小的一种二次能源,又称电力。
例如,小到日常生活中使用的手提电脑、手机、相机、摄像机……大到火箭上天、神州六号宇宙飞船遨游太空,这一切都依赖于电池的应用.那么,同学们一定想知道电池的结构、它的工作原理。
电池是怎样把化学能转变为电能的呢?今天我们用化学知识来揭开电池这个谜。
下面我们先认识什么是一次能源?什么是二次能源?一、化学能转化为电能活动一:认识能源的分类交流:“新知预习1"。
对应练习1.下列能源中,一次能源有(1)(2)(5)(6)(9)(10)(13)(14),二次能源有(3)(4)(7)(8)(11)(12)(15)(16).一次能源中可再生资源有(1)(5)(9)(10)(13)(14),不可再生资源有(2)(6)。
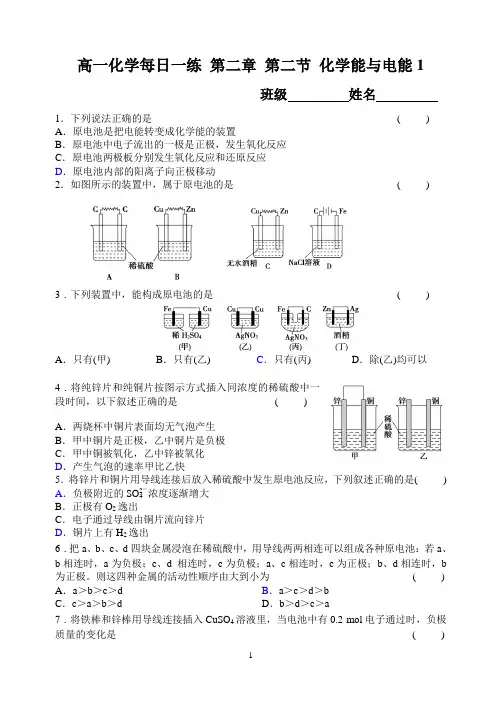
高一化学每日一练第二章第二节化学能与电能1班级姓名1.下列说法正确的是( ) A.原电池是把电能转变成化学能的装置B.原电池中电子流出的一极是正极,发生氧化反应C.原电池两极板分别发生氧化反应和还原反应D.原电池内部的阳离子向正极移动2.如图所示的装置中,属于原电池的是()3.下列装置中,能构成原电池的是()A.只有(甲) B.只有(乙) C.只有(丙) D.除(乙)均可以4.将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是()A.两烧杯中铜片表面均无气泡产生B.甲中铜片是正极,乙中铜片是负极C.甲中铜被氧化,乙中锌被氧化D.产生气泡的速率甲比乙快5.将锌片和铜片用导线连接后放入稀硫酸中发生原电池反应,下列叙述正确的是() A.负极附近的SO2-4浓度逐渐增大B.正极有O2逸出C.电子通过导线由铜片流向锌片D.铜片上有H2逸出6.把a、b、c、d四块金属浸泡在稀硫酸中,用导线两两相连可以组成各种原电池:若a、b相连时,a为负极;c、d 相连时,c为负极;a、c相连时,c为正极;b、d相连时,b 为正极。
则这四种金属的活动性顺序由大到小为() A.a>b>c>d B.a>c>d>bC.c>a>b>d D.b>d>c>a7.将铁棒和锌棒用导线连接插入CuSO4溶液里,当电池中有0.2 mol电子通过时,负极质量的变化是() A.增加5.6 g B.减少0.1 g C.减少6.5 g D.增加6.4 g8.有a 、b 、c 、d 四个金属电极,有关的实验装置及部分实验现象如下:由此可判断这四种金属活动性顺序是 ( )A .a >b >c >dB .b >c >d >aC .d >a >b >cD .a >b >d >c9.如图所示,杠杆AB 两端分别挂有体积相同、质量相同的空心铜球和空心铁球,调节杠杆使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO 4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中不考虑铁丝反应及两边浮力的变化)()A .杠杆为导体和绝缘体时, 均为A 端高B 端低B .杠杆为导体和绝缘体时, 均为A 端低B 端高C .当杠杆为绝缘体时,A 端低B 端高;为导体时,A 端高B 端低D .当杠杆为绝缘体时,A 端高B 端低;为导体时,A 端低B 端高10、先判断电极正负,再写出电极反应式和总反应的离子方程式总反应的离子方程式分别为A B C高一化学每日一练第二章第二节化学能与电能2班级姓名1.下列叙述不.正确的是() A.根据一次能源与二次能源的划分,氢气为二次能源B.电能是现代社会中应用最广泛、使用最方便、污染最小的一种二次能源C.火电是将燃料中的化学能直接转化为电能的过程D.在火力发电时,化学能转化为热能的过程实际上是氧化还原反应发生的过程,伴随着能量的变化2.随着人们生活质量的不断提高,废电池必须进行集中处理的问题被提到议事日程,其主要原因是() A.利用电池外壳的金属材料B.防止电池中汞、镉、铅等重金属离子对水和土壤的污染C.不使电池中渗泄的电解液腐蚀其他物品D.回收其中的石墨电极3.关于原电池的下列说法中错误的是() A.原电池中电流由负极流向正极B.原电池中,正极发生氧化反应C.充电电池在充电时,将电能转化为化学能贮存在电池中D.在燃料电池的负极上发生反应的通常是可燃性气体4.电池是人类生产和生活中重要的能量来源。

化学必修II《化学反应与能量》单元测验(A卷)班别姓名学号常用相对原子质量:Al:27 Fe:56 Cu:64 Zn:65一、选择题(每题4分,共36分,每题只有一个选项)1.近年来,广州市的大部分公交车及部分出租车已采用LPG(液化石油气)作为汽车的燃料,其主要目的在于A.防止石油短缺 B.降低成本 C.减少对大气的污染 D.加大发动机的动力2.对化学反应限度的叙述,错误的是A.任何可逆反应都有一定的限度B. 化学反应的限度是不可改变的C.化学反应的限度与时间的长短无关D. 化学反应达到限度时,正逆反应速率相等3.一定条件下,可逆反应2A B+3C,在四种状态中处于平衡状态的是正反应速率逆反应速率A υA=2mol/(l.min)υB=2mol/(l.min)B υA=2mol/(l.min)υC=2mol/(l.min)C υA=1mol/(l.min)υB=2mol/(l.min)D υA=1mol/(l.min)υC=1.5mol/(l.min)4.A、B、C都是金属,A和C分别放入同浓度的稀硫酸中,A的反应速率比C快,A与B 和硫酸铜溶液组成原电池时,A的质量增加。
A、B、C三种金属的活动性顺序为A.A>B>C B.A>C>B C.B>A>C D.C>A>B5.在一个密闭容器中,盛有N2和H2,它们的起始浓度分别是1.8 mol·L-1和5.4 mol·L-1,在一定的条件下它们反应生成NH3,10min后测得N2的浓度是0.8 mol·L-1,则在这10min 内NH3的平均反应速率是A.0.1mol.L-1.min-1B.0.2mol.L-1.min-1C.0.3mol.L-1.min-1D.0.6mol.L-1.min-1 6.下列说法正确的是A. 凡是放热反应的发生均无需加热B.凡是需要加热后才能发生的反应是吸热反应C.伴有能量变化的物质变化都是化学变化D. 物质发生化学反应都伴随着能量变化7.下列叙述正确的是:A.酸和碱发生中和反应放出的热叫中和热B.1 mol酸和1 mol碱反应放出的热叫中和热C.酸碱中和生成1 mol 水放出的热叫中和热D.任何反应生成1 mol水放出的热叫中和热8.某原电池的总反应的离子方程式是:Zn+Cu2+=Zn2++Cu,此反应的原电池的正确组成是正极负极电解质溶液A Cu Zn HClB Zn Cu CuS04C Cu Zn CuS04D Cu Zn ZnCl29.甲烷燃料电池的化学反应为CH4 + 2O2 = CO2 + 2H2O,其中1个电极反应式为2O2 + 8H4 + 8e- = 4H2O下列叙述不正确...的是A.CH4通入负极 B.O2通入正极 C.正极发生氧化反应D.负极的电极反应式为:CH4 + 2H2O – 8e- = CO2 + 8H+二.选择题(每题只有一至两个选项,每题4分,共20分)10.关于燃料充分燃烧的说法不正确的是A.空气量越大越好 B.固体燃料块越大越好C.液体燃料燃烧时可以雾状喷出 D.温度必须达到着火点11.金刚石和石墨都是碳的单质,石墨在一定条件下可以转化为金刚石并需要吸收能量。

2020-2021学年高一《新题速递·化学》3月刊专题二化学能与电能1.(2020·新疆生产建设兵团第四师第一中学高一期中)下面的能源中属于二次能源的是( )A.电能、蒸汽B.电能、风能C.蒸汽、风能D.煤、石油2.(2020·平罗中学高一月考)废旧电池最好的处理方法是A.深埋入地下B.丢弃C.回收利用D.烧掉3.(2020·宁波市北仑中学高一期中)“储存”在物质内部的化学能可通过原电池转化为电能,如图所示是某同学设计的几种装置,其中能构成原电池的是()A.③⑤⑦B.③④⑤C.④⑤⑦D.②⑤⑥4.(2020·衡东县欧阳遇实验中学高一期末)下列化学电池属于高效、环境友好电池的是A.镍镉电池B.锌锰电池C.氢氧燃料电池D.铅蓄电池5.(2020·江西宜春市·高安中学高一期中)原电池的电极名称不仅与电极的性质有关,也与电解质溶液有关,下列说法不正确的是A.由Zn、Cu、稀H2SO4组成原电池,其负极反应式为:Zn-2e-=Zn2+B.由Fe、Cu、FeCl3溶液组成原电池,其负极反应式为:Fe-2e-=Fe2+C.由Mg、Al、NaOH溶液组成原电池,其负极反应式为:Al-3e-=Al3+D.由Al、Cu、浓硝酸组成原电池,其负极反应式为:Cu-2e-=Cu2+6.(2020·四川省广安代市中学校高一期末)如图为发光二极管连接柠檬电池装置,下列说法不正确的是A.负极的电极反应为:Fe-2 e-=Fe2+B.电子由Fe 环经导线流向发光二极管C.铜线作为柠檬电池的正极D.可将柠檬替换成盛装酒精溶液的装置7.(2020·湖北省武汉市外国语学校美加分校高一期中)如图为锌、铜水果电池装置示意图,下列说法正确的是( )A.铜片为负极,发生还原反应B.锌片上发生还原反应:Zn-2e-=Zn2+C.电流由锌片沿导线流向铜极D.电子由锌片沿导线流向铜极8.(2020·海南海口市·琼山中学高一月考)某原电池工作时总的反应为Zn+Cu2+=Zn2++Cu,该原电池的组成可能是( )选项正极负极电解质溶液A Zn Cu CuCl2溶液B Cu Zn 稀H2SO4C Cu Zn CuSO4溶液D Fe Zn ZnSO4溶液9.(2020·新绛县第二中学高一月考)在用Zn片、Cu片和稀硫酸组成的原电池装置中,经过一段时间工作后,下列说法正确的是()A.锌片是正极,铜片上有气泡产生B.电流方向是从锌片流向铜片C.溶液中硫酸的物质的量浓度减小D.电解质溶液的pH保持不变10.(2020·泗洪县洪翔中学高一月考)在如右图所示的装置中,a的金属活泼性比氢要强,b为碳棒,下列关于此装置的叙述不正确的是()A.碳棒上有气体放出,溶液pH变大B.a是正极,b是负极C.导线中有电子流动,电子从a极到b极D.a极上发生了氧化反应11.(2020·海南海口市·琼山中学高一期中)某小组为研究电化学原理,设计如图装置。

学业分层测评(十一)化学能转化为电能化学电源(建议用时:45分钟)[学业达标]1.如图所示的装置,能够组成原电池产生电流的是()【答案】 D2.将纯锌片和纯铜片按图示方式插入同浓度同体积的稀硫酸中一段时间,下列叙述中正确的是()A.两烧杯中铜片表面均无气泡产生B.甲中铜片是正极,乙中铜片是负极C.两烧杯的溶液中H+浓度均减小D.乙装置中化学能转化为电能【解析】依据原电池的形成条件,甲是原电池,总反应为Zn+2H+===Zn2++H2↑;乙没用导线将两金属片相连,不能形成原电池,只能在Zn片上发生置换反应:Zn+2H+===Zn2++H2↑;分析可知,甲中铜片上有气泡产生,乙中锌片上有气泡产生。
【答案】 C3.(双选)下列有关原电池的叙述正确的是()A.构成原电池的正极和负极的材料必需是两种不同的金属B.原电池是将化学能转化为电能的装置C.在原电池中,电子流出的一极是负极D.原电池放电时,电路中的电流是从负极到正极【解析】构成原电池的电极可以是金属与金属,也可以是金属与非金属等,A项错误;原电池放电时,电流是从正极到负极,D项错误。
【答案】BC4.争辩人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源。
该电池以金属锂和钢板为电极材料,以LiOH为电解质,使用时加入水即可放电。
关于该电池的下列说法不正确的是()【导学号:39700036】A.水既是氧化剂又是溶剂B.放电时正极上有氢气生成C.放电时OH-向正极移动D.总反应为2Li+2H2O===2LiOH+H2↑【解析】金属锂比铁活泼,作原电池的负极,电极反应式为Li-e-===Li+,LiOH溶液中的阳离子有Li+和H+,由于氧化性H+>Li+,所以正极反应是2H++2e-===H2↑,由于H+来自于水的电离,所以H+放电的同时溶液产生了OH-,即该反应的总反应为2Li+2H2O===2LiOH+H2↑,水既是氧化剂又是溶剂。
在原电池的放电过程中,阳离子向正极移动,阴离子向负极移动,所以OH-向负极移动,C选项错误。

高一化学电化学试题答案及解析1.如图所示:甲为稀硫酸,乙为氯化铜溶液,电极材料用元素符号表示,则下列说法中正确的是A.甲装置将电能转变为化学能B.乙装置中左边的碳棒上有红色金属析出C.甲中Cu为阳极D.甲中Fe的质量少了0.56g,乙中右边的碳棒质量增加了0.64g【答案】D【解析】铁和稀硫酸反应生成氢气,则根据装置图可知,甲是原电池,乙是电解池,A不正确。
甲中铁是负极,铜是正极。
所以乙装置中左边的碳棒是阳极,溶液中的氯离子放电,生成氯气,B不正确;C不正确,D正确,0.56g铁是0.01mol,失去0.02mol,则根据电子的得失守恒可知,乙中右边的碳棒析出铜的物质的量是0.01mol,质量是0.64g,答案选D。
【考点】考查电化学原理的有关应用点评:该题是中等难度的试题,也是高考中的常见题型。
该题的关键是明确原电池和电解池的工作原理,然后结合题意和装置图灵活运用即可,有利于培养学生的逻辑推理能力和发散思维能力。
2.下列过程需要通电才能进行的是①电离②电解③电镀④电化学腐蚀A.①②B.②③C.②④D.全部【答案】B【解析】电离,是指在(物理性的)能量作用下,原子、分子形成离子的过程。
电解是指将电流通过电解质溶液或熔融态物质,而在阴极和阳极上引起氧化还原反应的过程。
电镀是利用电解的原理将导电体铺上一层金属的方法。
不纯的金属与电解质溶液接触时,会发生原电池反应,比较活泼的金属失去电子而被氧化,这种腐蚀叫做电化学腐蚀。
【考点】化学概念点评:化学概念是学习化学的基础,考生在备考过程中应注意区分各个概念,把握概念的关键词。
题型一般为选择题,难度较低。
3.下列叙述中,正确的是①电解池是将化学能转变成电能的装置②原电池是将电能转变成化学能的装置③金属和石墨导电均为物理变化,电解质溶液导电是化学变化④不能自发进行的氧化还原反应,通过电解的原理有可能实现⑤电镀过程相当于金属的“迁移”,可视为物理变化A.①②③④B.③④C.③④⑤D.④【答案】B【解析】电解池是将电能转变成化学能的装置,所以①错误;原电池是将化学能转变成电能的装置,故②错误;金属和石墨导电均为物理变化,电解质溶液导电是化学变化,故③正确;不能自发进行的氧化还原反应,通过电解的原理有可能实现,故④正确;电镀过程相当于金属的“迁移”,可视为化学变化,故⑤错误,所以③④的叙述是正确的,本题答案选B。


第六章《化学反应与能量》测试题一、单选题(共15题)1.在某一化学反应中,反应物A的浓度在10s内从0.8mol·L-1变为0.2mol·L-1,则在这10s内A的化学反应速率为A.0.02mol·L-1B.0.02mol·L-1·s-1C.0.06mol·L-1·s-1D.0.06mol·L-1·min-1 2.下列变化中属于吸热反应的是①冰融化成水①胆矾受热分解①三氧化硫溶于水①高锰酸钾分解制取氧气①生石灰与水反应生成熟石灰①石灰石高温分解①CO2+C 高温2CO①Ba(OH)2•8H2O与固体NH4Cl混合A.①①①①B.①①①①①C.①①①①①①D.①①①①①3.由下列实验中的操作及现象,不能够推出相关结论的是A.A B.B C.C D.D4.将镁片、铝片用导线连接并插入NaOH溶液中,关于该装置的叙述正确的是A.该装置将电能转化为化学能B.该装置使用的铝片不需要处理表面的氧化膜C.电子由镁片向铝片移动D.NaOH溶液更换为任何电解质溶液,铝片上都发生氧化反应5.一定条件下,可逆反应2A(g)B(g)+3C(g)处于平衡状态的是A .AB .BC .CD .D6.下列化学变化中,属于吸热反应的是 A .锌粒与稀硫酸的反应 B .()22Ba OH 8H O ⋅与4NH Cl 晶体的反应 C .甲烷在空气中燃烧D .Na 与2H O 反应7.已知某反应为放热反应,对于该反应,下列说法正确的是 A .生成物的总能量大于反应物的总能量B .已知石墨比金刚石稳定,可能是石墨转化为金刚石的反应C .可能是一个燃烧反应D .一定是在常温就能发生的反应8.化学与科技生产、生活环境等密切相关,下列说法错误的是 A .市售暖贴的发热原理是利用原电池加快氧化还原反应速率 B .电热水器用镁棒防止内胆腐蚀,利用了外加电源的阴极保护法 C .减少燃煤的使用改用风能、太阳能等能源,符合“低碳生活”理念 D .明矾能用于净水是因为铝离子水解生成的氢氧化铝胶体具有吸附性 9.下列说法中正确的是A .吸热反应的活化能大于放热反应的活化能B .用NaOH 溶液滴定盐酸,以甲基橙作指示剂,滴定终点时溶液pH=7C .向NaOH 溶液中滴加等体积等物质的量浓度的盐酸,溶液的导电性逐渐减小D .用23Na CO 溶液处理水垢中4CaSO 的离子方程式:2233Ca CO CaCO +-+=↓ 10.SO 2既是大气主要污染物之一,又在生产生活中具有广泛应用,如可生产SO 3并进而制得硫酸等,其反应原理为:2SO 2(g)+O 2(g)=2SO 3(g) ΔH=-196.6 kJ·mol -1。
单元素养评价(六)(第六章)(90分钟100分)(60分钟70分)一、选择题(本题包括12小题,每小题3分,共36分)1.下列设备工作时,将化学能主要转化为热能的是( )锂离子电池太阳能集热器硅太阳能电池燃气灶A B C D【解析】选D。
锂离子电池是把化学能转化为电能,故A不选;太阳能集热器是把太阳能转化为热能,故B不选;硅太阳能电池是太阳能转化为电能,故C不选;燃烧是放热反应,是化学能转化为热能,故D选。
2.某化学反应中生成物的总能量为60 kJ,如果该反应是放热反应,那么反应物的总能量可能是( )A.50 kJB.30 kJC.80 kJD.20 kJ【解析】选C。
因放热反应中,反应物的总能量高于生成物的总能量,生成物的总能量为60 kJ,所以反应物的总能量大于60 kJ。
3.(教材二次开发·教材习题改编)硫酸是一种重要的化工产品,硫酸的消耗量常被视为一个国家工业发展水平的一种标志。
目前的重要生产方法是“接触法”,有关接触氧化反应2SO 2+O22SO3的说法不正确的是( )A.该反应为可逆反应,故在一定条件下二氧化硫和氧气不可能全部转化为三氧化硫B.达到平衡后,反应就停止了,故此时正、逆反应速率相等且均为0C.一定条件下,向某密闭容器中加入2 mol SO2和1 mol O2,则从反应开始到达到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻,正、逆反应速率相等D.在利用上述反应生产三氧化硫时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题【解析】选B。
对于可逆反应来说,在一定条件下反应物不可能全部转化为产物,反应只能进行到一定限度。
在达到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,最终正、逆反应速率相等,即达到平衡,此时反应物和生成物的浓度都不再随时间的变化而变化,但反应并没有停止,正、逆反应都依然进行着。
4.2019年是京沪高铁迎来开通运营8周年。
【精品资源】临川一中新人教版化学必修1满分课堂化学能与热能5分钟训练(预习类训练,可用于课前) 1.下列反应中属于吸热反应的是( )A.镁与盐酸反应放出氢气B.氢氧化钠与盐酸的反应C.硫在空气或氧气中燃烧 ()2·8H 2O 与4反应 解析:本题主要考查学生对常见放热、吸热反应的了解状况。
金属与酸的置换反应、中和反应以与燃烧反应等均为放热反应,只有D 项为吸热反应。
答案:D2.下列说法不正确的是( )A.化学反应除了生成新物质外,还伴随着能量的改变B.放热反应不须要加热即可发生C.须要加热条件的化学反应都是吸热反应D.硫酸与足量氢氧化钠发生中和反应生成1 水所释放的热量称为中和热 解析:化学反应过程往往伴随着能量的改变,反应是放热还是吸热主要取决于反应物和生成物所具有的总能量的相对大小;有的放热反应起先也须要加热;反应起先时须要加热的反应可能是吸热反应,也可能是放热反应。
酸碱发生中和反应生成1 H 2O 时所释放的热量称为中和热。
答案:3.城市运用的燃料,现大多为煤气、液化石油气。
煤气的主要成分是、H 2的混合气体,它由煤炭与水蒸气在高温下反应制得,故又称水煤气。
试完成下列问题:(1)写出制取水煤气的主要化学方程式, 该反应是反应(填“吸热”或“放热”)。
(2)设液化石油气的主要成分为丙烷(C 3H 8 ),其充分燃烧后产物为2和 H 2O ,试比较完全燃烧等质量的C 3H 8与所需氧气的质量比为。
解析:(1)反应方程式为2高温2为吸热反应。
(2)C 3H 8+5O 232+4H 2O44m 5×44m×32 2 + O 22228m 21×28m×32 即完全燃烧等质量的C 3H 8与所需氧气的质量比为5×44m ×32∶21×28m×32=70∶11 答案:2高温2吸热 (2)70∶1110分钟训练(强化类训练,可用于课中)1.下列关于能量转化方式的叙述错误的是( )A.太阳能可转化为化学能B.化学能可转化为热能C.化学能可转化为电能D.化学能可干脆转化为机械能 解析:化学能是不能干脆转化成机械能的。
高一化学化学反应与能量变化试题答案及解析1.已知A、B、C、D均是气体,反应A+B C+D的能量变化如图所示,下列说法正确的是A.当A的正反应速率与C的逆反应速率相同时处于平衡状态B.当A、B、C、D的浓度相同时,反应处于平衡状态C.反应物的总键能量低于生成物的总键能D.该反应是放热反应【答案】A【解析】对于一个可逆反应,达到平衡状态,说明正反应速率与逆反应速率相等,各物质的浓度保持不变。
反应物的总能量低于生成物的总能量时,该反应是吸热反应,故答案选A【考点】考查化学平衡的相关知识点。
2.已知反应A+B=C+D的能量变化如图所示,下列说法正确的是()A.该反应为放热反应B.该反应为吸热反应C.反应物的总能量高于生成物的总能量D.该反应只有在加热条件下才能进行【答案】B【解析】A、根据题给图像知,反应物的总能量低于生成物的总能量,该反应为吸热反应,错误;B、根据题给图像知,反应物的总能量低于生成物的总能量,该反应为吸热反应,正确;C、根据题给图像知,反应物的总能量低于生成物的总能量,错误;D、某些吸热反应不需要加热也可以发生,如氢氧化钡晶体和铵盐发生的吸热反应,错误。
【考点】考查化学反应与能量变化。
3.已知化学反应2C(s)+O2(g) ="==" 2CO(g)、2CO(g)+O2(g) ===2CO2(g)都是放热反应。
据此判断,下列说法不正确的是(其他条件相同)()。
A.12 g C所具有的能量一定高于28 g CO所具有的能量B.56 g CO和32 g O2所具有的总能量大于88 g CO2所具有的总能量C.12 g C和32 g O2所具有的总能量大于44 g CO2所具有的总能量D.将一定质量的C燃烧,生成CO2比生成CO时放出的热量多【答案】A【解析】A.C燃烧产生CO2气体是放热反应,:C燃烧产生的产物CO气体放出热量,CO燃烧也是是放热反应,可见物质的燃烧程度不同,放出的热量就不同,不能说12 g C所具有的能量一定高于28 g CO所具有的能量,错误;B.由于2CO(g)+O2(g) ===2CO2(g)是放热反应,故56 gCO和32 g O2所具有的总能量大于88 g CO2所具有的总能量,正确;C. 2C(s)+O2(g) ="=="2CO(g) 是放热反应, 则12 g C和32 g O2所具有的总能量大于44 g CO2所具有的总能量,正确;D.由于化学反应2C(s)+O2(g) ="==" 2CO(g)、2CO(g)+O2(g) ===2CO2(g)都是放热反应,可见,物质的燃烧程度不同,反应放出的热量就不同,正确。
高一化学化学反应与能量变化试题1.已知:HCN(aq)与NaOH(aq)反应的∆H=-12.1kJ/mol;HCl(aq)与NaOH(aq)反应的∆H=-55.6kJ/mol。
则HCN在水溶液中电离的∆H等于( )A.-67.7 kJ/mol B.-43.5 kJ/mol C.+43.5 kJ/mol D.+67.7kJ/mol【答案】C【解析】HCN在水溶液中电离的∆H等于-12.1kJ/mol +55.6kJ/mol="+43.5" kJ/mol,故选项是C。
【考点】考查中和热与弱电解质电离能的关系的知识。
2.下列关于化学反应与能量的说法正确的是A.中和反应是吸热反应B.燃烧是放热反应C.化学键断裂放出能量D.反应物总能量与生成物总能量一定相等【答案】B【解析】中和反应是放热反应,A项错误;燃烧是放热反应,B项正确;化学键断裂吸收能量,C 项错误;反应物总能量与生成物总能量一定不等,D项错误。
【考点】考查化学反应与能量。
3.下列说法正确的是A.物质发生化学变化都伴随着能量变化B.任何反应中的能量变化都表现为热量变化C.物质变化时若伴有能量变化,则一定是化学变化D.没有物质的化学变化,也就没有能量的变化【答案】A【解析】A.物质发生化学变化就是旧化学键断裂和新化学键形成的过程,断键吸热,成键放热,所以化学反应的过程都伴随着能量变化,正确;B.任何反应中的能量变化通常表现为热量变化,也可能是光能、电能等形式,错误;C.物质变化时若伴有能量变化,则可能是化学变化,也可能是物理变化,错误;D.没有物质的化学变化,也可以有能量的变化,错误。
【考点】考查能量变化与化学变化的关系的知识。
4.已知:稀溶液中,强酸与强碱反应中和热的数值为57.3kJ/mol。
(1)用0.1molBa(OH)2配成的稀溶液跟足量的稀硝酸反应,放出______kJ的热量(2)1L0.1mol/LNaOH溶液分别与①醋酸溶液②浓硫酸③稀硝酸恰好反应时,放出的热量分别为Q1、Q2、Q3(单位:kJ),则它们由大到小的顺序是_________________________【答案】(1)11.46 (2)Q2> Q3> Q1[来【解析】由题意可知,H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ/mol;所以0.1molBa(OH)2配成的稀溶液跟足量的稀硝酸反应可生成0.2molH2O,放热11.46kJ;醋酸溶于水需吸收热量,浓硫酸溶于水放出热量,故三种酸与NaOH反应时放热由大到小为Q2> Q3> Q1[。
化学能与热能1 .天然气燃烧过程中的能量转化方式为2 .下列关于化学反应的说法中不正确的是()A.化学反应过程中一定有热量释放出来B.化学反应的特征是有新物质生成C.化学反应的过程实际上是一个旧键断裂、新键形成的过程D.在一确定的化学反应关系中,反应物的总能量与生成物的总能量一定不相等B.①③6.已知反应A 2+B 2===2AB,破坏1 mol A 2中的化学键吸收的能量为 Q i kJ,破 坏1 mol B 2中的化学键吸收的能量为 Q 2 kJ,形成1 mol AB 中的化学键放出的能量为Q 3 kJ,则下列说法中正确的是 ( )A.若A 2和B 2的总能量大于生成的AB 的总能量,则反应吸热A.化学能转化为热能B. 化学能转化为电能C.热能转化为化学能D. 化学能转化为机械能3. 卜列变化过程中,需要吸收能量的是()A. H+H —> H 2B, H + Cl —>HCl C. Cl 2-> Cl + ClD. H2+O2->H2O 4. 卜列说法中正确的是(A.任何化学反应都伴随着能量的变化B. H 2O (g )—>H 2O (l )该过程放出大量的热,所以该过程是化学变化C.化学反应中能量的变化都表现为热量的变化D.对于如图所示的过程,是吸收能量的过程5.某学生用如图所示的装置进行化学反应 X + 2Y-2Z 能量交化情况的研究。
当往试管中滴加试剂Y 时,看到试管中甲处液面下降,乙处液面上升。
关于该反应的下列叙述正确的是()①该反应为放热反应②反应物的总能量比生成物的总能量高An p L % ■ ③该反应过程可以看成是“贮存”于 X 、Y 内部的能量转化为热量而释放出来B.若A2和B2的总能量小于生成的AB的总能量,则反应放热C.若该反应为放热反应,则 Q l + Q2<Q3D.若该反应为吸热反应,则Q I +Q2>2Q37.已知2SO2+O2===2SC3为放热反应,对该反应的下列说法正确的是 ( )A.O2的能量一定高于SO2的能量B.SO2和O2的总能量一定高于SO3的总能量C.SO2的能量一定高于SO3的能量D.因该反应为放热反应,故不必加热就可发生8.白磷、红磷是磷的两种同素异形体。