经典中考化学题型
- 格式:doc
- 大小:356.12 KB
- 文档页数:9

化学初三经典试题及答案一、选择题(每题2分,共10分)1. 下列物质中,属于混合物的是()。
A. 氧气B. 空气C. 二氧化碳D. 水答案:B2. 根据质量守恒定律,下列反应中正确的是()。
A. 2H2O → 2H2 + O2B. 2H2 + O2 → 2H2OC. 2H2O → H2 + O2D. 2H2 + O2 → H2O答案:B3. 下列物质中,属于单质的是()。
A. 氧气B. 二氧化碳C. 氧化铜D. 氢气答案:A4. 根据酸碱中和反应的化学方程式,下列反应中正确的是()。
A. HCl + NaOH → NaCl + H2OB. H2SO4 + NaOH → Na2SO4 + H2OC. HCl + KOH → KCl + H2OD. H2SO4 + KOH → K2SO4 + H2O答案:C5. 下列物质中,属于氧化物的是()。
A. 氧气B. 二氧化碳C. 氧化铜D. 氢气答案:B二、填空题(每题2分,共10分)6. 写出下列物质的化学式:(1)氢氧化钠:________(2)碳酸钙:________(3)硫酸铜:________(4)硝酸银:________答案:(1)NaOH(2)CaCO3(3)CuSO4(4)AgNO37. 写出下列反应的化学方程式:(1)铁与稀盐酸反应:________(2)碳酸钠与盐酸反应:________(3)氢气燃烧:________(4)氧化铜与氢气反应:________答案:(1)Fe + 2HCl → FeCl2 + H2↑(2)Na2CO3 + 2HCl → 2NaCl + H2O + CO2↑(3)2H2 + O2 → 2H2O(4)CuO + H2 → Cu + H2O8. 根据题目所给的化学方程式,写出下列反应的离子方程式:(1)CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4(2)Ca(OH)2 + H2SO4 → CaSO4 + 2H2O答案:(1)Cu2+ + 2OH- → Cu(OH)2↓(2)Ca2+ + 2OH- + 2H+ + SO42- → CaSO4 + 2H2O9. 根据题目所给的化学方程式,写出下列反应的平衡方程式:(1)N2 + 3H2 → 2NH3(2)2H2O → 2H2 + O2答案:(1)N2 + 3H2 ⇌ 2NH3(2)2H2O ⇌ 2H2 + O210. 根据题目所给的化学方程式,写出下列反应的电子转移方程式:(1)Zn + CuSO4 → ZnSO4 + Cu(2)2Ag + CuCl2 → 2AgCl + Cu答案:(1)Zn → Zn2+ + 2e-,Cu2+ + 2e- → Cu (2)2Ag → 2Ag+ + 2e-,Cu2+ + 2e- → Cu三、计算题(每题10分,共20分)11. 计算下列化学反应中转移的电子数:(1)2H2 + O2 → 2H2O(2)2Al + 3Fe2O3 → 2Fe + Al2O3答案:(1)4e-(2)12e-12. 计算下列化学反应中生成物的质量:(1)2H2O → 2H2 + O2(2)CaCO3 → CaO + CO2答案:(1)32g(2)44g四、实验题(每题10分,共20分)13. 根据题目所给的实验装置图,写出下列实验中可能观察到的现象:(1)将氢氧化钠溶液滴入稀盐酸中:(2)将硫酸铜溶液滴入氢氧化钠溶液中:答案:(1)溶液由无色变为无色透明,无明显变化。

初三化学必考试题及答案一、选择题(每题3分,共30分)1. 下列物质中,属于混合物的是()A. 蒸馏水B. 矿泉水C. 氧气D. 纯碱答案:B2. 铁在氧气中燃烧生成的化合物是()A. 氧化铜B. 氧化铁C. 氧化铝D. 氧化镁答案:B3. 根据质量守恒定律,化学反应前后()A. 元素种类不变B. 元素质量不变C. 物质种类不变D. 物质质量不变答案:A4. 以下物质中,属于非金属单质的是()A. 铁C. 铜D. 氧气答案:B5. 用排水法收集氧气时,正确的操作是()A. 先将导管插入水中B. 先点燃酒精灯C. 先熄灭酒精灯D. 先移开导管答案:A6. 下列物质中,属于氧化物的是()A. 碳酸钙B. 硫酸铜C. 氢氧化钠D. 水答案:D7. 实验室制取氧气时,通常使用的药品是()A. 碳酸钙B. 碳酸钠C. 碳酸氢钠D. 碳酸钾答案:A8. 实验室中,用于点燃酒精灯的器具是()B. 打火机C. 蜡烛D. 点火器答案:A9. 根据酸碱中和反应的原理,下列物质中,能中和酸的是()A. 石灰石B. 纯碱C. 碳酸氢钠D. 氢氧化钠答案:D10. 根据金属活动性顺序,排在氢前面的金属能与酸反应生成氢气,下列金属中,不能与酸反应的是()A. 铁B. 锌C. 铜D. 镁答案:C二、填空题(每题4分,共20分)1. 根据金属活动性顺序,排在氢前面的金属能与酸反应生成氢气,排在氢后面的金属则不能与酸反应。
答案:正确2. 物质的量浓度是指单位体积溶液中所含溶质的物质的量,其单位是mol/L。
答案:正确3. 氧化还原反应是指在化学反应中,有元素的化合价发生变化的反应。
答案:正确4. 实验室中,用稀盐酸和锌反应制取氢气时,反应的化学方程式为:Zn + 2HCl → ZnCl₂ + H₂↑。
答案:正确5. 根据酸碱中和反应的原理,酸和碱反应生成盐和水。
答案:正确三、简答题(每题5分,共10分)1. 请简述实验室制取氧气的步骤。
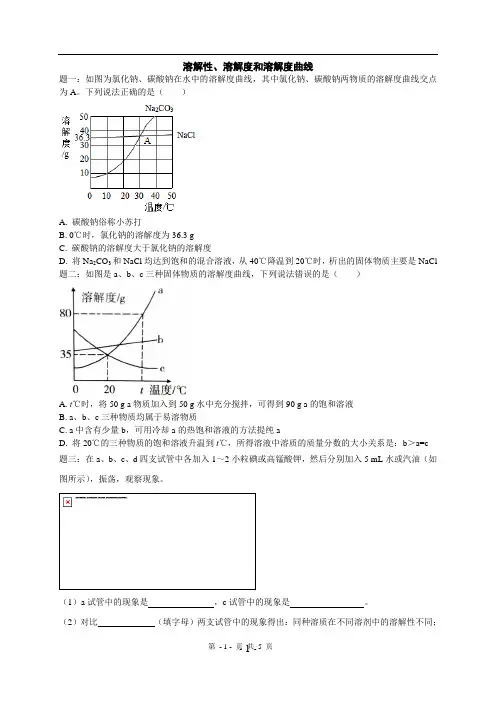
溶解性、溶解度和溶解度曲线题一:如图为氯化钠、碳酸钠在水中的溶解度曲线,其中氯化钠、碳酸钠两物质的溶解度曲线交点为A。
下列说法正确的是()A. 碳酸钠俗称小苏打B. 0℃时,氯化钠的溶解度为36.3 gC. 碳酸钠的溶解度大于氯化钠的溶解度D. 将Na2CO3和NaCl均达到饱和的混合溶液,从40℃降温到20℃时,析出的固体物质主要是NaCl 题二:如图是a、b、c三种固体物质的溶解度曲线,下列说法错误的是()A. t℃时,将50 g a物质加入到50 g水中充分搅拌,可得到90 g a的饱和溶液B. a、b、c三种物质均属于易溶物质C. a中含有少量b,可用冷却a的热饱和溶液的方法提纯aD. 将20℃的三种物质的饱和溶液升温到t℃,所得溶液中溶质的质量分数的大小关系是:b>a=c题三:在a、b、c、d四支试管中各加入1~2小粒碘或高锰酸钾,然后分别加入5 mL水或汽油(如图所示),振荡,观察现象。
(1)a试管中的现象是,c试管中的现象是。
(2)对比(填字母)两支试管中的现象得出:同种溶质在不同溶剂中的溶解性不同;对比a、c试管中的现象得出的结论是;(3)【提出问题】物质的溶解性除与溶质、溶剂的性质有关外,还与什么有关?【作出猜想】。
【设计方案】。
【观察现象】。
【得出结论】。
题四:小明陪妈妈到医院输液,不小心将护士手中的盘子打翻,其中的棉球落在了小明的白色衬衣上,白色衬衣上立即出现了一大片紫黑色痕迹。
为找到去掉白衬衣上的痕迹的最好方法,几位同学进行了讨论,提出了以下几个方案并进行实验:①用水洗;②用无水酒精洗;③用汽油洗;④用四氯化碳洗;⑤用肥皂水洗;⑥用淀粉溶液洗。
(1)你认为留在白色衬衣上的紫黑色物质是什么?(2)如果用白色布条进行实验,为使实验结果更加准确,你认为该实验中需要控制哪些实验条件?(3)一位同学按如图所示方法进行实验:结果是⑤、⑥几乎完全褪色;②略带颜色;③、④略微变浅;①几乎不变。

中考化学试题解读及答案一、选择题(本题共10小题,每小题2分,共20分。
每小题只有一个选项是正确的,请将正确选项的字母填入题后的括号内。
)1. 下列物质中,属于混合物的是()A. 氧气B. 蒸馏水C. 空气D. 酒精答案:C2. 根据质量守恒定律,化学反应前后不变的是()A. 元素种类B. 分子种类C. 原子种类D. 物质种类答案:A3. 下列物质中,属于化合物的是()A. 氧气B. 氮气C. 二氧化碳D. 氢气答案:C4. 根据酸碱中和反应的原理,下列物质中可以中和盐酸的是()A. 碳酸钠B. 氢氧化钠C. 氯化钠D. 硫酸答案:B5. 下列物质中,属于单质的是()A. 氧气B. 二氧化碳C. 氢气D. 氯化钠答案:A6. 根据金属活动性顺序,下列金属中活动性最强的是()A. 铁B. 铜C. 银D. 锌答案:D7. 下列物质中,属于氧化物的是()A. 氧气B. 二氧化碳C. 氢气D. 氯化钠答案:B8. 下列物质中,属于酸的是()A. 硫酸B. 氢氧化钠C. 氯化钠D. 碳酸钠答案:A9. 根据元素周期表,下列元素中属于非金属元素的是()A. 钠B. 氧C. 铁D. 钙答案:B10. 下列物质中,属于碱的是()A. 硫酸B. 氢氧化钠C. 氯化钠D. 碳酸钠答案:B二、填空题(本题共5小题,每小题4分,共20分。
)11. 化学方程式2H2 + O2 → 2H2O表示的意义是:氢气和氧气在点燃的条件下反应生成水。
12. 原子的相对原子质量是指该原子的质量与碳-12原子质量的1/12之比。
13. 根据金属活动性顺序,排在前面的金属可以置换出排在后面的金属。
14. 根据化学方程式计算时,需要遵循质量守恒定律。
15. 酸和碱发生中和反应时,生成盐和水。
三、简答题(本题共3小题,每小题10分,共30分。
)16. 请简述什么是氧化还原反应?答:氧化还原反应是指在化学反应中,原子或离子之间发生电子转移的过程。

化学计算题中考经典题型带答案1一、中考化学计算题1.有一赤铁矿样品(主要成分为Fe2O3),某学校化学兴趣小组为了测得样品中氧化铁的质量分数,进行了如下探究:小明取10 g赤铁矿样品(杂质不溶于水和酸),不断加入稀盐酸到固体的质量不再减少,加入稀盐酸的量如图所示。
求:(1)赤铁矿中氧化铁的质量分数是________________。
(2)计算所使用的稀盐酸的溶质质量分数____________。
【答案】 80% 10%【解析】氧化铁和稀盐酸反应生成易溶于水的氯化铁和水,所以反应中固体质量减少,最终不溶的固体是杂质,所以氧化铁的质量为:10g-2g=8g,设所使用的稀盐酸的溶质质量为x,Fe2O3+6HCl=2FeCl3+3H2O160 2198g x160/8g=219/xx=10.95g所以所使用的稀盐酸的溶质质量分数为:10.95g÷109.5g×100%=10%;答:略点睛:方程式的计算,关键根据化学反应方程式找出相关物质的质量关系,利用反应中物质的质量比不变进行列比例计算,易错点是,由方程式求质量比算数错误,所以这一步要仔细检查。
2.将含有NaCl杂质的某烧碱样品10 g完全溶于90 g水中,再向所得溶液中慢慢滴入溶质质量分数为7.3%的稀盐酸。
在实验过程中,溶液的pH与滴入稀盐酸的质量关系如图所示。
(1)求10 g该样品中氢氧化钠的质量。
(2)求a点时,溶液中溶质的质量分数(计算结果精确到0.1%)。
【答案】(1)8 g (2)6.9%【解析】当恰好完全反应时消耗的盐酸溶液的质量为100g,对应的HCl的质量为100g×7.3%=7.3g设氢氧化钠的质量为x,生成的氯化钠的质量为yNaOH+HCl═NaCl+H2O40 36.5 58.5x 7.3g y==x=8gy=11.7ga点时,溶液中溶质的质量分数为×100%≈6.9%答:(1)l0g该样品中氢氧化钠的质量为8g.(2)a点时,溶液中溶质的质量分数约为6.9%3.某课外活动小组为测定当地石灰石中含碳酸钙的质量分数,取来了一些矿石,准确称取25g放于盛有200g稀盐酸的烧杯中(杂质不溶于水,也不与稀盐酸反应,也不分解),恰好完全反应。

中招化学试题及答案一、选择题(每题2分,共20分)1. 下列物质中,属于混合物的是:A. 矿泉水B. 蒸馏水C. 氧气D. 氢气答案:A2. 根据质量守恒定律,化学反应前后不变的是:A. 元素种类B. 分子数目C. 分子种类D. 原子质量答案:A3. 金属活动性顺序中,排在氢前面的金属可以:A. 与酸反应生成氢气B. 与碱反应生成氢气C. 与盐反应生成氢气D. 与水反应生成氢气答案:A4. 下列物质中,属于非金属单质的是:A. 铜B. 硫磺C. 铁D. 汞答案:B5. 用化学方程式表示的化学反应中,反应物和生成物的量之比是:A. 任意的B. 一定的C. 可变的D. 不确定的答案:B6. 以下哪个选项是正确的化学方程式?A. 2H2 + O2 → 2H2OB. 2H2 + O2 → H2OC. H2 + O2 → 2H2OD. 2H2 + O2 → 2H2O2答案:A7. 根据元素周期表,元素的原子序数越大,其原子半径:A. 越大B. 越小C. 不变D. 先增大后减小答案:B8. 下列物质中,属于化合物的是:A. 氧气B. 氢气C. 水D. 铁答案:C9. 金属与非金属元素形成的化合物,其化学性质:A. 与金属相似B. 与非金属相似C. 介于两者之间D. 无法确定答案:C10. 下列物质中,属于酸的是:A. 硫酸B. 氢氧化钠C. 氯化钠D. 碳酸钙答案:A二、填空题(每题2分,共20分)1. 根据金属活动性顺序表,排在氢后面的金属不能与____反应。
答案:酸2. 元素周期表中,元素的排列顺序是按照____。
答案:原子序数3. 化学反应中,原子的____是不变的。
答案:种类4. 根据质量守恒定律,化学反应前后____不变。
答案:元素种类5. 金属与盐溶液反应时,金属的活泼性必须____。
答案:大于盐中金属6. 金属活动性顺序表中,排在氢前面的金属能与酸反应生成氢气,而排在氢后面的金属不能与酸反应生成氢气,这说明金属的活泼性与____有关。

初三化学必考试题及答案1. 题目:下列物质中,属于混合物的是()A. 空气B. 氧气C. 水D. 二氧化碳答案:A解析:混合物是由两种或两种以上物质组成的物质。
空气中含有氮气、氧气等多种气体,属于混合物。
2. 题目:下列物质中,属于化合物的是()A. 铁B. 氧气C. 水D. 氦气答案:C解析:化合物是由不同种元素组成的纯净物。
水是由氢元素和氧元素组成的化合物。
3. 题目:下列物质中,属于单质的是()A. 氧气B. 二氧化碳C. 氢气D. 氧化铁答案:A解析:单质是由同种元素组成的纯净物。
氧气是由氧元素组成的单质。
4. 题目:下列物质中,属于氧化物的是()A. 二氧化碳B. 氧气C. 氢气D. 氧化铁答案:D解析:氧化物是由两种元素组成,其中一种是氧元素的化合物。
氧化铁是由铁元素和氧元素组成的氧化物。
5. 题目:下列物质中,属于酸的是()A. 硫酸B. 氢氧化钠C. 氯化钠D. 碳酸钙答案:A解析:酸是电离时生成的阳离子全部是氢离子的化合物。
硫酸电离时生成的阳离子全部是氢离子,属于酸。
6. 题目:下列物质中,属于碱的是()A. 硫酸B. 氢氧化钠C. 氯化钠D. 碳酸钙答案:B解析:碱是电离时生成的阴离子全部是氢氧根离子的化合物。
氢氧化钠电离时生成的阴离子全部是氢氧根离子,属于碱。
7. 题目:下列物质中,属于盐的是()A. 硫酸B. 氢氧化钠C. 氯化钠D. 碳酸钙答案:C解析:盐是由金属离子和酸根离子组成的化合物。
氯化钠是由钠离子和氯离子组成的盐。
8. 题目:下列物质中,属于有机物的是()A. 甲烷B. 二氧化碳C. 水D. 氧化铁答案:A解析:有机物是含有碳元素的化合物。
甲烷是由碳元素和氢元素组成的有机物。
9. 题目:下列物质中,属于无机物的是()A. 甲烷B. 二氧化碳C. 水D. 氧化铁答案:B解析:无机物是不含碳元素的化合物。
二氧化碳是由碳元素和氧元素组成的无机物。
10. 题目:下列物质中,属于氧化物的是()A. 甲烷B. 二氧化碳C. 水D. 氧化铁答案:B解析:氧化物是由两种元素组成,其中一种是氧元素的化合物。

(化学)初中化学化学综合题解题技巧及经典题型及练习题(含答案)含解析一、中考化学综合题1.Ⅰ.请结合下图回答问题。
(1)写出图中有标号仪器的名称:①__________________。
(2)用高锰酸钾制取一瓶干燥的氧气,可选用装置组合为___________(选填序号);实验室制取二氧化碳和氧气可选用发生装置C或B,C装置的优点是__________________,用此装置制取O2的化学方程式是____________________;(3)实验室常用甲酸(HCOOH)溶液滴加到浓硫酸中制CO气体,可选用的制取装置是______(选填序号)。
该反应中浓硫酸既是催化剂又是脱水剂,试写出该反应的化学方程式________________。
Ⅱ.某同学将氢氧化钠溶液滴入到一定量的稀氯化铜溶液中,出现蓝绿色不溶于水的固体。
该同学对生成蓝绿色而不是蓝色固体的现象产生疑惑。
(查阅资料)(1).CuCl2溶液与NaOH溶液反应可生成蓝色固体(Cu(OH)2),在氢氧化钠较少的情况下会生成蓝绿色碱式氯化铜(Cu x(OH)y Cl z),其不溶于水,能与酸反应。
(2).Cu(OH) 2在60℃开始分解生成两种氧化物,100℃分解完全。
碱式氯化铜在300℃开始分解生成氧化铜、水和氯化氢,在400℃分解完全。
(猜想)蓝绿色固体可能是:①Cu(OH)2;②Cu x(OH)y Cl z晶体;③_______。
猜想①的理由是:________(用化学方程式表示)。
(验证)该同学取31.25g蓝绿色固体,加热至100℃出现黑色固体。
则猜想________不正确。
继续加热到400℃至质量不再改变,并使产生的气体全部缓缓通过如图_____(选填“甲”或“乙”)装置(装置中药品足量)。
(实验数据)①最终得到剩余固体24.00g;②与硝酸银溶液反应得到的沉淀经过滤、洗涤和低温烘干,得到固体14.35g;③浓硫酸装置中数据如表。
加热前100℃400℃250.00g251.80g253.60g(得出结论)猜想③成立,且碱式氯化铜中X∶Y:Z = _________。

中考化学常考题型
中考化学常考题型通常包括选择题、填空题和简答题。
以下列举了一些常见的中考化学题型及其特点:
1. 选择题:主要考察基础知识的掌握和应用能力。
通常给出一组选项,学生需要根据题干信息选出正确答案。
这类题目多为独立的题目,每题的内容和难度相对较为简单。
2. 填空题:主要考察对概念和计算方法的理解和运用能力。
题目一般给出一些条件和问题,学生需要填写答案,可以是一个单词、一个数字或一个简短的句子。
3. 简答题:主要考察对知识的理解和应用能力。
问题通常比较开放,要求学生进行分析、解释或比较。
学生需要给出清晰、连贯的回答,并能运用相关知识进行推理、解释或判断。
此外,中考化学还可能包括实验题,学生需根据实验现象、实验步骤或数据进行分析和解答问题,考察实验操作和实验数据分析能力。
需要注意的是,中考化学试题内容通常基于初中阶段的化学课本知识,但会强调基础知识的理解和运用,以及对相关知识的综合运用。
因此,学生在备考中应重点复习基础知识,并学会对知识进行灵活运用和综合应用。

初三化学经典题型汇总题目1:下列物质中,属于氧化物的是()。
A. 氯化钠B. 氧化铁C. 氢氧化钠D. 二氧化硅题目2:在下列化学反应中,放出热量的是()。
A. 氢气与氧气反应生成水B. 氢气与氧气反应生成液态水C. 氢气与氧气反应生成固体水D. 氢气与氧气反应生成水蒸气题目3:下列物质中,属于纯净物的是()。
A. 空气B. 氧气和氮气的混合气体C. 氧化铁D. 稀硫酸和蒸馏水的混合物题目4:下列物质中,属于纯净物的是()。
A. 氧气和氮气的混合气体B. 稀硫酸和蒸馏水的混合物C. 氧化铁D. 空气题目5:下列物质中,属于纯净物的是()。
A. 氧化铁B. 稀硫酸和蒸馏水的混合物C. 空气D. 氧气和氮气的混合气体题目6:下列物质中,属于纯净物的是()。
A. 稀硫酸和蒸馏水的混合物B. 空气C. 氧化铁D. 氧气和氮气的混合气体题目7:下列物质中,属于纯净物的是()。
A. 稀硫酸和蒸馏水的混合物B. 空气C. 氧化铁D. 氧气和氮气的混合气体题目8:下列物质中,属于纯净物的是()。
A. 稀硫酸和蒸馏水的混合物B. 空气C. 氧化铁D. 氧气和氮气的混合气体题目9:下列物质中,属于纯净物的是()。
A. 稀硫酸和蒸馏水的混合物B. 空气C. 氧化铁D. 氧气和氮气的混合气体题目10:下列物质中,属于纯净物的是()。
A. 稀硫酸和蒸馏水的混合物B. 空气C. 氧化铁D. 氧气和氮气的混合气体题目11:下列物质中,属于纯净物的是()。
A. 稀硫酸和蒸馏水的混合物B. 空气C. 氧化铁D. 氧气和氮气的混合气体题目12:下列物质中,属于纯净物的是()。
A. 稀硫酸和蒸馏水的混合物B. 空气C. 氧化铁D. 氧气和氮气的混合气体题目13:下列物质中,属于纯净物的是()。
A. 稀硫酸和蒸馏水的混合物B. 空气C. 氧化铁D. 氧气和氮气的混合气体题目14:下列物质中,属于纯净物的是()。
A. 稀硫酸和蒸馏水的混合物B. 空气C. 氧化铁D. 氧气和氮气的混合气体题目15:下列物质中,属于纯净物的是()。

(一)溶解度曲线及其应用类型一一条曲线获取的信息1,太空“冰雪”实验中,过饱和醋酸钠溶液形成的“液球”在接触绳子的一端后瞬间变成温热的“冰球”。
醋酸钠的溶解度曲线如图所示,下列说法不正确的是()A.常温下,醋酸钠易溶于水B.40 ℃时,饱和醋酸钠溶液的溶质质量分数是65.6%C.加水能使醋酸钠溶液从饱和变成不饱和D.过饱和醋酸钠溶液结晶过程释放热量初三化学第1部分(一)溶解度曲线及其应用(二)金属活动性顺序的探究及应用(三)物质的检验、鉴别、除杂、分离(四)物质的转化与推断类型二 两条曲线获取的信息2.KNO 3和NaCl 的溶解度曲线如图所示。
下列说法正确的是( )A.KNO 3的溶解度比NaCl 大B.将室温下KNO 3的饱和溶液升高温度,溶液仍饱和C.KNO 3和NaCl 均属于难溶物质D.除去KNO 3中少量NaCl 可用冷却热饱和溶液结晶的方法 类型三 三条曲线获取的信息3.(2023安徽中考)煤化工废水中含有NaCl 、Na 2SO 4、NaNO 3,这三种盐的溶解度曲线如图所示。
下列有关说法正确的是( )A.与NaNO 3相比,NaCl 更适合通过饱和溶液降温结晶得到B.a 1 ℃时,NaNO 3的饱和溶液溶质的质量分数为80%C.a 2 ℃时,NaCl 和Na 2SO 4的饱和溶液溶质质量分数相等D.40 ℃时,Na 2SO 4的饱和溶液升温到60 ℃变为不饱和溶液 类型四 图、表、线综合分析4.【学科素养·科学思维】(2023江苏扬州江都二模)MgSO 4和Na 2CO 3的溶解度表及溶解度曲线如下,下列说法正确的是 ( ) 温度/℃ 20304050607080溶解度 S /gMgSO 4 25.1 28.2 30.8 32.9 34.3 35.0 34.9 Na 2CO 321.5 39.7 49.0 48.5 46.0 45.2 43.9A.甲为MgSO4B.b、c点乙的饱和溶液溶质质量分数相等C.甲的饱和溶液从t1℃升温到t3℃,溶质质量分数增大D.等质量甲、乙饱和溶液从t3℃降温到t1℃,析出晶体的质量(不带结晶水):乙>甲5.(2023山西长治期末)在学习了“溶解度”的相关知识后,小晋用盛有150 g水的烧杯进行如图1所示的实验,图2是相关的溶解度曲线。
初三化学20题以下是针对初三化学的20道题目:1.请简述原子结构的基本组成,并解释原子与离子的区别。
2.什么是化合价?如何根据化合价确定化合物的化学式?3.写出氢气(H₂)和氧气(O₂)反应的化学方程式,并解释其反应类型。
4.如何通过实验验证水的组成?请描述实验步骤和现象。
5.什么是质量守恒定律?它在化学反应中有何应用?6.请解释酸碱指示剂的作用原理,并举例说明其在实验中的应用。
7.如何通过实验验证酸的性质?请描述实验步骤和现象。
8.写出氢氧化钠(NaOH)与二氧化碳(CO₂)反应的化学方程式,并解释其产物和反应类型。
9.什么是盐?请举例说明盐在水溶液中的电离过程。
10.如何通过实验验证金属的活动性顺序?请描述实验步骤和现象。
11.请解释什么是置换反应,并写出铁与硫酸铜溶液反应的化学方程式。
12.什么是溶液?溶液具有哪些基本特征?请举例说明。
13.如何通过实验确定某物质的溶解度?请描述实验步骤。
14.饱和溶液与不饱和溶液之间如何转化?请给出具体方法。
15.什么是乳化作用?它在日常生活中有哪些应用?16.请解释什么是化学变化中的能量变化,并举例说明。
17.如何通过实验验证燃烧的条件?请描述实验步骤和现象。
18.写出碳不完全燃烧的化学方程式,并解释其产物和危害。
19.请简述环境保护与化学的关系,并举例说明化学在环境保护中的应用。
20.回顾初三化学的学习内容,你认为哪些知识点对你理解化学世界和解决实际问题最有帮助?为什么?这些题目涵盖了初三化学的主要知识点,包括原子与离子、化合价与化学式、质量守恒定律、酸碱盐的性质与反应、金属活动性顺序、溶液与溶解度、化学变化中的能量变化、燃烧与环保等。
通过回答这些问题,学生可以巩固和拓展对化学知识的理解,提高对化学现象和原理的认识,同时培养解决实际问题的能力。
在实际教学中,教师可以根据课程内容和学生的实际情况进行适当的调整和补充。
中考化学试题及答案一、选择题(每题2分,共40分)1. 物质的量浓度相同的下列溶液中,pH最小的是()A. NaOH溶液B. HCl溶液C. CH3COOH溶液D. H2SO4溶液2. 下列物质中,属于混合物的是()A. 纯碱B. 空气C. 蒸馏水D. 食盐3. 以下哪种金属活动性最强?()A. 铜B. 铁C. 锌D. 银4. 以下哪种物质不属于氧化物?()A. CO2B. H2OC. NaClD. SO35. 以下哪种物质的溶液显酸性?()A. NaOHB. HClC. NaClD. Ca(OH)26. 以下哪种物质的溶液显碱性?()A. H2SO4B. NaOHC. HClD. CH3COOH7. 以下哪种物质的溶液显中性?()A. Na2CO3B. H2SO4C. HClD. H2O8. 以下哪种物质的溶液中,含有自由移动的离子?()A. 蒸馏水B. 酒精C. 氯化钠溶液D. 汽油9. 以下哪种物质的溶液中,含有自由移动的电子?()A. 蒸馏水B. 酒精C. 氯化钠溶液D. 金属铜10. 以下哪种物质的溶液中,含有自由移动的分子?()A. 蒸馏水B. 酒精C. 氯化钠溶液D. 金属铜11. 以下哪种物质的溶液中,含有自由移动的原子?()A. 蒸馏水B. 酒精C. 氯化钠溶液D. 金属铜12. 以下哪种物质的溶液中,含有自由移动的质子?()A. 蒸馏水B. 酒精C. 氯化钠溶液D. HCl溶液13. 以下哪种物质的溶液中,含有自由移动的电子?()A. 蒸馏水B. 酒精C. 氯化钠溶液D. 金属铜14. 以下哪种物质的溶液中,含有自由移动的分子?()A. 蒸馏水B. 酒精C. 氯化钠溶液D. 金属铜15. 以下哪种物质的溶液中,含有自由移动的原子?()A. 蒸馏水B. 酒精C. 氯化钠溶液D. 金属铜16. 以下哪种物质的溶液中,含有自由移动的质子?()A. 蒸馏水B. 酒精C. 氯化钠溶液D. HCl溶液17. 以下哪种物质的溶液中,含有自由移动的电子?()A. 蒸馏水B. 酒精C. 氯化钠溶液D. 金属铜18. 以下哪种物质的溶液中,含有自由移动的分子?()A. 蒸馏水B. 酒精C. 氯化钠溶液D. 金属铜19. 以下哪种物质的溶液中,含有自由移动的原子?()A. 蒸馏水B. 酒精C. 氯化钠溶液D. 金属铜20. 以下哪种物质的溶液中,含有自由移动的质子?()A. 蒸馏水B. 酒精C. 氯化钠溶液D. HCl溶液二、填空题(每空1分,共20分)21. 写出下列物质的化学式:A. 氢氧化钠:________B. 硫酸铜:________C. 碳酸钙:________D. 氯化钠:________22. 写出下列物质的离子符号:A. 钠离子:________B. 氯离子:________C. 硫酸根离子:________D. 氢氧根离子:________23. 写出下列物质的化学方程式:A. 铁与稀盐酸反应:________B. 氢气燃烧:________C. 碳酸钙与盐酸反应:________D. 氧化铜与氢气反应。
中考化学常考题型主要包括基础知识题、实验题、工业流程题、离子共存问题、溶液的计算题、有机化学题、化学反应原理题、金属活动性题、溶解度题以及生活中的化学题等。
以下是一些案例:
1. 基础知识题:
案例:某物质在氧气中燃烧生成二氧化碳和水,该物质是什么?
答案:该物质为有机物。
2. 实验题:
案例:某学生要制取氢气,应选择哪种方法?
答案:用锌和稀硫酸反应制取氢气。
3. 工业流程题:
案例:制盐工业通过海水晾晒可得粗盐,如何制备精盐?
答案:溶解、过滤、蒸发、结晶等步骤。
4. 离子共存问题:
案例:某无色透明的溶液中,下列各组离子能大量共存的是()。
答案:正确选项应满足无色透明、能大量共存两个条件。
5. 溶液的计算题:
案例:已知氯化钠溶液的浓度为10%,求200g氯化钠溶液中氯化钠的质量。
答案:20g。
6. 有机化学题:
案例:下列关于乙醇的描述正确的是()。
答案:乙醇可与水形成氢键。
7. 化学反应原理题:
案例:判断下列反应类型:碳与氧气反应生成二氧化碳。
答案:氧化还原反应。
8. 金属活动性题:
案例:将锌片放入硫酸铜溶液中,会发生什么现象?
答案:锌片上出现红色物质,溶液颜色变浅。
9. 溶解度题:
案例:某物质的溶解度随温度升高而降低,该物质是什么类型的化合物?
答案:难溶性盐。
10. 生活中的化学题:
案例:为什么在烹调过程中,食物的香气会四溢?
答案:食物中的分子在受热时会挥发,形成香气。
以上是中考化学常考题型和案例。
【化学】中考化学初中化学化学综合题解题技巧及经典题型及练习题(含答案)一、中考化学综合题1.某化学小组为测定一瓶失去标签的盐酸的溶质质量分数,分成甲、乙两组,分别用不同的方法进行测定。
实验设计:甲组:取纯净碳酸钙粉末5g于烧杯中,加入20g该盐酸溶液,充分反应后,过滤、洗涤、干燥,称量得剩余固体3g。
乙组:取纯净碳酸钙粉末5g于锥形瓶中,将20g该盐酸溶液加入分液漏斗,测定产生二氧化碳的体积0.4L(20℃、标准大气压,二氧化碳的密度为1.977g/L)计算盐酸浓度。
(数据处理):(1)你认为哪一种实验方法不准确,请说明原因_______________________________。
(2)请利用你认为实验合理的一组数据计算该盐酸的溶质质量分数为__________。
(写出计算过程)【答案】乙组数据不准确,原因:测量的水的体积小于生成气体的体积; B、C之间的导管内实验前无水,实验后有水;内外气压相同时,二氧化碳无法将相应体积的水压入量筒;二氧化碳可能溶解在A中反应后的溶液中 7.3%【解析】(1)乙组数据不准确,原因:测量的水的体积小于生成气体的体积;B、C之间的导管内实验前无水,实验后有水;内外气压相同时,二氧化碳无法将相应体积的水压入量筒;少量二氧化碳可能溶解在A中反应后的溶液中。
(2)根据甲数据计算,设参加反应的HCl质量为x,消耗碳酸钙质量为5g−3g=2g。
32222HCl+CaCO==CaCl+H O+CO↑73 100x 2g731002x g=x=1.46g盐酸的溶质质量分数为:1.46100%7.3% 20gg⨯=。
2.阅读下面材料,回答问题。
人类赖以生存的环境由自然环境和社会环境组成。
自然环境由生物圈、岩石圈、大气圈、水圈组成(如图所示),四个圈层经过漫长演化,既相对稳定、动态平衡,又相互作用、不断变化,各圈层之间的物质和能量不停循环,这些循环既跟物质的组成、结构和性质有关,也受人类活动的影响,并通过复杂的物理变化和化学变化实现。
中考化学试题真题及答案一、选择题(每题2分,共20分)1. 下列物质中,属于混合物的是()A. 蒸馏水B. 氧气C. 空气D. 二氧化碳答案:C2. 金属活动性顺序中,排在氢前面的金属可以与酸反应生成氢气,下列金属中活动性最强的是()A. 铁B. 铜C. 锌D. 镁答案:D3. 下列物质中,属于氧化物的是()A. 氯化钠B. 氢氧化钠C. 二氧化碳D. 硫酸答案:C4. 实验室制取氧气的方法是()A. 加热高锰酸钾B. 电解水C. 过氧化氢分解D. 以上都是答案:D5. 实验室中,用于吸收二氧化碳的试剂是()A. 氢氧化钠B. 硫酸C. 盐酸D. 碳酸钠答案:A6. 根据质量守恒定律,化学反应前后物质的总质量()A. 增加B. 减少C. 不变D. 无法确定答案:C7. 下列物质中,属于碱的是()A. 氢氧化钠B. 硫酸C. 碳酸钠D. 氯化钠答案:A8. 金属与酸反应生成氢气,下列金属中不能与酸反应的是()A. 铁B. 铜C. 锌D. 镁答案:B9. 实验室中,用于检验二氧化碳的试剂是()A. 氢氧化钠B. 硫酸C. 石灰水D. 碳酸钠答案:C10. 根据金属活动性顺序,排在氢后面的金属不能与酸反应生成氢气,下列金属中不能与酸反应的是()A. 铁B. 铜C. 锌D. 镁答案:B二、填空题(每题2分,共20分)1. 氧化铁的化学式为_______。
答案:Fe2O32. 实验室制取氧气的常用方法是_______。
答案:加热高锰酸钾3. 金属活动性顺序中,排在氢后面的金属不能与酸反应生成氢气,例如_______。
答案:铜4. 实验室中,用于吸收二氧化碳的试剂是_______。
答案:氢氧化钠5. 根据质量守恒定律,化学反应前后物质的总质量_______。
答案:不变6. 金属与酸反应生成氢气,下列金属中不能与酸反应的是_______。
答案:铜7. 实验室中,用于检验二氧化碳的试剂是_______。
答案:石灰水8. 金属活动性顺序中,排在氢前面的金属可以与酸反应生成氢气,例如_______。
【初中化学】中考化学经典题型:酸碱性与PH值
36.通常人体胃液的ph大约为0.9~1.5,胃液的酸碱性为()
a.酸性
b.碱性
c.中性
d.无法判断
37.融合下表中所列物质的ph推论,在以下各组物质中,分别能够并使紫色石蕊溶液
变白、不变色、变蓝的就是()
物质食盐水厕所清洁剂血浆牙膏肥皂水橘汁草木灰水柠檬汁
ph71.77.48.29.23.510.62.5
a.柠檬汁、食盐水、厕所清洁剂
b.牙膏、蒸馏水、肥皂水
c.草木灰、蒸馏水、柠檬汁
d.橘汁、食盐水、草木灰水
38.所列就是生活中一些物质的ph,有关它们的观点中错误的就是()
物质种类厕所清洁剂桔子汁牛奶草木灰水厨房清洁剂ph136.51112.5
a.牛奶的酸性比桔子汁弱
b.厕所清洁剂显出酸性
c……草木灰水显碱性d.胃酸过多的人不宜多吃桔子
39.高产稻种“就是现代农业生产常用科学方法,挑武当山特区某村土壤干料的溶液,重新加入五色酚酞溶液后显出红色。
下表列出四种农作物适合生长的ph范围,你指出该
村土壤比较适合栽种的农作物就是()
农作物水稻茶树玉米马铃薯ph6.0~7.06.0~7.07.0~8.14.8~5.5
a.玉米
b.茶树
c.水稻
d.马铃薯。
一、一步反应能否实现1、完成下列变化,能通过盐酸经一步反应实现的是 ( )①CaO-CaCl2 ②Fe2O3-FeCl3 ③Cu-CuCl2 ④Fe-FeCl2A.①②④ B. ②③ C. ①④ D. ④2、下列变化,只有加入酸才能一步实现的是( )A、Zn→ZnS04B、CaC03→C02C、MgO→MgCl2D、BaCl2→BaSO43、下列变化,不能由一步反应实现的是( )A、CaO-CaCl2B、CaC03→Ca(OH)2C、Cu→CuOD、BaCl2→BaSO44、下列物质的转化,不能一步反应实现的是()A、Fe2O3→FeB、CO2→H2CO3C、Zn→ZnCl2D、C→Na2CO35、下列物质的转化,不能一步反应实现的是()A、BaCl2→BaSO4B、CuO →Cu(OH)2C、NaOH→Na2CO3D、MgSO4→Mg(OH)26、下列物质的转化,不能一步反应实现的是()A、MgSO4→Mg(NO3)2B、C02→Na2C03C、Fe2O3→Fe (OH) 3D、BaCl2→BaSO4二、酸碱中和过量问题1、将质量为100克溶质质量分数为10%氢氧化钠溶液和质量为100克溶质质量分数为10%盐酸混合,所得溶液的PH植()A、PH>7B、PH<7C、PH=7D、无法判断2、将100克10%的氢氧化钠溶液和100克10%的稀硫酸充分混合,向混合后的溶液中滴加紫色石蕊试剂,最后溶液的颜色变为()A、红色B、蓝色C、紫色D、无色3、将质量为100克溶质质量分数为10%氢氧化钠溶液和质量为100克溶质质量分数为10%稀硫酸混合,混合后的溶液与下列物质不能发生反应的是()A、硝酸钡溶液B、氯化铜溶液C、铁D、氢氧化钡溶液4、将质量为100克溶质质量分数为10%氢氧化钠溶液和质量为100克溶质质量分数为10%盐酸混合,混合后的溶液与下列物质能发生反应的是()A、BaCl2B、CuSO4C、FeD、Ag5、将100克10%的氢氧化钠溶液和100克10%的稀硫酸充分混合,向混合后的溶液中加入下列物质的溶液① CuSO4② BaCl2 ③ FeCl3 ④ Na2C03能反应的是()A、①②③B、①②④C、①③④D、②③④三、平均值问题1、两种金属混合物30克与足量的稀硫酸充分反应,生成1克氢气,则该金属混合物可能是()A、Mg和AlB、Fe和ZnC、Mg和FeD、Zn和Cu2、某硝酸铵样品中混有一种其它氮肥,经分析样品中氮元素的质量分数为20%.那么该样品中可能含有氮肥是( )A、(NH4)2SO4B、NH4ClC、CO(NH2)2D、NH4HCO33、有一包不纯的CaCO3样品,其中只含一种杂质,现取该样品5克与足量稀盐酸反应生成2.3克CO2 ,则所混杂质可能是( )A、K2CO3B、Na2CO3C、MgCO3D、BaCO34、20克不纯的BaCl2样品与足量稀硫酸反应,生成23.3克白色沉淀,则BaCl2样品所混杂质可能是( )A、Ba(OH)2和KClB、Ba(NO3)2和NaClC、Ba(NO3)2和KClD、KCl 和NaCl5、不纯的CaCl2样品11.1克溶于适量水中,然后加入足量AgNO3溶液反应,生成29.7克白色沉淀,则CaCl2样品中可能所混杂质是( )A、NaClB、MgCl2C、ZnCl2D、BaCl26、某氯化钙样品中可能混有氯化铁、氯化镁、氯化钠和碳酸钠中的某些物质,取该样品11.1g溶于适量水中,得到澄清的无色溶液,然后向其中加入足量的硝酸银溶液,得到29.7g白色沉淀,则该样品组成的下列推断中,正确的是A.既无氯化铁,也无碳酸钠 B.只有氯化镁,没有氯化钠C .肯定有氯化镁,可能有氯化钠D .肯定有氯化镁,也有氯化钠四、溶质质量分数的问题1、将一定质量的CaO 加到饱和澄清石灰水溶液中,下列叙述正确的是 ( )A 、溶液中溶质的质量不变B 、溶液中溶质质量分数变大C 、溶液中溶质质量分数开始减少,然后逐渐增大到原来饱和澄清石灰水的质量分数D 、溶液中溶质质量分数开始增大,然后逐渐减小到原来饱和澄清石灰水的质量分数2、质量和溶质的质量分数一样的稀硫酸分别与足量的下列物质反应,所得溶液中溶质的质量分数最大的是( ),最小的是( ),相同的是( )A 、MgB 、MgOC 、Mg (OH )2D 、MgCO 33、溶质质量分数为10%的氢氧化钠溶液100克,如果使其溶质质量分数增加一倍可采用( )A 、将溶剂蒸发掉50克B 、将溶液中的水蒸发掉一半C 、加入10克氢氧化钠D 、加入100克10%的氢氧化钠4、向一定量的饱和NaOH 溶液中加入少量Na 20固体,恢复到原来的温度时,下列说法正确的是( )A 、溶液中的Na + 总数不变B 、溶液中溶质质量分数不变C 、溶液中溶剂质量不变D 、溶液质量不变5、将某稀硫酸分成两等份,分别向其中加入足量的ZnO 、ZnCO 3固体,充分反应,所得ZnSO 4溶液的溶质的质量分数(Y )与所加固体质量(X )关系正确的是( )1、在天平两托盘上的烧杯中,各放人质量相等的盐酸,天平平衡后分别向两边烧杯中各加入等质量的锌和镁,待金属完全消失后,天平的指针将 ( )A.偏向镁的一边B.仍停留在原位置不动C.偏向锌的一边D.左右不停地摆动2、在天平的两盘分别放入质量相等的烧杯,烧杯中各盛100克9.8%的硫酸溶液,两个烧杯中同时放入哪组金属,反应终止时天平仍保持平衡 ( )A 、锌、铁各7克B 、锌、铁各5克C 、锌、铁各4克D 、锌、铁各3克3、天平两端的烧杯中分别放入足量的、等溶质质量分数的稀硫酸,调节天平平衡后,向右端的烧杯中加入2.2克氧化钙,若仍使天平最终平衡,应向左端的烧杯中加入金属镁的质量是( )A 2gB 2.2gC 2.4gD 3.2g4、天平两边的托盘上分别放置盛有足量稀盐酸的烧杯,把天平调至平衡。
现向其中一只烧杯中投入5.3克碳酸钠,向另一只烧杯中投入适量铁片,要使天平最终仍保持平衡,投入铁片的质量应是( )A .5.6克B .5. 3克C .3.2克D .3.1克5、在托盘天平两边各放上一个盛有36.5g 溶质质量分数为20%的盐酸的烧杯,调节天平至平衡。
现将各一定量的两种物质分别放入两烧杯中,都恰好完全反应,此时天平仍保持平衡。
则加入的物质可能是( )A 、MgO 和MgCO 3B 、Mg 和MgCO 3C 、MgO 和Mg(OH)2D 、MgO 和Mg6、天平两端的烧杯中分别放入足量的、等溶质质量分数的稀硫酸,调节天平平衡后,向右端的烧杯中加入5.6克铁,若仍使天平最终平衡,应向左端的烧杯中加入CaCO 3的质量是( )A 5.4gB 5.6gC 9.64gD 10g六、气压问题1、 下图所示的锥形瓶内充满气体X ,胶头滴管内盛有液体Y 。
挤压胶头 滴管,使液体Y 进入瓶中,振荡.一会儿可见套在玻璃管下端的小气球a 鼓起。
气体X 和液体Y 可能是( )。
A .X 是CO 2,Y 是KOH 溶液B .X 是O 2,Y 是稀硫酸C.X是HCl,Y是AgNO3溶液D.X是CO,Y是石灰水2、如右图所示,烧瓶内盛有x气体,若挤压滴管的胶头a,使液体y进入烧瓶中,振荡烧瓶,并倒放在铁架台上,将导管伸入滴有z的水中,打开弹簧夹b,可见烧杯中液体如喷泉一样喷入烧瓶中,并出现颜色的改变,则x、y、z可能是()x气体y溶液z试剂A.O2H2SO4紫色石蕊试液B.CO2NaOH 无色酚酞试液C.CO Ca(OH)2无色酚酞试液D.HCl AgNO3紫色石蕊试液3、用下图装置做趣味实验:在用胶塞塞紧的烧瓶里充满某种气体X,烧瓶内导管的一端事先已绑好了一个气球。
拔开胶塞,迅速倒入另一种溶液Y,再立即塞紧胶塞,振荡,此时可以看到气球逐渐膨胀的是( )。
A.氯化氢X、澄清石灰水Y B.氧气X、氯化钾溶液YC.二氧化硫X、氢氧化钠溶液Y。
D.氢气X、硫酸锌溶液Y七、离子共存问题1、重金属离子有毒(重金属一般指密度大于4.5g/cm3的金属)。
实验室有甲、乙两种废液,均有一定毒性。
甲废液经化验呈碱性,主要有毒离子为Ba2+离子,如果将甲、乙两废液按一定比例混合,碱性、毒性明显降低。
乙废液中可能含有的离子是()A.Cu2+和SO42-B.Cu2+和Cl-C.K+和SO42-D、Na+和NO3-2、甲、乙两个相邻的化工厂,排放的污水中有以下八种离子Ag+、Ba2+、Fe3+、Na+、Cl-、SO42-、NO3-、OH-,其中甲、乙两厂各含四种离子且各不相同,经测定甲厂污水的PH > 7,试推断:乙厂污水中含有的四种离子是。
3、室温下,在pH=13的溶液中不可能大量共存的是()A.Fe3+、Ba2+、SO42-、Na+B.K+、SO42-、CO32-、Cl-C.K+、Na+、Ba2+、NO3-D.H+、CO32-、Cl-、Ca2+4、下列各组离子在水溶液中能大量共存的是()A.H+、Ba2+、NO3-、OH-B.K+、SO42-、Na+、Cl-C.K+、CO32-、Ba2+、NO3-D.H+、CO32-、Cl-、K+5、下列各组物质,在溶液中能共存的一组是 ( )A. HCl、NaCl、NaOHB. NaCl、CuSO4、Ba(OH)2C. Na2CO3、NaOH、CaCl2D. NaNO3、HCl、CaCl26、某学校化学课外活动小组,将一些可溶性化合物溶于水,配制成的甲、乙两溶液中,共含有H+、Ag+、K+、Ba2+、OH-、CI-、NO3-、CO32-8种离子,两种溶液里所含离子各不相同,已知向甲溶液里滴入石蕊试液,石蕊试液变成蓝色,则乙溶液里含有的4种离子应该是。
八、金属活动顺序问题1、今有X、Y、Z三种金属,它们间有下列反应事实:X+H2SO4→不发生反应;Z+H2SO4→ZSO4+H2↑;X+YCl→XCl+Y。
由此可判断这三种金属的活动性从左至右由强到弱( )A、X、Y、ZB、Y、X、ZC、Z、Y、XD、Z、X、Y2、只用一种试剂,一次性验证铜、铁、银三种金属的活动性强弱,该试剂是( )。
A、CuSO4溶液B、FeSO4溶液C、AgNO3溶液D、稀盐酸3、在ZnSO4和CuSO4的混合溶液中,加入过量的铁粉,充分反应过滤,留在滤纸上的物质是( )A.只有CuB.只有FeC.Zn和CuD.Fe和Cu4、(1)将一小块金属钠投入盛有适量水的烧杯中,剧烈反应,生成氢气;(2)向(1)反应后的溶液中滴加硫酸铜溶液,有蓝色沉淀生成。
写出实验(1)(2)中有关的化学方程式:(1)(2) .5、X、Y、Z分别是Fe、Cu、Ag、Hg四种金属元素中的一种,X的单质能够从Y的盐溶液中置换出Y,但不能从Z的盐溶液中置换出Z,也不和盐酸反应,Z的单质也能够从Y的盐溶液中置换出Y,但不能置换出酸中的氢。