燃料电池+蓄电池电动汽车动力系统的结构
- 格式:docx
- 大小:37.83 KB
- 文档页数:4





电动汽车动力储能装置包括所有动力蓄电池、超级电容、飞轮电池和燃料电池等储能元件及其以上各类电池的组合。
一、电池的基本组成电池通常由电极(正极和负极)、电解质、隔膜和外壳(容器)四部分组成。
电极是电池的核心部分,通常由活性物质和导电骨架组成。
活性物质是指可以通过化学反应释放出电能的物质,要求其电化学活性高、在电解液中的化学稳定性高以及电子导电性好。
活性物质是决定化学电源基本特性的重要部分。
导电骨架主要起传导电子及支撑活性物质的作用。
当电池通过外部电路(负载)放电时,电池的正极从外电路得到电子,而负极则向外电路输出电子;对于电池内部而言恰好相反。
电解质在电池内部阴、阳极之间担负传递电荷(带电离子)的作用。
电解质一般为液体或固体。
液体电解质常称为电解液,通常是酸、碱、盐的水溶液;固体电解质通常为盐类,由固体电解质组成的电池即称为干电池。
对电解液的要求是电导率高、溶液欧姆电压较小。
对一于固体电解质,要求具有离子导电性,而不具有电子导电性。
电解质的化学性质必须稳定,使其在储存期间与活性物质界面间的电化学反应速率小,这样电池自放电时容量损失减小。
为了避免电池内阴、阳极之间的距离较近而产生内部短路,产生严重的自放电现象,需要在其阴、阳极之间加放绝缘的隔膜,隔膜的形状一般为薄膜、板材或胶状物等。
对隔膜的要求是化学性质稳定,有一定的机械强度,对电解质离子运动的阻力小,是电的良好绝缘体,并可以阻挡从电极上脱落的活性物质微粒和枝晶的生长。
电池的外壳是盛放和保护电池电极、电解质、隔膜的容器。
通常要求外壳具有足够的机械强度和化学稳定性,耐振动、耐冲击、耐腐蚀。
二、电池的基础知识(1)电池的组合蓄电池作为动力源.通常要求有较高的电压和电流,因此需要将若干个单体电池通过串联、并联与复联的方式组合成电池组使用:电池组合中对单体电池性能具有严格的要求,在同一组电池中必须选择同一系列、同一规格、性能尽量一致的单体电池。
(2)电池的放电电池的放电是将电池内储存的化学能以电能方式释放出来的过程,即电池向外电路释放电流。



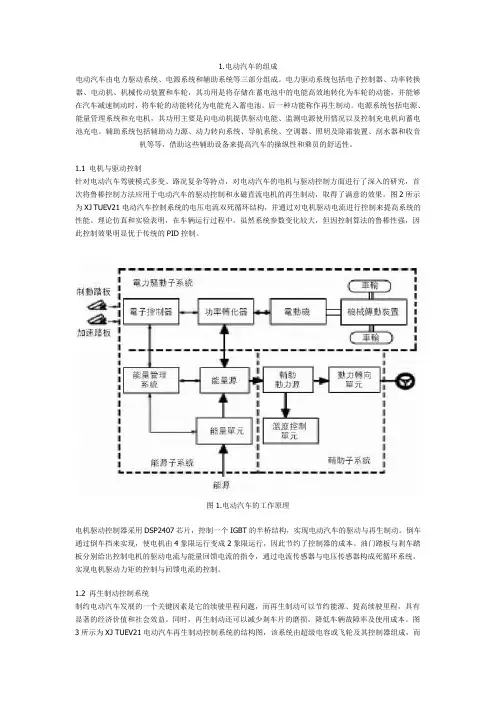
1.电动汽车的组成电动汽车由电力驱动系统、电源系统和辅助系统等三部分组成。
电力驱动系统包括电子控制器、功率转换器、电动机、机械传动装置和车轮,其功用是将存储在蓄电池中的电能高效地转化为车轮的动能,并能够在汽车减速制动时,将车轮的动能转化为电能充入蓄电池。
后一种功能称作再生制动。
电源系统包括电源、能量管理系统和充电机,其功用主要是向电动机提供驱动电能、监测电源使用情况以及控制充电机向蓄电池充电。
辅助系统包括辅助动力源、动力转向系统、导航系统、空调器、照明及除霜装置、刮水器和收音机等等,借助这些辅助设备来提高汽车的操纵性和乘员的舒适性。
1.1 电机与驱动控制针对电动汽车驾驶模式多变、路况复杂等特点,对电动汽车的电机与驱动控制方面进行了深入的研究,首次将鲁棒控制方法应用于电动汽车的驱动控制和永磁直流电机的再生制动,取得了满意的效果。
图2所示为XJ TUEV21电动汽车控制系统的电压电流双死循环结构,并通过对电机驱动电流进行控制来提高系统的性能。
理论仿真和实验表明,在车辆运行过程中,虽然系统参数变化较大,但因控制算法的鲁棒性强,因此控制效果明显优于传统的PID控制。
图1.电动汽车的工作原理电机驱动控制器采用DSP2407芯片,控制一个IGBT的半桥结构,实现电动汽车的驱动与再生制动。
倒车通过倒车挡来实现,使电机由4象限运行变成2象限运行,因此节约了控制器的成本。
油门踏板与剎车踏板分别给出控制电机的驱动电流与能量回馈电流的指令,通过电流传感器与电压传感器构成死循环系统,实现电机驱动力矩的控制与回馈电流的控制。
1.2 再生制动控制系统制约电动汽车发展的一个关键因素是它的续驶里程问题,而再生制动可以节约能源、提高续驶里程,具有显著的经济价值和社会效益。
同时,再生制动还可以减少剎车片的磨损,降低车辆故障率及使用成本。
图3所示为XJ TUEV21电动汽车再生制动控制系统的结构图,该系统由超级电容或飞轮及其控制器组成,而利用超级电容或飞轮吸收再生制动能量,具有非常突出的优点。
电动汽车动⼒传动系的结构与⼯作原理电动汽车动⼒传动系的结构与⼯作原理摘要:能源危机已经逐渐成为世界⾯临的最重⼤问题之⼀。
电动汽车的发展应运⽽⽣。
电动汽车的动⼒传动系统⼜是其核⼼技术,本⽂主要对电动汽车中的蓄电池,电动机以及控制器的结构和⼯作原理进⾏了阐述。
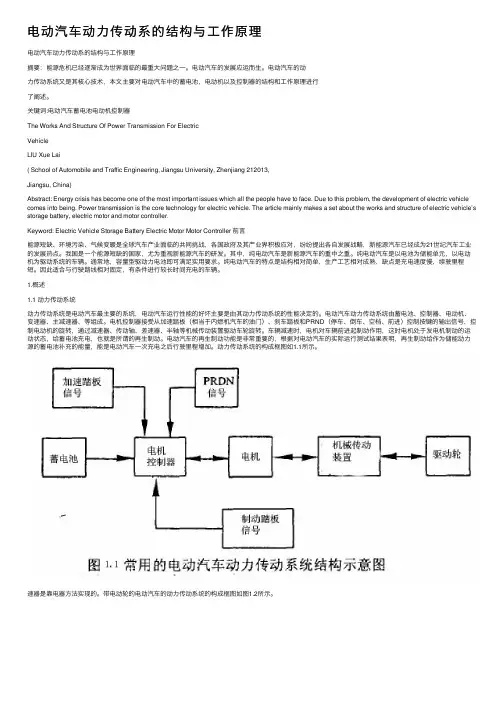
关键词:电动汽车蓄电池电动机控制器The Works And Structure Of Power Transmission For ElectricVehicleLIU Xue Lai( School of Automobile and Traffic Engineering, Jiangsu University, Zhenjiang 212013,Jiangsu, China)Abstract: Energy crisis has become one of the most important issues which all the people have to face. Due to this problem, the development of electric vehicle comes into being. Power transmission is the core technology for electric vehicle. The article mainly makes a set about the works and structure of electric vehicle’s storage battery, electric motor and motor controller.Keyword: Electric Vehicle Storage Battery Electric Motor Motor Controller 前⾔能源短缺、环境污染、⽓候变暖是全球汽车产业⾯临的共同挑战,各国政府及其产业界积极应对,纷纷提出各⾃发展战略,新能源汽车已经成为21世纪汽车⼯业的发展热点。
电动汽车-课后习题答案第一章1. 什么是电动车辆?有哪些特征?所谓电动车辆是指电能驱动电动机作为牵引或驱动行驶的车辆。
特征:电动车辆既有完整的动力装置,又有司机控制室等驾驶和控制设备,同时还能留出空间用于客运;电动车辆还具有编组的灵活性和电工设备分配的机动性。
2. 什么是电动汽车?目前分几类?电动汽车是电动车的一种,也是汽车的一种,即使之全部或者部分用电能驱动作为动力系统的汽车。
分类:蓄电池电动汽车,混合动力汽车,燃料电池汽车3. 电动汽车主要有几部分组成?各部分作用是什么?电源供给系统:驱动系统:作用是在司机的控制下高效率地将蓄电池或者发动机能量转化为车轮的动能,或者将车轮上的动能反馈到蓄电池中。
电动汽车管理系统:4. 电动汽车能实现“少排放”、“零排放”吗?为什么?以蓄电池、超级电容为动力的汽车没有排放物,可以实现零排放。
以纯氢氧为燃料的汽车在运行中只生成水(H2O),不排放任何有害气体,能够实现有害气体零排放。
以富氢气体为燃料的燃料电池,在富氢气体制取氢气的过程中,排出二氧化碳气体,但仅是内燃机排量的40%,燃料电池是以电化学原理发电,不经过内燃机燃烧过程的热能——机械能转换过程,几乎没有产生氮、硫氧化物的条件,所以对大气造成的危害甚少。
作业题一.填空题1. 现代电动汽车发展主要有蓄电池电动汽车、燃料电池汽车、混合动力汽车三种类型。
2. 电动汽车除具有汽车属性外,结构上形成了电源供给系统、驱动系统、控制系统和能源管理系统。
3. 电动汽车电源供给系统主要由储能装置、变换装置、电源馈电线路组成。
二.判断题1. 电动汽车是指以电作为动力源的汽车(对)2. 混合动力电动汽车是指“有两种和两种以上的储能器,能源或转换器作为驱动能源,其中至少有一种能提供电能的车辆称为混合电动汽车”。
燃料电池+蓄电池组合形式应称为混合电动汽车。
(错)3. 用太阳能电池作为动力源的汽车不属于电动汽车。
(错)4. 燃料电池电动汽车可以实现零排放。
第五章燃料电池电动汽车学习目标1.掌握燃料电池的类型及特点,并了解其工作原理。
2.掌握燃料电池电动汽车的类型及结构。
3.了解燃料电池电动汽车的产业发展状况。
4.了解燃料电池电动汽车的典型车型。
第一节燃料电池电动汽车的类型与基本结构一、燃料电池类型及其性能分析燃料电池是一种将氢和氧的化学能通过电极反应直接转换成电能的装置、燃料电池可分为碱性燃料电池(AFC)、磷酸燃料电池(PAFC)、熔融碳酸盐燃料电池(MCFC)、质子交换膜燃料电池(PEMFC)等。
11.质子交换膜燃料电池质子交换膜燃料电池单体主要由膜电极(阳极、阴极)、质子交换膜和集流板组成。
2.碱性燃料电池碱性燃料电池的电解质为碱性的氢氧化钾(KOH),故称为碱性燃料电池。
3.磷酸燃料电池磷酸燃料电池是以磷酸为电解质,故称为磷酸燃料电池。
4.熔融碳酸盐燃料电池熔融碳酸盐燃料电池(MCFC)通常采用含锂和钾的碳酸盐为电解质,阴极为镍的氧化物,阳极为镍合金,正常工作温度为650oC。
25.固体氧化物燃料电池固体氧化物燃料电池的电解质是固体氧化物,催化剂和电池的结构材料,也都是固体氧化物。
故称为固体氧化物燃料电池。
二、燃料电池电动汽车的类型与其结构燃料电池汽车定义:燃料电池电动汽车(FCEV)是利用氢气和空气中的氧在催化剂的作用下在燃料电池中经电化学反应产生的电能,并作为主要动力源驱动的汽车。
1.燃料电池单独驱动FCEV该结构只有燃料电池一个动力源,汽车的所有功率负荷都由3燃料电池承担。
图5-6纯燃料电池驱动的FCEV2.燃料电池与辅助蓄电池联合驱动FCEV。
该结构为一典型的串联式混合动力结构43.燃料电池与超级电容联合驱动FCEV这种结构形式与燃料电池+蓄电池结构相似,只是把蓄电池换成超级电容。
图5-8燃料电池与超级电容联合驱动4.燃料电池与辅助蓄电池和超级电容联合驱动的FCEV 燃料电池与蓄电池和超级电容联合驱动的电动汽车的动力系统结构也为串联式混合动力结构。
丰田燃料电池汽车的结构组成
《丰田燃料电池汽车的结构组成》
丰田燃料电池汽车是一种环保、高效的新型汽车,其结构组成主要包括燃料电池系统、驱动系统、储氢系统和整车控制系统。
燃料电池系统是汽车动力的核心部件,它由燃料电池堆、电池控制器和氢气贮罐组成。
燃料电池堆是通过氢气与氧气在催化剂作用下产生电能的装置,它是整个系统的能量源。
电池控制器负责管理燃料电池的工作状态,确保其安全、稳定地工作。
氢气贮罐用于储存汽车所需的氢气燃料,保障车辆的续航能力。
驱动系统是指汽车的动力传输系统,它包括电动机、电子变速器等部件。
电动机是燃料电池汽车的主要动力来源,它通过燃料电池系统提供的电能驱动汽车运行。
电子变速器则负责控制汽车的速度和扭矩输出,确保汽车的平稳、高效运行。
储氢系统是燃料电池汽车使用氢气作为燃料的关键环节,它包括氢气贮存系统和氢气供给系统。
氢气贮存系统用于储存和输送氢气燃料,确保汽车长时间的续航能力。
氢气供给系统则负责将储存的氢气燃料引入燃料电池系统,供给汽车动力需求。
整车控制系统是燃料电池汽车的智能管理系统,它通过传感器和控制器实时监测和调控汽车各部件的运行状态。
整车控制系统可以优化燃料电池系统的工作效率,提高汽车的动力性能和节能环保水平。
总的来说,丰田燃料电池汽车的结构组成综合了先进的燃料电池技术和智能的汽车控制技术,实现了高效、环保、安全的汽车动力系统,为汽车发展带来了新的机遇和挑战。
燃料电池和蓄电池是现代电动汽车动力系统中重要的组成部分,它们各自发挥着不同的作用,共同构成了高效、环保的动力系统。
本文将从燃料电池和蓄电池的组成结构、工作原理及优缺点等方面展开详细介绍,希望能够为读者对电动汽车动力系统有更深入的了解。
一、燃料电池的结构
1. 电解质膜:作为燃料电池中的主要组件之一,电解质膜起着将氢气和氧气分离开的作用,同时还能传导质子和电子。
2. 阳极:燃料电池的阳极为氢气的氧化反应提供了场所,并且促进了电子的运动,使其向阴极流动。
3. 阴极:阴极是氧气还原的场所,其表面覆盖着催化剂,促进氧气在此处与质子和电子结合,生成水。
4. 增湿板:增湿板用于控制燃料电池中的水分平衡,使得电解质膜的温度和湿度保持在适宜的范围内。
5. 氢气供应系统:燃料电池中需要氢气作为燃料,氢气供应系统会将氢气从储罐中引入燃料电池中进行反应。
二、燃料电池的工作原理
1. 氢氧反应:在阳极,氢气会发生氧化反应,生成氢离子和电子。
2. 电子流动:电子会沿着外部电路流向阴极,产生电流。
3. 氧还原:在阴极,氧气会与生成的氢离子和电子结合,生成水,释放出能量。
4. 电化学反应:整个过程是一个电化学反应,通过氢气、氧气在阳极
和阴极的反应,将化学能转化为电能。
三、燃料电池的优缺点
1. 优点:
1) 高能量密度:相比传统的锂电池,燃料电池具有更高的能量密度,能够提供更长的续航里程。
2) 快速加氢:与充电电池相比,燃料电池的加氢速度更快,且使用
过程更加便捷。
3) 长期使用寿命:燃料电池具有较长的使用寿命,且不会出现充放
电次数增加而引起的寿命下降。
2. 缺点:
1) 基础设施不完善:目前氢气加氢站的建设还比较少,用户在使用
燃料电池车辆时可能会受到基础设施限制。
2) 成本较高:燃料电池的制造成本较高,且目前的生产规模较小,
导致单车成本较高。
3) 能源转化率较低:燃料电池的能源转化率(氢气到电能)较低,依然存在能源浪费的问题。
四、蓄电池的结构
1. 正极:蓄电池的正极通常由氧化物制成,具有较高的氧化还原能力。
2. 负极:负极常由金属锂制成,锂的还原能力较强,能够提供电子。
3. 电解质:电解质是负极和正极之间的隔离层,能够传导锂离子。
4. 外壳:外壳作为蓄电池的保护层,能够固定电解质和正负极,同时
防止外界环境对蓄电池的影响。
五、蓄电池的工作原理
1. 充电过程:在充电过程中,正极的氧化物会释放出氧离子,同时负
极的锂会释放出电子,经过电解质,电子和氧离子会在正极和负极重
新结合,形成稳定的氧化物和金属锂结构。
2. 放电过程:在放电过程中,氧化物会吸收负极释放出的电子和离子,同时金属锂会释放锂离子,形成氧化物和金属锂的结构。
六、蓄电池的优缺点
1. 优点:
1) 成本较低:蓄电池的制造成本较低,且生产规模较大,能够降低
单车成本。
2) 能源转化效率高:蓄电池的能源转化效率较高,能够更好地利用
储存的电能。
3) 充放电次数多:蓄电池能够进行多次充放电循环,不会因为充放
电次数增加而影响使用寿命。
2. 缺点:
1) 能量密度低:相比燃料电池,蓄电池的能量密度较低,续航里程
相对较短。
2) 充电时间长:和燃料电池相比,蓄电池的充电时间较长,需要较
长时间才能够完成充电。
3) 重量较大:由于蓄电池的结构和材质,其重量较大,会对车辆的整体重量和能效比产生影响。
燃料电池和蓄电池分别具有各自的优势和劣势,在电动汽车动力系统中各自发挥着重要的作用。
未来随着技术的不断发展和完善,相信这两种动力系统都会得到更好的应用和推广,为汽车行业的可持续发展做出更大的贡献。