酵母蔗糖酶的提取及其性质研究精品PPT课件
- 格式:ppt
- 大小:861.50 KB
- 文档页数:25




实验九酵母蔗糖酶的提取及其性质的研究本实验为学生提供一个较全面的实践机会,学习如何提取纯化、分析鉴定一种酶,并对这种酶的性质,尤其是动力学性质作初步的研究。
自1860年Bertholet从酒酵母Sacchacomyces Cerevisiae中发现了蔗糖酶以来,它已被广泛地进行了研究。
蔗糖酶(invertase)(β—D—呋喃果糖苷果糖水解酶)(fructofuranoside fructohydrolase)(EC.3.2.1.26)特异地催化非还原糖中的α—呋喃果糖苷键水解,具有相对专一性。
不仅能催化蔗糖水解生成葡萄糖和果糖,也能催化棉子糖水解,生成密二糖和果糖。
本实验提取啤酒酵母中的蔗糖酶。
该酶以两种形式存在于酵母细胞膜的外侧和内侧,在细胞膜外细胞壁中的称之为外蔗糖酶(external yeast invertase), 其活力占蔗糖酶活力的大部分,是含有50% 糖成分的糖蛋白。
在细胞膜内侧细胞质中的称之为内蔗糖酶(internal yeast invertase),含有少量的糖。
两种酶的蛋白质部分均为双亚基,二聚体,两种形式的酶的氨基酸组成不同,外酶每个亚基比内酶多两个氨基酸,Ser和Met,它们的分子量也不同,外酶约为27万(或22万,与酵母的来源有关),内酶约为13.5万。
尽管这两种酶在组成上有较大的差别,但其底物专一性和动力学性质仍十分相似,因此,本实验未区分内酶与外酶,而且由于内酶含量很少,极难提取,本实验提取纯化的主要是外酶。
两种酶的性质对照表如下:实验中,用测定生成还原糖(葡萄糖和果糖)的量来测定蔗糖水解的速度,在给定的实验条件下,每分钟水解底物的量定为蔗糖酶的活力单位。
比活力为每毫克蛋白质的活力单位数。
本实验共有九个分实验:一、蔗糖酶的提取与部分纯化二、离子交换柱层析纯化蔗糖酶三、蔗糖酶各级分活性及蛋白质含量的测定四、反应时间对产物形成的影响五、pH对酶活性的影响和最适pH的测定六、温度对酶活性的影响和反应活化能的测定七、底物浓度对催化反应速度的影响及米氏常数K m和最大反应速度V max的测定八、尿素(脲)抑制蔗糖酶的实验九、棉子糖和果糖抑制蔗糖酶的实验(一)蔗糖酶的提取与部分纯化一、实验目的:学习酶的纯化方法,并为动力学实验提供一定量的蔗糖酶。

酵母蔗糖酶的制备及其动力学性质分析一、蔗糖酶(invertase or sucrase)简介蔗糖酶(EC.3.2.1.26)为水解酶类,主要存在于植物和微生物体内,专一性地催化蔗糖水解为果糖和葡萄糖的反应。
酵母蔗糖酶分子量约270000D,pI约5.0,最适pH4.6,耐酸和热,50℃保温30min 仍具有相当的活力,最适温度37℃。
耐乙醇,因此可用乙醇沉淀进行分离纯化。
二、酵母蔗糖酶的分离纯化本试验分离纯化酵母蔗糖酶分四步:甲苯抽提。
加热纯化。
乙醇分级沉淀。
纤维素柱层析分离纯化。
㈠、前三步分离纯化的原理如下:甲苯石英砂离心上层(甲苯层):脂溶性物质酵母细胞破细胞中层(水层):蔗糖酶,可溶性糖等研磨下层(沉淀):细胞碎片、变性蛋白等取中层50水浴中使热不稳定蛋白变性上清:蔗糖酶、可溶性糖等(水层)保温30分钟沉淀:变性蛋白取上清加乙醇使蔗糖酶沉淀上清:杂蛋白及可溶性糖等冰浴中20分钟沉淀:蔗糖酶、杂蛋白等㈡、纤维素柱层析分离纯化的原理1、离子交换柱层析分离混合物的基本原理离子交换层析(Ion Exchange Chromatography)是一种根据待分离物质的阳或阴离子和相对应的离子交换剂间的静电结合,即根据物质酸碱性、极性等差异,通过离子间的吸附和脱吸附而将溶液中各组分分开的一种技术。
离子交换层析是一种液-固相层析技术。
其中,液相称洗脱液,固相的惰性支持介质称离子交换剂。
在离子交换剂上具有带电基团,不同的交换剂所具有的带电基团的电荷性质不同,如交换剂上的带电基团带正电荷,则可结合溶液(液相)中的阴离子,这样的交换剂称为阴离子交换剂,如DEAE纤维素、强碱型的离子交换树脂等。
反之,如交换剂上的带电基团带负电荷,则可结合溶液中的阳离子,这样的交换剂称为阳离子交换剂,如CM-纤维素、强酸性的离子交换树脂等。
离子与交换剂的静电结合作用具如下特点:选择性:离子所带的电荷越多,离子半径越小,越易结合。
遵循质量作用定理:对某一特定离子,随离子浓度的增大,则遵循质量作用定理向与交换剂结合方向进行可逆性:在一定条件下,结合在交换剂上的离子可被其它)离子取代而离开交换剂并随洗脱液流出层析柱。
酵母蔗糖酶的提取及其性质的研究一、蔗糖酶的制备1、提取称取14.997g干酵母粉于250ml小烧杯中,少量多次地加入50ml蒸馏水,搅拌均匀。
成糊状后加入1.499g乙酸钠、25ml乙酸乙酯,搅匀。
再于35℃恒温水浴中搅拌30min,然后补加30ml蒸馏水,搅匀,盖好,于35℃恒温过夜。
之后,1000r/min离心10min,抽取酯层后再次离心,得到无细胞提取液。
用1M HCl将其PH调至5.0,即可得到级分Ⅰ。
(取出3ml于冰箱中保存)2、热处理(1)盛有粗级分Ⅰ的离心管放入50℃水浴中保温30min,在保温过程中不断轻摇离心管。
(2)取出离心管,于冰浴中迅速冷却,用4℃,1000r/min离心10min。
(3)上清液即为热级分Ⅱ。
(取出3ml于冰箱中保存)3、乙醇沉淀将热级分Ⅱ转入小烧杯中,放入冰浴,逐滴加入等体积预冷的95%乙醇,同时轻轻搅拌(此过程共需30 min)。
然后在冰浴中静置10 min,以沉淀完全。
然后4℃,1000r/min离心10min。
倾去上清,并滴干。
将沉淀保存于离心管中,冷冻保存,此即级分Ⅲ。
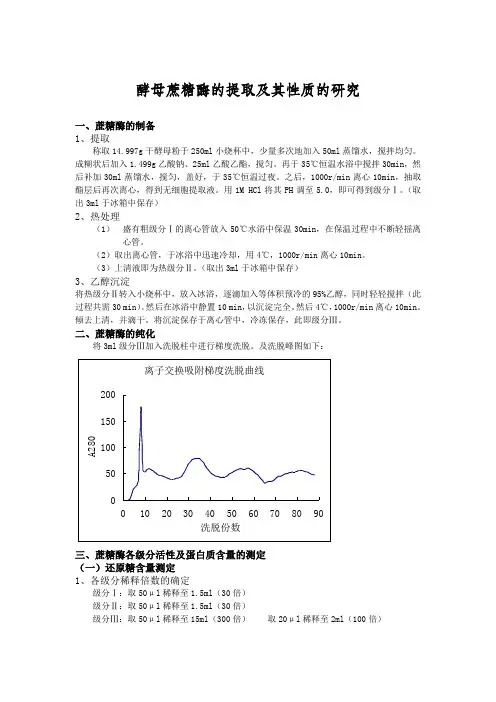
二、蔗糖酶的纯化将3ml级分Ⅲ加入洗脱柱中进行梯度洗脱。
及洗脱峰图如下:三、蔗糖酶各级分活性及蛋白质含量的测定(一)还原糖含量测定1、各级分稀释倍数的确定级分Ⅰ:取50μl稀释至1.5ml(30倍)级分Ⅱ:取50μl稀释至1.5ml(30倍)级分Ⅲ:取50μl稀释至15ml(300倍)取20μl稀释至2ml(100倍)释100倍。
在上述表格中,Glu含量是由标准曲线求得的,E'=Glu含量*稀释倍数/(10 min*0.6 ml)Units=0.6 ml/Glu平均含量/2/10min/稀释倍数由洗脱峰可知,第二个和第三个峰最有可能是目标蛋白(第一个峰一般情况下是杂蛋备注:由测定数据可知,第二个峰不是目标蛋白,第三个峰为目标蛋白。
(二)蛋白质含量测定1、各级分稀释倍数的确定由以上数据可知,级分Ⅰ和级分Ⅱ不需稀释,级分Ⅲ需稀释5倍。

酵母蔗糖酶的提取方法摘要:采用甲苯自溶法、冻融法、SDS抽提法3种方法从酵母中提取蔗糖酶,经质量分数50%的乙醇分级沉淀、MonoQ阴离子交换柱层析纯化后,制得高纯度的酵母蔗糖酶。
比较了上述3种提取方法并对该酶的部分性质进行了研究。
纯化的酶经等电聚焦测定,等电点为5.6,SDS-PAGE鉴定其相对分子质量为60kD。
以蔗糖为底物测得酵母蔗糖酶的表观米氏常数Km为0.013mol/L。
结果显示3种提取方法各有优劣,冻融法和SDS抽提法的提取效率远高于传统的甲苯自溶法。
其中SDS抽提法的效率最高,加之其操作简便,更适合于酵母蔗糖酶大规模的制备提取。
关键词:酵母;蔗糖酶;提取;纯化蔗糖酶(Sucrase,EC 3.2.1.26)又称转化酶(Invertase)。
可作用于B一1,2糖苷键,将蔗糖水解为D-葡萄糖和D-果糖。
由于果糖甜度高,约为蔗糖的1.36~1.60倍,在工业上具有较高的经济价值。
可用以转化蔗糖,增加甜味,制造人造蜂蜜,防止高浓度糖浆中的蔗糖析出,制造含果糖和巧克力的软心糖,还可为果葡糖浆的工业化生产提供新的方法。
目前关于酵母中蔗糖酶提取纯化方面的研究较多,以甲苯自溶法最为常见。
作者采用甲苯自溶法、冻融法、SDS抽提法3种不同的方法从酵母中提取蔗糖酶,将冻融法和SDS法提取的蔗糖酶进一步纯化,并对其基本性质进行了研究。
通过不同提取方法的比较,为酵母蔗糖酶在食品工业中的应用和蔗糖酶基因工程产品的下游技术开发,提供了实验依据。
1材料与方法1.1材料酵母,安琪酵母股份有限公司提供;MonoQ(10/10)阴离子交换层析柱、PhastGelIEF3-9胶,Amersham公司提供。
1.2主要化学试剂和仪器十二烷基硫酸钠(SDS),Serva公司提供;等电点标准品,Amersham公司提供;其余试剂均为国产分析纯或生化试剂。
UV一2201型紫外可见光分光光度计,Shimadzu公司制造;Waters650型高级蛋白纯化系统,Waters公司制造;PhastSystem全自动快速水平电泳仪,Amersham公司制造;高速冷冻离心机,Hitachi公司制造;冷冻干燥器,Labconco公司制造;电泳仪,Bio-Rad公司制造;精密酸度计,Orion公司制造。


酵母蔗糖酶的提取及性质测定引论及原理酶的分离制备在酶学以及生物大分子的结构功能研究中有重要意义。
本实验属综合性实验,接近研究性实验,包括八个连续的实验内容,通过对蔗糖酶的提纯和性质测定,了解酶的基本研究过程;同时掌握各种生化技术的实验原理、基本操作方法。
本实验技术多样化,并且多个知识点互相联系,实验内容逐步加深,构成了一个综合性整体,为学生提供一个较全面的实践机会,学习如何提取纯化、分析鉴定一种酶,并对这种酶的性质,尤其是动力学性质作初步的研究。
蔗糖酶(invertase )(β—D —呋喃果糖苷果糖水解酶)(fructofuranoside fructohydrolase )(EC.3.2.1.26)特异地催化非还原糖中的α—呋喃果糖苷键水解,具有相对专一性。
不仅能催化蔗糖水解生成葡萄糖和果糖,也能催化棉子糖水解,生成密二糖和果糖。
每水解1mol 蔗糖,就生成2mol 还原糖。
还原糖的测定有多种方法,本实验采用Nelson 比色法测定还原糖量,由此可得知蔗糖水解的速度。
在研究酶的性质、作用、反应动力学等问题时都需要使用高度纯化的酶制剂以避免干扰。
酶的提纯工作往往要求多种分离方法交替应用,才能得到较为满足的效果。
常用的提纯方法有盐析、有机溶剂沉淀、选择性变性、离子交换层析、凝胶过滤、亲和层析等。
酶蛋白在分离提纯过程中易变性失活,为能获得尽可能高的产率和纯度,在提纯操作中要始终注意保持酶的活性如在低温下操作等,这样才能收到较好的分离效果。
啤酒酵母中,蔗糖酶含量丰富。
本实验用新鲜啤酒酵母为原料,通过破碎细胞,热处理,乙醇沉淀,柱层析等步骤提取蔗糖酶,并对其性质进行测定。
一、蔗糖酶的提取与部分纯化(一)实验目的学习酶的提取和纯化方法,掌握各步骤的实验原理,并为后续实验提供一定量的蔗糖酶。
(二)实验原理(略) (三)实验仪器、材料及试剂 仪器1. 高速冷冻离心机、恒温水浴箱、-20℃冰箱2. 电子天平、研钵(>200ml )、制冰机、50ml 烧杯3. 离心管(2ml ,10ml ,30ml 或50ml )、移液器(1000ul )或滴管、量筒 材料及试剂1. 市售鲜啤酒酵母(低温保存)+ H 2O 蔗糖酶O HH O2.石英砂(海沙)、甲苯(使用前预冷到0℃以下)3.95%乙醇(预冷-20℃)、去离子水(使用前冷至4℃左右)4.Tris-HCl(pH7.3)缓冲液(四)操作步骤1. 提取(1)将市售鲜啤酒酵母2000 rpm,离心10 min,除去大量水分。

