示差光度法
- 格式:ppt
- 大小:1.20 MB
- 文档页数:46


第8章习题答案1.已知KMnO4的ε545=2.2×103,计算此波长下浓度为0.002%(m/v)KMnO4溶液在3.0cm吸收池中的透射比。
若溶液稀释一倍后透射比是多少?答案:若稀释一倍,A=0.432.以丁二酮肟光度法测定镍,若络合物NiDx2的浓度为1.7×10-5mol·L-1,用2.0cm吸收池在470nm波长下测得的透射比为30.0%。
计算络合物在该波长的摩尔吸光系数。
答案:3.以邻二氮菲光度法测定Fe (Ⅱ),称取试样0.500g,经处理后,加入显色剂,最后定容为50.0mL,用1.0 cm吸收池在510 nm波长下测得吸光度A=0.430,计算试样中的w(Fe)(以百分数表示);当溶液稀释一倍后透射比是多少?(ε510=1.1×104)答案:溶液稀释一倍,4.根据下列数据绘制磺基水杨酸光度法测定Fe(Ⅲ)的工作曲线。
标准溶液是由0.432g铁铵矾[NH4Fe(SO4)2·12H2O]溶于水定容到500.0mL配制成的。
取下列不同量标准溶液于50.0mL容量瓶中,加显色剂后定容,测量其吸光度。
V(Fe(Ⅲ))(mL) 1.00 2.00 3.00 4.00 5.00 6.00A0.0970.2000.3040.4080.5100.618测定某试液含铁量时,吸取试液5.00mL,稀释至250.0mL,再取此稀释溶液2.00mL置于50.0mL容量瓶中,与上述工作曲线相同条件下显色后定容,测得的吸光度为0.450,计算试液中Fe(Ⅲ)含量(以g/L表示)。
答案:V(Fe),mL 1.00 2.00 3.00 4.00 5.00 6.00c(Fe), mg/50mL0.1000.2000.3000.4000.5000.600A0.0970.2000.3040.4080.5100.618绘制A~c(Fe)工作曲线(略),由工作曲线查得A=0.450时,c(Fe)=0.440mg/50mL根据样品稀释情况,Fe的含量为:5.有两份不同浓度的某一有色络合物溶液,当液层厚度均为1.0cm时,对某一波长的透射比分别为:(a)65.0%;(b)41.8%。

示差分光光度法示差分光光度法1示差法的原理吸光光度法一般仅适用于微量组分的测定,当待测定组分浓度过高或过低,亦即吸光度测量值过大或过小时,从上节的测量误差的讨论得知,在这种情况下即使没有偏离朗伯—比耳定律的现象,也会有很大的测量误差,导致精准度大为降低。
采纳示差法可克服这一缺点。
目前重要有高浓度示差法,稀溶液示差法和使用两个参比溶液的精密示差法。
其中以高浓度示差法应用*多,本节将侧重讨论。
示差光度法和一般的光度法不同之处重要在于,示差法不是以空白溶液(不含待测组分的溶液)作为参比溶液,而是采纳比待测溶液浓度稍低的标准溶液作参比溶液,然后测量待测溶液的吸光度,再从测得的吸光度求出它的浓度。
这样便大大提高测定结果的精准度。
设用作参比的标准溶液浓度为cs,待测溶液浓度为cx,且cxcs,依据朗伯—比耳定律得到Ax=εcxbAs=εcsb两式相减:A相对=Ax—As=εb(cx—cs)=εbΔc(2—12)实际操作是:用已知浓度的标准溶液作参比,调整其吸光度为零(透光率100%),然后测量待测溶液的吸光度。
这时测得的吸光度实际是这两种溶液吸光度的差值(相对吸光度)。
从(2—12)式可知,所测得的吸光度差值与这两种溶液的浓度差成正比。
这样便可以把空白溶液为参比的稀溶液标准曲线作为ΔA对应于Δc的工作曲线,依据测得的ΔA找出相应的Δc值,从cx=cs+Δc,便可求出待测溶液之浓度,这就是示差法定量测定的基本原理。
2示差法的误差用示差法测定浓度过高或过低试液,其精准度比一般分光光度法高。
这可从图2—3看出。
设图2—3示差法标尺原理按一般分光光度法用试剂空白作参比溶液,测得溶液的透光率Tx=6%,明显,这时的测量读数误差是很大的。
采纳示差法时,假如按一般分光光度法测得的Ts=10%的标准溶液作参比溶液,使其透光率从标尺上Ts1=10%处调至Ts2=100%处,相当于把检流计上的标尺扩展到原来的十倍(TS2/TS1=100/10=10),这样待测试液透光率原来为6%,读数落在光度计标尺刻度很密,测量误差很大的区域,改用示差法测定时,透光率则是60%,读数落在测量误差很小的区域,从而提高了测定的精准度。

示差分光光度法
示差分光光度法是一种在分子取向反应或光谱特性中应用广泛的
分析方法。
首先,示差分光光度法通过比较两种不同取向下的吸收光谱,来
探测反应中的分子结构变化。
通过这种方法,我们可以更好地理解反
应的机理和特性。
其次,示差分光光度法在不同波长或时间段内测量光谱信号,可
以得到很高的灵敏度和分辨率。
这使得该方法在许多不同领域都有应用,如化学、生物学、医学等等。
此外,示差分光光度法还可以用于探测微量物质的存在和浓度变化。
这种方法可以用于监测环境污染、药物代谢等方面。
需要注意的是,示差分光光度法需要设备精细和技术娴熟的操作。
对于初学者来说,需要认真学习理论知识和实验技能,才能获得准确
的测量结果。
总之,示差分光光度法是一种应用广泛、灵敏度高、分辨率高的
分析方法。
在化学、生物学、医学等领域都有广泛的应用前景。
如今,随着技术的不断发展和创新,示差分光光度法将会得到更广泛的应用
和挖掘。


分析化学测试题(附答案)一、单选题(共50题,每题1分,共50分)1、消除随机误差的方法是()。
A、做多次平行测定,取平均值B、把所使用的所有仪器进行严格校正C、使用分析纯的试剂D、非常认真细致地操作正确答案:A2、若试样的分析结果精密度很好,但准确度不好,可能原因是()。
A、试样不均匀B、使用试剂含有影响测定的杂质C、有过失操作D、使用校正过的容量仪器正确答案:B3、浓度和体积相同的两份KHC2O4·H2C2O4溶液,一份可与VmL0.1500mol/LNaOH溶液完全中和,另一份加H2SO4后,用KMnO4溶液滴定至终点,也需要VmLKMnO4溶液。
该KMnO4溶液的浓度为()mol/L。
A、0.1000B、0.04000C、0.02000D、0.1500正确答案:B4、在pH=9的氨性缓冲溶液中,lG.Zn(NH3)=5.49,用0.02mol/L的EDTA 滴定同浓度的Zn2+,化学计量点pZn.计为()。
A、9.2B、5.8C、11.6D、6.5正确答案:B5、分析实验所用的仪器①滴定管、②移液管、③容量瓶、④锥形瓶中,使用时需要用操作液漂洗的是()。
A、①②③B、②③C、③④D、①②正确答案:D6、滴定分析要求相对误差≤.0.2%,若称取试样的绝对误差为.0.2mg,则至少称取试样()。
A、0.1gB、0.3gC、0.4gD、0.2g正确答案:A7、用高锰酸钾法测定(滴定)H2O2时,应该()。
A、在HAc介质中进行B、加热至75~85.CC、在氨性介质中进行D、不用另加指示剂正确答案:D8、涂好油的酸式滴定管,转动其旋塞时,发现有纹路,说明()。
A、油涂得太少了B、油涂得太多了C、油的质量很好D、油堵住了塞孔正确答案:A9、称取仅含NaOH和Na2CO3的混合物0.4120g,溶于适量水中,然后以甲基橙为指示剂,用0.2000mol/LHCl溶液滴定至终点时消耗HCl溶液45.00mL。

一、填空题紫外-可见吸收光谱是由分子的振动和转动能级跃迁产生的,红外吸收光谱是由分子的振动能级跃迁产生的。
红外吸收光谱法测定固体样品的处理方法有研糊法、KBr压片法和薄膜法。
原子吸收分析中,对同一类型的火焰按其燃气和助燃气的比例不同可分为化学计量火焰、富燃火焰和贫燃火焰三种类型。
在液-液分配色谱中,对于亲水固定液采用疏水性流动相,正相色谱法的流动相的极性小于固定液的极性(填大于,或小于),极性小的组分先流出,极性大的组分后流出。
(填先或后)反相色谱法的流动相的极性大于固定液的极性(填大于,或小于),极性小的组分后流出,极性大的组分先流出。
(填先或后)示差光度法的测定方法与普通分光光度法相同,只是调100% T和调0%T的方式有所不同。
在相同条件下配制样品溶液和标准溶液,其浓度分别为c x(待测)和c s,在最佳波长λ最佳处测得两者的吸光度分别为Ax和As,则样品浓度c x可表示为C X=[A X/(As-AX)]*C0。
盐桥的作用是保持溶液电中性,沟通回路。
总离子强度调节剂(TISAB)的作用:保持较大且稳定的离子强度,使活度系数恒定、维持溶液在适宜的pH范围内,满足离子电极的要求、掩蔽干扰离子。
线性的振动自由度可表示为3n-5,CO2分子的振动自由度为4。
非线性的振动自由度可表示为3n-6,H2O分子的振动自由度为 3 。
电极极化包括浓差极化和电化学极化。
增强溶剂的极性使π→π*跃迁红移和使n→π*跃迁蓝移无机化合物分子的紫外-可见光谱是由电荷转移跃迁和配位体场跃迁产生。
化学位移是由于氢核具有不同的屏蔽常数σ,产生核磁共振现象时,引起外磁场或共振频率的移动的现象。
气相色谱法的两个基本理论为塔板理论和速率理论。
采用紫外可见分光光度计测定试样中组分含量,所使用的显色剂和试剂无吸收,应选择纯溶剂或水(溶剂空白)作参比溶液。
气相色谱分析中,分离极性物质,一般选用极性固定液,试样中各组分按溶解度不同分离,ﻫ极性小的组分先流出色谱柱,极性大的组分后流出色谱柱。

培训试题(第十三章-第十六章)一、填空(55分)1、紫外可见分光光度法所用的光谱区域为 200~780 nm ,红外光谱法为 2.5~1000 um 。
2、利用比较溶液颜色深浅的方法来确定溶液中有色物质含量的方法就称为比色法。
3、分光光度法特别适用于低含量、微量组分的测定,不适用于高含量组分的测定。
4、由价电子跃进而产生的光谱称为电子光谱。
5、光吸收程度最大处得波长称为最大吸收波长。
6、测量物质分子对不同波长的光的吸收强度的仪器称为紫外可见分光光度计,分光光度计的主要部件包括光源、单色器、吸收池、检测器、测量系统。
7、分光光度计的检测器是一种光电转换设备,它将光强度转变为电讯号显示出来,常用的有光电池、光电管、或光电倍增管。
8、显色反应一般可以分为两类:络合反应、氧化还原反应。
9、分光光度计测定样品时一般控制投射比为 15%~65% ,吸光度为 0.2~0.8 时,测量的相对误差较小,这就是适宜的吸光度范围。
可以采用调节溶液浓度和吸收池厚度来实现。
10、利用紫外分光光度进行定量分析一般不需要选用显色剂,测定条件的选择主要是选择测定最佳波长和溶剂。
11、由分子的振动和转动能级跃迁产生的连续吸收光谱称为分子光谱。
12、红外吸收光谱仪最常用的光源为能斯特灯和硅碳棒。
13、原子吸收光谱与共振荧光光谱互为逆过程。
14、原子吸收光谱仪由光源、原子化系统、分光系统、检测系统 4部分组成。
15、空心阴极灯的工作电流可以采用额定电流的 40%~60% 。
16、火焰原子化器由喷雾器、雾化室和燃烧器 3部分组成。
17、火焰原子化器燃烧器的作用是原子化。
18、采用石墨炉原子化分析过程中灰化是为了除去气体,以减少共存元素的干扰。
19、化学干扰是原子吸收光谱分析中的主要干扰。
20、实现色谱分离的先决条件是必须具备固定相和流动相。
固定相可以是固体吸附剂和涂渍于惰性载体表面上的液态薄膜,流动相可以是具有惰性的气体、液体或超临界流体。
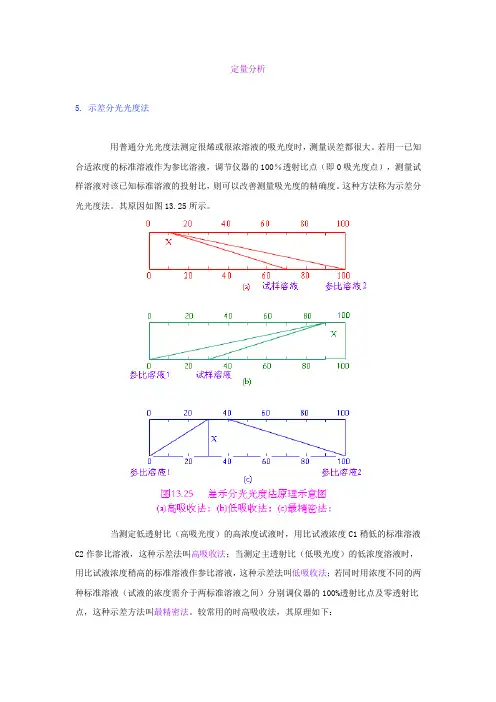
定量分析5. 示差分光光度法用普通分光光度法测定很烯或很浓溶液的吸光度时,测量误差都很大。
若用一已知合适浓度的标准溶液作为参比溶液,调节仪器的100%透射比点(即0吸光度点),测量试样溶液对该已知标准溶液的投射比,则可以改善测量吸光度的精确度。
这种方法称为示差分光光度法。
其原因如图13.25所示。
当测定低透射比(高吸光度)的高浓度试液时,用比试液浓度C1稍低的标准溶液C2作参比溶液,这种示差法叫高吸收法;当测定主透射比(低吸光度)的低浓度溶液时,用比试液浓度稍高的标准溶液作参比溶液,这种示差法叫低吸收法;若同时用浓度不同的两种标准溶液(试液的浓度需介于两标准溶液之间)分别调仪器的100%透射比点及零透射比点,这种示差方法叫最精密法。
较常用的时高吸收法,其原理如下:根据吸收定律有则即用C2作参比测得的A为示差法实质上是相当于把仪器的测量标尺放大,以提高测定的精确度。
如果C2以常规法测得的透射比为10%,在示差法用调至透射比为100%,意味着标尺扩大了10倍。
若待测试液以常规法的最终分析法得的透射比为5%,用C2作参比的示差法测得透射比为50%。
示差法的最终分析结果准确度比常规法高,这是因为尽管示差法测出的很小的ΔC,而测得的误差dC也很大,则仍很大,但最终分析结果的相对误差为,Cs是标准参比溶液,Cs相对很大,所相对误差仍然很小。
6. 光度滴定法分光光度滴定法是利用被测组分或滴定剂或反应产物在滴定过程中的吸光度的变化来确定滴定终点,并由此计算试液中被测组分含量的方法。
分光光度滴定曲线是在某一给定波长处在滴定过程中所测得的吸光度与已知浓度的滴定剂体积之间的关系曲线,其曲线的形状取决于反应体系中样品组分、滴定剂或产物的吸光程度,如图13.26所示。
图13.26(a)是用有色滴定剂(其摩尔吸光系数εt>0)滴定含非吸收组分(εs>0)的试液,生成的产物也无吸收(εp=0),即εt>0,εs=εp=0;(b)是εp>0,εs=εt=0;(c)是εs>0,εp=εt=0;(d)是εs>0,εt=εp=0;(e)是εp >0,εs=εt=0;(f)是εs>0,εp=εt=0。

邻菲罗啉示差分光光度法测定铁矿石中全铁含量概述邻菲罗啉示差分光光度法(Differential Spectrophotometric Method with Phenanthroline)是一种常用于测定铁矿石中全铁含量的分析方法。
该方法基于邻菲罗啉与亚铁离子的络合反应,通过测定络合物的吸光度来间接测定样品中的全铁含量。
原理邻菲罗啉与亚铁离子反应生成橙色络合物,该络合物在510 nm波长处有最大吸光度。
当样品中的亚铁离子与邻菲罗啉反应生成络合物时,溶液吸光度会随着亚铁离子浓度的增加而增大。
通过测量样品在510 nm波长处的吸光度,可以间接推算出样品中的全铁含量。
实验步骤试剂及设备准备•邻菲罗啉试剂(0.1% 邻菲罗啉溶液)•硫酸(浓度为3.5%)•氢氧化钠(浓度为1.5 M)•铁矿石样品•分光光度计样品预处理1.取一定量的铁矿石样品,加入一些硫酸溶液,用玻璃棒搅拌均匀。
2.将溶液加热至沸腾,持续加热10分钟,使铁矿石样品完全溶解。
3.将溶液冷却至室温,用硫酸调节pH值。
4.加入适量氢氧化钠溶液,使溶液中的亚铁氧化成铁离子。
5.将溶液转移到容量瓶中,并用去离子水定容。
准备标准曲线1.取一系列不同浓度的亚铁标准溶液,分别加入邻菲罗啉溶液和硫酸。
2.将上述溶液转移到容量瓶中,并用去离子水定容。
3.在分光光度计上设置波长为510 nm。
4.分别测量每个标准溶液的吸光度,并记录结果。
测定样品1.将经过预处理的样品溶液转移到比色皿中。
2.在分光光度计上设置波长为510 nm。
3.测量样品溶液的吸光度,并记录结果。
绘制标准曲线与计算全铁含量1.将标准溶液的浓度与吸光度值绘制成图表,并进行线性拟合。
2.根据拟合曲线,计算样品中的全铁含量。
数据分析与结果展示标准曲线以亚铁标准溶液的浓度为横坐标,吸光度值为纵坐标绘制标准曲线,根据曲线方程可以计算出样品中的全铁含量。
亚铁标准溶液浓度(M)吸光度0.001 0.2140.002 0.4260.003 0.6330.004 0.8410.005 1.055样品测定结果测得样品的吸光度为0.725。
第8章 吸光光度法思考题参考答案1. 与化学分析法相比,吸光光度法的主要特点是什么?答:吸光光度法主要用于测定试样中的微量组分,与化学分析法相比具有以下特点: (1) 灵敏度高。
常可不经富集用于测定质量分数为210-~510-的微量组分。
(2) 准确度虽无化学分析法高,但符合微量分析的要求。
一般目视比色法的相对误差为5%~l0%,分光光度法为2%~5%。
(3) 应用广泛。
几乎所有的无机离子和许多有机化合物都可以直接或间接地用分光光度法进行测定。
(4) 仪器简单,操作方便,快速。
有时可不经分离直接进行比色或分光光度测定。
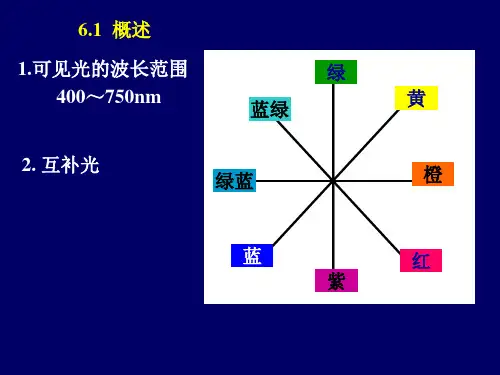
2. 何谓单色光、复合光、互补光、可见光?答:将仅具有某一波长的光称为单色光; 由不同波长的光组成的光称为复合光;如果把两种适当颜色的单色光按一定强度比例混合能得到白光。
那么这两种单色光称为互补光;人眼能感觉到的光的波长大约在400~750 nm 之间,称为可见光。
3. 朗伯-比耳定律的物理意义是什么?什么是透光度?什么是吸光度?二者之间的关系是什么?答:物理意义为:当一束平行的单色光通过单一均匀的、非散射的吸光物质溶液时,溶液的吸光度A 与吸光物质的浓度和光通过的液层厚度的乘积成正比。
透过光强度I 与入射光强度I 0之比称为透光度,用T 表示。
即 T = I / I 0 。
lg (I 0/I ) 表明了溶液对光的吸收程度,定义为吸光度。
透光度与吸光度的关系是A = – lg T4. 摩尔吸收系数的物理意义是什么?其大小和哪些因素有关?答:摩尔吸收系数是吸光物质在特定波长和溶剂情况下的一个特征常数,在数值上等于浓度为1mol·L -1吸光物质在1cm 光程中的吸光度,是物质吸光能力的量度。
它可以作为定性鉴定的参数,也可以估量定量方法的灵敏度。
值越大,说明有色物质对入射光的吸收能力越强,显色反应的灵敏度高。
其大小与入射光波长、溶液的性质以及温度等因素有关,而与溶液的浓度及液层厚度无关。
一、单选题1. UV-Vis 吸收光谱是由( )A. 最内层原子轨道上的电子跃迁产生B. 原子最外层电子跃迁产生C. 分子价电子能级跃迁产生D. 分子振动和转动产生2. 下列有关有机化合物外层电子能级跃迁的哪种表述是正确的( )A. σ→σ*有最低的能量B. π→π*最低的能量C. n →π*有最低的能量D. n→σ*可产生波长最大的吸收3. 某化合物在己烷和乙醇中的λmax 分别为305和307 nm ,则该化合物的跃迁是下列哪种跃迁( )A. π→π*B. n →π*C. n →σ*D. σ→σ*4. 下列哪种化合物中不存在π→π*跃迁( )A. 乙烯B. 丙酮C. 苯乙炔D. 乙醇5. 当pH 由酸性变为碱性,苯酚的最大吸波长将发生何种变化( )A. 红移B. 蓝移C. 不变D. 不能确定6. 分光光度计中控制波长纯度的元件是( )A. 棱镜B. 光栅C. 狭缝D. 光栅+狭缝7. 某浓度待测物的透射比为T ,若其它条件不变,浓度增大一倍后的透射比应为( )A. 2TB. 2/TC. T 2D. T8. 在符合朗伯-比尔定律的范围内,有色物质的浓度、最大吸收波长和吸光度三者的关系为( )A. 增大、增大、增大B. 减小、不变、减小C. 减小、增大、减小D. 增大、减小、不变9. 指出下列哪种因素不会产生对朗伯-比尔定律的偏差( )A. 溶质的离解作用B. 杂散光进入检测器C. 溶液的折射指数增加D. 改变吸收光程长度10. 下列哪种化合物不太适合作为UV 光谱测定时的溶剂( )A. 环己烷B. 甲醇C. 乙腈D. 甲苯11. 质量相同的A 、B 物质(摩尔质量M A >M B ),经过显色测量后所得吸光度相等,则它们的摩尔吸光系数的关系为( )A. εA >εBB. εA <εBC. εA =εBD. εA <1/2εB12. 在符合朗伯-比尔定律的范围内,以下说法正确的是( )A. 溶液透射比T 越大,说明对光的吸收越强B. 透射比T 与浓度成正比C. 摩尔吸光系数随λ改变,但与浓度无关D. 摩尔吸光系数随λ和浓度而改变13.以下说法正确的是()A. 透射比与浓度呈直线关系B. 助色团可使生色团的吸收波长红移C. 比色法测定FeSCN+时,应选用红色滤光片D. 玻璃棱镜适合紫外光区14.在吸收光谱曲线中,吸光度的最大值是偶数阶导数光谱曲线的()A. 极大值B. 极小值C. 零D. 极大或极小值15. 双波长分光光度计和单波长分光光度计的主要区别在于()A. 光源个数B. 检测器个数C. 吸收池个数D. 使用单色器个数16. 双波长分光光度计的输出信号是()A. 试样吸收与参比吸收之差B. 试样在λ1与λ2处的吸收之差C. 试样在λ1与λ2处的吸收之和D. 试样在λ1和参比在λ2处的吸收之差17. 示差分光光度法与普通分光光度法的不同之处是()A. 标准溶液不同 D. 所选测定波长不同B. 参比溶液不同 D. 使用的光程不同18. 用普通分光光度法测定标液c1的透射比为20%,试液透过率为12%;若以示差光度法测定,以c1为参比,则试液的透射比透光度为()A. 40%B. 50%C. 60%D. 70%19. 某分光光度计的测量误差∆T=0.01,在透射比T=70%时,由测量引起的浓度相对误差为()A. 2%B. 8%C. 6%D. 4%20. 邻二氮菲法测定铁时,应在加入盐酸羟胺摇匀后应放置至少2分钟后再加显色剂邻二氮菲,若放置时间不足,则分析结果很可能会()A. 无影响B. 不一定C. 偏低D. 偏高21. 邻二氮菲法测定水中微量铁含量的分析步骤是()A. 还原-发色-调节pH-比色-酸化B. 酸化-还原-调节pH-发色-比色C. 发色-酸化-还原-调节pH-比色D. 调节pH-发色-还原-酸化-比色22. 在吸光光度法中,有时会出现标准曲线不通过原点的情况,下列哪种情况不会引起这一现象()A. 吸收池位置放置不当B. 参比溶液选择不当C. 吸收池光学玻璃不洁净D. 显色反应灵敏度较低23.用紫外吸收光谱区别共轭烯烃和α,β-不饱和酮可根据下列哪种吸收带出现与否来判断()A. K带 B. R带 C. E带 D. B带24. 下列四种化合物λmax的顺序为()(a)CH CH CH CH2(b)CH CH2C2H5(c)CH CH CH CH2(d)CH CH2C2H5A. b>c>d>aB. a>d>c>bC. b>d>c>aD. a>c>d>b25. 下列关于荧光发射光谱的叙述中正确的是()A. 发射与激发光谱在任何情况下都是镜像关系B. 发射光谱的形状与激发波长无关C. 发射光谱位于激发光谱的左侧D. 发射光谱就是分子的吸收光谱26. 用波长300 nm的入射光激发硫酸奎宁的稀硫酸溶液时,所产生的300 nm的发射光是()A. 荧光B. 磷光C. Reyleigh散射D. 无法判断27.分子荧光分光光度计常用的光源是()A. 空心阴极灯B. 氙灯C. 氘灯D. 碳硅棒28. 荧光分析法是通过测定那种类型的光而达到对物质定性或定量分析的目的()A. 激发光B. 磷光C. 发射光D. 散射光29. 下列是化学发光仪必须的元件是()A. 光电倍增管B. 光栅C. 氘灯D. 氙灯30. 荧光物质,随溶液的温度降低,其荧光量子率将()A. 减小B. 增大C. 不变D. 不能确定31. 极性溶剂会使被测物质的UV-Vis吸收光谱()A. 消失B. 精细结构更明显C. 发生位移D. 分裂32. 分子的UV-Vis吸收光谱为带状光谱,其原因是()A. 分子中价电子运动的离域性质B. 分子中价电子能级的相互作用C. 分子振动能级的跃迁伴随着转动能级的跃迁D. 分子电极能级的跃迁伴随着振动、转动能级的跃迁33. 某化合物分子式为C5H8O,其UV光谱上有两个吸收带:λmax=204 nm(εmax=9750);λmax=314 nm (εmax=38)。
邻菲罗啉示差分光光度法测定铁矿石中全铁含量
邻菲罗啉示差分光光度法是一种常用于测定铁矿石中全铁含量的方法。
该方法基于邻菲罗啉与铁离子之间的络合反应,通过测定络合物的光
学旋光度差来计算铁离子的含量。
具体操作步骤如下:
1. 样品制备:将铁矿石样品粉碎至均匀细粉末,取约0.5克样品加入100毫升锥形瓶中,加入10毫升盐酸和10毫升硝酸,加热至沸腾,
使样品完全溶解,冷却至室温。
2. 邻菲罗啉试剂制备:取适量邻菲罗啉试剂加入100毫升去离子水中,摇匀,制备成0.01mol/L的邻菲罗啉试剂。
3. 样品处理:取10毫升样品溶液加入50毫升锥形瓶中,加入10毫
升邻菲罗啉试剂,摇匀,静置5分钟。
4. 光度测定:将样品转移到比色皿中,用去离子水稀释至50毫升,用紫外-可见分光光度计测定在400纳米处的吸光度值。
5. 示差测定:将样品转移到示差皿中,用示差光度计测定在546纳米
处的旋光度差。
6. 计算全铁含量:根据标准曲线计算出样品中的铁离子含量,再乘以
样品中全铁的相对含量系数,即可计算出样品中的全铁含量。
邻菲罗啉示差分光光度法具有灵敏度高、准确度高、重现性好等优点,适用于测定铁矿石中全铁含量。
但需要注意的是,样品制备过程中要
避免铁离子的污染,同时要注意邻菲罗啉试剂的保存和使用,以保证
测定结果的准确性。
二、原子吸收及荧光光谱法练习题一、选择题1. 在原子吸收光谱分析中,若组分较复杂且被测组分含量较低时,为了简便准确地进行分析,最好选择何种方法进行分析? ( )(1) 工作曲线法(2) 内标法(3) 标准加入法(4) 间接测定法2. 原子吸收测定时,调节燃烧器高度的目的是( )(1) 控制燃烧速度(2) 增加燃气和助燃气预混时间(3) 提高试样雾化效率(4) 选择合适的吸收区域3. 采用调制的空心阴极灯主要是为了( )(1)延长灯寿命(2) 克服火焰中的干扰谱线(3) 防止光源谱线变宽(4) 扣除背景吸收4. 用有机溶剂萃取一元素,并直接进行原子吸收测定时,操作中应注意( )(1) 回火现象(2) 熄火问题(3) 适当减少燃气量(4) 加大助燃比中燃气量5. 可见光的能量应为( )(1) 1.24×104~1.24×106eV (2) 1.43×102~71 eV (3) 6.2 ~3.1 eV (4)3.1 ~1.65 eV6. 在原子吸收分析中,如灯中有连续背景发射,宜采用( )(1)减小狭缝(2) 用纯度较高的单元素灯(3) 另选测定波长(4) 用化学方法分离7. 欲测某有色物的吸收光谱,下列方法中可以采用的是( )(1) 比色法(2) 示差分光光度法(3) 光度滴定法(4) 分光光度法8. X 荧光是由下列哪种跃迁产生的?( )(1) 辐射能使气态基态原子外层电子产生跃迁(2) 辐射能使气态基态原子内层电子产生跃迁(3) 辐射原子最内层电子产生跃迁(4) 辐射能使分子外层电子从第一激发态的最低振动能级跃迁至基态9. 为了消除火焰原子化器中待测元素的发射光谱干扰应采用下列哪种措施?( )(1) 直流放大(2) 交流放大(3) 扣除背景(4) 减小灯电流10. 下列哪种原子荧光是反斯托克斯荧光?( )(1) 铬原子吸收359.35nm,发射357.87nm(2) 铅原子吸收283.31nm,发射283.31nm(3) 铅原子吸收283.31nm,发射405.78nm(4) 铊原子吸收377.55nm,发射535.05nm11. 下列哪种原子荧光是反斯托克斯荧光?( )(1) 铬原子吸收359.35nm,发射357.87nm(2) 铅原子吸收283.31nm,发射283.31nm(3) 铅原子吸收283.31nm,发射405.78nm(4) 铊原子吸收377.55nm,发射535.05nm12. 由原子无规则的热运动所产生的谱线变宽称为:( )(1) 自然变度(2) 斯塔克变宽(3) 劳伦茨变宽(4) 多普勒变宽13. 原子化器的主要作用是:( )(1) 将试样中待测元素转化为基态原子(2) 将试样中待测元素转化为激发态原子(3) 将试样中待测元素转化为中性分子(4) 将试样中待测元素转化为离子14 .在原子吸收分光光度计中,目前常用的光源是( )(1) 火焰(2) 空心阴极灯(3) 氙灯(4) 交流电弧15. 质量浓度为0.1 g/mL 的Mg在某原子吸收光谱仪上测定时,得吸光度为0.178,结果表明该元素在此条件下的1% 吸收灵敏度为( )(1) 0.0000783(2) 0.562(3) 0.00244(4) 0.0078316. 已知原子吸收光谱计狭缝宽度为0.5mm 时,狭缝的光谱通带为1.3nm,所以该仪器的单色器的倒线色散率为:( )17. 某台原子吸收分光光度计,其线色散率为每纳米1.0 mm,用它测定某种金属离子,已知该离子的灵敏线为403.3nm,附近还有一条403.5nm 的谱线,为了不干扰该金属离子的测定,仪器的狭缝宽度达:( ) (1) < 0.5mm(2) < 0.2mm(3) < 1mm(4) < 5mm18. 原子吸收光谱分析过程中,被测元素的相对原子质量愈小,温度愈高,则谱线的热变宽将是( )(1) 愈严重(2) 愈不严重(3) 基本不变(4) 不变19. 空心阴极灯的主要操作参数是( )(1) 灯电流(2) 灯电压(3) 阴极温度(4) 内充气体的压力20. 在原子吸收分析法中, 被测定元素的灵敏度、准确度在很大程度上取决于( )(1) 空心阴极灯(2) 火焰(3) 原子化系统(4) 分光系统二、填空题1. 在原子吸收分析中,为了定量的描述谱线的轮廓,习惯上引入了两个物理量,即__和___ 。
一、填空题1.紫外-可见吸收光谱是由分子的振动和转动能级跃迁产生的.红外吸收光谱是由分子的振动能级跃迁产生的。
2.红外吸收光谱法测定固体样品的处理方法有研糊法、 KBr压片法和薄膜法。
3.原子吸收分析中.对同一类型的火焰按其燃气和助燃气的比例不同可分为化学计量火焰、富燃火焰和贫燃火焰三种类型。
4.在液-液分配色谱中.对于亲水固定液采用疏水性流动相.正相色谱法的流动相的极性小于固定液的极性(填大于.或小于).极性小的组分先流出.极性大的组分后流出。
(填先或后)5.反相色谱法的流动相的极性大于固定液的极性(填大于.或小于).极性小的组分后流出.极性大的组分先流出。
(填先或后)6.示差光度法的测定方法与普通分光光度法相同.只是调100% T和调0%T的方式有所不同。
7.在相同条件下配制样品溶液和标准溶液.其浓度分别为c x(待测)和c s.在最佳波长λ最佳处测得两者的吸光度分别为A x和A s.则样品浓度c x可表示为 C X=[A X/(As-A X)]*C0。
8.盐桥的作用是保持溶液电中性.沟通回路。
9.总离子强度调节剂(TISAB)的作用:保持较大且稳定的离子强度.使活度系数恒定、维持溶液在适宜的pH范围内.满足离子电极的要求、掩蔽干扰离子。
10.线性的振动自由度可表示为 3n-5 .CO2分子的振动自由度为 4 。
11.非线性的振动自由度可表示为 3n-6 .H2O分子的振动自由度为 3 。
12.电极极化包括浓差极化和电化学极化。
13.增强溶剂的极性使π→π*跃迁红移和使n→π*跃迁蓝移14.无机化合物分子的紫外-可见光谱是由电荷转移跃迁和配位体场跃迁产生。
15.化学位移是由于氢核具有不同的屏蔽常数σ.产生核磁共振现象时.引起外磁场或共振频率的移动的现象。
16.气相色谱法的两个基本理论为塔板理论和速率理论。
17.采用紫外可见分光光度计测定试样中组分含量.所使用的显色剂和试剂无吸收.应选择纯溶剂或水(溶剂空白)作参比溶液。