急性、慢性和亚慢性毒性实验(20201111083305)
- 格式:docx
- 大小:10.94 KB
- 文档页数:3


毒理学实验技术总结毒理学作为一门研究外源性化学物质对生物体产生有害作用的学科,其实验技术对于评估化学物质的毒性、安全性以及环境风险具有至关重要的意义。
在这篇文章中,我们将对常见的毒理学实验技术进行总结和介绍。
一、急性毒性实验急性毒性实验是评估化学物质在短时间内对生物体产生毒性作用的重要方法。
实验通常采用经口、经皮、吸入等途径给予受试物,观察受试动物在 24 小时至 14 天内的中毒症状和死亡情况。
通过计算半数致死剂量(LD50)或半数致死浓度(LC50)来衡量化学物质的急性毒性强度。
急性毒性实验可以初步了解化学物质的毒性特征,为后续的慢性毒性实验和风险评估提供基础数据。
在进行急性毒性实验时,需要严格控制实验条件,如受试动物的种类、年龄、体重、性别等,以及受试物的给予剂量和方式。
同时,要密切观察受试动物的行为、生理和病理变化,及时记录和处理实验数据。
二、慢性毒性实验慢性毒性实验是研究化学物质长期低剂量暴露对生物体产生的毒性作用。
实验周期通常为数月至数年,旨在观察受试动物在长期接触受试物后的生长发育、生殖功能、免疫功能、致癌性等方面的变化。
慢性毒性实验可以更全面地评估化学物质的潜在危害,为制定安全标准和防护措施提供依据。
慢性毒性实验的设计和实施较为复杂,需要考虑受试物的蓄积性、代谢途径、靶器官等因素。
实验过程中要定期对受试动物进行体检、血液生化指标检测、组织病理学检查等,以评估受试物对各个系统和器官的影响。
三、遗传毒性实验遗传毒性实验用于检测化学物质对生物体遗传物质(DNA)的损伤作用。
常见的遗传毒性实验方法包括基因突变实验(如 Ames 试验)、染色体畸变实验(如微核试验)和 DNA 损伤修复实验等。
这些实验可以帮助评估化学物质的致癌性和致畸性风险。
Ames 试验是一种常用的基因突变实验,通过检测受试物对鼠伤寒沙门氏菌的回复突变率来判断其致突变性。
微核试验则是通过观察细胞中的微核形成情况来评估染色体损伤程度。


仔泻康口服液的急性毒性和亚慢性毒性试验研究雒利蓉;王慧;崔东安;王富河;王胜义【摘要】试验旨在通过小鼠急性毒性试验和大鼠亚慢性毒性试验对仔泻康口服液进行安全性评价,为临床安全用药提供理论依据.在急性毒性试验中,采用最大给药剂量对36只昆明小鼠进行灌胃给药.在亚慢性毒性试验中,将80只大鼠,随机均分成高、中、低剂量组和对照组,高、中、低剂量组分别按24、12和6 g/kg体重灌胃给药,对照组给予等体积生理盐水,连续给药30 d,停药后称量大鼠体重、检测血常规指标、血液生化指标、计算脏器指数并观察组织病理变化等.结果显示,在急性毒性试验中,各剂量组均无小鼠死亡,无法计算LD50,最大耐受量试验也无死亡情况;在亚慢性毒性试验中,该口服液对大鼠生长发育没有影响;经剖检,仅高剂量组可见中央静脉远端的肝细胞有不同程度的肿大,但未见坏死和炎性反应,其他各剂量组的实质器官均未发现异常变化;各剂量组血液学指标、血液生化指标和脏器指数均在正常范围内,与对照组相比均无显著差异(P>0.05).结果表明,根据外源化学物急性毒性分级(WHO)标准,该制剂属于无毒物质,安全性较高,在合理剂量下,临床使用仔泻康口服液是安全的.【期刊名称】《中国畜牧兽医》【年(卷),期】2018(045)009【总页数】9页(P2582-2590)【关键词】仔泻康口服液;急性毒性试验;亚慢性毒性试验【作者】雒利蓉;王慧;崔东安;王富河;王胜义【作者单位】新疆农业大学动物医学院,乌鲁木齐830000;中国农业科学院兰州畜牧与兽药研究所,农业部兽药创制重点实验室,兰州730000;中国农业科学院兰州畜牧与兽药研究所,农业部兽药创制重点实验室,兰州730000;中国农业科学院兰州畜牧与兽药研究所,农业部兽药创制重点实验室,兰州730000;中国农业科学院兰州畜牧与兽药研究所,农业部兽药创制重点实验室,兰州730000;中国农业科学院兰州畜牧与兽药研究所,农业部兽药创制重点实验室,兰州730000【正文语种】中文【中图分类】S853.76仔猪腹泻是困扰全球养猪业的重大疾病之一,给养猪业带来了巨大的经济损失。



急性、慢性和亚慢性毒性实验急性毒性试验(一)经典的急性致死性毒性试验通过试验得到化合物引起动物死亡的剂量一反应关系并求得LD50 ( LC50)1、实验动物常用的实验动物是小鼠或大鼠。
一般受试动物应是雌、雄各半;若雌、雄动物对待测化学物毒性的敏感程度有明差异,则应分别求出各自的LD50;如果试验是为畸形试验做剂量准备,也可仅做雌性动物的LD50试验。
小动物每组10只,狗等大动物可每组6只。
2、染毒剂量设计首先要了解化学毒物的结构式、分子量、常温常压下的状态、纯度、杂质成分与含量、溶解度、挥发度、PH等理化性质。
对于新的受试化学物,找出与受试化学毒物结构与理化性质近似的化学物的毒性资料,并以文献资料中相同的动物种系和相同接触途径所测得的LD50(LC50)值作为受试化学物的预期毒性中值,先用少量动物,以较大的剂量间隔(一般按几何级数)染毒,找出找出10%~90%(或0% ~100%)的致死剂量范围,然后在这个剂量范围内设几个剂量组。
改良寇氏法最好设5个剂量组,每组10只动物,雌雄各半,剂量组要求以等比级数设置。
根据以下公式计算出剂量分组:i=(lgLD90-lgLD10) / (n-1) 或:i=(lgLD100-lgLD0) / (n-1)式中i为组距(相邻的两个剂量组对数剂量之差);n 为设计的剂量组数。
有的毒性较小,此时可不再求其LD50,而应进行限量试验。
在用大鼠或小鼠进行试验时,一般用20只动物,雌雄各半。
单次染毒剂量一般限定为5g/kg (体重),对于食品毒理学试验,限量要求为15g/kg (体重)。
如果实验动物无死亡或仅有个别动物死亡(死亡率低于50%), 则可得出LD50大于限量的结论。
3、观察染毒后一般要求观察14天,依据14天内动物的总死亡情况计算LD50。
在实际工作中,依据受试物有关测试规程要求确定观察期的长短。
观察内容包括:(1)动物死亡情况:包括动物死亡数及各自的死亡时间。

毒理学实验技术总结毒理学作为一门研究外源性化学物质对生物体产生有害作用的学科,其实验技术的发展对于评估化学物质的安全性和风险至关重要。
以下是对常见毒理学实验技术的总结。
一、急性毒性实验急性毒性实验是评估化学物质在短时间内(通常 24 小时至 2 周)对生物体造成的毒性效应。
实验动物通常选用小鼠或大鼠,通过不同的给药途径(如经口、经皮、吸入等)给予一定剂量的受试物。
观察指标包括动物的死亡情况、临床症状(如行为异常、呼吸困难等)、体重变化等。
根据实验结果,可以计算出半数致死剂量(LD50)或半数致死浓度(LC50),这是衡量化学物质急性毒性的重要指标。
二、亚急性和亚慢性毒性实验亚急性毒性实验的时间通常为 28 天至 90 天,亚慢性毒性实验则为90 天至 180 天。
这些实验旨在观察化学物质在较长时间内低剂量暴露下对生物体的潜在毒性。
除了观察一般症状和体重变化外,还会检测血液生化指标(如肝功能、肾功能指标)、组织病理学变化(如肝脏、肾脏、心脏等器官的组织形态改变)等。
三、慢性毒性实验慢性毒性实验的周期较长,一般为 1 年以上,甚至可能持续动物的整个生命周期。
这种实验更能反映化学物质长期暴露对生物体的影响,包括致癌性、致畸性、致突变性等。
检测指标与亚急性和亚慢性毒性实验类似,但更加注重对肿瘤发生、生殖系统影响以及遗传物质损伤的评估。
四、遗传毒性实验遗传毒性实验用于检测化学物质对生物体遗传物质(DNA)的损伤作用。
常见的方法包括:1、细菌回复突变试验(Ames 试验):通过观察受试物是否能引起细菌基因突变来评估其遗传毒性。
2、染色体畸变试验:观察细胞染色体结构和数量的变化。
3、微核试验:检测细胞中微核的形成,反映染色体的损伤。
五、生殖毒性实验生殖毒性实验主要研究化学物质对生殖系统的影响,包括对生殖器官、生殖细胞、胚胎发育等方面的作用。
实验分为三段:1、Ⅰ段:生育力与早期胚胎发育毒性实验,评估对雌雄动物生殖能力和早期胚胎发育的影响。
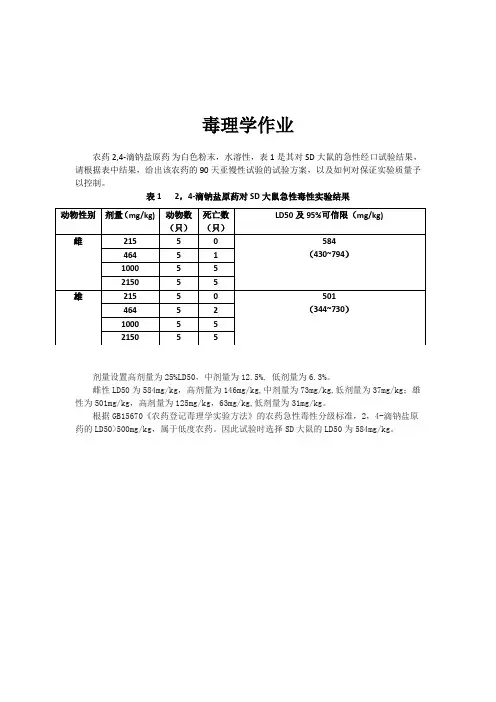
毒理学作业农药2,4-滴钠盐原药为白色粉末,水溶性,表1是其对SD大鼠的急性经口试验结果,请根据表中结果,给出该农药的90天亚慢性试验的试验方案,以及如何对保证实验质量予以控制。
表1 2,4-滴钠盐原药对SD大鼠急性毒性实验结果剂量设置高剂量为25%LD50,中剂量为12.5%, 低剂量为6.3%。
雌性LD50为584mg/kg,高剂量为146mg/kg,中剂量为73mg/kg,低剂量为37mg/kg;雄性为501mg/kg,高剂量为125mg/kg,63mg/kg,低剂量为31mg/kg。
根据GB15670《农药登记毒理学实验方法》的农药急性毒性分级标准,2,4-滴钠盐原药的LD50>500mg/kg,属于低度农药。
因此试验时选择SD大鼠的LD50为584mg/kg。
农药2,4-滴钠盐原药SD大鼠亚慢性毒性试验目的;研究喂饲农药2,4-滴钠盐原药对大鼠的亚慢性毒性。
方法:取初断乳 SD大鼠80只,雌雄各半按照体重随机分为4组。
将2,4-滴钠盐原药按146、73、37mg/kg mg/kg剂量分别拌入饲料内经口喂饲染毒90d。
观察:大鼠外观体征、体质量、进食情况等。
在实验中期和末期采血检测检测血液学。
试验末期检测血生化指标以及尿常规检查。
实验结束时处死实验动物,计算脏器指数,并对主要脏器进行病理组织学观察。
1 材料和方法1.1 受试物农药2,4-滴钠盐原药,白色粉末,水溶性,由某地某农药公司提供。
SPF级初断乳大鼠80只,雌雄各半,体质量50~100 g,由XXX实验动物研究所繁育场提供,动物合格证号为医动字第XX-XXXX号。
1.2 饲养与管理SPF 环境条件下,同组同性别两只一笼喂养,自由进食和饮水。
环境温度 21~25℃,相对湿度 40%~60%。
严格控制昼夜交替。
1.3实验方法试验前将雌、雄大鼠各半按体重随机分为3个剂量组和1个对照组,每组20只,将2,4-滴钠盐原药按146、73、37mg/kg mg/kg剂量分别均匀混入饲料中制成颗粒饲料辐照灭菌后分别供高、中、低剂量组动物食用,连续每日一次喂养90d;对照组给予不加受试物的正常饲料。

波棱瓜子总木脂素的急性和亚慢性毒性试验目录一、内容简述 (2)1.1 研究背景与意义 (2)1.2 国内外研究现状 (3)1.3 研究目的与内容 (4)二、材料与方法 (5)2.1 实验材料 (6)2.2 实验仪器与试剂 (7)2.3 实验设计 (7)2.4 样本制备与剂量设置 (8)2.5 数据采集与分析方法 (9)三、急性毒性试验结果与分析 (10)3.1 实验动物与剂量选择 (11)3.2 急性毒性症状观察 (12)3.3 生物毒性评价指标 (13)3.4 急性毒性试验结论 (13)四、亚慢性毒性试验结果与分析 (14)4.1 实验动物与剂量选择 (15)4.2 亚慢性毒性症状观察 (16)4.3 亚慢性毒性生理指标变化 (17)4.4 亚慢性毒性组织器官损伤评估 (17)4.5 亚慢性毒性试验结论 (18)五、波棱瓜子总木脂素的安全性评价 (18)5.1 急性和亚慢性毒性综合分析 (19)5.2 安全性评价标准与方法 (20)5.3 波棱瓜子总木脂素的安全性评级 (21)5.4 安全性应用建议 (21)六、结论与展望 (22)6.1 研究成果总结 (23)6.2 存在问题与不足 (24)6.3 未来研究方向与应用前景 (25)一、内容简述本试验旨在研究波棱瓜子总木脂素(total oleanolic acid,TOA)的急性和亚慢性毒性。
通过观察不同剂量下波棱瓜子提取物对实验小鼠的生长、行为、器官功能以及血液生化指标的影响,评价TOA的毒性水平。
本试验采用3种不同剂量和200 mgkg)的波棱瓜子提取物,分别进行急性和亚慢性毒性试验。
在试验过程中,对各组小鼠进行定期观察,记录生长情况、活动能力、食欲、体重变化等指标,并对主要器官如肝脏、肾脏、心脏、肺等进行病理学检查。
测定血液生化指标如血清谷丙转氨酶(ALT)、血清谷草转氨酶(AST)、肌酐(Cr)、尿素氮(BUN)等,以评估TOA对小鼠的肝肾功能的影响。

急性毒性:实验动物一次接触或者24小时内多次接触某一化合物而引起的毒效应,甚至死亡。
亚慢性毒性:人或者动物连续接触较长时间、较大剂量的外源性化学物质所出现的中毒效应。
接触时间介于单次染毒和10%动物寿命的范围。
没有严格的界限,通常为1-6个月。
慢性毒性:指人或者实验动物长期(甚至终生)反复接触低剂量的外源化合物所出现的毒性效应。
一般是2年。
对于大鼠相当于终身,兔相当于生命的36%,狗20%,猴13%。
《毒理学基础第5版》90天亚慢性毒性试验来判断慢性毒性效应基本得到认可。
瑞鲍迪甙A急性毒性和亚慢性毒性试验李楠;王建明;周泽伟;郑玲敏;余峥嵘;张雨梅【期刊名称】《安徽农业科学》【年(卷),期】2015(000)002【摘要】[目的]为评价瑞鲍迪甙A作为饲料甜味剂的安全性,进行了瑞鲍迪甙A大鼠、小鼠的急性毒性及亚慢性毒性试验.[方法]急性毒性试验采用灌胃给予;亚慢性毒性试验中,瑞鲍迪甙A以20、4和l g/kg拌料给予大鼠90d,每周称量大鼠体重和饲料消耗,并在喂养45和90d时剖检,分别进行血液细胞学和血液生化指标检测,计算主要脏器系数以及进行相应的组织病理学检查.[结果]瑞鲍迪甙A对大、小鼠的经口LD50分别大于34.0和45.0 g/kg b.w.;亚慢性毒性试验各剂量组大鼠的采食、体重、脏器系数、血液细胞学及血液生化指标、大体解剖及组织病理学检查结果与正常对照组比较无明显差异.[结论]瑞鲍迪甙A属于实际无毒级别物质,亚慢性毒性试验对大鼠无明显有害作用.【总页数】4页(P103-105,177)【作者】李楠;王建明;周泽伟;郑玲敏;余峥嵘;张雨梅【作者单位】扬州大学兽医学院,江苏扬州225009;扬州大学兽医学院,江苏扬州225009;江苏省动物重要疫病与人兽共患病防控协同创新中心,江苏扬州225009;扬州大学兽医学院,江苏扬州225009;扬州大学兽医学院,江苏扬州225009;扬州大学兽医学院,江苏扬州225009;扬州大学兽医学院,江苏扬州225009;江苏省动物重要疫病与人兽共患病防控协同创新中心,江苏扬州225009【正文语种】中文【中图分类】S567【相关文献】1.瑞鲍迪甙A对大鼠的致畸作用 [J], 王雨晶;鲁倩倩;余峥嵘;郑玲敏;周泽伟;李楠;张雨梅2.速康解毒口服液对小白鼠的急性毒性试验和亚慢性毒性试验 [J], 权晓弟;郝宝成;薛慧文;王学红;刘建枝;王保海;卢超;梁剑平3.几种常用消毒剂对杂色鲍幼鲍的急性毒性试验 [J], 柯浩;彭绪运;陈毕生4.应激宁小鼠急性毒性试验及亚慢性毒性试验 [J], 肖飞;吴艳丽5.澳新批准瑞鲍迪甙M作为甜味剂用于食品 [J],因版权原因,仅展示原文概要,查看原文内容请购买。
湖南农业大学学报(自然科学版)2020, 46(3):358–363. DOI:10.13331/ki.jhau.2020.03.016Journal of Hunan Agricultural University (Natural Sciences)引用格式:闫志强,陈春林,付文贵,郑华,翟少钦.女黄颗粒对小鼠的急性毒性和大鼠的亚慢性毒性试验[J].湖南农业大学学报(自然科学版),2020,46(3):358–363.YAN Z Q, CHEN C L, FU W G, ZHENG H, ZHAI S Q. Tests of the acute toxicity in mice and subchronic toxicityin rats of Nühuang granules[J].Journal of Hunan Agricultural University(Natural Sciences), 2020, 46(3): 358–363.投稿网址:女黄颗粒对小鼠的急性毒性和大鼠的亚慢性毒性试验闫志强,陈春林,付文贵,郑华,翟少钦*(重庆市畜牧科学院,重庆 402460)摘 要:依据《兽药研究技术指导原则汇编》中“兽药急性毒性试验指导原则”和“兽药30天和90天喂养试验指导原则”,研究中药女黄颗粒对小鼠的急性毒性和对大鼠的亚慢性毒性。
药物组以16、4、1、0.5 g/kg的剂量一次性灌服女黄颗粒药液,观察7 d并记录小鼠的表现及死亡情况,测定女黄颗粒的半数致死量(LD50);以90 g/kg 的剂量灌服女黄颗粒药液,观察14 d并记录小鼠的反应及死亡情况,测定女黄颗粒的最大给药剂量;药物组以18、6、2 g/kg的剂量连续灌服女黄颗粒药液30 d,期间观察大鼠的临床表现和体质量变化,试验结束时检测其血液学、血液生化指标和组织病理学指标,确定其亚慢性毒性。
结果表明:急性毒性试验中,女黄颗粒各剂量组均未发现小鼠死亡,无法测出女黄颗粒的LD50;最大给药量试验期间,小鼠临床表现正常,未发现死亡,女黄颗粒的最大给药量为90 g/kg;亚慢性毒性试验期间,大鼠精神状态良好,血液学、血液生化指标均在正常范围内,组织病理学检查未发现病变。
急性毒性试验
(-)经典的急性致死性毒性试验
通过试验得到化合物引起动物死亡的剂量一反应关系并求得LD50 ( LC50)
1、实验动物
常用的实验动物是小鼠或大鼠。
一般受试动物应是雌、雄各半;若雌、雄动物对待测化学物毒性的敏感程度有明差异,则应分别求出各自的LD50;如果试验是为畸形试验做剂量准备,也可仅做雌性动物的LD50试验。
小动物每组10只,狗等大动物可每组6只。
2、染毒剂量设计
首先要了解化学毒物的结构式、分子量、常温常压下的状态、纯度、杂质成分与含量、溶解度、挥发度、PH等理化性质。
对于新的受试化学物,找出与受试化学毒物结构与理化性质近似的化学物的毒性资料,并以文献资料中相同的动物种系和相同接触途径所测得的LD50(LC50)值作为受试化学物的预期毒性中值,先用少量动物,以较大的剂量间隔(一般按几何级数)染毒,找出找出10%、90% (或0%~100%)的致死剂量范围,然后在这个剂量范围内设几个剂量组。
改良寇氏法最好设5个剂量组,每组10只动物,雌雄各半,剂量组要求以等比级数设置。
根据以下公式计算出剂量分组:
i=(lgLD90-lgLD10) / (n-1)或:i=(lgLD100-lgLD0)/ (n-1) 式中i为组距(相邻的两个剂量组对数剂量之差);
n为设计的剂量组数。
有的毒性较小,此时可不再求其LD50,而应进行限量试验。
在用大鼠或小鼠进行试验时,一般用20只动物,雌雄各半。
单次染毒剂量一般限定为5g/kg (体重),对于食品毒理学试验,限量要求为15g/kg (体重)。
如果实验动物无死亡或仅有个别动物死亡(死亡率低于50%), 则可得出LD50大于限量的结论。
3、观察
染毒后一般要求观察14天,依据14天内动物的总死亡情况计算LD50o在实际工作中,依据受试物有关测试规程要求确定观察期的长短。
观察内容包括:
(1)动物死亡情况:包括动物死亡数及各自的死亡时间。
(2)动物体重:于染毒前、染毒后每周和死亡时测定体重。
(3)中毒反应症状:临床观察每天至少一次,观察皮肤、被毛、眼睛和粘膜改变,呼吸、
循环、自主和中枢神经系统以及四肢活动和行为方式的变化等,特别要注意有无震颤、
惊厥、腹泻、嗜睡等现象。
神经毒性:惊厥、共济失调和死亡。
植物神经兴奋:腹泻或
竖毛。
(4)病理学检查:解剖进行尸检,观察各器官有无改变,对肉眼观察有变化的脏器需进
行组织病理学检查。
4、LD50计算
(1)霍恩氏法
(2)简化寇氏法
M=X - i (S p - 0. 5)
式中:m―logLD50,
X—最高剂量组剂量对数值,
p—死亡率(用小数表示),
工p—死亡率总和,
i—相邻两组剂量对数之差。
(3)直接回归法:
死亡频率呈正态分布,则变化曲线为典型的“钟罩”型;死亡频率化为累积死亡频率,反应曲线呈s形;累积死亡频率化为概率单位时,反应曲线呈直线。
(二)急性毒性试验的其他方法
1.固定计量法
2.急性毒性分级法
3•上、下移动法
亚慢性毒性和慢性毒性的评价方法1、
实验动物
要求选拔两种实验动物,一种为啮齿类,首选是大鼠,另一种为非啮齿类,首选是狗。
亚慢性毒性试验一般每个剂量组20只大鼠,或每组4'6只狗。
慢性毒性试验每组40只大鼠,狗每组8只或以上。
2、染毒途径
常用的染毒途径是经胃肠道、经呼吸道和经皮肤染毒。
3、染毒期限
工业毒理学——3—6个月
食品毒理学一一6个月一1年
环境毒理学一一6个月一1年
致癌试验一一接近或等于动物的预期寿命
4、剂量分组
(1)亚慢性毒性的剂量选择:
阴性对照组,低剂量组,中剂量组,高剂量组
急性毒性的阈剂量:l/20'l/5LD50
组距:3、10倍,最低不小于2倍
(2)慢性毒性的剂量选择
阴性对照组,低剂量组,中剂量组,高剂量组
亚慢性阈剂量:l/50'l/5LD50
组距:2~5倍,最低不小于2倍
5、观察指标
(1)中毒症状(行为和外观)
(2)体重:每周称量一次
(3)食物利用率(试验动物每食入100g饲料所增长的体重克数)
(4)实验室检查
1)血液学检查
2)尿液检查
3)血液生化学检查
(5)病理及病理组织学检查
对濒死动物进行解剖。
试验结束及恢复期结束时,活杀实验动物。
1)系统解剖:消化道、肺、肝、肾、淋巴腺、眼、皮肤等,记录有无肉眼可见的异常变化。
2)脏器系数:是指某个脏器质量与体重的比值,又称脏体比值。
常以100g体重或lg 体重计。
需称量脏器湿重并计算其脏器系数。
3)组织病理学检查
(6)特界性指标
6、结果分析:选择适当的统计学方法进行各剂量组与阴性对照组的比较。