高中酸碱盐溶解度表(全)
- 格式:doc
- 大小:107.00 KB
- 文档页数:2
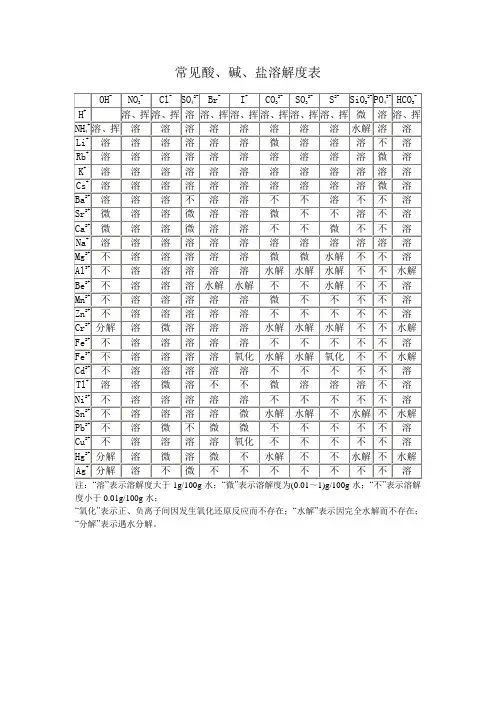
![常见酸、碱、盐溶解度表[1]](https://uimg.taocdn.com/6d7b525fd0d233d4b04e69c3.webp)
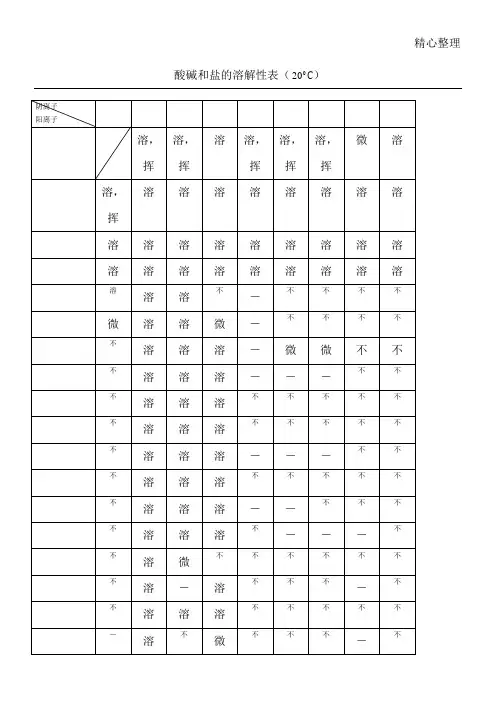
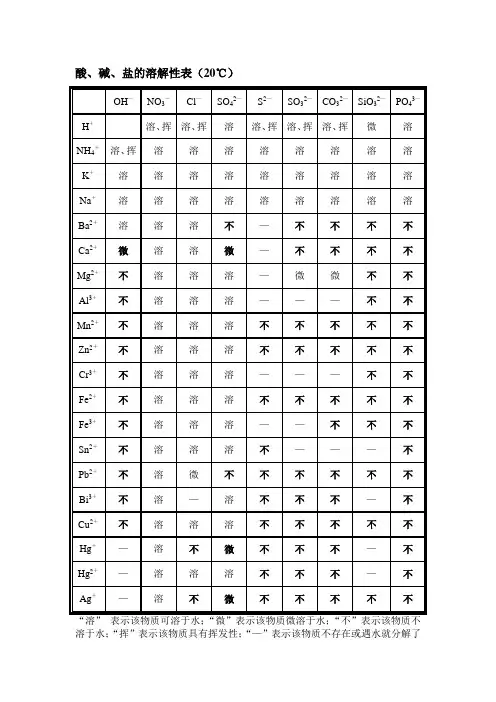
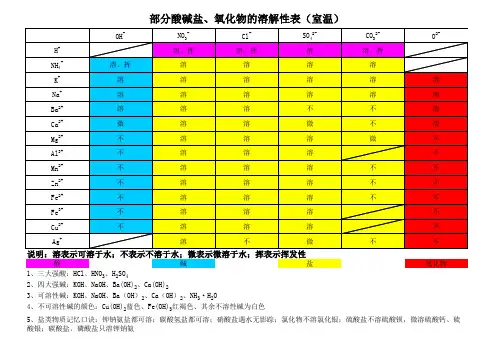
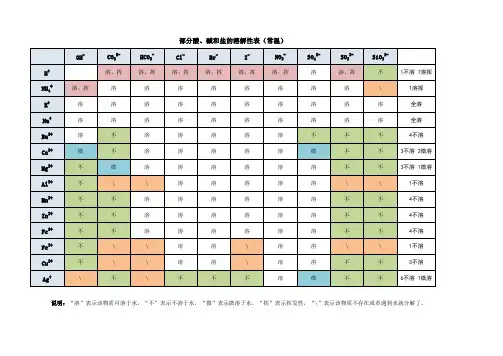
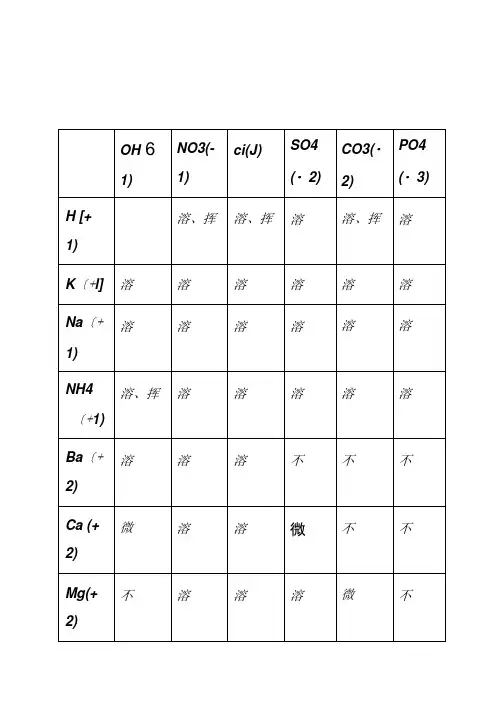
说明:此为2(rc时的情况。
"溶"表示那种物质可溶于水, "不"表示不溶于水,"微"表示微溶于水,"挥"表示挥发性,表示那种物质不存在或遇到水就分解了背诵口诀1 •钾钠鞍盐都可溶,氯化物不溶氯化银硫酸盐钙银微溶换不溶硝酸盐遇水影无踪钾钠锁钙碱可溶红褐铁,蓝絮铜其它沉淀白色呈注:4初中用够了.红褐铁,代表铁盐沉淀为红褐色[fe(oh)2氢氧化亚铁除外】,蓝絮铜代表,铜盐为蓝色絮状沉淀。
2•氯化银【不溶酸】,碳酸钙,碳酸换,硫酸顿【不溶酸】,氢氧化铝.氢氧化镁,为白色沉淀。
氢氧化铁〔红褐色〕氢氧化铜〔蓝色〕说明【】内为前一物质的特点2•钾钠镀盐全都溶其他全都不能溶AgCL BaSO4酸也不溶-氧气的性质:4〕单质与氧气的反响:〔化合反响〕1. 镁在空气中燃烧:2Mg + 02点燃2MgO2. 铁在氧气中燃烧:3Fe + 202点燃Fe3O43.铜在空气中受热:2Cu + 02加热2CuO4.铝在空气中燃烧:4A! + 302点燃2AI2O35.氢气中空气中燃烧:2H2 + 02点燃2H2O6•红磷在空气中燃烧〔研究空气组成的实验〕:4P + 502点燃2P2O57. 硫粉在空气中燃烧:S + 02点燃SO28. 碳在氧气中充分燃烧:C+O2点燃CO29. 碳在氧气中不充分燃烧:2C + 02点燃2CO(2)化合物与氧气的反响:10. 一氧化碳在氧气中燃烧:2CO + 02点燃2CO211. 甲烷在空气中燃烧:CH4 + 202点燃CO2 + 2H2O12. 酒精在空气中燃烧:C2H5OH + 302点燃2CO2 +3H2O⑶氧气的来源:13 •玻义耳研究空气的成分实验2HgO加热Hg+ 02 t14 •加热高猛酸钾:2KMnO4协热K2MnO4 + MnO2 + 02 t〔实验室制氧气原理A15 •过氧化氢在二氧化猛作催化剂条件下分解反响:H2O2MnO22H2O+ 02 t〔实验室制氧气原理2]二自然界中的水:电2H2T+ 02 t17. 生石灰溶于水:CaO + H2O == Ca(OH)218. 二氧化碳可溶于水:H2O + CO2==H2CO319.镁在空气中燃烧:2Mg + 02点燃2MgO 21.氢气复原氧化铜:H2 + CuO加热Cu + H2O 22.镁复原氧化铜:Mg + CuO加热Cu + MgO四、碳和碳的氧化物:⑴碳的化学性质23.碳在氧气中充分燃烧:C + 02点燃CO2 24 .木炭复原氧化铜:C+ 2CuO高温2Cu + CO2t 25.焦炭复原氧化铁:3C+ 2Fe203高温4Fe + 3CO2T⑵煤炉中发生的三个反响:〔几个化合反响〕26 •煤炉的底层:C + 02点燃CO2 27.煤炉的中层:CO2 + C高温2CO 28.煤炉的上部蓝色火焰的产生:2CO + 02点燃2CO2⑶二氧化碳的制法与性质:29 •大理石与稀盐酸反响〔实验室制二氧化碳〕:CaCO3 + 2HC! == CaC!2 + H2O + CO2t 30・碳酸不稳定而分解:H2CO3 == H2O + CO2t 31・二氧化碳可溶于水:H2O +CO2== H2CO332 •高温熾烧石灰石〔工业制二氧化碳〕:CaCO3高温CaO + CO2t 33 •石灰水与二氧化碳反响[鉴别二氧化碳〕:Ca(OH)2 + CO2 === CaCO3 1+ H2O⑵金属单质+盐+氢气 〔詈换反⑷一氧化碳的性质:34 . 一氧化碳复原氧化铜:CO + CuO 加热Cu + CO2 35. 一氧化碳的可燃性:2CO + 02点燃2CO2五燃料及其利用:37.甲烷在空气中燃烧:CH4 + 202点燃CO2 + 2H2O 38 •酒精在空气中燃烧:C2H5OH + 302点燃2CO2 + 3H2O 39.氢气中空气中燃烧:2H2 + 02点燃2H2O/u 金属(1)金属与氧气反响:40・镁在空气中燃烧:2Mg + 02点燃2MgO 41・铁在氧气中燃烧:3Fe + 202点燃Fe3O4 42. 铜在空气中受热:2Cu + 02加热2CuO43. 铝在空气中形成氧化膜:4A! + 302 = 2AI2O344. 锌和稀硫酸 Zn + H2SO4 = ZnSO4 + H2t 45. 铁和稀硫酸 Fe + H2SO4 = FeSO4 + H2t 46. 镁和稀硫酸 Mg + H2SO4 = MgSO4 + H2t 47. 铝和稀硫酸2AI +3H2SO4 = A!2(SO4)3 +3 H2!其它反响:Na2CO3辖幕醫Zn+ 2HC_n n znc_2+ H2T萍幕醫Fe+ 2HC一n n艮一2+H2T棘幕鬣Mg+ 2HC一n h Mgc_2+ H2T・茄君帝聆嬲2A_+ 6HC一nu2A_C一3+ 3 H2T二的翻般网+即〔两蒔〕..................鬓專+器 B 1B^8 - Fe + CCSO4n n FeSO4 +Cu盘〔匕霍+的a ...即+釧川〔总〔2〕糜+的醫喜....... 弱+为 56・ 咕e2O3+6HC一HH2Fec_3+3H257・$203 + 3H2SO4n n+ 3H2O58・ - a c o+ 2HC_Hucuc一2 + H2O59・ ^s s ss -aco+H2SO4n n CUSO4 + H.〔〕嬲+気弱;s ^s7二一(4)另一种酸61. 盐酸和氢氧化钙反响:2HCI + Ca(OH)2 == CaCI2 + 2H2O62. 氢氧化铝药物治疗胃酸过多:3HCI + AI(OH)3 == A/C/3 + 3H2O63. 硫酸和烧碱反响:H2SO4 + 2NaOH == Na2SO4 + 2H2O 64 .大理石与稀盐酸反响:CaCO3 + 2HC! == CaC!2 + H2O + CO2t 65碳酸钠与稀盐酸反响:Na2CO3 + 2HCI = = 2NaC! + H2O+ CO2t 66 •碳酸氢钠与稀盐酸反响:NaHCO3 + HC!== NaC! + H2O + CO2t67.硫酸和氯化坝溶液反响:H2SO4 + BaCI2== BaSO4 !+ 2HC!2、碱的化学性质⑴碱+非金属氧化物 .............. 盐+水68 •苛性钠暴露在空气中变质:2NaOH + CO2 == Na2CO3 + H2O69 •苛性钠吸收二氧化硫气体:2NaOH + SO2 == Na2SO3 + H2O盐+水74.铁和,铜溶液另一种酸70 •苛性钠吸收三氧化硫气体:2NaOH + SO3 == Na2SO4 + H2O71 •消石灰放在空气中变质:Ca(OH)2 + CO2二二CaCO3 I + H2O72.消石灰吸收二氧化硫:Ca(OH)2 + SO2 == CaSO3 1+ H2O〔3〕碱+盐 ......... 另_种碱+另一种盐73.氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 == CaCO3l+ 2NaOH 3.盐的化学性质(1)盐〔溶液〕+金属单质・……另一种金属+另一种盐 75碳酸钠与稀盐酸反响:Na2CO3 + 2HCI==2NaCI + H2O + CO2t碳酸氢钠与稀盐酸反响:NaHCO3 + HC/== NaCI + H2O + CO2t⑶盐+碱 ............ 另一种碱+另一种盐76.氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 == CaCO3!+ 2NaOH⑷盐+盐两种新盐77•氯化钠溶液和硝酸银溶液:NaCI + AgNO3二二AgClJ +〔2〕碱 +⑵盐+NaNO3 78・硫酸钠和氯化锁:Na2SO4 + BaC/2 == BaSO4l + 2NaC!钾钠硝钱均可溶.盐酸盐不溶AgCI.硫酸盐不溶BaSO4,碳•溶解性口诀一钾钠链盐溶水快,◎硫讎除去坝铅钙。
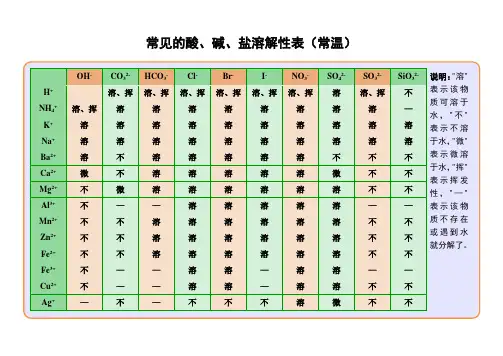
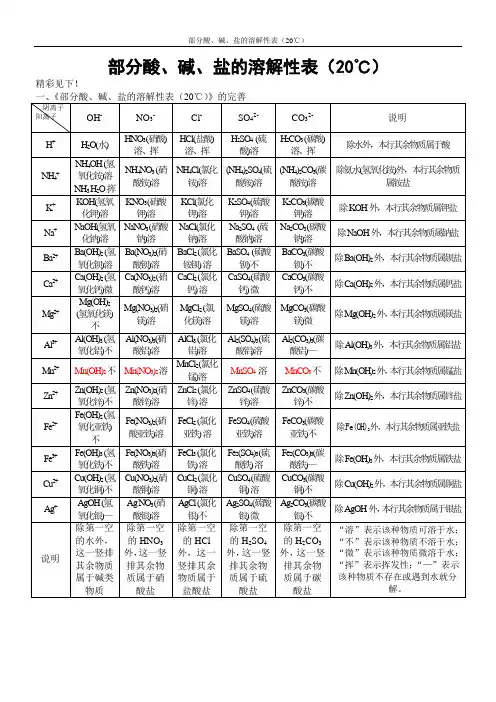
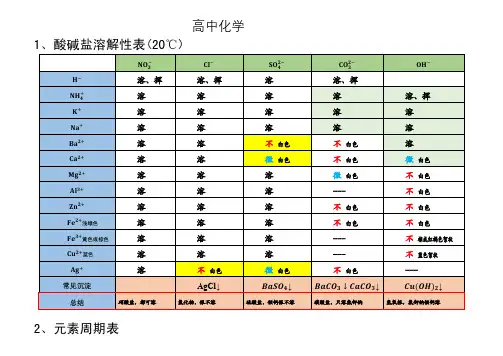

一、干燥剂 1. 使用干燥剂的目的是除去气体中混有的水蒸气。
2.我们学过的干燥剂有氢氧化钠、浓硫酸、氧化钙、氯化钙等。
氢氧化钠易潮解;浓硫酸具有吸水性;而氧化钙可以与水反应:CaO+H 2O=Ca(OH)2 3.氢氧化钠氢氧化钠等碱性干燥剂不能干燥氯化氢、二氧化碳、二氧化硫等酸性气体。
4. 浓硫酸浓硫酸等酸性干燥剂不能干燥氨气等碱性气体。
二、酸的定义和分类酸:物质溶于水时,形成的阳离子全部是H +的化合物。
由于酸、碱、盐溶于水时会电离出阴、阳离子,所以酸、碱、盐的水溶液具有导电性。
酸的电离:HCl=H ++Cl -,H 2SO 4=2H ++SO 42-三、碱的定义和分类碱:物质溶于水时,形成的阳离子全部是OH -的化合物。
四、氢氧化钠和氢氧化钙部分变质 1.氢氧化钠部分变质的证明方法:① 取样,(如果是固体,就需要加适量水,使固体完全溶解),加过量的氯化钙(或硝酸钙)溶液,如果有白色沉淀产生,说明碳酸钠存在:Na 2CO 3+CaCl 2=2NaCl+CaCO 3↓ 或 Na 2CO 3+Ca(NO 3)2=2NaNO 3+CaCO 3↓② 过滤,向滤液中滴加酚酞溶液,如果滤液变红,说明氢氧化钠存在,氢氧化钠部分变质。
2.氢氧化钙固体部分变质的证明方法:① 取样,加适量水使固体完全溶解,加入过量的稀盐酸,如果有气泡产生,说明碳酸钙存在:CaCO 3+2HCl=CaCl 2+H 2O+CO 2↑② 另取少量固体,加氯化铵(或硫酸铵)研磨,如果闻到刺激性氨味,说明氢氧化钙存在,氢氧化钙部分变质:Ca(OH)2+2NH 4Cl=CaCl 2+2NH 3↑+2H 2O 或 Ca(OH)2+(NH 4)2SO 4=CaSO 4+2NH 3↑+2H 2O 3.在所有的复分解反应中,中和反应优先发生,并且反应可以瞬时完成。
中和反应是放热的反应。
中和反应同氧化反应、还原反应一样,是特征反应,不属于四大基本反应类型。