有机化学章节整理
- 格式:pdf
- 大小:213.42 KB
- 文档页数:13

大学有机化学知识点提纲(一)绪论共价键价键理论(杂化轨道理论);分子轨道理论;共振论.共价键的属性:键能;键长;键角;键的极性.键的极性和分子极性的关系;分子的偶极矩.有机化合物的特征(二)烷烃和环烷烃基本概念烃及其分类;同分异构现象;同系物;分子间作用力;a键,e键;构型,构象,构象分析,构象异构体;烷基;碳原子和氢原子的分类(即1,2,3碳,氢;4碳);反应机理,活化能.对于基本概念,不是要求记住其定义,而是要求理解它们,应用它们说明问题.命名开链烷烃和环烷烃的IUPAC命名,简单的桥环和螺环的命名.烷烃和环烷烃的结构碳原子sp3杂化和四面体构型;环烷烃的结构(小环的张力).烷烃的构象开链烷烃的构象,能量变化;环烷烃的构象:重点理解环己烷和取代环己烷的构象及能量变化,稳定构象,十氢萘及其它桥环的稳定构象.烷烃的化学性质自由基取代反应—卤代反应及机理;碳游离基中间体—结构,稳定性;不同的卤素在反应中的活性和选择性;反应过程中的能量变化.环烷烃的化学性质自由基取代反应(与烷烃一致);小环(3,4元环)性质的特殊性—加成.(三)烯烃烯烃的结构特点碳的sp2杂化和烯烃的平面结构;键和键.烯烃的同分异构,命名碳架异构,双键位置异构,顺反异构(Z,E).烯烃的物理和化学性质烯烃的亲电加成及其机理,马氏规则;碳正离子中间体—结构,稳定性,重排.其它加成反应:催化加氢(立体化学,氢化热);硼氢化—氧化(加成取向,立体化学);羟汞化—脱汞(加成取向);与HBr/过氧化物加成(加成取向);其它游离基加成.氧化反应:羟基化反应—邻二醇的形成;KMnO4/H+的氧化,臭氧化反应,烯烃结构的测定.α-位取代反应:烯丙基型取代反应(高温卤代和NBS卤代)及机理—烯丙基自由基.(四)炔烃和二烯烃炔烃①结构:碳的sp杂化和碳-碳三键;sp杂化,sp2杂化和sp3杂化的碳的电负性的差异及相应化合物的偶极矩.②同分异构体③化学性质:末端炔烃的酸性及相关的反应;三键的加成:催化加氢,亲电加成,亲核加成;碳—碳三键与H2/Lindlar催化剂反应(顺式烯烃);碳—碳三键与Na/液氨的反应(反式烯烃);加卤素;加HX(马氏规则);加H2O(羰基化合物的形成);加HBr/过氧化物;硼氢化—氧化;加HCN及乙炔的二聚;氧化反应:KMnO4氧化和臭氧化.二烯烃①共轭二烯烃的稳定性:键能和键长平均化,共轭效应.②二烯烃的化学反应:1,2-加成和1,4-加成(反应机理);反应的动力学控制和热力学控制(反应过程中的能量变化);烯丙型碳正离子的稳定性(p-共轭);Diels-Alder反应.(五)波谱分析紫外光谱理解各种跃迁(,n,,n)和各自的吸收能量波长;发色团和助色团;溶剂效应;最重要的是能够从一张UV谱图中得到有用的信息(判断结构)(不要求利用经验规则去计算某化合物之吸收波长).红外光谱理解IR光谱之基本原理,最重要的是利用IR光谱(结合其它波谱)推测有机分子的结构,这就要求对各类官能团的红外吸收范围有清楚的了解,并清楚影响峰位置变化的因素.核磁共振谱(1H NMR)(碳谱不要求)了解基本原理;基本概念:化学位移,内标,外标,偶合,偶合常数,屏蔽,去屏蔽等.清楚不同类型的枝质子的化学位移范围及影响因素;最重要的是利用NMR谱(结合其它波谱)推测有机分子的结构.质谱了解基本原理;几种重要的开裂方式(包括重要的重排开裂如麦氏重排,逆Diels-Alder重排等);最重要的是利用MS得出的分子离子峰(并结合其它波谱方法)推测有机分子的结构.本章最重要的是利用几种波谱方法结合推测有机分子的结构.(六)芳香烃苯的结构和芳香性理解芳香性的概念和判断芳香性的Hückel规则,能用此规则判断一给定的分子(或离子)是否是芳香性的.苯的异构,同系物和命名苯及其同系物的物理性质和波谱性质主要了解其波谱特征,例如芳香烃的NMR谱学特征,不同取代苯在IR指纹区的特征等.化学性质亲电取代反应及机理;傅氏反应的特点及局限;氯甲基化反应;Gatterman-Koch反应;芳香环上取代基的定位效应;其它反应:侧链氧化;侧链取代;芳香环上的还原:催化加氢,Birch还原.萘的结构和化学性质(七)立体化学基本概念对映异构(体);手性分子;镜像;旋光性,旋光度;对映体;非对映体;差向异构体;内消旋体;外消旋体;手征性;手性中心.对映异构体构型的表示法R/S法(次序规则).熟悉各类手性分子含1—3个手性碳原子的手性分子;不含手性碳原子的手性分子;环状化合物.立体异构体的制备和反应熟悉能产生立体异构体的化学反应及机理,象烯烃与卤素的反式加成,环氧乙烷的开环,羰基化合物的加成(Cram规则)等等.(八)卤代烃异构,分类,命名波谱性质,尤其是NMR谱化学性质亲核取代反应及机理(SN1,SN2);影响亲核取代及机理的因素;亲核试剂的亲核性;SN2反应的立体化学;SN1反应中的重排;邻基参与.消除反应及机理(E1,E2,E1cb):消除反应的取向(Saytzeff规则)和立体化学;消除反应和取代反应的竞争.卤代烃与Mg,Li,Na等的反应:Grignard试剂,有机锂试剂及其应用.(九)醇,酚,醚结构,分类,命名醇的物理性质和光谱性质氢键对其物理性质的影响;IR光谱和NMR谱的特征.醇的化学性质醇的酸性(与其它类型化合物如H2O,酚,羧酸酸性的比较);与酸性有关的反应(与金属如Na,Mg,Al的反应);醇的氧化(形成醛/酮,羧酸);熟悉各种氧化剂;醇的成酯反应:与无机酸成酯,与有机酸成酯(机理);卤化反应;用SOCl2卤化的立体化学及机理;用HX的卤代反应(Lucas试剂用来区别六个碳原子以下1,2和3醇);Wagner-Meerwein重排.醇的脱水反应:反应机理/扎依切夫规律;反应活性;重排;分子间脱水成醚.多元醇的反应:与HIO4或Pb(OAc)4的反应;片呐醇重排反应及机理.酚的物理性质和光谱性质酚的化学性质酸性及与之相关的反应;Fries重排;芳环上的亲电取代:卤代,硝化,磺化;其它亲电取代:与醛的作用;与CO2的作用;Reimer-Tiemann反应;酚的氧化反应.酚的制备方法异丙苯氧化法;氯苯水解法;苯磺酸碱熔法.醚的反应与HX的反应(醚键断裂)及机理;Claisen重排;环氧乙烷的反应.醚的合成方法Williamson合成法.(十)醛和酮醛酮的反应①加成反应,亲核加成以上反应适用于醛,脂肪族甲基酮和八个碳原子以下的环酮.②—碳原子上卤仿反应:③氧化和还原醛酮的制法①烃类氧化②醇的氧化及去氢③Friedel-Crafts酰化反应3.,—不饱和醛,酮的反应:(十一)羧酸及其衍生物羧酸的反应:①酸性:羧酸的酸性比碳酸强,比无机酸弱.②羧酸中羟基的取代反应③还原羧酸的制法①氧化法②水解法③Grignard试剂与二氧化碳作用羧酸衍生物的反应①水解都生成羧酸②醇解酰氯,酸酐和酯的醇解都生成酯,酯与醇作用生成原酸酯或酯.③氨解酰氯,酸酐和酯的氨解都生成酰胺④酸解生成平衡混合物羧酸衍生物的制法①酰氯:羧酸与无机酰氯作用;②酸酐:酰氯与羧酸盐作用;③酯:直接酯化: ④酰胺:羧酸的铵盐去水或酯的氨解;⑤腈:酰胺去水或卤代烃与氰化钠作用.(十二)取代羧酸卤代酸的反应①与碱的反应,产物与卤素和羧基的相对位置有关.-卤代酸羟基酸-卤代酸,-不饱和酸或-卤代酸内酯②Darzen反应诱导效应共轭效应醇酸的反应①去水,产物与羟基的相对位置有关-醇酸交酯-醇酸,-不饱和酸-醇酸内酯②分解:乙酰乙酸乙酯在合成上的应用①合成甲基酮:②合成酮酸丙二酸酯在合成上的应用①合成一元羧酸②合成二元羧酸(十三)胺和含氮化合物胺的化学性质①碱性②烃化③酰化(Hinsberg反应)④与亚硝酸的反应胺的制法①硝基混合物的还原②氨或胺的烃化③还原烃化④Gabriel合成法⑤Hofmann重排:芳香族重氮盐的反应①取代反应②还原反应③偶联反应(十四)含硫,含磷化合物硫醇的制备和性质①酸性和金属离子形成盐,还原解毒剂;②氧化反应,二硫化物,磺酸;③和烯键及炔键的加成反应.磺酸基的引入和被取代在合成上应用了解磺胺药物一般制备方法.磷Ylide的制备及Wittig反应在合成中的应用.(十五)杂环化合物杂环化合物的分类和命名呋喃,噻吩,吡咯的结构和芳香性.芳香性: 苯>噻吩>吡咯>呋喃离域能(kJ/mol—1) 150.6,121.3,87.6,66.9呋喃,噻吩,吡咯的性质①亲电取代:卤代,硝化,磺化,乙酰化;②呋喃易发生;Diels-Alder反应;③吡咯的弱碱性;④吡啶的碱性;⑤吡啶的氧化,还原性质;⑥Fischer吲哚合成法和Skraup喹啉合成法.(十六)周环反应在协同反应中轨道对称性守恒电环化反应的选择规律电子数基态激发态4n 顺旋对称4n+2 对旋顺旋环化加成反应的选择规律(同一边)电子数基态激发态4n 禁阻允许4n+2 允许禁阻迁移反应的选择规律(同一边)i+j 4n 4n+2基态禁阻允许Cope重排Claisen重排(十七)碳水化合物单糖的结构与构型①Fischer构型式的写法:羰基必须写在上端;②构型:编号最大手性碳原子上OH在竖线右边为D-型,在左边为L-型;③Haworth式:己醛糖的Haworth式中C1上的OH与C5上的CH2OH在环同一边为位异构体.单糖的反应①氧化:醛糖用溴水氧化生成糖酸,用稀硝酸氧化生成糖二酸②还原:用NaBH4还原生成多元醇③脎的生成:糖与苯肼作用——成脎.(十八)氨基酸,多肽,蛋白质1.①氨基酸的基本结构天然的-氨基酸,只有R取代基的差别.②等电点:等电点时氨基酸以两性离子存在,氨基酸溶解度最小;③氨基酸-茚三酮的显色的反应;④Sanger试剂及应用;⑤氨基酸的制备:a. -卤代酸的氨解,b. 醛和酮与氨,氢氰酸加成物水解,c. 二丙酸酯合成法;⑥多肽的合成方法.(十九)萜类和甾体化合物①掌握萜类化合物的基本结构:碳骨架由异戊二烯单位组成的;会划分萜类化合物中的异戊二烯单位.②掌握一些重要的萜类天然产物常规性质:如法尼醇;牛儿酮;栊牛儿奥;山道年;维生素A;叶绿醇;角鲨烯.-胡萝卜素.③了解甾体化合物的四环结构和命名.④了解萜类和甾体化合物的生物合成。

有机化学相关内容整理归纳总结有机化学是对有机物的结构、性质、合成、反应及应用等方面的研究,是化学学科中非常重要的一个分支。
有机化学的研究范围极其广泛,涉及到了从基础研究到应用研究的方方面面。
下面我们对有机化学相关的内容进行整理归纳总结。
1.有机化学的基础知识有机化学中的基础知识主要包括以下几个方面:(1)化学键和分子构型:了解分子中的共价键、反应的类型和方向、分子的构型类型等。
(2)有机化合物的性质:有机化合物的物理性质和化学性质,尤其是它们的反应类型、热力学和动力学。
(3)元素和分子的电子构型:元素和分子的电子构型可用于预测有机化合物的物理和化学性质,尤其是反应类型。
(4)共轭体系和杂环化合物:学习共轭体系和杂环化合物的电子结构和反应类型。
(5)手性和对映异构体:掌握手性和对映异构体概念,了解手性的应用和研究进展。
2.有机化学的反应类型有机化学中的反应类型主要有以下几个方面:(1)酸碱性反应:如酸碱滴定和分级机理。
(2)加成反应:如加成反应的类型和机制。
(3)消除反应:如消除反应的类型和机制。
(4)缩合反应:如缩合反应的类型和机制。
(5)取代反应:如核取代反应的类型和机制。
(6)氧化还原反应:如酮还原反应、氧化反应的类型和机制。
(7)重排反应:如重排反应的类型和机制。
3.有机合成有机合成是有机化学的重要分支之一,其研究内容涉及有机化合物的合成方法、反应机制、分析和表征等方面。
有机合成技术的快速发展,使得人们可以合成更多、更复杂、更有功能性的化合物,从而推动了生命科学、药学、材料科学等领域的发展。
人们在有机合成过程中,还需要考虑如下几个方面:(1)反应条件:包括温度、压力、溶剂等因素。
(2)催化剂:不同的催化剂对反应的速率和选择性均有影响。
(3)保护基:合成复杂化合物时需要使用保护基,以保护某些官能团。
(4)功能化修饰:化合物的功能化修饰对化合物的特定化学、物理性质具有深刻影响。
(5)多步合成:常常需要多步合成来得到目标化合物。

基础有机化学-----------------------------------------------------预备知识-----------------------------------------------------一. 原子结构1. 波尔理论对氢原子光谱的解释:氢原子在正常状态总是处于能量最低的基态,在受到光照射或放电等作用时,吸收能量,原子中的电子跳到能量较高的激发态。
但在激发态不稳定,回到低能量轨道时放出能量产生与能量对应的光,从而产生光谱。
hv E =∆。
2. 四个量子数:(1)主量子数n :n 为不同的电子层层数。
(2)角量子数l :同一电子层还可以分为不同的亚层,对应于n ,l =0~1-n 。
其中当0=l 时,为s 电子,1=l ,为p 电子,以此类推…(3)磁量子数m :用来描述同一亚层原子轨道和电子云的方向。
它受到l 的影响,当0=l 时,0=m ;1=l 时,1-=m 、0、1+,即p 电子有3种空间取向,分别为x p 、y p 、z p ;当2=l 时,可有五种空间取向,即2z d 、xz d 、yz d 、xy d 、22y x d -。
(4)自旋量子数s m :电子除绕核运转外,还有自旋运动。
电子自旋量子数只有2个取值,21+和21-,即电子有2个相反的自旋方向。
3. 原子轨道:我们常把电子层、电子亚层和空间取向都确定的运动状态称作原子轨道,即s 层有一个原子轨道,p 层有3个等等。
空间取向不同,并不影响电子的能量,因此同一亚层的几个原子轨道能量完全相同,这样的轨道称为等价轨道或简并轨道。
4. 原子轨道分布图描述的是解薛定谔方程得到的波函数ψ的值,函数值可以为正也可以为负。
形成共价键时要求同号重叠,即对成型匹配原则。
电子云角度分布图全为正。
5. 屏蔽效应:在多电子原子中,电子不但受到原子核的吸引,而且电子和电子之间也存在着排斥作用。
也就是说其余电子屏蔽了或削弱了原子核对该电子的吸引作用。

有机化学笔记整理有机化学是一门研究含碳化合物的结构、性质、合成与反应的科学。
它不仅在化学领域中占据着重要地位,还与生物学、医学、材料科学等多个学科密切相关。
以下是我对有机化学的一些笔记整理,希望能对大家有所帮助。
一、有机化合物的结构1、碳原子的成键特点碳原子最外层有 4 个电子,能形成 4 个共价键。
碳原子之间可以通过单键、双键或三键相连,形成不同长度和形状的碳链或碳环。
2、共价键的类型有机化合物中的共价键包括σ 键和π 键。
σ 键是原子轨道沿键轴方向“头碰头”重叠形成的,比较稳定;π 键是原子轨道平行“肩并肩”重叠形成的,不如σ 键稳定。
3、同分异构体同分异构体是指具有相同分子式但结构不同的化合物。
它们可以分为构造异构体(如碳链异构、官能团位置异构)和立体异构体(如顺反异构、对映异构)。
4、有机物的表示方法常见的表示方法有结构式、结构简式、键线式等。
结构式能准确地表示出分子中原子的连接顺序和价键类型;结构简式则省略了一些价键;键线式用线段表示碳碳键,端点和交点表示碳原子。
二、有机化合物的分类1、按碳骨架分类可以分为链状化合物(如乙烷、丁烯)、环状化合物(如环己烷、苯)。
环状化合物又分为脂环化合物(如环己烷)和芳香化合物(如苯)。
2、按官能团分类官能团决定了有机物的化学性质。
常见的官能团有碳碳双键(C=C)、碳碳三键(—C≡C—)、羟基(—OH)、醛基(—CHO)、羧基(—COOH)、酯基(—COO—)等。
三、有机化合物的命名1、烷烃的命名选择最长的碳链作为主链,根据主链上碳原子的数目称为“某烷”。
从距离支链最近的一端开始给主链碳原子编号,确定支链的位置。
2、烯烃和炔烃的命名选择含有双键或三键的最长碳链作为主链,编号时使双键或三键的位置最小。
3、苯的同系物的命名以苯环为母体,侧链作为取代基。
编号时从简单的取代基开始,使取代基的位置之和最小。
四、有机化合物的物理性质1、状态常温下,碳原子数小于 4 的烃为气态,5 16 个碳原子的烃为液态,17 个碳原子以上的烃为固态。

基础有机化学有机化学理论部分基础知识点1.保里不相容原理原子轨道理论 2.能量最低原理(基态) 3.洪特规则1.自旋反向平行规则价键理论 2.共价键的饱和性3.共价键的方向性激发态 4.能量相近轨道形成杂化轨道1.能量相近分子轨道理论 2.电子云最大重叠3.对称性相同规范性示例化学反应的基本模式:A试剂溶剂条件 B补充知识点Lewis酸的三种类型:Lewis碱的三种类型:第三章:立体化学1.无对称面1.分子手性的普通判据2.无对称中心3.无S4 反轴注:对称轴Cn不能作为判别分子手性的判据2. 外消旋体(dl体或+/-体)基本概念 1.绝对构型与相对构型2.种类:外消旋化合物/混合物/固体溶液基本理论非对映体差向异构体端基差向异构体内消旋体(meso-)e.g 酒石酸举例名词解释可能考察的:相对/绝对构型对映体/非对映体外消旋体潜不对称分子/原手性分子差向异构体3.立体异构部分⑴含手性碳的单环化合物:判别条件:一般判据 无S 1 S 2 S 4 相关:构象异构体eeaa eaae构象对映体主要考查:S 1=对称面的有无相关实例:1.1,2-二甲基环己烷 1,3二甲基环己烷 1,4二甲基环己烷 ⑵含不对称原子的光活性化合物 N 稳定形式S P 三个不同的基团⑶含手性碳的旋光异构体丙二烯型旋光异构体 1.狭义c c c条件:a b 两基团不能相同2.广义:将双键看成环,可扩展一个或两个cc c联苯型旋光异构体 (阻转异构现象- 少有的由于单键旋转受阻而产生的异构体)BA ab构型命名方法:选定一环,大基团为1,小基团为2.另一环,大集团为3,将其小基团转到环后最远处。
⑷含手性面的旋光异构体分子内存在扭曲的面而产生的旋光异构体,e.g 六螺苯4.外消旋化的条件⑴若手性碳易成碳正离子、碳负离子、碳自由基等活性中间体,该化合物极易外消旋化。
⑵若不对称碳原子的氢是羰基的α-H ,则在酸或碱的作用下极易外消旋化。
有机化学复习总结一.有机化合物的命名1.能够用系统命名法命名各种类型化合物:包括烷烃,烯烃,炔烃,烯炔,脂环烃(单环脂环烃和多环置换脂环烃中的螺环烃和桥环烃),芳烃,醇,酚,醚,醛,酮,羧酸,羧酸衍生物(酰卤,酸酐,酯,酰胺),多官能团化合物(官能团优先顺序:-COOH>- SO3H>- COOR>- COX>- CN>- CHO> >C= O>- OH(醇 ) >- OH(酚 ) >- SH>- NH2>- OR> C = C>- C≡C-> ( -R>- X>- NO2),并能够判断出Z/E 构型和 R/S 构型。
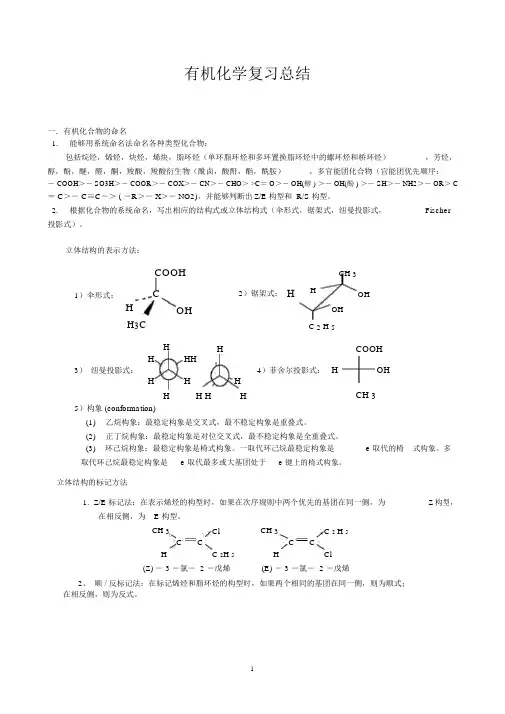
2. 根据化合物的系统命名,写出相应的结构式或立体结构式(伞形式,锯架式,纽曼投影式,Fischer 投影式)。
立体结构的表示方法:COOH CH 31)伞形式: C 2)锯架式:H H OHH OHOHH3C C 2 H 5H H COOHH HH4)菲舍尔投影式:H OH 3)纽曼投影式:H H HCH 3H H H H5)构象 (conformation)(1)乙烷构象:最稳定构象是交叉式,最不稳定构象是重叠式。
(2)正丁烷构象:最稳定构象是对位交叉式,最不稳定构象是全重叠式。
(3) 环己烷构象:最稳定构象是椅式构象。
一取代环己烷最稳定构象是 e 取代的椅式构象。
多取代环己烷最稳定构象是 e 取代最多或大基团处于 e 键上的椅式构象。
立体结构的标记方法1. Z/E 标记法:在表示烯烃的构型时,如果在次序规则中两个优先的基团在同一侧,为Z 构型,在相反侧,为 E 构型。
CH 3 Cl CH 3 C 2 H 5C C C CH C 2H 5 H Cl(Z) - 3 -氯- 2 -戊烯(E) - 3 -氯- 2 -戊烯2、顺 / 反标记法:在标记烯烃和脂环烃的构型时,如果两个相同的基团在同一侧,则为顺式;在相反侧,则为反式。
CH3 CH3 CH3 H CH3 CH3 H CH3C C C CH H H CH3 H H CH3 H顺- 2-丁烯反- 2-丁烯顺- 1,4-二甲基环己烷反- 1,4-二甲基环己烷3、 R/S 标记法:在标记手性分子时,先把与手性碳相连的四个基团按次序规则排序。

第七章有机化合物第一节认识有机化合物一、有机化合物中碳原子的成键特点1、甲烷是最简单的有机化合物,甲烷的分子式为CH4,电子式为,结构式为。
2、有机物中碳原子的结构及成键特点(1)有机物中,碳原子可以形成4个共价键。
(2)碳原子间成键方式多样①碳碳之间的结合方式有单键()、双键()、三键(—C≡C—)。
②多个碳原子之间可以结合成碳链,也可以结合成碳环(且可带支链)。
(3)有机物分子可能只含有一个或几个碳原子,也可能含有成千上万个碳原子。
注意:有机物中碳原子成键特点和碳原子间的连接特点决定了有机物种类繁多。
二、烷烃1.烷烃的结构(1)甲烷的结构甲烷的空间结构是正四面体结构,碳原子位于正四面体的中心,4个氢原子位于4个顶点上。
分子中的4个C—H的长度和强度相同,相互之间的夹角相同,为109°28′。
(2)空间示意图是。
甲烷的球棍模型为,空间填充模型为。
2、烷烃——只含有碳和氢两种元素(1)示例:乙烷的结构式为,分子式为C2H6,丙烷的结构式为,分子式为C3H8。
(2)结构特点①分子中碳原子之间都以单键结合;②碳原子的剩余价键均与氢原子结合,使碳原子的化合价都达到“饱和”,称为饱和烃,又称烷烃。
(3)分子组成通式:链状烷烃中的碳原子数为n,氢原子数就是2n+2,分子通式可表示为C n H2n+2。
(4)烷烃的一般命名①方法碳原子数(n)及表示n≤1012345678910甲乙丙丁戊己庚辛壬癸n>10相应汉字数字②示例:C4H10称丁烷,C8H18称辛烷,C12H26称十二烷。
3、同系物(1)概念:结构相似,在分子组成上相差一个或若干个CH2原子团的化合物。
(2)实例:CH4、C2H6、C3H8互为同系物。
4、同分异构体(1)概念①同分异构现象:化合物具有相同的分子式,但具有不同结构的现象。
同分异构现象是有机物种类繁多的重要原因之一。
②同分异构体:具有同分异构现象的化合物互称为同分异构体。
(2)写出C4H10的同分异构体:CH3CH2CH2CH3和,其名称分别为正丁烷和异丁烷。

有机化学知识整理1.甲烷的空间结构为正四面体型结构。
⒉烷烃的化学性质:烷烃在常温下比较稳定,不与强酸、强碱、强氧化剂起反应。
⑴取代反应:有机物分子中的原子或原子团被其它原子或原子团所替代的反应。
如:Cl2与甲烷在光照条件下可以发生取代反应,生成CH3Cl,CH2Cl2,CHCl3,CCl4及HCl的混合物。
取代反应,包括硝化、磺化、酯化及卤代烃或酯类的水解等。
⑵氧化:烷烃可以燃烧,生成CO2及H2O ⑶高温分解、裂化裂解。
⒊根、基:①根:带电的原子或原子团,如:SO42-,NH+4,Cl-。
②基:电中性的原子或原子团,一般都有未成对电子。
如氨基—NH2、硝基—NO2、羟基—OH。
4.同系物:结构相似,在分子组成相差一个或若干个—CH2原子团的物质互相称为同系物。
判断方法:所含有的官能团种类和数目相同,但碳原子数不等。
①结构相似的理解:同一类物质,即含有相同的官能团,有类似的化学性质。
②组成上相差“—CH2”原子团:组成上相差指的是分子式上是否有n个—CH2的差别,而不限于分子中是否能真正找出—CH2的结构差别来。
⒌乙烯分子为 C2H4,结构简式为CH2=CH2,6个原子共平面,键角为120°。
规律:碳碳双键周围的六个原子都共平面。
⒍乙烯的实验室制法:①反应中浓H2SO4与酒精体积之比为3:1。
②反应应迅速升温至170C,因为在140℃时发生了如下的副反应(乙醚)。
③反应加碎瓷片,为防止反应液过热达“爆沸”。
浓H2SO4的作用:催化剂,脱水剂。
⒎烯烃的化学性质(包括二烯烃的一部分)①加成反应:有机物分子中的双键或叁键发生断裂,加进(结合)其它原子或原子团的反应。
Ⅰ.与卤素单质反应,可使溴水褪色,CH2=CH2+Br2→CH2B—CH2BrⅡ.当有催化剂存在时,也可与H2O、H2、HCl、HCN等加成反应。
②氧化反应:I.燃烧II.使KmnO4/H+褪色Ⅲ.催化氧化:2CH2=CH2+O2 2CH3CHO有机反应中,氧化反应可以看作是在有机分子上加上氧原子或减掉氢原子,还原反应可看作是在分子内加上氢原子或减掉氧原子。

有机化学重点整理第二章:烷烃和环烷烃甲烷methane 己烷hexane 庚菀heptane乙烷ethane 丙烷propane 辛烷octane 丁烷butane 壬烷nonane 戊烷pentane 癸烷decane正normal n- 异iso- 新neo- 优先次序:异丙基>异丁基>丁基>丙基>乙基>甲基构象conformation ——由于碳碳单键的旋转,导致分子中原子或原子团在空间的不同排列方式构象异构体conformational isomer因单键的旋转而产生的异构体(构象异构属于立体异构)稳定性:对位交叉式>邻位交叉式>部分重叠式>全重叠式交叉式—稳定的优势构象烷烃的物理性质:bp、mp、密度:随C原子数↑而↑ 2.烷烃支链↑bp ↓正烷烃密度<0.8g.cm-3甲烷的卤代反应属于自由基的链反应:链引发、链增长、链终止三个阶段①链引发(形成自由基)②链增长(延续自由基,形成产物)③链终止(消除自由基)活性顺序:F2 > Cl2 > Br2 > I2 叔氢> 仲氢> 伯氢离解能越小,自由基越稳定,越易形成R3C > R2CH>RCH2> CH3环烷烃稳定性影响因素:环张力(角张力、扭转张力、空间张力)环丙烷、环丁烷——易开环发生加成,不与KMnO4反应(所有的环烷烃)开环发生在连氢原子最多和连氢原子最少的两个碳原子之间。
氢卤酸中的氢原子加在连氢原子较多的碳原子上,卤原子加在连氢原子较少的碳原子上。
椅式构象是最稳定的优势构象,较大基团在e键的构象是稳定构象(横E竖A),e键取代基最多的构象是优势构象第三章:烯烃和炔烃ζ键和π键的主要特点:ζ键:可以单独存在,存在于任何共价键中。
成键轨道沿键轴“头碰头”重叠,重叠程度较大,键能较大,键较稳定。
电子云呈柱状,对键轴呈圆柱形对称。
电子云密集于两原子之间,受核的约束大,键的极化性(度)小。

2598 含氮及杂环化合物内容提要本章主要讲述含C 、H 、O 、N 、X 等原子的化合物,着重阐述硝基化合物,胺类化合物以及胺的衍生物。
一些简单实用的杂环化合物也是本章学习的重点。
从结构上理解它们的性质,且掌握这些化合物的应用价值。
有机化合物除了含C 、H 外,还可含O 、N 、X 等杂原子。
前面讨论了含O ,X 的有机化合物,本章着重介绍有机含氮及杂环化合物。
前面章节中学过了腈、酰胺等含氮化合物,本章重点讨论硝基化合物、胺、季銨盐、重氮化合物、偶氮化合物和叠氮化合物。
它们的一般结构通式为:R-NO 2(Ar-NO 2) R-NH 2(Ar-NH 2) R 4N X ArN 2X(RN 2X) Ar-N=N-Ar(Ar')硝基化合物胺季銨盐类重氮化合物偶氮化合物由结构通式可知它们是不同氧化态的含氮有机物,因此,它们的性质和制备方法既有区别又有关联。
此外,本章还讨论C 与杂原子(如O 、N 、S)组成的环状化合物,即杂环化合物。
8.1 硝基化合物8.1.1 硝基化合物的命名和结构特征分子中含有硝基-NO 2的化合物称为硝基化合物,结构通式为:R-NO 2(Ar-NO 2)。
硝基化合物从结构上可看作烃的一个或多个氢原子被硝基取代的产物,可分为脂肪族硝基化合物和芳香族硝基化合物,脂肪族硝基化合物又可分为伯、仲、叔硝基化合物。
硝基化合物的命名类似于卤代烃,即以硝基为取代基命名,例如:CH 3NO 2CH 3CHCH 3NO 2CH 3O 2N硝基甲烷 2-硝基丙烷 对硝基甲苯在硝基化合物中,N 原子为sp 2杂化态,形成三个共平面的σ键,未参加杂化的具有一孤对电子的p 轨道与两个氧原子的p 轨道形成π43共轭体系。
两个N=O 键是等价的。
但习惯上写成R NO, 也有的写成R NO O 。
硝基甲烷分子的键长和键角为:H 3C N OC -N 147pm ,N -O 122pm ,∠ONO 为 127°两个N -O 键的键长相等,说明它们没有区别。

高中化学有机化学知识点归纳有机化学是化学的一个重要分支,研究含碳的化合物的结构、性质和反应。
在高中化学学习过程中,有机化学是一个重要的内容,以下是对高中化学有机化学知识点的归纳:1. 有机化合物的命名有机化合物的命名是有机化学的基础,主要有两种命名法,一种是按照IUPAC命名法,另一种是通用命名法。
按照IUPAC命名法,有机化合物命名顺序为:找到最长碳链、确定主链的编号方向、找出取代基的位置、命名取代基、确定双键或环烷的位置等。
通用命名法则是直接根据化学结构,给予化合物一个通用名称。
2. 有机物的结构式有机物的结构式包括:分子式、结构式、分子结构式、键线结构式、空间结构式等。
结构式能直观表现出有机物的结构,有助于理解有机化合物的性质和反应。
3. 有机物的同分异构体同分异构体是指化学式相同,结构式和物理性质却不同的化合物。
同分异构体主要有链式异构体、支链异构体、环状异构体、位置异构体等。
4. 有机物的性质有机物的性质主要包括:饱和、不饱和、烷烃、烯烃、炔烃、芳香烃等。
有机物在化学反应中常常表现出特定的性质和反应活性。
5. 有机物的化学反应有机物的化学反应包括:燃烧、卤代反应、加成反应、消除反应、重排反应、酯化反应、醇醚反应等。
有机化合物在不同条件下会发生不同的化学反应。
6. 有机物的制备方法有机化合物的制备方法包括:实验室制备、化学合成、生物合成等。
根据有机物的结构和性质,可以采取不同的方法来制备有机化合物。
总的来说,高中有机化学知识点的归纳包括有机物的命名、结构式、同分异构体、性质、化学反应和制备方法等内容。
通过系统的学习和积累,可以更好地理解和掌握有机化学知识,为日后的学习和研究打下坚实的基础。
希望以上内容对您有所帮助。
高中数学第五章-平面向量考试内容:向量.向量的加法与减法.实数与向量的积.平面向量的坐标表示.线段的定比分点.平面向量的数量积.平面两点间的距离、平移. 考试要求:(1)理解向量的概念,掌握向量的几何表示,了解共线向量的概念. (2)掌握向量的加法和减法.(3)掌握实数与向量的积,理解两个向量共线的充要条件.(4)了解平面向量的基本定理,理解平面向量的坐标的概念,掌握平面向量的坐标运算.(5)掌握平面向量的数量积及其几何意义,了解用平面向量的数量积可以处理有关长度、角度和垂直的问题,掌握向量垂直的条件.(6)掌握平面两点间的距离公式,以及线段的定比分点和中点坐标公式,并且能熟练运用掌握平移公式.§05. 平面向量 知识要点1.本章知识网络结构2.向量的概念(1)向量的基本要素:大小和方向.(2)向量的表示:几何表示法 AB ;字母表示:a ;坐标表示法 a =xi+yj =(x,y). (3)向量的长度:即向量的大小,记作|a |. (4)特殊的向量:零向量a =O ⇔|a |=O .单位向量a O 为单位向量⇔|a O |=1.(5)相等的向量:大小相等,方向相同(x1,y1)=(x2,y2)⎩⎨⎧==⇔2121y y x x(6) 相反向量:a =-b ⇔b =-a ⇔a +b =0(7)平行向量(共线向量):方向相同或相反的向量,称为平行向量.记作a ∥b .平行向量也称为共线向量.3.向量的运算 运算类型几何方法坐标方法运算性质向量的 加法 1.平行四边形法则 2.三角形法则向量的减法三角形法则ABBA =-,AB OA OB =-数 乘向 量1.a λ是一个向量,满足:||||||a a λλ=2.λ>0时, a a λ与同向; λ<0时, a a λ与异向; λ=0时, 0a λ=.向 量 的 数 量积a b ∙是一个数1.00a b ==或时,0a b ∙=.2.00||||cos(,)a b a b a b a b ≠≠=且时,4.重要定理、公式 (1)平面向量基本定理e 1,e 2是同一平面内两个不共线的向量,那么,对于这个平面内任一向量,有且仅有一对实数λ1, λ2,使a =λ1e 1+λ2e 2.(2)两个向量平行的充要条件a ∥b ⇔a =λb (b ≠0)⇔x 1y 2-x 2y 1=O. (3)两个向量垂直的充要条件 a ⊥b ⇔a ·b =O ⇔x 1x 2+y 1y 2=O. (4)线段的定比分点公式设点P 分有向线段21P P 所成的比为λ,即P P 1=λ2PP ,则OP =λ+111OP +λ+112OP (线段的定比分点的向量公式)⎪⎪⎩⎪⎪⎨⎧++=++=.1,12121λλλλy y y x x x (线段定比分点的坐标公式) 当λ=1时,得中点公式:OP =21(1OP +2OP )或 (5)平移公式设点P (x ,y )按向量a =(h,k)平移后得到点P ′(x ′,y ′),则P O '=OP +a 或⎩⎨⎧+='+='.,k y y h x x曲线y =f (x )按向量a =(h,k)平移后所得的曲线的函数解析式为: y -k=f (x -h) (6)正、余弦定理 正弦定理:.2sin sin sin R Cc B b A a === 余弦定理:a 2=b 2+c 2-2bc cos A, b 2=c 2+a 2-2ca cos B , c 2=a 2+b 2-2ab cos C .(7)三角形面积计算公式:设△ABC 的三边为a ,b ,c ,其高分别为h a ,h b ,h c ,半周长为P ,外接圆、内切圆的半径为R ,r . ①S △=1/2ah a =1/2bh b =1/2ch c ②S △=Pr ③S △=abc/4R④S △=1/2sin C ·ab=1/2ac ·sin B=1/2cb ·sin A ⑤S △=()()()c P b P a P P --- [海伦公式] ⑥S △=1/2(b+c-a )r a [如下图]=1/2(b+a-c )r c =1/2(a+c-b )r b[注]:到三角形三边的距离相等的点有4个,一个是内心,其余3个是旁心. 如图: 图1中的I 为S △ABC 的内心, S △=Pr 图2中的I 为S △ABC 的一个旁心,S △=1/2(b+c-a )r a 附:三角形的五个“心”; 重心:三角形三条中线交点.外心:三角形三边垂直平分线相交于一点. 内心:三角形三内角的平分线相交于一点.ABCOabc IA BCDE F IABCD E Fr ar ar ab c aa bc A CBNEF垂心:三角形三边上的高相交于一点.旁心:三角形一内角的平分线与另两条内角的外角平分线相交一点.⑸已知⊙O 是△ABC 的内切圆,若BC =a ,AC =b ,AB =c [注:s 为△ABC 的半周长,即2cb a ++] 则:①AE=a s -=1/2(b+c-a ) ②BN=b s -=1/2(a+c-b ) ③FC=c s -=1/2(a+b-c )综合上述:由已知得,一个角的邻边的切线长,等于半周长减去对边(如图4). 特例:已知在Rt △ABC ,c 为斜边,则内切圆半径r =cb a abc b a ++=-+2(如图3). ⑹在△ABC 中,有下列等式成立C B A C B A tan tan tan tan tan tan =++. 证明:因为,C B A -=+π所以()()C B A -=+πtan tan ,所以C BA BA tan tan tan 1tan tan -=-+,∴结论!⑺在△ABC 中,D 是BC 上任意一点,则DC BD BCBCAB BD AC AD ⋅-+=222.证明:在△ABCD 中,由余弦定理,有 B BD AB BD AB AD cos 2222⋅⋅-+=① 在△ABC 中,由余弦定理有 BC AB AC BC AB B ⋅-+=2cos 222②,②代入①,化简可得,DC BD BCBCAB BD AC AD ⋅-+=222(斯德瓦定理)①若AD 是BC 上的中线,2222221a cb m a -+=; ②若AD 是∠A 的平分线,()a p p bc cb t a -⋅+=2,其中p 为半周长; ③若AD 是BC 上的高,()()()c p b p a p p ah a ---=2,其中p 为半周长.⑻△ABC 的判定:⇔+=222b a c △ABC 为直角△⇔∠A + ∠B =2π2c <⇔+22b a △ABC 为钝角△⇔∠A + ∠B <2π 2c >⇔+22b a △ABC 为锐角△⇔∠A + ∠B >2π 附:证明:abc b a C 2cos 222-+=,得在钝角△ABC 中,222222,00cos c b a c b a C +⇔-+⇔⑼平行四边形对角线定理:对角线的平方和等于四边的平方和.空间向量1.空间向量的概念:具有大小和方向的量叫做向量注:⑴空间的一个平移就是一个向量⑵向量一般用有向线段表示同向等长的有向线段表示同一或相等的向量DACB图5⑶空间的两个向量可用同一平面内的两条有向线段来表示2.空间向量的运算定义:与平面向量运算一样,空间向量的加法、减法与数乘向量运算如下 运算律:⑴加法交换律:a b b a+=+⑵加法结合律:)()(c b a c b a++=++⑶数乘分配律:b a b aλλλ+=+)( 3 共线向量表示空间向量的有向线段所在的直线互相平行或重合,则这些向量叫做共线向量或平行向量.a平行于b 记作b a //.当我们说向量a 、b 共线(或a //b )时,表示a 、b的有向线段所在的直线可能是同一直线,也可能是平行直线.4.共线向量定理及其推论:共线向量定理:空间任意两个向量a 、b (b ≠0 ),a //b 的充要条件是存在实数λ,使a=λb .推论:如果l 为经过已知点A 且平行于已知非零向量a的直线,那么对于任意一点O ,点P 在直线l 上的充要条件是存在实数t 满足等式t OA OP +=a.其中向量a叫做直线l 的方向向量. 5.向量与平面平行:已知平面α和向量a ,作OA a =,如果直线OA 平行于α或在α内,那么我们说向量a 平行于平面α,记作://a α.通常我们把平行于同一平面的向量,叫做共面向量说明:空间任意的两向量都是共面的6.共面向量定理:如果两个向量,a b 不共线,p 与向量,a b 共面的充要条件是存在实数,x y 使p xa yb =+推论:空间一点P 位于平面MAB 内的充分必要条件是存在有序实数对,x y ,使MP xMA yMB =+或对空间任一点O ,有OP OM xMA yMB =++ ① ①式叫做平面MAB 的向量表达式7 空间向量基本定理:如果三个向量,,a b c 不共面,那么对空间任一向量p ,存在一个唯一的有序实数组,,x y z ,使p xa yb zc =++推论:设,,,O A B C 是不共面的四点,则对空间任一点P ,都存在唯一的三个 有序实数,,x y z ,使OP xOA yOB zOC =++8 空间向量的夹角及其表示:已知两非零向量,a b ,在空间任取一点O ,作,OA a OB b ==,则AOB ∠叫做向量a 与b 的夹角,记作,a b <>;且规定0,a b π≤<>≤,显然有,,a b b a <>=<>;若,2a b π<>=,则称a 与b 互相垂直,记作:a b ⊥.9.向量的模:设OA a =,则有向线段OA 的长度叫做向量a 的长度或模,记作:||a . 10.向量的数量积: a b ⋅=||||cos ,a b a b ⋅⋅<>.已知向量AB a =和轴l ,e 是l 上与l 同方向的单位向量,作点A 在l 上的射影A ',作点B 在l 上的射影B ',则A B ''叫做向量AB 在轴l 上或在e 上的正射影.可以证明A B ''的长度||||cos ,||A B AB a e a e ''=<>=⋅. 11.空间向量数量积的性质:(1)||cos ,a e a a e ⋅=<>.(2)0a b a b ⊥⇔⋅=.(3)2||a a a =⋅. 12.空间向量数量积运算律:(1)()()()a b a b a b λλλ⋅=⋅=⋅.(2)a b b a ⋅=⋅(交换律)(3)()a b c a b a c ⋅+=⋅+⋅(分配律).空间向量的坐标运算一.知识回顾:(1)空间向量的坐标:空间直角坐标系的x 轴是横轴(对应为横坐标),y 轴是纵轴(对应为纵轴),z 轴是竖轴(对应为竖坐标).①令a =(a 1,a 2,a 3),),,(321b b b b =,则),,(332211b a b a b a b a ±±±=+))(,,(321R a a a a ∈=λλλλλ332211b a b a b a b a ++=⋅ a ∥)(,,332211R b a b a b a b ∈===⇔λλλλ332211b a b a b a ==⇔0332211=++⇔⊥b a b a b a b a 222321a a a a a a ++=⋅=(用到常用的向量模与向量之间的转化:a a a a a a ⋅=⇒⋅=2)②空间两点的距离公式:212212212)()()(z z y y x x d -+-+-=.(2)法向量:若向量a 所在直线垂直于平面α,则称这个向量垂直于平面α,记作α⊥a ,如果α⊥a 那么向量a 叫做平面α的法向量. (3)用向量的常用方法:①利用法向量求点到面的距离定理:如图,设n 是平面α的法向量,AB 是平面α的一条射线,其中α∈A ,则点B 到平面α的距离为||||n n AB ⋅.②利用法向量求二面角的平面角定理:设21,n n 分别是二面角βα--l 中平面βα,的法向量,则21,n n 所成的角就是所求二面角的平面角或其补角大小(21,n n 方向相同,则为补角,21,n n 反方,则为其夹角).③证直线和平面平行定理:已知直线≠⊄a 平面α,α∈⋅∈⋅D C a B A ,,且CDE 三点不共线,则a ∥α的充要条件是存在有序实数对μλ⋅使CE CD AB μλ+=.(常设CE CD AB μλ+=求解μλ,若μλ,存在即证毕,若μλ,不存在,则直线AB 与平面相交).。
《有机化学基础》重点归纳一、重要的物理性质1.有机物的溶解性:易溶于水的有:低级的[一般指N(C)≤4]醇、醛、羧酸及盐、氨基酸及盐、单糖、二糖。
(它们都能与水形成氢键)。
2.有机物的密度:大于水的密度,且与水(溶液)分层的有:多氯代烃(CCl4等)、溴代烃(溴苯等)、碘代烃、硝基苯3.常温常压为气态的有机物:① 烃类:一般N(C)≤4的各类烃注意:新戊烷[C(CH3)4]亦为气态② 衍生物类:一氯甲烷(....)....HCHO.....CH..3.Cl..).甲醛(4.有机物的颜色☆绝大多数有机物为无色气体或无色液体或无色晶体,少数有特殊颜色,常见的如下所示:☆三硝基甲苯(俗称梯恩梯TNT)为淡黄色晶体;☆部分被空气中氧气所氧化变质的苯酚为粉红色;☆三溴苯酚为白色、难溶于水的固体(但易溶于苯等有机溶剂);☆苯酚溶液与Fe3+(aq)作用形成紫色溶液;☆淀粉溶液遇碘(I2)变蓝色溶液;☆含有苯环的蛋白质溶胶遇浓硝酸会有白色沉淀产生,加热后,沉淀变黄色。
二、重要的反应1.能使溴水(Br2/H2O)褪色的物质(1)有机物①通过加成反应使之褪色:含有、—C≡C—的不饱和化合物②通过取代反应使之褪色:酚类注意:苯酚溶液遇浓溴水时,除褪色现象之外还产生白色沉淀。
③ 通过氧化反应使之褪色:含有—CHO(醛基)的有机物(有水参加反应)注意:纯净的只含有—CHO(醛基)的有机物不能使溴的四氯化碳溶液褪色④通过萃取(物理变化)使之褪色:液态烷烃、环烷烃、苯及其同系物、卤代烃、酯(2)无机物①通过与碱发生歧化反应 Br2 + 2OH- == Br- + BrO- + H2O②与还原性物质发生氧化还原反应,如H2S、S2-、SO2、SO32-、I-、Fe2+2.能使酸性高锰酸钾溶液KMnO4/H+褪色的物质(1)有机物:含有、—C≡C—、—OH、—CHO、苯的同系物(与苯不反应)(2)无机物:与还原性物质发生氧化还原反应,如H2S、S2-、SO2、SO32-、Br-、I-、Fe2+3.与Na反应的有机物:含有—OH、—COOH的有机物与NaOH反应的有机物:常温下,易与含有酚羟基...、—COOH的有机物反应加热时,能与卤代烃、酯反应(水解反应)与Na2CO3反应的有机物:含有酚.羟基的有机物反应生成酚钠和NaHCO3;含有—COOH的有机物反应生成羧酸钠,并放出CO2气体;与NaHCO3反应的有机物:含有—COOH的有机物反应生成羧酸钠并放出等物质的量的CO2气体。
一、各类烃的代表物的结构、特性类别烷烃烯烃炔烃苯及同系物通式C n H2n+2(n≥1) C n H2n(n≥2) C n H2n-2(n≥2) C n H2n-6(n≥6) 代表物结构式H—C≡C—H相对分子质量Mr16 28 26 78碳碳键长(×10-10m)键角109°28′约120°180°120°分子形状正四面体6个原子共平面型4个原子同一直线型12个原子共平面(正六边形)主要化学性质光照下的卤代;裂化;不使酸性KMnO4溶液褪色跟X2、H2、HX、H2O、HCN加成,易被氧化;可加聚跟X2、H2、HX、HCN加成;易被氧化;能加聚得导电塑料跟H2加成;FeX3催化下卤代;硝化、磺化反应二、烃的衍生物的重要类别和各类衍生物的重要化学性质类别通式官能团代表物分子结构结点主要化学性质卤代烃一卤代烃:R—X多元饱和卤代烃:C n H2n+2-m X m卤原子—XC2H5Br(Mr:109)卤素原子直接与烃基结合β-碳上要有氢原子才能发生消去反应水溶液共热发生取代反应生成醇生成烯醇一元醇:R—OH饱和多元醇:C n H2n+2O m醇羟基—OHCH3OH(Mr:32)C2H5OH(Mr:46)羟基直接与链烃基结合,O—H及C—O均有极性。
β-碳上有氢原子才能发生消去反应。
α-碳上有氢原子才能被催化氧化,伯醇氧化为醛,仲醇氧化为酮,叔醇不能被催化氧化。
2卤化氢或浓氢卤酸反应生成卤代烃:乙醇140℃分子间脱水成醚170℃分子内脱水生成烯或酮5.一般断O—H键与羧酸及无机含氧酸反应生成酯醚R—O—R′醚键C2H5O C2H5(Mr:74)C—O键有极性性质稳定,一般不与酸、碱、氧化剂反应酚酚羟基—OH(Mr:94)—OH直接与苯环上的碳相连,受苯环影响能微弱电离。
生成沉淀3呈紫色醛醛基HCHO(Mr:30)(Mr:44)HCHO相当于两个—CHO有极性、能加成。
有机化学复习一、物性1、溶解性:①所有的烃、卤代烃、酯都难溶于水②低级(含C少)的醇、醛、酸易溶于水③高级(含C多)的醇、醛、酸难溶于水④含多个亲水基(-OH、-COOH)的物质易溶于水⑤有机物一般易溶于有机物(相似相溶)。
2、熔沸点:①常温下为气态的有机物C1-C4的烃、 C(CH3)4新戊烷、甲醛(HCHO)、 CH3Cl 、CH3CH2Cl(氯乙烷) 、CH2=CHCl(氯乙烯)②互为同系物的有机物,随着分子中碳原子的增加熔沸点增大③互为同分异构体的烃,结构中支链越多,熔沸点降低3、密度:① 所有的烃、酯的密度比水小② 卤代烃中脂肪烃的一氟代烃、一氯代烃的密度比水小,其余的卤代烃密度比水大(如CCl4、溴乙烷、溴苯的密度比水大)二、结构类别代表物结构特点脂肪烃烷烃CH4正四面体结构(取代反应:取代1个H消耗1个X2) 烯烃CH2=CH2 6个原子处于一个平面二烯烃CH2=CH-CH=CH22个平面以单键连接炔烃CH≡CH 4个原子处于一条直线芳香烃苯12个原子处于一个平面苯的同系物侧链为烷基,苯环只有1个三、性质官能团及名称代表物质主要反应C=C碳碳双键CH2=CH2①CH2=CH2+Br2 CH2BrCH2Br 1,2-二溴乙烷(溴水褪色,发生加成反应)②CH2=CH2+H2O CH3CH2OH(工业制酒精)③CH2=CH2+HCl CH3CH2Cl(原子利用率100%)④使KMnO4(H+)褪色(氧化反应,氧化产物为CO2)⑤nCH2=CH2(加聚反应)C≡C碳碳叁键CH≡CH①CH≡CH+HCl CH2=CHCl (部分加成反应)②CH≡CH+2H2CH3CH3(加成反应)③使KMnO4(H+)褪色(氧化反应)④nCH≡CH(聚乙炔,加聚反应)苯环(不是官能团)苯(易取代难加成能氧化)+ HBr(取代反应)① + Br2② +HO-NO2 + H2O③ + 3H2 (环己烷)(加成反应)苯不能使酸性KMnO4和溴水褪色,但可以萃取溴使原溴水层褪色苯的同系物能使酸性KMnO4褪色(氧化反应)不能使溴水褪色但能萃取溴-X CH3H2Br ①CH3CH2Br +NaOH CH2=CH2↑+ NaBr + H2O②CH3CH2Br +NaOH CH3CH2OH + NaBr③X检验:先加NaOH加热、再加过量HNO3,最后加AgNO3,根据沉淀的颜色确定X是什么-OH (羟基)CH3CH2OH①2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ 2-OH~2Na~H2②2CH3CH2OH+O2 2CH3CHO(乙醛)+2H2O③2CH3CH(OH)CH3+O22CH3COCH3(丙酮)+2H2O(结构要求:α-C上有2个H(-CH2OH)氧化为醛;有1个H氧化为酮;无H不能氧化)④CH3CH2OH CH2=CH2↑+H2O(结构要求:β-C上有H)⑤2CH3CH2OH CH3CH2OCH2CH3+H2O⑥CH3CH2OH+CH3COOH CH3COOCH2CH3+H2O⑦CH3CH2OH+HBr CH3CH2Br+H2O (工业制卤代烃)苯酚①弱酸性:+NaOH→+H2O②+Na2CO3→+NaHCO3③+CO2→+NaHCO3(CO2少量或过量)④(邻对位取代,浓溴水过量)⑤易被氧化⑥遇Fe3+显紫色-CHO (醛基)CH3CHO-CHO → -CH2OH (与H2反应)-CHO → -COOH(与O2、KMnO4(H+)、溴水、银氨溶液、新制Cu(OH)2)①CH3CHO+H2 CH3CH2OH②CH3CHO+2Ag(NH3)2OH CH3COONH4+H2O +2Ag↓+3NH3(-CHO ~ 2Ag)③CH3CHO+2Cu(OH)2+NaOH CH3COONa+Cu2O↓+3H2O(-CHO ~Cu2O)(羰基)CH3COCH3(丙酮)CH3COCH3+H2 CH3CH(OH)CH3-COOH (羧基)CH3COOH酸性(与Na、与NaOH、与Na2CO3、与NaHCO3)、酯化反应(2-COOH ~CO32-~CO2)(-COOH ~HCO3-~CO2)-COO- (酯基)CH3COOCH2CH3①CH3COOCH2CH3+H2O CH3COOH+CH3CH2OH (可逆)②CH3COOCH2CH3+NaOH CH3COONa+CH3CH2OH (不可逆)(-COOR ~NaOH)葡萄糖和多糖:①CH2OH(CHOH)4 CHO+ H2 CH2OH(CHOH)4CH2OH②CH2OH(CHOH)4CHO + 2Ag(NH3)2OH CH2OH(CHOH)4COONH4 + 2Ag↓ + 3NH3 + H2O③CH2OH(CHOH)4CHO + 2Cu(OH)2 +NaOH CH2OH(CHOH)4COONa + Cu2O↓ + 3H2O④C6H12O62CH3CH2OH + 2CO2⑤C12H22O11(蔗糖) + H2O C6H12O6(葡萄糖) + C6H12O6(果糖)⑥C12H22O11(麦芽糖) + H2O 2C6H12O6(葡萄糖)⑦(C6H10O5)n(淀粉) + nH2O n C6H12O6(葡萄糖)⑧(C6H10O5)n (纤维素) + nH2On C6H12O6(葡萄糖)⑨(硝酸纤维素酯) 油脂(油脂的氢化或硬化)(皂化反应)三、重要的反应类型反应类型反应特征典型反应名称取代反应有进有出(类似复分解)卤代反应、硝化反应、酯化反应、水解反应、醇分子间脱水成醚加成反应有进无出C=C、C≡C(与H2、HX、X2、H2O)苯环、羰基、醛基(与H2)消去反应无进有出醇(浓硫酸,170℃)、卤代烃(NaOH醇溶液,加热)氧化反应有机物得O或失H 燃烧、 C=C、C≡C、-CHO、-OH等被KMnO4(H+)、O2等氧化还原反应有机物失O或得H 与H2加成加聚反应打开不饱和键含双键、叁键就能发生加聚。
有机化学基础知识点整理有机化学与化学生物学的关系有机化学基础知识点整理:有机化学与化学生物学的关系有机化学是研究碳元素化合物的结构、性质、合成和反应机理的学科。
随着化学领域的发展,有机化学不仅仅是一门基础学科,也涉及到各个应用领域,其中与化学生物学的关系尤为密切。
本文将对有机化学基础知识点进行整理,并探讨有机化学与化学生物学的关系。
一、碳的化合价碳是有机化合物最基本的元素,其化合价决定了有机化合物的结构和性质。
通常情况下,碳的化合价为4,这意味着一个碳原子可以与其他4个原子或者基团进行共价键的形成,从而形成一系列不同的有机化合物。
二、键的类型与键能有机化合物中常见的键包括单键、双键和三键。
单键由一个σ键组成,双键和三键除了包括σ键外,还包括一个或两个π键。
键的类型决定了分子间的键能大小,从而影响了有机化合物的稳定性和反应性。
三、共轭体系共轭体系是指由相邻的双键或者三键构成的π键所组成的化合物。
共轭体系的存在可以增加分子的稳定性,并影响分子的吸光性质和光谱特征。
共轭体系还可以影响化合物的反应性,如亲电性和自由基反应等。
四、官能团官能团是指有机化合物中具有特殊化学性质的基团。
常见的官能团包括羟基、羰基、羧基、醇基、胺基等。
官能团的存在决定了有机化合物的化学性质和反应性,不同的官能团具有不同的反应性质和反应机制。
五、立体化学立体化学是有机化学中非常重要的一个方向,研究分子的立体构型对其结构和性质的影响。
手性化合物是立体化学的重要内容,它们存在镜像异构体,具有不对称的结构和性质。
手性化合物在生物学中具有重要的作用,如药物的立体选择性和酶的立体选择性。
六、有机合成有机合成是有机化学中的核心内容之一,研究如何通过化学反应来合成目标有机化合物。
有机合成涉及到多种反应类型和合成策略,如取代反应、缩合反应、重排反应等。
有机合成在药物合成、材料合成和天然产物合成等领域具有广泛应用。
有机化学与化学生物学的关系有机化学与化学生物学之间存在着密不可分的关系。