初中化学常见化学用语
- 格式:doc
- 大小:156.50 KB
- 文档页数:3

初中化学全册必背知识点一、化学用语1、常见元素及原子团的名称和符号非金属: O氧 H氢 N氮 Cl氯 C碳 P磷 S硫金属: K钾 Ca钙 Na钠 Mg镁 Al铝 Zn锌 Fe铁 Cu铜 Hg汞 Ag银 Mn锰 Ba钡原子团(根):氢氧根硝酸根碳酸根硫酸根铵根OH- NO3- CO32- SO4 2- NH4+2、(1) 常见元素化合价口诀:一价氯氢钾钠银,二价氧钙钡镁锌,二三铁二四碳,二四六硫都齐全;铜汞二价最常见,三铝四硅五氮磷,单质零价要记清。
(2) 常见原子团(根)化学价口诀:负一硝酸氢氧根,负二硫酸碳酸根,正一价的是铵根。
4、必须熟记的制取物质的化学方程式(1)实验室制取氧气一: 2KMnO4===K2MnO4+MnO2+O2↑(2)实验室制取氧气二: 2H2O2 ===2H2O+O2↑(3) 实验室制取氧气三: 2KClO3===2KCl+3O2↑(4)实验室制法CO2: CaCO3+2HCl==CaCl2+H2O+CO2↑(5)实验室制取氢气: Zn+H2SO4==ZnSO4+H2↑ Zn + 2HCl= ZnCl2 +H2↑(6)电解水制取氢气: 2H2O===2H2↑+O2↑(7)湿法炼铜术(铁置换出铜):Fe+CuSO4==FeSO4+Cu (Fe与盐、酸反应都生成的是+2价亚铁离子)(8)炼铁原理: 3CO+Fe2O3===2Fe+3CO2 (Fe2O3与酸反应生成的是+3价铁离子)(9)熟灰水[Ca(OH)2 ]的制取方法:CaO+H2O==Ca(OH)2(10)生石灰(氧化钙)制取方法:CaCO3 ===CaO+CO2↑二.金属活动性顺序:金属活动性由强至弱: K Ca Na Mg Al , Zn Fe Sn Pb (H) ,Cu Hg Ag Pt Au 。
(按5个一句顺序背诵)钾钙钠镁铝,锌铁锡铅(氢),铜汞银铂金。
三、常见物质的颜色、状态1、黑色固体:炭粉、铁粉、CuO、MnO2、Fe3O42、红色固体:Cu、Fe2O3、红磷▲硫磺:淡黄色▲绿色:碱式碳酸铜(铜锈,俗称铜绿)3、溶液的颜色:含Cu2+的溶液呈蓝色(如CuSO4溶液);含Fe2+的溶液呈浅绿色(如FeCl2溶液);含Fe3+的溶液呈棕黄色(如FeCl3溶液),其余溶液一般为无色。
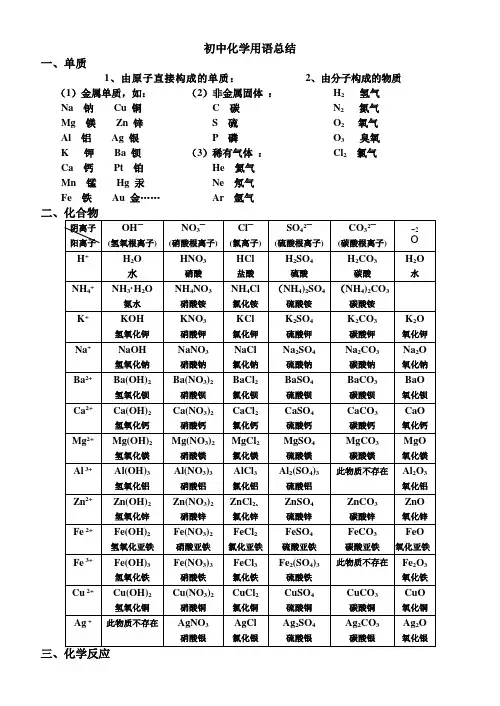
初中化学用语总结一、单质1、由原子直接构成的单质:2、由分子构成的物质(1)金属单质,如:Na 钠Cu 铜Mg 镁Zn 锌Al 铝Ag 银K 钾Ba 钡Ca 钙Pt 铂Mn 锰Hg 汞Fe 铁Au 金……(2)非金属固体:C 碳S 硫P 磷(3)稀有气体:He 氦气Ne 氖气Ar 氩气H2氢气N2氮气O2 氧气O3臭氧Cl2氯气(一)、化合反应:“多变一”1、氯化氢和氨气反应:氯化铵氨气氯化氢−→−+ Cl NH NH HCl 43===+2、红磷燃烧: 五氧化二磷氧气磷点燃−−→−+ 522O P 2O 5P 4点燃+ 3、硫的燃烧: 二氧化硫氧气硫点燃−−→−+ 22SO O S 点燃+ 4、铁在氧气中燃烧:四氧化三铁点燃氧气铁−−→−+ 432O e F O 2e F 3点燃+5、镁的燃烧: 氧化镁氧气镁点燃−−→−+ O Mg 2O 2Mg 2点燃+ 6、铝的燃烧: 氧化铝氧气铝点燃−−→−+ 322O Al 2O 34Al 点燃+7、铜在空气中加热:氧化铜氧气铜加热−−→−+ O Cu 2O Cu 22△+8、氢气的燃烧: 水氧气氢气点燃−−→−+ O H 2O 2H 222点燃+ 9、木炭燃烧: 二氧化碳氧气碳点燃−−→−+ 22CO O C 点燃+ 10、碳在不足量氧气中燃烧:一氧化碳氧气碳点燃−−→−+ CO 2O C 22点燃+ 11、一氧化碳的燃烧:二氧化碳氧气一氧化碳点燃−−→−+ 22CO 2O CO 2点燃+12、二氧化碳溶于水:碳酸水二氧化碳→+13、生石灰遇水反应:氢氧化钙水氧化钙→+(二)、分解反应:“一变多”1、氧化汞加热分解: 氧气汞氧化汞加热+−−→− ↑+2O Hg 2Og H 2△2、过氧化氢催化分解:氧气水过氧化氢二氧化锰+−−−−→− ↑+22O Mn 22O O H 2O 2H 23、高锰酸钾加热分解:氧气二氧化锰锰酸钾高锰酸钾加热++−−→−4、氯酸钾与二氧化锰混合加热:5、电解水: 氢气氧气水通电+−−→− ↑+↑222O H 2O2H 通电6、碳酸分解: 二氧化碳水碳酸+→7、碱式碳酸铜(孔雀石)热分解:水二氧化碳氧化铜碱式碳酸铜加热++−−→−8、电解熔融氧化铝制铝:氧气铝氧化铝通电+−−→− ↑+232O 3Al 4O l A 2通电9、碳酸钙高温分解: 二氧化碳氧化钙碳酸钙高温+−−→− ↑+23CO O a C aCO C 高温(三)、置换反应:“单质+化合物 — 化合物+单质 A+BC — AC+B ”1、 氢气还原氧化铜:铜水氧化铜氢气加热+−−→−+2、 碳还原氧化铜:铜二氧化碳氧化铜碳高温+−−→−+ 金属活动顺序:3、 镁与稀盐酸反应:氢气氯化镁盐酸镁+→+4、 铝与稀盐酸反应:氢气氯化铝盐酸铝+→+5、 锌与稀盐酸反应:氢气氯化锌盐酸锌+→+6、 铁与稀盐酸反应:氢气氯化亚铁盐酸铁+→+7、 镁与稀硫酸反应:氢气硫酸镁稀硫酸镁+→+8、 锌与稀硫酸反应:氢气硫酸锌稀硫酸锌+→+ 9、 铝与稀硫酸反应:氢气硫酸铝稀硫酸铝+→+10、铁与稀硫酸反应:氢气硫酸亚铁稀硫酸铁+→+11、铝与硫酸铜反应:铜硫酸铝硫酸铜铝+→+12、铁与硫酸铜反应:铜硫酸亚铁硫酸铜铁+→+13、铁与氯化铜反应:铜氯化亚铁氯化铜铁+→+(四)、复分解反应:1、氯化钾与硝酸银反应:氯化银硝酸钾硝酸银氯化钾+→+2、盐酸与硝酸银反应:氯化银硝酸硝酸银盐酸+→+3、氧化铜与硫酸反应:水硫酸铜硫酸氧化铜+→+4、氧化镁与硫酸反应:水硫酸镁硫酸氧化镁+→+5、氧化铁与盐酸反应:水氯化铁盐酸氧化铁+→+6、盐酸与氢氧化钠反应:水氯化钠氢氧化钠盐酸+→+7、硫酸与氢氧化钠反应:水硫酸钠氢氧化钠硫酸+→+ 8、硝酸与氢氧化铜反应:水硝酸铜氢氧化铜硝酸+→+9、氯化钡与硫酸反应:水硫酸钡硫酸氯化钡+→+ 9、氯化钡与碳酸钠反应:氯化钠碳酸钡碳酸钠氯化钡+→+10、氢氧化钠硫酸铜反应:硫酸铜氢氧化铜硫酸铜氢氧化钠+→+11、氢氧化钙与氯化铁反应:氯化钙氢氧化铁氯化铁氢氧化钙+→+(五)、其他反应: 1、汽车尾气催化转换:氮气二氧化碳一氧化氮一氧化碳+−−→−+铂、钯22dP t P N CO 2NO2CO 2++,2、二氧化碳与氢氧化钙反应(澄清石灰水变浑浊):水碳酸钙氢氧化钙二氧化碳+→+3、大理石与盐酸反应:二氧化碳水氯化钙盐酸碳酸钙++→+4、甲烷(天然气的主要成分)燃烧:水二氧化碳氧气甲烷点燃+−→−+O H 2CO O 2CH 2224++点燃5、一氧化碳还原氧化铁:二氧化碳铁一氧化碳氧化铁高温+−−→−+ 232CO 32Fe COO e F ++高温6、一氧化碳还原氧化铜:二氧化碳铜一氧化碳氧化铜加热+−−→−+ 2CO u C COCuO ++加热10、碳酸氢铵与氢氧化钙混合:氨气水碳酸钙氢氧化钙碳酸氢铵++→+11、硫酸铵与氢氧化钠溶液混合加热:氨气水硫酸钠氢氧化钠硫酸铵△++−→−+(NH 4)2SO 4+2NaOH Na 2SO 4+ H 2O + NH 3·H 2O7、葡萄糖在酶作用下的反应:水二氧化碳氧气葡萄糖酶+−→−+。

一分耕耘一分收获初中化学全册必背知识点一、化学用语1、常见元素及原子团的名称和符号非金属:O氧H氢N氮Cl氯C碳P磷S硫金属:K钾Ca钙Na钠Mg镁Al铝Zn锌Fe铁Cu铜Hg汞Ag银Mn锰Ba钡原子团 ( 根 ) :氢氧根硝酸根碳酸根硫酸根铵根--OH NO 32-CO 32-+SO4NH 42、 (1) 常见元素化合价口诀:一价氯氢钾钠银,二价氧钙钡镁锌,二三铁二四碳,二四六硫都齐全;铜汞二价最常见,三铝四硅五氮磷,单质零价要记清。
(2)常见原子团 ( 根 ) 化学价口诀:负一硝酸氢氧根,负二硫酸碳酸根,正一价的是铵根。
3、必须熟记的常见物质的俗称、化学名称、化学式、用途俗称化学名称化学式用途金刚石、石墨、木炭等碳单质 C 金刚石做钻头、切割玻璃石墨做铅笔芯、电极干冰二氧化碳固体CO 人工降雨,致冷剂2水水H2O 最常见溶剂铁锈氧化铁Fe2O3生石灰氧化钙CaO 食品干燥剂熟石灰、消石灰(澄清石灰水)氢氧化钙Ca(OH)2 改良酸性土壤石灰石、大理石(蛋壳、水垢等)碳酸钙CaCO 建筑材料、工业制取 CO3 2 火碱、烧碱、苛性钠氢氧化钠NaOH 氢氧化钠固体作干燥剂、化工原料、清洁剂盐酸( 氯化氢 ) HCl 除铁锈、胃酸主要成分纯碱、苏打碳酸钠23玻璃、造纸、纺织、洗涤Na CO碳酸氢钠小苏打 3 发酵粉、治疗胃酸过多NaHCO天然气、沼气、瓦斯甲烷CH4 燃料酒精乙醇C2H5OH 燃料、乙醇汽油4、必须熟记的制取物质的化学方程式(1)实验室制取氧气一: 2KMnO4===K2MnO4+MnO2+O2↑( 2)实验室制取氧气二:2H 2O2 ===2H2O+O2↑(3)实验室制取氧气三: 2KClO 3===2KCl+3O2↑(4)实验室制法 CO2: CaCO3+2HCl==CaCl2+H2O+CO2↑( 5)实验室制取氢气:Zn+H 2SO4==ZnSO4+H2↑ Zn + 2HCl = ZnCl 2 +H2↑(6)电解水制取氢气: 2H 2O===2H↑ +O2↑( 7)湿法炼铜术(铁置换出铜):Fe+CuSO4==FeSO4+Cu(Fe与盐、酸反应都生成的是+2 价亚铁离子)( 8)炼铁原理:3CO+Fe2O3===2Fe+3CO(Fe2O3与酸反应生成的是+3 价铁离子)(9)熟灰水 [Ca(OH) 2 ] 的制取方法: CaO+H2O==Ca(OH)2(10)生石灰 ( 氧化钙 ) 制取方法: CaCO3 ===CaO+CO2↑二.金属活动性顺序:金属活动性由强至弱:K Ca Na Mg Al,Zn Fe Sn Pb (H),Cu Hg Ag Pt Au。

初中化学必背知识点打印版一、化学用语。
1. 元素符号。
- 前20号元素:氢(H)、氦(He)、锂(Li)、铍(Be)、硼(B)、碳(C)、氮(N)、氧(O)、氟(F)、氖(Ne)、钠(Na)、镁(Mg)、铝(Al)、硅(Si)、磷(P)、硫(S)、氯(Cl)、氩(Ar)、钾(K)、钙(Ca)。
- 常见金属元素:铁(Fe)、铜(Cu)、锌(Zn)、银(Ag)、金(Au)、汞(Hg)等。
2. 化学式。
- 单质化学式。
- 金属单质:用元素符号表示,如铁(Fe)、铜(Cu)等。
- 固态非金属单质:一般用元素符号表示,如碳(C)、硫(S)等;但碘(I₂)除外。
- 稀有气体:用元素符号表示,如氦气(He)、氖气(Ne)等。
- 气态非金属单质:在元素符号右下角写上表示分子中所含原子数的数字,如氢气(H₂)、氧气(O₂)、氮气(N₂)等。
- 化合物化学式。
- 书写原则:正价在前,负价在后,根据化合物中正负化合价代数和为零的原则确定原子个数比。
- 例如:水(H₂O),其中氢元素化合价为 + 1,氧元素化合价为 - 2;氯化钠(NaCl),钠元素化合价为+1,氯元素化合价为 - 1。
3. 化学方程式。
- 书写原则。
- 一是必须以客观事实为基础;二是要遵守质量守恒定律,等号两边各原子的种类和数目必须相等。
- 例如:- 镁在空气中燃烧:2Mg + O₂{点燃}{===}2MgO。
- 实验室制取氧气:- 加热高锰酸钾:2KMnO₄{}{===}K₂MnO₄+MnO₂+O₂↑。
- 过氧化氢分解:2H₂O₂{MnO_2}{===}2H₂O+O₂↑。
- 化学方程式的意义。
- 质的方面:表示反应物、生成物和反应条件。
如氢气和氧气在点燃条件下反应生成水。
- 量的方面:- 宏观上:表示反应物、生成物之间的质量比。
在2H₂+O₂{点燃}{===}2H₂O中,氢气、氧气和水的质量比为4:32:36 = 1:8:9。
- 微观上:表示反应物、生成物之间的粒子个数比。

初中化学用语汇总1. 原子:构成分子的最小粒子。
2. 元素:由同种原子组成的物质。
4. 分子:由两个及以上原子组成的不带电荷的粒子。
6. 原子量:一个原子质量单位。
8. 周期表:元素根据其原子核结构的排列方式排列的表格。
9. 金属:具有良好的导电性和热传导性质的物质。
11. 金属元素:处于周期表左侧的元素。
16. 原子核:由质子和中子组成的原子中心部分。
17. 共价键:由电子对共享形成的键。
18. 离子键:带正电荷和负电荷之间的相互作用。
21. 化学键:元素通过共享或转移电子形成的化学物质的力。
22. 化学式:用元素符号表示化合物的组成。
23. 反应物:在化学反应中参与反应的物质。
25. 化学反应:物质之间的化学相互作用。
26. 酸:会释放出氢离子的物质。
28. 盐:由阳离子和阴离子组成的离子化合物。
30. 溶解:由固体或气体转变为液体。
31. 溶质:溶解在溶剂中的物质。
34. 沉淀:在溶液中形成的固体颗粒。
36. 电离:在溶液中将电解质分解为离子。
39. 化学平衡:反应物和生成物在化学反应中达到平衡状态。
40. 配位化合物:由中心金属离子和其它分子和离子中的原子和分子共价结合而成的化合物。
41. 化学式计算:根据化学式计算元素的质量。
42. 摩尔质量:化学式中一个摩尔的质量。
43. 密度:单位体积内的物质质量。
44. 燃烧:化合物与氧气彻底反应的化学反应。
46. 温度:温度代表了物体内部分子的平均运动速度。
47. 热力学系统:研究热和压力与化学反应之间的关系。
48. 热能:热能是物体或系统储存的能量。
49. 热动力学:热的能量学,研究物质内部热运动的规律。
50. 热量:由于温度差异而流动的能量。
51. 热容:物质单位质量的温度变化时吸收或释放的热量。
52. 热传导:热能通过物质的传递。
53. 热平衡:两个物体之间热能的交换达到相同的温度。
54. 热力学第一性原理:能量守恒。
55. 内能:热力学系统内分子内部相互作用引起的能量总和。

初三化学全册必背知识点(精华)初中化学全册必背知识点一、化学用语1、常见元素及原子团的名称和符号非金属: O 氧 H 氢 N 氮 Cl 氯 C 碳 P 磷 S 硫 金属: K 钾 Ca 钙 Na 钠 Mg 镁 Al 铝 Zn 锌 Fe 铁 Cu 铜 Hg 汞 Ag 银 Mn 锰 Ba 钡 原子团(根):氢氧根 硝酸根 碳酸根 硫酸根 铵根 OH - NO 3- CO 32- SO 4 2- NH 4+ 2、(1) 常见元素化合价口诀:一价氯氢钾钠银,二价氧钙钡镁锌,二三铁二四碳,二四六硫都齐全;铜汞二价最常见,三铝四硅五氮磷,单质零价要记清。
(2) 常见原子团(根)化学价口诀:负一硝酸氢氧根,负二硫酸碳酸根,正一价的是铵根。
3、必须熟记的常见物质的俗称、化学名称、化学式、用途俗称化学名称化学式用途金刚石、石墨、木炭等碳单质C 金刚石做钻头、切割玻璃石墨做铅笔芯、电极干冰二氧化碳固体CO 2人工降雨,致冷剂水水H 2O 最常见溶剂铁锈氧化铁Fe 2O 3生石灰氧化钙CaO 食品干燥剂熟石灰、消石灰(澄清石灰水)氢氧化钙Ca(OH)2改良酸性土壤石灰石、大理石(蛋壳、水垢等)碳酸钙CaCO 3建筑材料、工业制取CO 2火碱、烧碱、苛性钠氢氧化钠NaOH 氢氧化钠固体作干燥剂、化工原料、清洁剂盐酸(氯化氢)HCl 除铁锈、胃酸主要成分纯碱、苏打碳酸钠Na 2CO 3玻璃、造纸、纺织、洗涤碳酸氢钠小苏打NaHCO3发酵粉、治疗胃酸过多天然气、沼气、瓦斯甲烷CH4燃料酒精乙醇C2H5OH燃料、乙醇汽油4、必须熟记的制取物质的化学方程式(1)实验室制取氧气一: 2KMnO4===K2MnO4+MnO2+O2↑(2)实验室制取氧气二: 2H2O2 ===2H2O+O2↑(3) 实验室制取氧气三: 2KClO3===2KCl+3O2↑(4)实验室制法CO2: CaCO3+2HCl==CaCl2+H2O+CO2↑(5)实验室制取氢气: Zn+H2SO4==ZnSO4+H2↑ Zn + 2HCl= ZnCl2 +H2↑(6)电解水制取氢气: 2H2O===2H2↑+O2↑(7)湿法炼铜术(铁置换出铜):Fe+CuSO4==FeSO4+Cu (Fe与盐、酸反应都生成的是+2价亚铁离子)(8)炼铁原理:3CO+Fe2O3===2Fe+3CO2 (Fe2O3与酸反应生成的是+3价铁离子)(9)熟灰水[Ca(OH)2 ]的制取方法:CaO+H2O==Ca(OH)2(10)生石灰(氧化钙)制取方法:CaCO3 ===CaO+CO2↑二.金属活动性顺序:金属活动性由强至弱: K Ca Na Mg Al , Zn Fe SnPb (H) ,Cu Hg Ag Pt Au 。
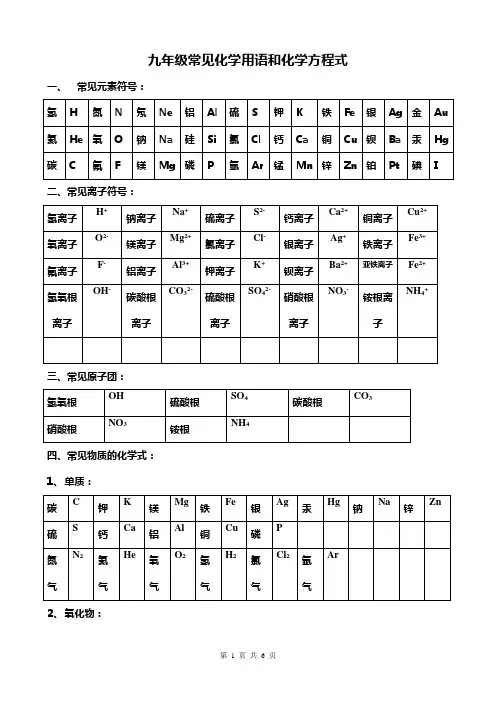
九年级常见化学用语和化学方程式五、课本中的化学方程式:第二单元:1、红磷在氧气中燃烧4 P + 5 O2 2 P2O52、碳在氧气中燃烧 C + O2CO23、硫在氧气中燃烧S + O2 SO24、铁在氧气中燃烧 3 Fe + 2 O2Fe3O45、铝在氧气中燃烧 4 Al + 3 O2 2 Al2O36、用过氧化氢制氧气 2 H2O2 2 H2O + O2↑7、用高锰酸钾制氧气2KMnO4K2MnO4+ MnO2+ O2↑8、用氯酸钾和二氧化锰的混合物制氧气 2 KClO3 2 KCl + 3 O2↑第三单元:9、水通电分解(电解水) 2 H2O 2 H2↑+ O2↑10、汞受热2Hg+O22HgO11、氧化汞受热分解2HgO2Hg+O2↑12、氢气在空气中燃烧 2 H2 + O2 2 H2O13、氢气还原氧化铜H2 + CuO Cu + H2O第四单元:第五单元:14、铁和硫酸铜溶液反应Fe + CuSO 4FeSO4 + Cu15、碳酸钠和盐酸反应Na 2CO3+2HCl2NaCl+H2O+CO2↑16、镁条在空气中燃烧 2 Mg + O2 2 MgO17、高温煅烧石灰石(二氧化碳的工业制法)CaCO3CaO + CO2↑第六单元:2 CO18、碳在氧气中不充分燃烧 2 C + O2 (不足)19、碳跟氧化铜反应 C + 2 CuO 2 Cu + CO2↑20、碳跟氧化铁反应 3 C + 2 Fe2O3 4 Fe + 3 CO2 ↑21、碳跟二氧化碳反应C+CO22CO+ 2HCl CaCl2 + CO2↑+ H2O22、实验室制取二氧化碳CaCO23、二氧化碳与水反应CO 2 + H2O H2CO324、碳酸分解H 2CO3CO2 ↑+ H2O25、二氧化碳与氢氧化钙溶液反应(二氧化碳的检验方法)CO 2 + Ca(OH)2CaCO3↓+ H2O26、一氧化碳燃烧 2 CO + O2 2 CO227、一氧化碳还原氧化铜CO +CuO Cu + CO228、一氧化碳还原氧化铁 3 CO +Fe2O3 2 Fe + 3 CO2第七单元:29、甲烷燃烧CH4 + 2 O2CO2 + 2 H2O30、酒精燃烧C2H5OH + 3 O2 2 CO2 + 3 H2O第八单元:31、镁和稀盐酸反应镁和稀硫酸反应Mg + 2 HCl MgCl+ H2↑Mg + H2SO4MgSO4 + H2↑32、锌和稀盐酸反应锌和稀硫酸反应(实验室制取氢气)Zn + 2 HCl ZnCl+ H2↑Zn + H2SO4ZnSO4 + H2↑33、铁和稀盐酸反应铁和稀硫酸反应+ H2↑Fe + H2SO4FeSO4 + H2↑Fe + 2 HCl FeCl34、铝和稀盐酸反应铝和稀硫酸反应+3H2↑2Al+ 3H2SO4Al2(SO4)3 +3 H2↑2Al+6HCl2AlCl35、铝和硫酸铜溶液反应 2 A l + 3 CuSO 4Al2(SO4)3 + 3CuCu(NO3)2 + 2 Ag36、铜和硝酸银溶液反应Cu + 2 AgNO第十单元:37、铁锈与稀盐酸反应铁锈与稀硫酸反应FeO3+6HCl2FeCl3+3H2O Fe2O3+3H2SO4Fe2(SO4)3+3H2O38、氧化铜与稀硫酸反应H2SO4+ CuO Cu SO4+ H2O39、氧化钙与水的反应CaO+HO Ca(OH)240、氢氧化钠溶液与二氧化碳反应2NaOH+CO 2Na2CO3+H2O41、二氧化硫与氢氧化钠溶液反应2NaOH+SO 2Na2SO3+H2O42、三氧化硫与氢氧化钠溶液反应2NaOH+SO 3Na2SO4+H2O43、氢氧化钠与盐酸反应氢氧化钠与硫酸反应NaOH+HCl NaCl+H 2O 2NaOH+H2SO4Na2SO4+H2O44、氢氧化钙与盐酸反应氢氧化钙与硫酸反应+2HCl CaCl2+2H2O Ca(OH)2+H2SO4CaSO4+2H2OCa(OH)第十一单元:45、碳酸氢钠与盐酸反应NaHCO 3+HCl NaCl+H2O+CO2↑CO3+Ca(OH)2CaCO3↓+2NaOH46、碳酸钠溶液与氢氧化钙溶液反应Na初中化学常见物质的颜色(后面是物质化学式或物质名称,前面是颜色)1. 常见物质的颜色:多数气体为无色,多数固体化合物为白色,多数溶液为无色。

初中化学必背知识点化学是一门充满神奇和奥秘的学科,对于初中生来说,掌握一些必背的知识点是学好化学的基础。
以下就为大家梳理一下初中化学中的重要知识点。
一、化学用语1、元素符号要记住常见元素的符号,如氢(H)、氧(O)、碳(C)、氮(N)、钠(Na)、镁(Mg)、铝(Al)等。
元素符号不仅表示一种元素,还能表示这种元素的一个原子。
2、化学式用元素符号表示物质组成的式子叫化学式。
例如,水的化学式为H₂O,表示一个水分子由两个氢原子和一个氧原子构成。
氧气的化学式为 O₂,二氧化碳的化学式为 CO₂。
3、化学方程式用化学式来表示化学反应的式子叫化学方程式。
例如,氢气燃烧生成水的化学方程式为:2H₂+ O₂点燃 2H₂O 。
书写化学方程式要遵循质量守恒定律,即反应前后原子的种类、数目和质量不变。
二、物质的性质和变化1、物理变化和化学变化物理变化是没有生成新物质的变化,比如水的蒸发、玻璃的破碎等。
化学变化是生成新物质的变化,比如铁的生锈、蜡烛的燃烧等。
2、物理性质和化学性质物理性质是物质不需要发生化学变化就表现出来的性质,如颜色、状态、气味、熔点、沸点、硬度、密度等。
化学性质是物质在化学变化中表现出来的性质,如可燃性、氧化性、还原性、酸碱性等。
三、常见的物质1、空气空气的成分按体积计算,大约是氮气 78%、氧气 21%、稀有气体094%、二氧化碳 003%、其他气体和杂质 003%。
氧气能支持燃烧和供给呼吸,氮气化学性质不活泼,可用作保护气。
2、水水是由氢、氧两种元素组成的无机物。
电解水实验证明了水是由氢元素和氧元素组成的,化学方程式为:2H₂O 通电 2H₂↑ + O₂↑ 。
3、氧气氧气是一种无色无味的气体,不易溶于水,密度比空气略大。
氧气具有氧化性,能支持燃烧和供给呼吸。
实验室制取氧气的方法有加热高锰酸钾、分解过氧化氢溶液等。
4、二氧化碳二氧化碳是一种无色无味的气体,能溶于水,密度比空气大。
它能使澄清石灰水变浑浊,化学方程式为:CO₂+ Ca(OH)₂= CaCO₃↓+ H₂O 。

初三化学常化学用语必背“化学是一门记忆加实验的科学”,这也许不太符合一些同学的思维习惯。
下面是小偏整理的初三化学常化学用语必背,感谢您的每一次阅读。
初三化学常化学用语必背一、熟记下列元素名称及符号: 1、H氢O氧 N氮 Cl氯 C碳 P 磷 S硫 2、K钾 Ca钙 Na钠 Mg镁 Al铝 Zn锌 Fe铁 Cu铜 Hg汞 Ag 银 Mn锰 Ba钡二、熟记下列物质的化学式: 1、单质: H2氢气 O2氧气 N2氮气 C碳 P磷 S硫 Fe铁 Cu铜 Hg汞 2、化合物 (1)氧化物:H2O水CO2二氧化碳CO一氧化碳SO2二氧化硫SO3三氧化硫P2O5五氧化二磷 Fe2O3氧化铁Fe3O4四氧化三铁 CaO氧化钙 MgO氧化镁 CuO氧化铜 ZnO氧化锌 FeO氧化亚铁MnO2二氧化锰-Na2O氧化钠(2)酸:HCl盐酸H2SO4硫酸HNO3硝酸 H2CO3碳酸 -H2SO3亚硫酸(3)碱:NaOH氢氧化钠KOH氢氧化钾Ca(OH)2氢氧化钙Ba(OH)2氢氧化钡 Cu(OH)2氢氧化铜Fe(OH)3氢氧化铁Fe(OH)2氢氧化亚铁Al(OH)3氢氧化铝Mg(OH)2氢氧化镁(4)盐:NaCl氯化钠Na2CO3碳酸钠NaHCO3碳酸氢钠 CaCO3碳酸钙 CaCl2氯化钙 KCl氯化钾ZnCl2氯化锌AgCl氯化银FeCl3氯化铁FeCl2氯化亚铁AlCl3氯化铝 BaCl2氯化钡 Na2SO4硫酸钠CuSO4硫酸铜FeSO4硫酸亚铁Fe2(SO4)3硫酸铁ZnSO4硫酸锌BaSO4硫酸钡KClO3氯酸钾KMnO4高锰酸钾K2MnO4锰酸钾KNO3硝酸钾 Ag NO3硝酸银 Cu(NO3)2硝酸铜-NH4Cl氯化铵-NH4NO3硝酸铵-(NH4)2SO4硫酸铵- NH4HCO3碳酸氢铵(5)有机物:CH4甲烷C2H5OH乙醇(酒精) C6H12O6葡萄糖(C6H10O5)n淀粉 -CO(NH2)2尿素三、熟记下列元素在化合物中的化合价:(1) 正价(多为金属)+1 +1 +1 +1 +2 +2 +2 +2 +2 +3 +2 +3 H K Na Ag Ca Mg Zn Ba Cu Al Fe(FeO) Fe(Fe2O3) (2) 负价(非金属)-2 -1 -2 O Cl S (3) 原子团+1 -1 -1 -1 -1 -2 -2 -2 -3 -1 NH4 OH NO3 ClO3 MnO4(KMnO4) CO3 SO4 SO3 PO4 HCO3四、熟记下列常用离子(比较与相应化合价的联系)(1)阳离子H+ K+ Na+ Ca2+ Fe2+ Mg2+ Cu2+ Fe3+(2)阴离子Cl- OH - NO3- CO32- SO4 2-五、熟记下列化学方程式:(一)化合反应(A+B→C):1、木炭在氧气中燃烧:C+O2 点燃CO2 2、硫在氧气中燃烧:S+O2 点燃SO2 3、镁在空气中燃烧:2Mg+O2 点燃 2MgO 4、铁在氧气中燃烧: 3Fe+2O2 点燃 Fe3O4 5、磷在氧气中燃烧:4P+5O2 点燃2P2O5 6、铜在空气中加热:2Cu+O2 △ 2CuO 7、氢气在氧气中燃烧:2H2+O2 点燃 2H2O8、一氧化碳在空气中燃烧:2CO+O2 点燃2CO2 9、碳不充分燃烧:2C+O2(不充分)点燃2CO 10、二氧化碳通过灼热的碳层:CO2 + C 高温2CO 11、二氧化碳与水反应:CO2+H2O === H2CO3-12、三氧化硫溶于水:SO3+H2O === H2SO4 (酸雨的成因)13、生石灰和水化合:CaO+H2O === Ca(OH)2(二)分解反应(C→A+B):14 过氧化氢用二氧化锰作催化剂分解(实验室制O2):2H2O2 2 H2O + O2↑15、氯酸钾与二氧化锰共热(实验室制O2):2KClO3 2KCl+3O2↑ 16、加热高锰酸钾:2KMn O4 △ K2MnO4 + MnO2 + O2↑ 17、电解水:2H2O通电2H2↑ + O2↑18、碳酸不稳定分解:H2CO3 === H2O + CO2↑19、高温煅烧石灰石:CaCO3 高温 CaO + CO2↑-20、氢氧化铜受热分解:Cu(OH)2 △ CuO + H2O(三)置换反应(A+BC→B+AC):21、锌和稀硫酸反应(实验室制H2):Zn+H2SO4 === ZnSO4 + H2↑ 22、锌和盐酸的反应:Zn+2HCl === ZnCl2 + H2↑ 23、铁和盐酸: Fe+2HCl === FeCl2 + H2↑ 24、铁和稀硫酸:Fe+H2SO4 === FeSO4 + H2↑ 25、氢气还原氧化铜:H2+CuO △ Cu + H2O26、氢气还原氧化铁:3H2 + Fe2O3 △ 2Fe + 2H2O27、木炭还原氧化铜:C+2CuO高温2Cu + CO2↑ 28、焦碳还原氧化铁:3C+2Fe2O3 高温4Fe+3CO2↑ 29、铁和硫酸铜溶液:Fe + CuSO4 === Cu + FeSO4 30、铜和硝酸银溶液:Cu + 2AgNO3 === 2Ag + Cu(NO3)231、铝和稀硫酸:2Al+3H2SO4 === Al2(SO4)3 + 3H2↑32、铝和硫酸铜溶液:2Al + 3CuSO4 === 3Cu + Al2(SO4)3-33、钠和水反应:2Na+2H2O === 2NaOH+H2↑(四)复分解反应(AB+CD→AD+CB):34、大理石和稀盐酸(实验室制CO2):CaCO3 + 2HCl === CaCl2 + H2O + CO2↑ 35、碳酸钠和盐酸(灭火器原理):Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑36、碳酸氢钠和盐酸:NaHCO3 + HCl === NaCl + H2O + CO2↑37、碳酸钾(草木灰)和盐酸:K2CO3 + 2HCl === 2KCl + H2O + CO2↑38、盐酸和氢氧化钠(中和反应):HCl + NaOH === NaCl + H2O 39、硫酸和氢氧化钠溶液:H2SO4 + 2NaOH === Na2SO4 + 2H2O 40、硫酸与氯化钡溶液:H2SO4 + BaCl2 === BaSO4↓(白)+ 2HCl 41、盐酸与硝酸银溶液:HCl + AgN O3 === AgCl↓(白)+ HNO342、氢氧化钠和硫酸铜:2NaOH+CuSO4 === Cu(OH)2↓(蓝色) + Na2SO443、氢氧化钠和氯化铁溶液:3NaOH+FeCl3 === Fe(OH)3↓(红褐色)+ 3NaCl44、碳酸钠和石灰水:Na2CO3 + Ca(OH)2 === CaCO3↓ + 2NaOH45、硫酸钠和氯化钡:Na2SO4 + BaCl2 === BaSO4↓ + 2NaCl 46、氯化钠和硝酸银:NaCl + AgNO3 === AgCl↓ + NaNO347、氢氧化铝和盐酸(中和胃酸):Al(OH)3 + 3HCl === AlCl3 + 3H2O 48、氢氧化镁和盐酸(去除水垢):Mg(OH)2 + 2HCl === MgCl2 + 2 H2O 49、盐酸除铁锈:Fe2O3 + 6HCl === 2FeCl3 + 3H2O 50、氧化铜和硫酸:CuO + H2SO4 === CuSO4 + H2O -51、硝酸铵和氢氧化钠:NH4NO3 + NaOH △ NaNO3 + H2O + NH3↑(五)其他:52、二氧化碳使澄清石灰水变浑浊(实验室用于鉴定CO2):CO2 + Ca(OH)2 === CaCO3↓ + H2O 53、二氧化碳通入氢氧化钠溶液(实验室用于吸收CO2): CO2 + 2NaOH === Na2CO3 + H2O 54、用氢氧化钠溶液吸收三氧化硫:SO3 + 2NaOH === Na2SO4 + H2O 55、一氧化碳还原氧化铜:CO + CuO △ Cu + CO256、一氧化碳还原氧化铁(炼铁):3CO + Fe2O3 高温 2Fe + 3CO257、甲烷在空气中燃烧:CH4 + 2O2 点燃 CO2 + 2H2O 58、乙醇在空气中燃烧:C2H5OH+3O2 点燃 2CO2+3H2O-59、葡萄糖在人体组织中氧化:C6H12O6 + 6O2 =酶6CO2+6H2O化学学习经典方法技巧一:形成网络,优化忆技巧二:突出关键,浓缩记忆技巧三:分析对比,理解记忆技巧四:形象比喻,增强记忆技巧五:口诀韵语,灵活记忆技巧六:前后联想,巩固记忆“化学是一门记忆加实验的科学”,这也许不太符合一些同学的思维习惯。

初中化学方程式总结一、化合反应:“多变一”2、红磷燃烧:522O P 2O 5P 4点燃+3、硫的燃烧:22SO O S 点燃+4、铁在氧气中燃烧:432O e F O 2e F 3点燃+5、镁的燃烧:O Mg 2O 2Mg 2点燃+6、铝的燃烧:322O Al 2O 34Al 点燃+7、铜在空气中加热:O Cu 2O Cu 22△+8、氢气的燃烧:O H 2O 2H 222点燃+9、木炭燃烧:22CO O C 点燃+10、碳在不足量氧气中燃烧:CO 2O C 22点燃+11、一氧化碳的燃烧:22CO 2O CO 2点燃+12、二氧化碳溶于水:13、生石灰遇水反应:二、分解反应:“一变多”1、氧化汞加热分解: 氧气汞氧化汞加热+−−→− ↑+2O Hg 2Og H 2△ 2、过氧化氢催化分解:氧气水过氧化氢二氧化锰+−−−−→− ↑+22O Mn 22O O H 2O 2H 23、高锰酸钾加热分解:氧气二氧化锰锰酸钾高锰酸钾加热++−−→− 4、氯酸钾与二氧化锰混合加热:5、电解水: 氢气氧气水通电+−−→− ↑+↑222O H 2O2H 通电6、碳酸分解: 二氧化碳水碳酸+→7、碱式碳酸铜(孔雀石)热分解:水二氧化碳氧化铜碱式碳酸铜加热++−−→−8、电解熔融氧化铝制铝:氧气铝氧化铝通电+−−→− ↑+232O 3Al 4O l A 2通电9、碳酸钙高温分解: 二氧化碳氧化钙碳酸钙高温+−−→− ↑+23CO O a C aCO C 高温 10、碳酸氢钠分解:氧气铝氧化铝通电+−−→− ↑++22323CO Na 2Na CO O H HCO V11、碳酸氢铵分解: 二氧化碳氧化钙碳酸钙高温+−−→− ↑+2O Hg 2Og H 2△(三)、置换反应:“单质+化合物 — 化合物+单质 A+BC — AC+B ”1、 氢气还原氧化铜:铜水氧化铜氢气加热+−−→−+2、 碳还原氧化铜:铜二氧化碳氧化铜碳高温+−−→−+3、 氢气还原氧化铁:铜二氧化碳氧化铜碳高温+−−→−+4、 碳还原氧化铁:铜二氧化碳氧化铜碳高温+−−→−+金属活动顺序:5、 镁与稀盐酸反应:氢气氯化镁盐酸镁+→+6、 铝与稀盐酸反应:氢气氯化铝盐酸铝+→+7、 锌与稀盐酸反应:氢气氯化锌盐酸锌+→+8、 铁与稀盐酸反应:氢气氯化亚铁盐酸铁+→+9、 镁与稀硫酸反应:氢气硫酸镁稀硫酸镁+→+10、 锌与稀硫酸反应:氢气硫酸锌稀硫酸锌+→+11、 铝与稀硫酸反应:氢气硫酸铝稀硫酸铝+→+10、铁与稀硫酸反应:氢气硫酸亚铁稀硫酸铁+→+11、铝与硫酸铜反应:铜硫酸铝硫酸铜铝+→+12、铁与硫酸铜反应:铜硫酸亚铁硫酸铜铁+→+13、铁与氯化铜反应:铜氯化亚铁氯化铜铁+→+(四)、复分解反应:1、氯化钾与硝酸银反应:氯化银硝酸钾硝酸银氯化钾+→+2、盐酸与硝酸银反应:氯化银硝酸硝酸银盐酸+→+3、氧化铜与硫酸反应:水硫酸铜硫酸氧化铜+→+4、氧化镁与硫酸反应:水硫酸镁硫酸氧化镁+→+5、氧化铁与盐酸反应:水氯化铁盐酸氧化铁+→+6、盐酸与氢氧化钠反应:水氯化钠氢氧化钠盐酸+→+7、硫酸与氢氧化钠反应:水硫酸钠氢氧化钠硫酸+→+8、硝酸与氢氧化铜反应:水硝酸铜氢氧化铜硝酸+→+9、氯化钡与硫酸反应:水硫酸钡硫酸氯化钡+→+9、氯化钡与碳酸钠反应:氯化钠碳酸钡碳酸钠氯化钡+→+10、氢氧化钠硫酸铜反应:硫酸铜氢氧化铜硫酸铜氢氧化钠+→+11、氢氧化钙与氯化铁反应:氯化钙氢氧化铁氯化铁氢氧化钙+→+(五)、其他反应:1、汽车尾气催化转换:氮气二氧化碳一氧化氮一氧化碳+−−→−+铂、钯 22d P t P N CO 2NO2CO 2++,2、二氧化碳与氢氧化钙反应(澄清石灰水变浑浊):水碳酸钙氢氧化钙二氧化碳+→+3、大理石与盐酸反应:二氧化碳水氯化钙盐酸碳酸钙++→+4、甲烷(天然气的主要成分)燃烧:水二氧化碳氧气甲烷点燃+−→−+O H 2CO O 2CH 2224++点燃5、一氧化碳还原氧化铁: 二氧化碳铁一氧化碳氧化铁高温+−−→−+ 232CO 32Fe COO e F ++高温 6、一氧化碳还原氧化铜:二氧化碳铜一氧化碳氧化铜加热+−−→−+ 2CO u C CO CuO ++加热10、碳酸氢铵与氢氧化钙混合:氨气水碳酸钙氢氧化钙碳酸氢铵++→+11、硫酸铵与氢氧化钠溶液混合加热:氨气水硫酸钠氢氧化钠硫酸铵△++−→−+(NH 4)2SO 4+2NaOH Na 2SO 4+ H 2O + NH 3·H 2O7、葡萄糖在酶作用下的反应:水二氧化碳氧气葡萄糖酶+−→−+。

初中化学常用词组大全
1. 溶解:固体在液体中消失,称为溶解,如糖溶于水中。
2. 水溶性:物质在水中溶解的能力,称为水溶性。
3. 不溶性:物质不能在水中完全溶解,称为不溶性。
4. 沸点:液态物质在给定的压力下从液体变为气体的温度,称为沸点。
5. 密度:物体单位体积的质量。
6. 酸性:具有酸性的物质的水溶液有酸味、能腐蚀金属并使植物染色。
7. 碱性:具有碱性的物质的水溶液有苦味、具有腐蚀性并容易吸收水分。
8. 中性:不呈酸性或碱性的状态。
9. 化学反应:物质经过变化生成新物质的过程。
10. 氧化:物质失去电子或氢原子的过程。
11. 还原:物质获得电子或氢原子的过程。
12. 合成反应:多个物质反应生成新物质的过程。
13. 分解反应:化合物分解成两个或更多的物质的反应。
14. 烷烃:由碳和氢组成的一类物质,包括甲烷、乙烷等。
15. 烯烃:由碳和氢组成的一类物质,分子中有一个或多个碳
双键,包括乙烯、丙烯等。
16. 炔烃:由碳和氢组成的一类物质,分子中有三条及以上的碳—碳三键,包括乙炔、丙炔等。
17. 离子:原子或单原子离子失去或获得电子形成的带电粒子。
18. 离子键:由正负离子间的静电相互作用形成的化学键。
19. 共价键:两个原子通过共用它们的价电子对形成的化学键。
20. 化合价:化学元素与其他化学元素化合时所能借出的电子
数或能接受的电子数的最大值。
21. 分子式:化合物分子中各元素原子的种类、数目与相对位
置表达式。
51.铝和稀盐酸2Al + 6HCl =2AlCl3 + 3 H2↑(3)金属单质 + 盐(溶液) ------- 新金属 + 新盐52. 铁和硫酸铜溶液反应:Fe + CuSO4 = FeSO4 + Cu53. 锌和硫酸铜溶液反应:Zn + CuSO4 =ZnSO4 + Cu54. 铜和硝酸汞溶液反应:Cu + Hg(NO3)2= Cu(NO3)2 + Hg(3)金属铁的治炼原理:55.3CO+ 2Fe2O3高温 4Fe + 3CO2↑七、酸、碱、盐56. 氧化铁和稀盐酸反应:Fe2O3 + 6HCl =2FeCl3 + 3H2O57. 氧化铁和稀硫酸反应:Fe2O3 + 3H2SO4 =Fe2(SO4)3 + 3H2O58. 氧化铜和稀盐酸反应:CuO + 2HCl =CuCl2 + H2O59. 氧化铜和稀硫酸反应:CuO + H2SO4 =CuSO4 + H2O(3)酸 + 碱 -------- 盐 + 水(中和反应)60.盐酸和烧碱起反应:HCl + NaOH = NaCl +H2O61. 盐酸和氢氧化钙反应:2HCl + Ca(OH)2 = CaCl2 + 2H2O62. 氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 = AlCl3 + 3H2O63. 硫酸和烧碱反应:H2SO4 + 2NaOH =Na2SO4 + 2H2O(4)酸 + 盐 -------- 另一种酸 + 另一种盐64.大理石与稀盐酸反应:CaCO3 + 2HCl = CaCl2 + H2O + CO2↑65.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑66.碳酸氢钠与稀盐酸反应:NaHCO3 + HCl= NaCl + H2O + CO2↑67. 硫酸和氯化钡溶液反应:H2SO4 + BaCl2 == BaSO4 ↓+ 2HCl 2、碱的化学性质(1)碱 + 非金属氧化物 -------- 盐 + 水68.苛性钠暴露在空气中变质:2NaOH + CO2 = Na2CO3 + H2O 69.苛性钠吸收二氧化硫气体:2NaOH + SO2 =Na2SO3 + H2O 70.苛性钠吸收三氧化硫气体:2NaOH + SO3 = Na2SO4 + H2O 71.消石灰放在空气中变质:Ca(OH)2 + CO2 = CaCO3↓+ H2O72. 消石灰吸收二氧化硫:Ca(OH)2 + SO2 = CaSO3↓+ H2O(2)碱 + 酸-------- 盐 + 水(中和反应,方程式见上)(3)碱 + 盐 -------- 另一种碱 + 另一种盐73. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 =CaCO3↓+ 2NaOH3、盐的化学性质(1)盐(溶液) + 金属单质------- 另一种金属 + 另一种盐74. 铁和硫酸铜溶液反应:Fe + CuSO4 = FeSO4 + Cu(2)盐 + 酸-------- 另一种酸 + 另一种盐75.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl =2NaCl + H2O + CO2↑碳酸氢钠与稀盐酸反应:NaHCO3 + HCl= NaCl + H2O + CO2↑(3)盐 + 碱 -------- 另一种碱 + 另一种盐76. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 =CaCO3↓+ 2NaOH (4)盐 + 盐 ----- 两种新盐77.氯化钠溶液和硝酸银溶液:NaCl + AgNO3 =AgCl↓ + NaNO3 78.硫酸钠和氯化钡:Na2SO4 + BaCl2 == BaSO4↓ + 2NaCl。
初中化学必背知识点
一、化学用语
1、原子:由核、电子及中子等构成的最小的原子粒子。
2、元素:不可分解的物质,其中包括质子、中子等原子核粒子。
3、分子:原子之间相互结合成的最小的化学单位,也可以是否定离子。
4、化合物:由不同的原子构成的物质,由不同的元素组成的分子。
5、混合物:是由不同的纯物质(元素或化合物)混合而成的物质。
6、溶液:是溶解物以不等的比例混合而成的物质,溶解度可以被称
为浓度。
7、反应物:是参加化学反应的各种原料,它们在反应过程中的相对
位置可以用方程式表示。
8、生成物:是反应的结果,它们与反应物在化学方程式中拥有相同
的位置。
9、滴定:是一种用来测定特定溶液中其中一种物质含量的实验方法,它可以用滴定液的滴定曲线来表示。
10、量热:是一种用来测量特定物质吸热或放热能力的实验方法,它
可以用量热曲线来表示。
二、基本概念
1、原子的构成:原子由核、电子及中子等组成,电子质量很小,但占原子质量的很大一部分,核是很小的一部分,但质量是原子质量中的一大部分,中子是原子质量中的一部分。
2、原子核的结构:原子核的结构可以用质子和中子的模型来表示,原子核中的质子数量与原子序数相等,而中子的数量则取决于原子序数与元素类型。
初中化学用语一、元素符号元素符号就像是化学世界里每个元素的小名片。
比如说氧元素,它的符号是“O”,这小小的字母可代表着咱们呼吸离不开的氧气哦。
还有氢元素“H”,这可是组成水的重要元素呢。
记忆元素符号的时候呀,就像认识新朋友,多和它们打打交道就熟悉啦。
咱们可以编一些小口诀来记,像“氧是O,氮是N,镁的符号Mg真迷人”,这样俏皮的口诀,是不是让元素符号的记忆变得轻松又好玩啦?而且元素符号可是写化学方程式的基础呢,就像盖房子的小砖块,缺了它们可不行。
二、化学式化学式呢,就像是元素们组合在一起的小家庭的名字。
像水的化学式是H₂O,这表示一个水分子是由两个氢原子和一个氧原子组成的。
你看,这就像一个小家庭里有两个氢宝宝和一个氧妈妈。
二氧化碳的化学式是CO₂,这就告诉我们一个二氧化碳分子里有一个碳原子和两个氧原子。
在写化学式的时候呀,我们要遵循一定的规则,化合价就是这个规则里很重要的一部分呢。
就像在这个化学小家庭里,每个元素都有自己的地位和价值,这个价值就体现在化合价上啦。
如果化合价搞错了,那这个化学式可就写错啦,就像给人家小家庭乱起名字一样,可不行哦。
三、化学方程式化学方程式可算是化学用语里的大明星啦。
它就像一个故事,讲述了化学反应是怎么发生的。
比如说氢气和氧气反应生成水的化学方程式2H₂+O₂=2H₂O。
这个方程式就像在说,两个氢气小家庭和一个氧气小家庭在一起发生了奇妙的变化,最后变成了两个水小家庭。
在化学方程式里,等号左边的是反应物,就像故事的开头;等号右边的是生成物,那就是故事的结尾啦。
而且化学方程式要遵循质量守恒定律呢,就像在这个故事里,原子的种类和数目可不能变,就像参加派对的人数不能突然变多或者变少一样。
我们在写化学方程式的时候,要先把反应物和生成物的化学式写对,然后再根据质量守恒定律去配平。
这就像搭积木一样,要一块一块地搭好,让两边的原子数目相等,这样化学方程式才是正确的呢。
四、离子符号离子符号也很有意思哦。
初一化学用语归纳总结化学作为一门科学,研究物质的性质、结构、组成和变化规律,是初中阶段学生学习的重要科目之一。
在初一化学学习中,我们接触到了许多基础的化学用语。
本文将对初一化学学习中常见的用语进行归纳总结,以帮助初中生更好地掌握化学知识。
一、物质的分类1.元素:构成物质的基本单位,无法分解成其他物质。
例如氧气(O2)、氢气(H2)等。
2.化合物:由两种或两种以上元素化合而成的物质。
例如水(H2O)、二氧化碳(CO2)等。
3.混合物:由两种或两种以上的纯物质混合而成的物质。
例如沙子和水、空气等。
二、物质的物理性质1.固体:形状固定,体积固定,不易流动。
例如铁、木头等。
2.液体:形状不固定,体积固定,易流动。
例如水、牛奶等。
3.气体:形状不固定,体积不固定,能够流动。
例如氧气、二氧化碳等。
4.熔点:物质从固态变为液态的温度。
5.沸点:物质从液态变为气态的温度。
三、化学反应1.反应物:参与化学反应的物质。
2.生成物:化学反应得到的新物质。
3.离子:带电的原子或原子团。
4.离子键:由阳离子和阴离子之间的静电力所形成的化学键。
5.同化反应:化合物生成反应。
6.分解反应:化合物分解为两个或更多物质。
7.氧化反应:物质与氧气反应的过程。
8.还原反应:物质失去氧或增加氢的过程。
四、化学符号和化学式1.化学符号:用来表示元素的一到两个字母缩写。
例如氧的化学符号是O,氢的化学符号是H。
2.化学式:用化学符号表示化合物的组成。
例如水的化学式是H2O,二氧化碳的化学式是CO2。
五、常用实验室器材1.试管:用来装载少量反应物或生成物的玻璃器材。
2.烧杯:用来装载溶液或反应物的玻璃器材。
3.量筒:用来测量液体容积的玻璃器材。
4.滴管:用来滴加少量溶液的玻璃器材。
5.量管:用来测量气体体积的玻璃器材。
六、常见化学实验操作1.称量:用天平测量物质的质量。
2.加热:使用火焰或电炉将反应物加热。
3.滴加:使用滴管将溶液逐滴加入反应中。
初中化学全册必背常识点一、化学用语1、常见元素及原子团的名称和符号非金属:0氧H氢N氮C1氯C碳P磷S硫金属:K钾Ca钙Na钠Mg镁A1铝Zn锌Fe铁Cu铜Hg汞Ag银Mn镒Ba颌原子团(根):氢氧根硝酸根碳酸根硫酸根铉根OH-- CO:— S0i 2~ NH.,+2、(1)常见元素化合价口诀:一价氯氢钾钠银,二价重钙钥镁锌,二三铁二四碳,二四六硫都齐全;铜汞二价最常见,三铝四硅五氮磷,单质零价要记清。
(2)常见原子团(根)化学价口诀:负一硝酸氢氧根,负二硫酸碳酸根,正一价的是铉根。
3、必须熟记的常见物质的俗称、化学名称、化学式、用途4、必须熟记的制取物质的化学方程式(1)尝试室制取氧气一:2KMn04===K2Mn0.i+Mn02+02 t(2)尝试室制取氧气二:2H2O2 ==2H20+02 t(3)尝试室制取氧气三:2KC1O.3==2KC1+3O2 t(4)尝试室制法C02:CaCO3+2HC 1 ==CaC 12+H20+C021(5)尝试室制取氢气:Zn+HzSO户二ZnSOi+Hz t Zn + 2HC1 = ZnCl2+也t(6)电解水制取氢气:2氏0==2也t +O21(7)湿法炼铜术(铁置换出铜):Fe+CuSOF=FeSO4+Cu(Fe与盐、酸反映都生成的是+2价亚铁离子)(8) 炼铁原理:3C0+Fe 203===2Fe+3C02 (Fe2()3与酸反映生成的是+3价铁离子)(9) 熟灰水[Ca(OH) 2]的 制取方式:CaO+H 2O==Ca(OH)(10)生石灰(氧化钙)制取方式:CaC03 ===Ca0+C02 t二.金属运动性次序:棕黄色(如FeCL 溶液),其余溶液一样为无色。
(高猛酸钾溶液为紫红色)4、 (1)具有刺激性气体的气体:NH 3 (氨气)、SO?、HC1 (皆为无色)金属运动性由强至弱:K Ca Na Mg Al , Zn Fe Sn Pb (H) Cu Hg Ag Pt Au o(按5个一句次序背诵) 钠镁铝,锌 (氢),铜汞 银钳金。
初中化学常见化学用语(一)引言概述:初中化学是中学学习阶段的一门基础科学课程,在学习过程中,学生需要熟悉并掌握一些常见的化学用语。
本文将介绍一些初中化学中常见的化学用语,以帮助学生更好地理解和应用化学知识。
正文:一、化学物质分类1.元素:构成物质的基本单位,例如氧、碳等。
2.化合物:由不同元素通过化学反应结合而成,例如水、二氧化碳等。
3.混合物:由两种或多种不同物质物理性质混合而成,例如空气、沙土等。
4.纯净物:只由一种元素或化合物组成,例如纯水、纯金等。
5.溶液:溶质溶解在溶剂中形成的混合物,例如盐水、糖水等。
二、物质的性质1.物理性质:可通过观察和测量得到的性质,例如颜色、形状、大小等。
2.化学性质:物质在进行化学变化时表现出的性质,例如燃烧、氧化等。
3.可燃性:物质能够在适当条件下燃烧的性质,例如木材、纸张等。
4.不可燃性:物质不能燃烧的性质,例如玻璃、水等。
5.氧化性:物质与氧气发生反应的性质,例如铁锈、火焰等。
三、化学反应与化学方程式1.化学反应:物质之间发生的变化过程,例如酸碱中和反应、金属与酸反应等。
2.反应物:参与化学反应并被消耗的物质,例如金属、酸等。
3.生成物:化学反应中生成的新物质,例如盐、水等。
4.化学方程式:用化学符号和化学式表示化学反应过程的方程式,例如2H₂+O₂→2H₂O。
5.平衡反应:反应物与生成物浓度稳定的化学反应,例如酸碱中和反应等。
四、酸碱中和反应1.酸:味酸、导电性强、与碱反应可生成盐和水的物质,例如硫酸、盐酸等。
2.碱:味苦、导电性弱、与酸反应可生成盐和水的物质,例如氢氧化钠、氢氧化钙等。
3.酸碱指示剂:可通过颜色变化表达酸碱性强弱的物质,例如酚酞、苏丹红等。
4.酸碱中和反应:酸与碱反应生成盐和水的化学反应,例如氢氧化钠与盐酸中和反应等。
5.酸雨:大气中的二氧化硫、氮氧化物溶解在水中形成的酸性降雨。
五、溶液与浓度1.浓溶液:溶液中溶质的质量或体积相对较多的溶液,例如浓盐酸溶液、浓硫酸溶液等。