羧酸及其衍生物的分类结构和物理性质
- 格式:docx
- 大小:36.90 KB
- 文档页数:2



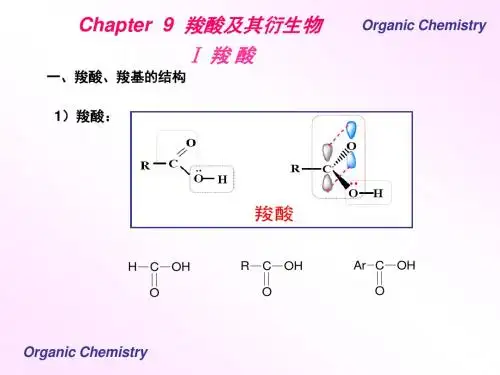
第十一章羧酸及其衍生物的结构与性质引言羧基()是羧酸的官能团,是由羰基和羟基组成的。
由于羰基的碳氧双键与羟基氧原子的共轭效应的作用,使羟基中氧原子电子向羰基转移,羟基的氢易离解而显酸性。
羧基中羟基也能被其它基团取代生成羧酸衍生物。
羧基是吸电子基,α-H具有活性,可以被卤代。
此外羧酸还能被还原和发生脱羧反应。
这里所讨论的羧酸衍生物主要是指羧基中羟基被取代后生成的酰卤(),酸酐(),酯(),酰胺()以及由酰胺脱水后生成的产物腈()。
在羧酸衍生物中羰基与卤素,酰胺基,烷氧基和氨基相连,由于卤素,氧原子和氮原子的负电性以及孤对电子的作用,使羰基碳上正电性不同,因此它们发生亲核反应性质也有差别。
羧酸衍生物还能发生还原反应。
11.1 羧酸的酸性羧酸是弱酸,能与强碱反应生成盐:羧酸酸性的强弱与所连的基团有关,连吸电子基团的羧酸酸性较强,而连供电子基团的酸性相对较弱。
如下列化合物酸性强弱顺序为:11.2 羧酸衍生物的生成羧基中的羟基被卤素、酰胺基、烷氧基和氨基取代形成酰卤、酸酐、酯和酰胺等羧酸衍生物。
1、酰卤的形成羧酸与SO2Cl,PCl5,PCl3等氯化剂直接反应生成酰卤:因为POCl3沸点低易除去,此法可制备高沸点的酰氯。
H3PO3沸点高,可制备低沸点的酰氯。
该法产生的SO2,HCl易除去,因此生成的酰氯纯度高,后处理容易。
2、酸酐的形成羧酸在脱水剂(如乙酰氯、乙酸酐)存在下加热,失去一分子水而生成酸酐。
二元酸可以分子内脱水生成二酸酐:3、酯化反应羧酸和醇在催化剂(H2SO4、HCl或苯磺酸等)作用下回流生成酯:酯化反应由多种机理,在大多数情况下,是羧酸中羟基与醇中羟基氢结合生成水,表观上看是一种亲核取代反应,实际上是一个亲核加成-消除反应的机理:决定反应速度的一步是亲核加成,因此羧基中碳的正电性以及羧基所连的基团大小核亲核试剂R'OH中R'体积大小都影响反应的速度,下列羧酸与甲醇酯化反应的相对速度的快慢顺序为:4、形成酰胺的反应羧酸与氨立即反应生成盐,在加热条件下,脱水生成酰胺,生成酰胺的反应是可逆的,如果把生成的水从反应体系中除去,反应可趋于完全。

了解羧酸及其衍生物的性质羧酸及其衍生物是一类重要的有机化合物,具有许多独特的性质和广泛的应用。
本文将对羧酸及其衍生物的性质进行探讨,以便更好地了解这一类化合物。
一、羧酸的定义和结构羧酸是一类化合物,其分子结构中含有一个或多个羧基(-COOH)。
羧基是由一个碳原子与一个羟基(-OH)和一个氧原子形成的。
羧酸的结构式通常用R-COOH表示,其中R表示有机基团。
根据羧基所连接的碳原子数目不同,可以将羧酸分为单官能团羧酸和多官能团羧酸两类。
二、羧酸的物理性质1. 熔点和沸点:羧酸的熔点和沸点通常较高,这是因为羧基中的羧基氧原子具有较高的极性,导致分子间的相互作用增强。
2. 溶解性:大多数羧酸可以在水中溶解,形成羧酸离子和氢离子。
溶解度受到羧酸结构、环境条件以及其它物质的影响。
3. 酸性:羧酸具有明显的酸性,可以与碱反应生成盐和水。
强酸性主要来自羧基中的羟基和带负电荷的氧原子。
三、羧酸的化学性质1. 与碱的反应:羧酸可以与碱反应生成相应的盐。
反应中羧酸中的羧基给出一个负电荷,碱给出一个正电荷,形成盐并释放水。
2. 与醇的酯化反应:羧酸可以与醇反应生成酯。
在反应中,羧酸中的羧基与醇中的氢原子发生取代反应,生成酯和水。
3. 与卤素的取代反应:羧酸中的羟基和羧基都可以与卤素发生取代反应,生成相应的羧酸衍生物。
4. 与羟胺的芳香胺反应:羧酸中的羧基可以与羟胺反应生成相应的芳香胺。
四、羧酸衍生物的性质1. 酯:羧酸与醇反应生成的酯具有较好的挥发性和溶解性,常用于香料、溶剂和聚合物合成等领域。
2. 盐:羧酸与碱反应生成的盐通常具有较高的溶解度和稳定性,在药物、染料和表面活性剂等领域有广泛应用。
3. 胺:羧酸中的羧基与氨或胺反应生成的胺具有一定的碱性,可用于药物合成和化妆品生产中。
4. 酸酐:羧酸中的羧基与无水酸反应生成的酸酐具有良好的环境稳定性,广泛应用于有机合成反应中。
综上所述,羧酸及其衍生物具有多样的性质和广泛的应用价值。


有机化学羧酸及衍生物有机羧酸及其衍生物是有机化学中应用最广泛的重要化合物之一,几乎所有的有机物都是结构和功能性的羧酸衍生物。
它们由非常复杂的结构,从一种亲水性的、具有一个或者多个氢原子的,比较简单的醛与醇体积式羧酸,到脂溶性的、具有脂类或碳酸酯等有机基组成的、比较复杂的多羟基羧酸。
它们都具有很好的化学稳定性和匹配性,在生物体内具有独特的生物活性,因此被广泛应用于各种科学领域。
有机羧酸及其衍生物可分为两大类:一类是单羟基羧酸,它们是由醛与醇有机化合物组成;另一类是多羟基羧酸,它们含有一个以上的羟基,而且具有脂溶性的有机基。
单羟基羧酸有很多种,具体分类如下:呋喃酸、玻璃酸、环酸、乙醇酸、丙酸、乳酸、鞣酸等;多羟基羧酸也有很多种,主要有有机醋酸、有机磷酸、有机碳酸和有机磷脂等。
有机羧酸及其衍生物在化学领域有着广泛的应用。
羧酸及其盐是常用的表面活性剂,羧酸与碱可缓解环境中硫氧化物及酸雨的危害;多羟基羧酸的衍生物是生物体的重要组成部分,包括DNA及RNA的碱基,也是酶的活性中心及核糖体的结构化合物。
此外,它们也可进一步衍生出有机键、芳环等,与功能性化合物相连,用于制造药物和高科技中的医疗器械。
有机羧酸及其衍生物应用广泛,必将深刻影响人们的日常生活,是实现未来科学社会化十分重要的一环。
Organic carboxylic acids and their derivatives are one of the most widely used important compounds in organic chemistry, almost all organic compounds are structural and functional carboxylic acid derivatives. They have very complex structures, from a comparatively simple hydrophilic and one or more hydrogen small molecular alcohol aldehyde carboxylic acid, to lipophilic and composed of lipids or esters and other organic base, more complex polyhydroxy carboxylic acid. They all have good chemical stability and matching, unique biological activity in organisms, and are widely used in various scientific fields.Organic carboxylic acids and their derivatives can be divided into two categories: one is monohydroxy carboxylic acid, which is composed of aldehyde and alcohol organic compounds; the other is polyhydroxy carboxylic acid, which contains one or more hydroxyl groups, and has lipophilic organic base. Monohydroxy carboxylic acid has many kinds, the specific classification is following: furan carboxylic acid, glacial acetic acid, cyclo carboxylic acid, ethyl alcohol carboxylic acid, propionic acid, lactic acid, tannic acid and so on; polyhydroxy carboxylic acid also has many kinds, mainly include organic acetic acid, organic phosphoric acid, organic carbonic acid and organic phospholipid.Organic carboxylic acids and their derivatives have a wide range of applications in chemical field. Carboxylic acid and its salts are commonly used surfactants, and carboxylic acid and alkali。


目前位置:首页—>羧酸及其衍生物—>K2羧酸及其衍生物的物理性质羧酸及其衍生物的物理性质教学目标:1.了解羧酸一般物理性质及其影响因素。
2.掌握羧酸及其衍生物IR 特征。
教学重点:IR特征教学安排:B—>K2;10min5, K1一、一般物理性质的羧酸有一定挥发性,并且有较强的刺激性;低级的一元羧酸(C1-C9)是液体,C1-C3C4-C9的羧酸不同程度地具有腐败气味,并且是具有一定粘度的油状液体。
C10以上的羧酸则是石蜡状固体,气味很小。
二元羧酸以及芳香族羧酸都是晶体。
羧酸的沸点较分子量相近的醇高,这是由于羧基的强极性和分子间的氢键所致。
在气态时,甲酸、乙酸等是以双分子缔合形态出现。
与烷烃相似,偶数碳原子的羧酸其熔点要比与之相邻的奇数碳原子羧酸的熔点高。
C1-C4的正构羧酸由于分子的极性大,与水分子可很好地形成氢键,所以它们的溶解度很大;但正戊酸在水中的溶解度只有3.7g/100g水。
高级的一元酸在水中的溶解度非常小,甚至不溶于水。
常见的二元酸在水中都有很好的溶解度。
酰氯、酸酐和酯的沸点与分子量相近的醛酮大体相近,酰胺由于分子间可形成氢键,而具有很高的沸点。
低级的酯和酰胺在水中有一定的溶解度;但低级的酰氯和酸酐在水中容易发生水解。
一般情况下,酰氯和酯的熔点比较低,酰胺的熔点较高,不同的酸酐的熔点变化是较大的。
低级的酰氯和酸酐都有刺鼻气味,而低级的酯却有芳香气味并可用作香料;低级的酰胺是良好的非质子型极性溶剂。
常见的羧酸及其衍生物在一般的有机溶剂中有良好的溶解性。
一些常见的羧酸衍生物的熔点和沸点如下表:二、光波谱性质由于羧酸分子的羟基之间可形成氢键,在3300cm-1 处有非常强而宽的羟基的特征峰,并且该峰可含盖烃基中的CH3和CH2 的C-H 键伸缩振动吸收峰的区域;在2500-2700cm-1 处,还有O-H 键的伸缩振动。
另外,OH 的弯曲摆动(面外摇摆)在925cm-1处有一个比较宽的特征吸收峰。


羧酸及其衍生物的结构特点分析
羧酸是有机化合物的一类,其通式为R-COOH,其中R为有机基团。
羧酸的结构特点包括官能团、酸性、羧基的构型和胺脱氨反应等方面。
首先,羧酸的结构中含有一个羧基(-COOH),这是羧酸的官能团,也是羧酸的命名基团。
羧基是由一个碳氧双键和一个羟基组成,通常以双键碳上的氧为羰基(-C=O),羟基中的氧为羟氧基(-OH)。
其次,羧酸是弱酸性物质。
羧基中的碳氧双键极性较强,具有较高的电负性,因此能够进行H+的解离,生成羧酸根离子(-COO-)和一个氢离子(H+)。
羧酸的酸性可以通过它的电离常数(Ka)来衡量。
第三,关于羧基的构型,碳氧双键的特殊性使得羧酸中的碳原子存在一个空杂化p轨道,形成一个带有正电荷的共轭碳阳离子。
这使得羧酸具有一定的构象选择性,即平面构象和非平面构象。
平面构象中,羧基的两个键(羧基与羰基)在同一个平面上。
非平面构象中,羧基的两个键呈现弯曲的构象。
最后,羧酸可以发生胺脱氨反应,在适当的条件下,羧酸与氨或胺反应,生成酰胺。
这个反应的条件包括反应物的浓度、反应温度和反应时间等。
胺脱氨反应对于合成酰胺具有重要的意义,因为酰胺在生物体中广泛存在,是许多生物活性物质的重要结构单元。
综上所述,羧酸及其衍生物具有许多结构特点,包括官能团、酸性、羧基的构型和胺脱氨反应等。
对这些结构特点的分析可以帮助我们更好地理解羧酸及其衍生物的性质和反应行为。
第十章羧酸及其衍生物羧酸及其衍生物❖羧酸及其衍生物的结构特征;❖羧酸及其衍生物的物理和化学性质;❖乙酰乙酸乙酯和丙二酸酯的特性及其在有机合成上的应用;❖蜡和油脂,碳酸衍生物重点要求掌握羧酸及其衍生物的化学性质;乙酰乙酸乙酯在有机合成上的应用。
10.1 羧酸10.1.1 羧酸的构造、分类和命名1、羧酸的构造和分类分子中具有羧基的化合物,称为羧酸。
它的通式为 RCOOH。
2、命名由它的来源命名:甲酸最初是由蚂蚁蒸馏得到的,称为蚁酸。
乙酸最初是由食用的醋中得到,称为醋酸。
还有草酸、琥珀酸、苹果酸、柠檬酸。
系统命名:含羧基最长的碳链作为主链,根据主链上碳原子数目称为某酸.编号从羧基开始.3,4-二甲基戊酸3-甲基-2-丁烯酸芳香族羧酸可以作为脂肪酸的芳基取代物命名:羧酸常用希腊字母来标名位次,即与羧基直接相连的碳原子为α,其余位次为β、γ…,距羧基最远的为ω位。
二元酸命名:10.1.2 羧酸的物理性质在室温下10个碳原子以下的饱和一元羧酸是液体。
10个碳原子以上的羧酸为石蜡固体,挥发性很低,无气味。
4~9个碳原子的脂肪酸具有腐败恶臭、动物的汗液和奶油发酸变坏的气味。
饱和一元羧酸的沸点比相对分子质量相似的 醇还要高。
饱和一元羧酸的熔点随分子中碳原子数目的增加呈锯齿状的变化。
低级脂肪酸易溶于水,但随分子量的增高而降低。
甲酸与水通过氢键缔合在固态和液态,羧酸主要以二聚体形式存在。
低级的羧酸,在气相时仍以双分子缔合状态存在。
10.1.3 羧酸的化学性质OOH H HOH O HH HHOCRCOOHOORHO ORHCC2HOR H O HC Cα10.1.3.1 酸性羧酸具有弱酸性,在水溶液中存在着如下平衡:乙酸的离解常数K a 为1.75×10-5 甲酸的K a =2.1×10-4 , p Ka =3.75其他一元酸的K a 在1.1~1.8×10-5之间, p Ka 在4.7~5之间。
羧酸及其衍生物的分类结构和物理性质羧酸是一类具有羧基(-COOH)的有机化合物,它是碳链上的一个碳原子与一个羧基团相连形成的化合物。
羧基团由一个碳原子与一个氧原子以及一个氢原子组成。
根据羧基的位置不同,羧酸可以分为两类:取代羧酸和芳香羧酸。
取代羧酸是指羧基连接在碳链上,而芳香羧酸则是指羧基连接在芳香环上。
在取代羧酸中,根据羧基所连接到的碳原子的取代原子(或基团)的不同,可以进一步分为单取代羧酸、二取代羧酸和多取代羧酸。
单取代羧酸是指羧基所连接的碳原子上只有一个取代原子(或基团),如乙酸(CH3COOH)。
二取代羧酸是指羧基所连接的碳原子上有两个取代原子(或基团),如丙酸(CH3CH2COOH)。
多取代羧酸是指羧基所连接的碳原子上有多个取代原子(或基团),如苯甲酸(C6H5COOH)。
芳香羧酸是指羧基连接在芳香环上的羧酸化合物。
芳香羧酸通常以其常见的名称命名,如苯甲酸(C6H5COOH)和苯乙酸(C6H5CH2COOH)等。
羧酸及其衍生物通常具有一些共同的物理性质。
首先,羧酸具有高沸点和高熔点,这是因为羧酸分子之间通过氢键形成二聚体或多聚体结构。
其次,由于羧酸中的羧基是极性官能团,因此羧酸具有很强的溶解性。
它们可以与水中的氢氧根离子形成氢键,也可以通过与有机溶剂(如醇、醚和酯)的酯化反应溶解。
此外,羧酸还具有一定的酸性,可以在水中与碱进行中和反应。
羧酸的反应性与羧基的酸性和碳原子的电子密度有关。
具有更高电子密度的碳原子上的羧基更容易释放负电荷,在水溶液中呈现更强的酸性。
此外,羧基的芳香羧酸比取代羧酸更酸。
总之,羧酸及其衍生物是一类具有羧基的有机化合物。
根据羧基的位置和取代原子的不同,羧酸可以分为取代羧酸和芳香羧酸。
羧酸具有高沸点、高熔点、良好的溶解性和一定的酸性。
这些属性使得羧酸在许多领域都有广泛的应用,如有机合成、染料工业、食品添加剂等。