人教版高中化学必修1:氨
- 格式:pptx
- 大小:2.06 MB
- 文档页数:21

考点14 氨的性质【考点定位】本考点考查氨的性质,涉及氨的结构与物理性质、氨气的还原性及氨水的弱碱性,掌握氨水喷泉实验的操作要点及常见氨气的制备原理与实验装置。
【精确解读】1.氨的物理性质:①氨是无色、有刺激性气味的气体,比空气轻;②氨易液化.在常压下冷却或常温下加压,气态氨转化为无色的液态氨,同时放出大量热.液态氨气化时要吸收大量的热,使周围的温度急剧下降;③氨气极易溶于水.在常温、常压下,1体积水中能溶解约700体积的氨气(因此,氨气可进行喷泉实验);④氨对人的眼、鼻、喉等粘膜有刺激作用.若不慎接触过多的氨而出现病症,要及时吸入新鲜空气和水蒸气,并用大量水冲洗眼睛.2.氨分子的结构:NH3的电子式为,结构式为,氨分子的结构为三角锥形,N原子位于锥顶,三个H原子位于锥底,键角107°18′,是极性分子.3.氨的化学性质:①跟水反应.氨气溶于水时(氨气的水溶液叫氨水),大部分的NH3分子与H2O分子结合成NH3•H2O(叫一水合氨).NH3•H2O为弱电解质,只能部分电离成NH4+和OH-:NH3+H2O⇌NH3•H2O⇌NH4++OH-a.氨水的性质:氨水具有弱碱性,使无色酚酞试液变为浅红色,使红色石蕊试液变为蓝色.氨水的浓度越大,密度反而越小(是一种特殊情况).NH3•H2O不稳定,故加热氨水时有氨气逸出:NH4++OH-=NH3↑+H2Ob.氨水的组成:氨水是混合物(液氨是纯净物),其中含有3种分子(NH3、NH3•H2O、H2O)和3种离子(NH4+和OH-、极少量的H+).c.氨水的保存方法:氨水对许多金属有腐蚀作用,所以不能用金属容器盛装氨水.通常把氨水盛装在玻璃容器、橡皮袋、陶瓷坛或内涂沥青的铁桶里.d.有关氨水浓度的计算:氨水虽然大部分以NH3•H2O形式存在,但计算时仍以NH3作溶质.②跟氯化氢气体的反应:NH3+HCl=NH4C1说明:a.当蘸有浓氨水的玻璃棒与蘸有浓盐酸的玻璃棒靠近时,产生大量白烟.这种白烟是氨水中挥发出来的NH3与盐酸挥发出来的HCl化合生成的NH4C1晶体小颗粒.b.氨气与挥发性酸(浓盐酸、浓硝酸等)相遇,因反应生成微小的铵盐晶体而冒白烟,这是检验氨气的方法之-.c .氨气与不挥发性酸(如H 2SO 4、H 3PO 4等)反应时,无白烟生成.③跟氧气反应:4NH 3+5O 2催化剂 △4NO+6H 2O 说明:这一反应叫做氨的催化氧化(或叫接触氧化),是工业上制硝酸的反应原理之一.4.氨气的用途:①是氮肥工业及制造硝酸、铵盐、纯碱的原料;②是有机合成工业如合成纤维、塑料、染料、尿素等的常用原料;③用作冰机中的致冷剂【精细剖析】1.喷泉实验的原理中学教材中喷泉实验装置如右图所示。


高中化学人教版氨的教案
一、教学目标
1. 知识目标:了解氮气的性质及用途,掌握氨的物理性质和化学性质;
2. 能力目标:能够分析氨的合成反应,勾画氨的制备工艺流程,运用氨的化学性质解决实际问题;
3. 情感目标:培养学生对环境保护和能源利用的意识,培养学生勤奋学习、积极探究的品质。
二、教学重点和难点
1. 了解氨的制备方法和应用;
2. 掌握氨的物理性质和化学性质。
三、教学过程
1. 导入新课:介绍氨的性质,引发学生对氨的好奇和探究欲望。
2. 学习氨的物理性质和化学性质,进行实验验证,巩固学生对氨的认识。
3. 结合实际案例,讨论氨的应用领域和环保意义。
4. 学习氨的制备方法和化学合成反应,引导学生分析氨的合成原理。
5. 分组讨论,设计氨的制备工艺流程,展示学生的创造力和解决问题的能力。
6. 总结本节课的知识点,激励学生对化学学科的探索和研究。
四、教学评价
1. 课堂表现:听课认真、思维活跃、能积极回答问题、能有效运用所学知识解决问题;
2. 作业表现:书写规范、内容详实、用词准确、理解透彻;
3. 实验操作:注意安全、操作规范、数据准确、结论明确。
五、教学反思
通过本节课的教学,学生对氨的性质和应用有了更深入的理解,同时也加深了对氨制备方法和化学反应的认识。
在未来的教学中,可以增加更多案例引导学生探究氨在环保和生产中的重要性,激发学生的学习兴趣,提高学生的学习效果。

教学目标:1. 理解氨的物理性质和化学性质。
2. 掌握氨的制备方法和用途。
3. 能够解决相关氨化学问题。
教学重点和难点:重点:氨的性质和用途。
难点:氨的化学性质和其与其他物质的反应。
教学准备:实验器材:氨水、盐酸、氢氧化钠等。
课本:有关氨的知识点。
图表:相关实验原理和结果图表。
教学过程:一、导入:通过有趣的实例引入氨的概念和作用,激发学生对氨的兴趣。
二、讲解氨的性质:1. 介绍氨的物理性质(无色、刺激性气味、易挥发等)和化学性质(碱性、与酸等物质发生反应)。
2. 展示实验现象,让学生亲自操作观察和体会氨的性质。
三、探讨氨的制备方法:1. 介绍氨的制备方法(氨水和氢氧化铵的反应、氨气与氢氮气的合成等)。
2. 分析不同制备方法的优缺点,并让学生进行讨论。
四、探讨氨的用途:1. 介绍氨在工业生产、医药、化肥等方面的广泛应用。
2. 分析氨的用途对人类生活和环境的影响,让学生思考如何合理利用和管理氨资源。
1. 安排相关实验,让学生进行氨的制备和性质实验。
2. 引导学生观察、记录实验现象并进行分析。
六、总结回顾:对本节课学习内容进行总结,强调氨的重要性和用途,激发学生对化学的兴趣和探究欲望。
板书设计:氨的性质:物理性质、化学性质氨的制备方法:氨水和氢氧化铵的反应、氨气与氢氮气的合成氨的用途:工业生产、医药、化肥等作业布置:1. 思考并写出氨在不同领域的应用情况。
2. 撰写氨的化学性质及与其他物质的反应实验报告。
教学反思:本节课注重通过实验操作,引导学生深入理解氨的性质和用途,培养学生独立思考和解决问题的能力。
同时,激发学生对化学知识的兴趣和探究欲望,使得化学教学更生动有趣。


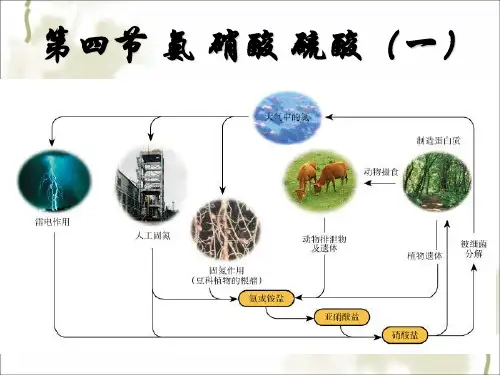



氨和铵盐【学习目标】1、了解氨的物理性质,理解氨的化学性质。
2、掌握氨气的实验室制法,了解氨气的工业制法。
3、了解铵盐的性质,掌握氨气和铵离子的检验方法。
【要点梳理】要点一、氨气1、物理性质通常状况下,氨是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水(常温常压下,体积比为1∶700),氨的水溶液称为氨水。
氨在加压下容易液化,液氨气化时吸收大量的热,使周围环境温度急剧降低,工业上可使用液氨作制冷剂。
2、化学性质(1)与水反应:NH3+H2O NH3·H2O NH4++OH-要点诠释:NH3·H2O是弱碱,氨水显弱碱性,具有碱的通性。
氨水可使紫色石蕊试液变蓝,故常用湿润的红色石蕊试纸检验NH3的存在。
氨水是混合物,溶液中存在的微粒有三种分子:NH3·H2O、NH3、H2O;三种离子:NH4+、OH-及少量的H+。
(2)与酸反应:氨气与酸反应生成铵盐NH3+HCl=NH4Cl(白烟)NH3+HNO3=NH4NO3(白烟)2NH3+H2SO4=(NH4)2SO4(3)与某些盐反应:一般生成难溶的碱,如氯化铁溶液与氨水反应:Fe3++3NH3·H2O==Fe(OH)3↓+3NH4+(4)还原性氨分子中的氮元素呈-3价,因此氨气在一定条件下具有还原性,在一定条件下可被某些强氧化剂氧化。
8NH3+3Cl2==N2+6NH4Cl【高清课堂:氨和铵盐ID:395522#氨气的实验室制法】3、氨气的实验室制法(1)原理:利用复分解反应强碱制弱碱2 NH4Cl +Ca(OH)2CaCl2+2NH3↑+2H2O要点诠释:药品的选择②碱:一般用熟石灰,不用NaOH或KOH,因为NaOH或KOH易吸水结块,而且对玻璃仪器腐蚀性较强。
(2)装置:固-固反应加热装置(同制O2)干燥:碱石灰(或固体NaOH、固体CaO)(不能用浓H2SO4、CaCl2干燥,CaCl2与NH3反应:CaCl2+8NH3= CaCl2·8 NH3)要点诠释:①发生装置的试管口略向下倾斜;②加热温度不宜过高,并用酒精灯外焰由前向后逐渐加热。
高中化学必修一氨气教案
一、教学目标
1. 了解氨气的性质和制备方法。
2. 掌握氨气的物理性质和化学性质。
3. 了解氨气的用途及危害,培养安全使用氨气的意识。
二、教学重点和难点
1. 氨气的性质和制备方法。
2. 氨气的物理性质和化学性质。
三、教学过程
1. 导入:通过实验或图片展示氨气,引导学生了解氨气在生活中的应用和危害。
2. 学习氨气的制备方法,并通过实验观察氨气的物理性质。
3. 学习氨气的化学性质,包括氨气的焰色反应和与氧化剂的反应。
4. 了解氨气的用途及危害,鼓励学生讨论氨气的安全使用方法。
5. 总结:对氨气的性质、制备方法、物理性质和化学性质进行总结,巩固学习成果。
四、作业布置
1. 阅读相关资料,了解氨气的其他性质和应用。
2. 完成相关练习题,巩固所学知识。
3. 思考氨气在生活中的应用和如何安全使用氨气。
五、教学反思
教师应根据学生的实际情况和反馈调整教学方法,确保学生能够充分理解氨气的性质和用途,培养安全使用氨气的意识。
同时,通过实验和讨论引导学生主动参与学习,提高学习效果。
氨高中化学教案一、知识目标:1. 了解氨的物理性质和化学性质。
2. 掌握氨的制备方法及其反应机理。
3. 学会应用氨的性质及制备方法解决相关问题。
二、能力目标:1. 能够描述氨气的颜色、气味和溶解性等物理性质。
2. 能够描述氨气的与酸碱指示剂的反应,了解氨的碱性。
3. 能够根据氨的制备方法解答与氨相关的问题。
三、教学重点与难点:1. 教学重点:氨的物理性质、化学性质及制备方法。
2. 教学难点:氨的与酸碱指示剂的反应机理。
四、教学过程:1. 氨的物理性质:-让学生观察氨气在室温下的状态,包括颜色、气味和溶解性等。
-引导学生理解氨气的颜色为无色,气味为刺激性气味,易溶于水。
2. 氨的化学性质:-介绍氨气与酸碱指示剂的反应,观察溶液颜色的变化。
-解释氨气的碱性,引导学生理解碱性与酸碱指示剂的颜色变化之间的关系。
3. 氨的制备方法:-介绍氨的工业制备方法和实验室制备方法,包括氨的合成反应方程式和实验操作步骤。
-引导学生思考氨的制备方法与氨的应用之间的关系。
五、课堂练习:1. 请描述氨气的颜色、气味和溶解性等物理性质。
2. 氨气与酸碱指示剂的反应结果是什么?请解释其原因。
3. 环境中氨的主要来源是什么?如何利用氨的制备方法来进行环境治理?六、作业布置:1. 完成相关课后习题。
2. 思考氨的制备方法与应用之间的关系,并撰写一篇小论文。
七、教学反思:通过本节课的教学,学生应该能够全面了解氨的性质与制备方法,并能够灵活运用所学知识解决相关问题。
同时,教师也应及时总结教学过程中的不足,不断优化教学方法,提高教学效果。
第四节氨、硝酸和硫酸第一课时氨及氨的实验室制法【课时目标】1.了解氨的物理性质和氨的化学性质。
2.理解氨的实验室制法。
【基础知识导航】一、氨的固定将___的氨转变为___的方法叫做氨的固定,工业上固氮的方法为_________(用化学方程式表示)二、氨的性质1、氨的物理性质【实验探究】氨溶于水的喷泉实验现象结论2、氨的化学性质(1)NH3与水的反应NH3·H2O很不稳定,受热会分解【液氨与氨水的比较】(2)NH3与酸的反应氨与氯化氢的反应的化学方程式上述反应的现象是______________________,为什么?____________________【注意】上述反应可用于检验氯化氢气体或氨气的检验氨与硫酸的反应化学方程式【思考】氨与硫酸反应有没有类似氨与氯化氢反应的现象?为什么?_______________三、铵盐的性质1、铵盐受热易分解写出氯化铵受热分解的反应方程式______________________________________________ 写出碳酸氢铵受热分解的方程式【思考】氯化氨的分解与生成的反应是不是可逆反应?为什么?____________________2、铵盐与碱的反应写出硝酸铵与氢氧化钠溶液反应的方程式______________________________________ 写出上述反应的离子方程式________________________________________【思考】实验室如何检验铵盐?___________________________________四、氨的实验室制法1、反应原理2、装置:“+”加热装置;发生装置与制相似。
3、收集:法;收集的试管口塞上棉团,作用是。
4、干燥:5、检验:(1)(2)6、实验室能不能用氢氧化钠与氯化铵反应制备氨气?为什么?______________________7、实验室制备氨气的其它方法(1)直接加热浓氨水(2)浓氨水与固体烧碱或生石灰混合五、氨的用途【典例导析】例题1:氨下列关于氨和氨水的说法中正确的是()A、氨水和液氨的成分相同B、氨水可使酚酞指示剂变红C、氨水中共有5中粒子,其中物质的量浓度最大的粒子是OH-D、氨水随着质量分数的增大,溶液密度也随之增大【点拨】A中一个是混合物一个是纯净物,B氨水显碱性,C中氨水的电离程度很小,D中应为氨的密度小,规律也应该反的。
考点12 铵盐与氨根离子的检验【考点定位】本考点考查铵盐与氨根离子的检验,明确铵盐的不稳定性及不同铵的分解产物,学会鉴别溶液中的氨根离子,注意加热条件及使用湿润的红色石蕊试纸检验生成的气体。
【精确解读】1.铵盐是离子型化合物,都是白色晶体,易溶于水,溶于水时吸热;2.受热分解(不稳定性):NH4Cl △NH3↑+HCl↑、NH4HCO3≜NH3↑+CO2↑+H2O;①氯化铵受热分解为氯化氢和氨气,遇冷时二者又重新结合为氯化铵,NH4HCO3加热则完全气化,也出现类似“升华”的现象;②铵盐受热分解的产物要根据具体情况分析,一般以温度和铵盐里的酸根的氧化性等诸多因素有关.如:NH4NO3△N2O↑+2H2O;3.与碱反应:NH4++OH-=NH3↑+H2O;可以用来检验NH4+,也可用来制备氨气,用湿润的红色石蕊试纸在瓶口验满。
【精细剖析】1.在含铵根离子的试剂中加入强碱(常用氢氧化钠)并加热,如有氨气(可用湿润的红色石蕊试纸变蓝并闻气味的方法检验氨气)放出可确定有铵根离子。
【典例剖析】试管中盛有少量白色固体,可能是铵盐,检验的方法是( )A.加水,将湿润的红色石蕊试纸放在试管中B.加NaOH溶液,加热,滴入酚酞试剂C.加NaOH溶液,加热,滴入紫色石蕊试剂D.加NaOH溶液,加热,将湿润的红色石蕊试纸放在试管口【答案】D误;C.氢氧化钠和氨水均是碱性的,均能使石蕊试液显示蓝色,如果氢氧化钠相对于氨水过量则会干扰检验,故C错误;D.将白色固体放入试管加热,用湿润的红色石蕊试纸放在试管口,湿润红色石蕊试纸会变蓝色,证明产生的气体是氨气,证明该盐中含有铵根离子,这是检验铵盐的方法,故D正确;故答案为D。
【变式训练】检验铵盐的方法是将待检物取出少量放在试管中,然后( )A.加热,将湿润的红色石蕊试纸放在试管口观察颜色变化B.加水溶解,用红色石蕊试纸检验溶液酸碱性C.加入NaOH浓溶液,加热,将湿润的红色石蕊试纸放在试管口观察颜色变化D.加入强碱溶液,加热,再滴入酚酞试液【答案】C【实战演练】1.为了检验某固体物质中是否含有NH4+,你认为下列试纸和试剂一定用不到的是( )①蒸馏水②NaOH溶液③红色石蕊试纸④蓝色石蕊试纸⑤稀硫酸.A.①⑤B.④⑤C.①③⑤D.①④⑤【答案】B【解析】铵根离子和氢氧化钠溶液反应生成氨气,氨气能使湿润的红色石蕊试纸变蓝色,则需要红色石蕊试纸,且需要蒸馏水润湿试纸,则不需要的物质是蓝色石蕊试纸及稀硫酸,故答案为B。