链霉素效价测定方案
- 格式:doc
- 大小:33.50 KB
- 文档页数:4

抗生素效价的测定方法1. 磁敏感性法:该方法是将细菌和抗生素共同培养在琼脂平板上,然后在琼脂平板的一侧放置磁性探针,通过磁力对菌落的影响,测定抗生素效价。
这种方法操作简单,结果可重复性好。
2. 微量滴定法:该方法是将不同浓度的抗生素加入含有微生物的培养基中,控制每次加量相同,直至培养基中出现明显的抑菌圈,然后根据最小抑菌浓度来测定抗生素的效价。
这种方法对药物浓度的变化比较敏感,但误差较大。
3. 黏度测定法:该方法是根据细菌代谢后产生的黏性物质的变化,来测定抗生素的效价。
该方法操作简单,但对试验条件较为严格。
4. 限制性酶切割法:该方法是将抗生素和细菌混合后,通过限制性酶将其切割成小片段,进而测定抗生素的效价。
这种方法需使用限制性酶切割试剂和设备,相对较为复杂。
5. 形态学观察法:该方法是观察抗生素对细菌的形态和结构的影响,来判断抗生素的效价。
这种方法适用于细菌的菌落比较大的情况,但操作比较繁琐。
6. 代谢产物测定法:该方法是根据细菌代谢产物的变化,来测定抗生素的效价。
这种方法操作比较简单,但对试验条件较为严格。
7. 荧光标记法:该方法是将抗生素用荧光标记,然后与细菌共同培养,通过荧光强度的变化,来测定抗生素的效价。
这种方法对试验条件要求比较高,但结果可靠性较高。
8. 酶联免疫吸附测定法:该方法是将抗生素用于特定的抗体结合,然后通过检测抗体与细菌结合的情况,来测定抗生素的效价。
这种方法的优点是灵敏度高,同时避免了细菌对抗生素的耐药性。
9. 质谱法:该方法是使用质谱仪分析样品中的分子质量的变化,来测定抗生素的效价。
这种方法可分析多种抗生素,但设备价格昂贵。
10. 核磁共振法:该方法是使用核磁共振仪测定样品中的氢、碳、氮等原子的共振频率和空间结构,来测定抗生素的效价。
这种方法对试验条件的要求非常高,且设备也价格昂贵。
测定抗生素效价的方法有很多种,每种方法都有其特点和适用范围。
在实际应用中,应根据具体情况选择合适的方法,以确保测定结果的准确性和可靠性。

农用硫酸链霉素所使用的标识量是效价,那效价是什么意思?1000万单位的农链应该有多少克?1000万单位的农用链霉素应该有多少克。
效价,从字面上就可以有所理解,也就是单位量的物质有多大的作用,是从功能上来计量的。
1000万单位的农用链霉素,和100克的20%农用链霉素可湿性粉剂,所用的计量标准不同,在没有其他条件限制的情况下,两者难以确定一个准确的对比关系。
就像1克水和1毫升水,1克水,只有在特定的条件下才是1毫升水,在绝大多数情况下两者是不相等的,因为在不同的温度条件下水的体积是不同的。
用高中化学中摩尔当量的概念来类比说明效价和重量的关系,更为确切些。
1摩尔当量的硫酸溶液,只要其中的氢离子为1摩尔就可以,无论硫酸溶液是1公斤还是10公斤,它在中和碱时的效用是能中和1摩尔的氢氧根离子。
1000万单位的农用链霉素,是像摩尔当量一样,按效用来计量的。
它可以是10片每片10克、效价为100万单位的农用链霉素,也可以是10片每片20克、效价为100万单位的农用链霉素,也可以是20片每片20克、效价为50万单位的农用链霉素,尽管药片总质量不同,但它们用于防治病害,其效果是一致的。
用质量单位克来计量农用链霉素可湿性粉剂,比较符合大众的用药习惯。
由于不同厂家、不同剂型的产品,其单位有效成分所能发挥的效用有所不同,所以不如按效价计量来得准确。
但在一般情况下,特定厂家的产品,或者说合格产品,其单位质量的药剂其效用还是相对稳定的,所以完全可以用质量单位克来计量农用链霉素可湿性粉剂。
从上次回复的两个数据,100万单位农用链霉素泡腾片的亩用量为750-900万单位,农用链霉素可湿性粉剂的纯药亩用量为7-20克,大致可以知道,一片100万单位农用链霉素泡腾片,其效用相当于农用链霉素可湿性粉剂1克左右纯药的效用。

实验一制霉菌素发酵、提取与效价测定1. 实验目的与要求(1) 了解抗生素发酵的一般过程及发酵过程中一些重要理化指标检测方法;(2) 学习抗生素(制霉菌素)的提取纯化工艺;(3) 了解制霉菌素化学效价测定的原理;(4) 掌握抗生素生物效价测定的常规方法——管碟法的原理与操作。
2. 实验原理2.1制霉菌素制霉菌素(nystatin, mycostatin or fungicidin)是由诺尔斯链霉菌(Streptomyces noursei)产生的一种多烯大环内酯类(polyene macrolides) 抗真菌抗生素。
此类抗生素的结构特点是在分子中既有经内酯化作用而闭合的大碳环,又有一系列的共轭双键。
制霉菌素存在于菌丝体中,其纯品为淡黄色微细晶体;不溶于水、氯仿和丙酮等;稍溶于低级醇等;溶于吡啶、冰醋酸和NaOH溶液,但均能使其破坏而失效;对较高和较低的pH以及光和热均不稳定。
临床上使用的制霉菌素,其主要成分为制霉菌素A1,化学结构式如下图所示:它的氨基糖部分是氨基海藻糖,即3-氨基-3,6-二脱氧-D-吡喃甘露糖,非糖部分为38员的多烯大环内酯。
制霉菌素对各种真菌如白色念珠菌、隐球菌、荚膜组织胞浆菌及球孢子菌等有抑制作用。
主要用于白色念珠菌感染,如消化道念珠菌病、鹅口疮、念珠菌性阴道炎及外阴炎等。
但口服治疗全身性真菌感染或深部真菌感染则无效。
制霉菌素的作用机理是与真菌细胞膜上的特异甾醇相结合,导致原生质膜破坏,通透性改变,以致重要的细胞内容物外漏而死亡,从而杀灭真菌。
由于细菌原生质膜上不含甾醇,故本品对细菌无效;对肠道正常菌丛也无作用。
2.2 抗生素发酵生产工艺简介抗生素液体发酵共分为三大工序:菌种、发酵和提取。
配合三个工序进行分析化验和有关产物测定。
具体而言,其过程为菌种→孢子制备→种子制备→发酵→发酵液预处理→提取与精制→成品包装。
菌种一般采用液氮超低温保藏或沙土管保藏。
一般生产用菌种经多次转接往往会发生变异而退化,故必须经常进行菌种选育和纯化,以提高其生产能力。

用管碟法(2.2)法,测定链霉素活菌剂的效价,估计效价为1 000 000 u/g,供试品最终浓度为1.4u/ml 及0.7u/ml。
链霉素的效价测定抗生素微生物检定法本法系在适宜条件下,根据量反应平行线原理设计,通过检测抗生素对微生物的抑制作用,计算抗生素活性(效性)的方法。
抗生素微生物检定包括两种方法,即管碟法和浊度法。
测定结果经计算所得的效价,如低于估计效价的90%或高于估计效价的110%时,应调整其估计效价,重新试验。
除另有规定外,本法的可信限率不得大于5%。
第一法管碟法本法系利用抗生素在琼脂培养基内的扩散作用,比较标准品与供试品两者对接种的试验菌产生抑菌圈的大小,以测定供试品效价的一种方法。
菌悬液的制备枯草芽孢杆菌(Bacillus subtilis)悬液取枯草芽孢杆菌[CMCC(B)63501]的营养琼脂斜面培养物,接种于盛有营养琼脂培养基的培养瓶中,在35~37℃培养7日,用革兰氏染色法涂片镜检,应有芽孢85%以上。
用灭菌水将芽孢洗下,在65℃加热30分钟,备用。
短小芽孢杆菌(Bacillus pumilus)悬液取短小芽孢杆菌[CMCC(B)63202]的营养琼脂斜面培养物,照上述方法制备。
金黄色葡萄球菌(Staphylococcus aureus)悬液取金黄色葡萄球菌[CMCC(B)26003]的营养琼脂斜面培养物,接种于营养琼脂斜面上,在35~37℃培养20~22小时。
临用时,用灭菌水或0.9%灭菌氯化钠溶液将菌苔洗下,备用。
藤黄微球菌(Micrococcus luteus)悬液取藤黄微球菌[CMCC(B)28001]的营养琼脂斜面培养物,接种于盛有营养琼脂培养基的培养瓶中,在26~27℃培养24小时,或采用适当方法制备的菌斜面,用培养基Ⅲ或0.9%灭菌氯化钠溶液将菌苔洗下,备用。
大肠杆菌(Escherichia coli)悬液取大肠杆菌[CMCC(B)44103]的营养琼脂斜面培养物,接种于营养琼脂斜面上,在35~37℃培养20~22小时。
链霉素的生产灰色链霉菌的扩大培养与保藏种子扩大培养:简称种子扩培.是发酵工程的一个组成部分,其实指将保存在砂土管、冷冻干燥管中处休眠状态的生产菌种接入试管斜面活化后,再经过扁瓶或摇瓶及种子罐逐级扩大培养,最终获得一定数量和质量的纯种过程。
种子扩培所得的纯种培养物称为种子。
种子扩培的一般过程:斜面菌种 → 一级种子培养(摇瓶) → 二级种子培养(种子罐) → 发酵● 种子应具备要求● 总量及浓度能满足要求。
● 生理状况稳定,个体与群体区隔明显。
● 活力强,移种发酵后,能够迅速生长。
无杂菌污染。
● 种子扩培的目的● 接种量的需要。
● 菌种的训化。
缩短发酵时间,保证生产水平。
种子的制备工艺实验室种子制备阶段:1琼脂斜面 2 固体培养基扩大培养 3摇瓶液体培养生产种子制备阶段:种子罐扩大培养斜面孢子培养● 将砂土管(或冷冻管)保持的链霉菌孢子接种到斜面培养基,于27℃下培养7天。
摇瓶种子培养 待斜面长满孢子后,制成悬浮液接入装有培养基的摇瓶中,于27℃下培养45-48小时,待菌丝生长旺盛。
链霉素的生产灰色链霉菌的扩大培养与保藏 链霉素的发酵与过程监控 链霉素的分离与效价测定种子罐扩大培养取若干个摇瓶,合并其中的培养液将其接种10%于种子罐内已灭菌的培养基,通入无菌空气搅拌,在罐温27℃下培养62-63小时,然后接入发酵罐内已灭菌的培养基中,通入无菌空气,搅拌培养,在罐温27℃下,发酵约7-8天。
幻灯片8斜面孢子培养:将砂土管(或冷冻管)菌种接种到斜面培养基上,经培养后即得原始斜面。
斜面培养基:可溶性淀粉20g,硝酸钾1g,氯化钠0.5g,磷酸氢二钾0.5g,硫酸镁0.5g,硫酸亚镁0.01g,琼脂20g,水1000毫升,PH7.2-7.4(配置时注意,可溶性淀粉要先用冷水调匀后再加入到以上培养基中)配制:按配方称量药品,加热搅拌至琼脂完全熔化,补水至1000ml。
趁热分装于18ml*180ml 试管,斜面以8ml为宜。

链霉素发酵工艺验证方案1.目的:确认链霉素发酵系统工艺流程,确认种子工艺、小小罐工艺、小罐工艺、中罐工艺、大罐发酵工艺,验证该发酵系统工艺的稳定性和可靠性及制备的发酵液能否达到中间体规格要求。
2.范围:此方案包括一个50吨大罐链霉素发酵液的生产过程。
2.1验证地点:403车间发酵工段:2.2验证对象:2.2.1原斜面2.2.2代1、代2斜面2.2.3母瓶2.2.4子瓶2.2.5小小罐2.2.6小罐2.2.7中罐2.2.8大罐2.3验证步骤:确定验证方案,确定验证计划,内容、步骤,以便准确验证链霉素发酵系统。
3.验证措施概要:3.1生产记录:原斜面:冷藏期≤10天外观无菌外观集落:白色丰满、正常代1或代2斜面:冷藏期≤14天外观无菌外观集落:白色丰满、正常母瓶:无菌斜面及外观无菌菌丝粘稠、色泽米黄、无颗粒状菌丝效价68小时≥1700u/ml效价96小时≥3500u/ml效价120小时≥6700u/ml冷藏期≤5天菌龄50~64小时菌丝II—III子瓶:无菌斜面及外观无菌菌丝粘稠、色泽米黄、无颗粒状菌丝效价120小时≥7000u/ml效价144小时≥7500u/ml冷藏期≤7天菌龄30~44小时菌丝II—III小小罐:菌丝II—III镜检无菌放罐效价≥800u/ml,残C≤3.5g/100ml,残N≤140mg/100ml,PH≤7.5小罐:菌丝II—III镜检无菌放罐效价≥1200u/ml,残C≤3.5g/100ml,残N≤140mg/100ml,PH≤7.5中罐:菌丝II—III镜检无菌放罐效价≥1800u/ml,残C≤3.5g/100ml,残N≤140mg/100ml,PH≤7.5大罐:放罐残糖≤2.0克/100毫升放罐残氮≤120毫克/100毫升放罐透光度≥40%放罐效价≥14000u/ml3.2原材料:生产过程中所用的各种原材料及其规格(见原材料一览表)3.3设备:生产链霉素所及设备见设备一览表。

硫酸链霉素皮试液的快速含量测定
徐敏
【期刊名称】《浙江大学学报(理学版)》
【年(卷),期】1994(000)003
【摘要】对硫酸链霉素的效价测定,中国药典采用微生物测定法。
微生物检测法虽然有效可靠,但操作繁琐,测定要求高,不适合基层医院快检室对自制药剂的质量控制。
链霉素皮试液是各医院的常用自制药剂,由于它含量低,化学方法和微生物法都难以
达到快速测定的要求,本文应用自动旋光仪对硫酸链霉素皮试液进行含量测定,得到
满意的结果。
1 标准液的配制与测量仪器硫酸链霉素标准液:取效价为740u/mg
的硫酸链霉素标准品,用生理盐水配成2×10~4u/ml的水溶液。
【总页数】1页(P343)
【作者】徐敏
【作者单位】不详;不详
【正文语种】中文
【中图分类】R978.12
【相关文献】
1.硫酸链霉素滴鼻乳剂的含量测定 [J], 胡琳;程桂林
2.硫酸链霉素滴鼻液的含量测定及有效期确定 [J], 潘莉;岳晓燕;卢登华
3.硫酸链霉素滴鼻乳剂的比色法含量测定 [J], 杨小骏;李红;江国振
4.青霉素皮试液含量测定方法及稳定性的实验研究 [J], 邢丽;王丽;郎奕
5.头孢唑啉钠皮试液的快速含量测定 [J], 徐敏[1];黄德华[2]
因版权原因,仅展示原文概要,查看原文内容请购买。

硫酸链霉素检验SOPGMP管理文件一、目的:建立硫酸链霉素检验的标准操作规程,保证正确操作。
二、依据:《中国兽药典》(2000年版一部)。
三、适用范围:适用于硫酸链霉素的检验。
四、责任者:QC检验员五、正文:1.质量标准:(见硫酸链霉素质量标准)。
2.试剂:2.01 乙醇 2.02 氯仿2.03 氢氧化钠试液 2.04 0.1%8-羟基喹啉的乙醇溶液 2.05 次溴酸钠试液 2.06 硫酸铁铵溶液2.07 氯化钡试液 2.08 盐酸2.09 醋酸铅试液2.10氢氧化钠试液2.11 五氧化二磷2.12氯化钠注射液2.13 0.9%无菌氯化钠溶液(以上均见试液、标准液、溶液配制标准操作规程)3.仪器与用具3.01 酸度计 3.02 薄膜过滤器3.03 干燥箱 3.04 平皿3.05 电子天平 3.06 培养箱3.07 微生物自动测量分析仪4.1 性状本品为白色或类白色的粉末;无臭或几乎无臭,味微苦;有引湿性。
本品在水中易溶,在乙醇或氯仿中不溶。
则判定该项合格。
4.2 鉴别:4.2.1 取本品约0.5mg,加水4ml溶解后,加氢氧化钠试液2.5ml与0.1%8-羟基喹啉的乙醇溶液1ml,放冷至约15℃,加次溴酸钠试液3滴,即显橙红色。
4.2.2取本品约20mg,加水5ml溶解后,加氢氧化钠试液0.3ml,置水浴上加热 5分钟,加硫酸铁铵溶液〔取硫酸铁铵0.1g,加0.5mol/L硫酸溶液5ml 使溶解〕0.5ml,即显紫红色。
4.2.3 本品的水溶液显硫酸盐的鉴别反应(详见硫酸盐检验标准操作规程)。
4.2.4结果判定:上述三项均呈正反应,则判定该项合格。
4.3 检查4.3.1 酸碱度取本品,加水制成每1ml中含20万单位的溶液,照PH值测定法测定(详见PH值测定法标准操作规程),PH值应为4.5-7.0,则判定该项合格。
4.3.2 溶液的澄清度与颜色取本品5份,各1.5g分别加水5ml使溶解,溶液应澄清无色;如显浑浊,与2号浊度标准液(详见溶液的澄清度检查标准操作规程)比较,均不得更浓;如显色,与各色5号标准比色液(详见溶液的颜色检查法标准操作规程第一法)比较,均不得更深,则判定该项合格。

蜂蜜中链霉素和双氢链霉素的测定(Copure®HLB)链霉素和双氢链霉素属于氨基糖苷类抗生素,对革兰氏阴性菌具有抑菌活性,可以预防多种动物疾病。
在养蜂行业中,链霉素和双氢链霉素能够有效地治疗蜜蜂的腐蛆病,但由于管理和使用的不科学,常造成蜂产品中该类物质的残留。
本实验参考国标BJS202103,对样品前处理进行优化后,建立了一个稳定可靠,回收率高,且适合动物源性蜂蜜中链霉素和双氢链霉素残留量测定的SPE-UPLC-MS/MS方法。
一、样品提取准确称取5g试样于50mL离心管中,加入10mL提取液(含2%三氯乙酸的磷酸盐缓冲溶液),涡旋混匀1min,超声提取10min,再加入10mL提取液并定容至25mL,涡旋混匀1min后超声提取5min,在10000r/min离心5min,待净化。
二、样品净化(Copure®HLB,60mg/3mL)活化:依次用3mL甲醇,3mL水活化Copure®HLB固相萃取小柱;上样:取5mL待净化液至已活化好的固相萃取小柱;淋洗:用2mL水淋洗固相萃取小柱两次,抽干小柱;洗脱:用1mL甲酸-乙腈-水(2:10:88,v:v:v)溶液洗脱,收集洗脱液,用2%氨化乙腈1mL定容至2mL,涡漩,过滤膜,上机测试。
三、标曲配制选同类型空白样品,依次加入适量混合标准中间溶液,按照样品提取和净化的步骤进行操作,配制成上机浓度分别为2.5ng/mL、5ng/mL、10ng/mL、20ng/mL、50ng/mL、100ng/mL的标准曲线。
四、仪器条件(Thermo Fisher TSQ Endura)液相部分:色谱柱:Hilic(2.1mm×100mm,2.7μm)流动相:A:5mmol/L乙酸铵溶液(含0.3%甲酸)B:乙腈(含0.3%甲酸)流速:0.3mL/min柱温:35℃进样量:10μL洗脱程序:梯度洗脱表1表1梯度洗脱程序时间/min A/%B/%0.010900.510902.590104.090104.110905.01090质谱条件:离子源:HESI电喷雾电压:3500V鞘气压力:40arb 辅气压力:10arb离子传输管:350℃辅气温度:375℃表2组分名称、保留时间及特征离子一览表(*为定量离子)名称母离子子离子链霉素582.2246.2,263.2*双氢链霉素584.2246.0,263.0*五、实验结果5.1测试数据表3加标回收率结果化合物5.00μg/kg10.0μg/kg20.0μg/kg回收率%RSD%(n=3)回收率%RSD%(n=3)回收率%RSD%(n=3)链霉素81.6 6.1286.1 5.2593.8 4.41双氢链霉素83.5 5.9490.8 5.11101 3.89 5.2测试色谱图图1蜂蜜加标样品总离子流图(20.0μg/kg)订购信息货号描述包装COHLB360Copure®HLB,60mg/3mL50支/盒SDC-3000-D biocomma®多管涡旋混匀仪1台/箱SF130-22-NL尼龙针式过滤器,直径13mm,孔径0.22μm,有机系100个/盒BN24智能水浴氮吹仪1台/箱SC2-12mL蓝色聚丙烯盖,白色PTFE/红色硅胶垫,9-425100个/盒V2-AL2mL螺纹棕色样品瓶,带书写处11.6*32mm,9-425100个/盒。

链霉素发酵实验分析及总结一、实验目的通过链霉素发酵获得链霉素,并测定相关参数;了解发酵的各个环节,综合运用本科阶段所学习的技能及知识。
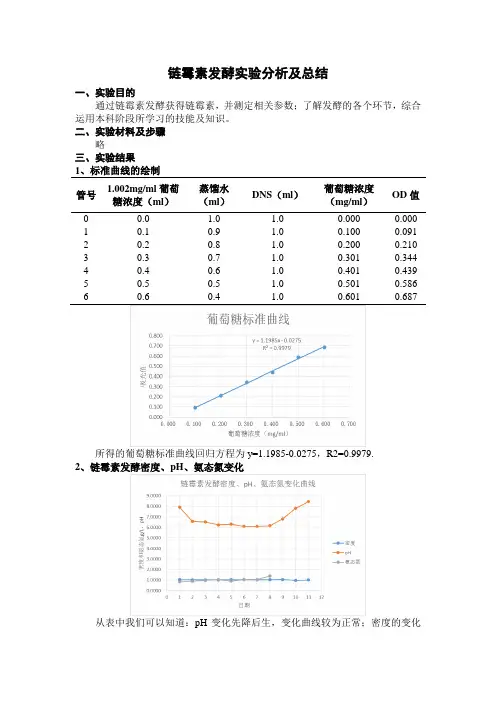
二、实验材料及步骤略三、实验结果1、标准曲线的绘制管号1.002mg/ml葡萄糖浓度(ml)蒸馏水(ml)DNS(ml)葡萄糖浓度(mg/ml)OD值0 0.0 1.0 1.0 0.000 0.0001 0.1 0.9 1.0 0.100 0.0912 0.2 0.8 1.0 0.200 0.2103 0.3 0.7 1.0 0.301 0.3444 0.4 0.6 1.0 0.401 0.4395 0.5 0.5 1.0 0.501 0.5866 0.6 0.4 1.0 0.601 0.687所得的葡萄糖标准曲线回归方程为y=1.1985-0.0275,R2=0.9979.2、链霉素发酵密度、pH、氨态氮变化从表中我们可以知道:pH变化先降后生,变化曲线较为正常;密度的变化处于平稳状态;而氨态氮含量缓慢上升。
3、链霉素发酵还原糖、总糖、菌体湿重变化从图中可知:还原糖、总糖含量一直在减小,菌体湿重总体上升。
四、实验分析及感想本次发酵实验做的较为失败,没有发酵出链霉素,效价无法检测。
可能原因有以下几点:第一,实验过程中发生过空压机的“罢工”,具体多少时间也不知道导致罐内缺氧;第二,链霉菌虽然生长,但可能是因为缺乏表达活性,无法表达链霉素;第三,通过镜鉴前期菌体量在逐步增加,后4-8天菌体量基本不变,到最后菌体量有所衰减,这样的现象可能是环境导致。
实验虽然没有成功,但实验过程中我收获良多:我学会了用dns法,见习了发酵罐的用法和接种的火焰圈法。
还有发酵罐的使用注意事项,对分光光度计有了更深的认识和了解,我相信这对我以后会有很大的帮助。
还有和同学共同完成实验的经验。
链霉素检验方法1. 试剂与材料1.1 链霉素试剂盒,德国r-Biopharm公司。
1.2 甲醇(99%),分析纯。
1.3 PBS缓冲液:0.62g NaH2PO4•2 H2O + 5.73g Na2HPO4•12 H2O + 9gNaCl,加双蒸水定容至1000ml1.4 提取缓冲液:2.0g庚烷-磺酸钠盐+ 1.90g Na3PO4•12 H2O; 加双蒸水定容至200ml,用磷酸调PH=2.02.仪器与设备2.1微孔板酶标仪,MuLtisKan Ascent,芬兰Labsystens公司。
2.2 8道移液器,50-300uL。
2.3 单道移液器,5-50ul,20-200ml,100-1000ul,1-5ml。
2.4 离心机。
2.5 旋转蒸发器,配真空冷却系统。
2.6 液体混匀器。
2.7 固相萃取装置。
3.样品前处理3.1样品提取称取约1g(准确至0.01g)蜂蜜于20ml具塞试管中,加入9ml提取缓冲液,在混匀器上混匀10分钟。
将上述样液转至10ml离心管中,以4300转/分离心17分钟至清亮。
3.2净化用RIDA C18柱(Art.No.:R2002)纯化提取物。
(所有试剂和样品处理必须在室温下进行)用2ml甲醇(99%)及2ml双蒸水洗涤柱子,流速为1滴/分钟;5ml离心管中提取液进柱,10滴/分钟;用3ml双蒸水洗涤柱子(以上洗脱液均弃去);用正压去除残留的液体并且用空气干柱子;用2ml甲醇(99%)洗脱,流速为10滴/分钟,洗脱液收集在一试管中,在40-50度减压旋转蒸干,用10mlPBS缓冲液溶解干燥的残留物,此为样品溶液,供酶标仪测定。
4.测定4.1 酶标仪测定条件酶标仪测定波长为450nm。
4.2 酶标测定(以下操作在20-24℃室温条件下进行)。
4.2.1测定之前的准备工作将链霉素酶试剂盒附带的所有试剂回升至室温20-24℃。
其中链霉素酶标记物、链霉素抗体用缓冲液1以1∶11的比例稀释,在吸取浓缩液之前,要仔细振摇使之充分混匀。
抗生素效价测定的方法
抗生素效价测定是用来评估抗生素药物对特定微生物的杀菌或抑菌能力的方法。
以下是几种常见的抗生素效价测定方法:
1. 系列稀释法:通过将抗生素药物制剂按照一定比例进行稀释,然后将每个浓度的药物与一定数量的微生物接种在培养基上,观察药物对微生物生长的影响。
根据微生物的生长情况,确定能抑制或杀灭微生物生长的最小药物浓度,即最低抑菌浓度(MIC)。
2. 纸片扩散法:将含有一定浓度抗生素的纸片放置在含有微生物的琼脂平板上,通过抗生素扩散至琼脂中的方式,形成药物浓度递减的梯度。
培养一段时间后,观察纸片周围菌落的生长情况,根据纸片周围菌落的性状和大小,判断抗生素在不同浓度下对微生物的效果。
3. 悬浮液法:将一定浓度的微生物悬浮液与不同浓度的抗生素药物混合,在一定时间后,通过感光度测定、比色法或荧光法等方法,测定混合液中微生物的生长情况,根据微生物的生长情况确定抗生素的效价。
4. 动物试验法:选择一种特定的动物模型,如小鼠、兔子等,将不同浓度的抗生素药物注射或灌胃给动物,观察抗生素对动物体内微生物的杀菌或抑菌效果。
根据动物的生理反应、细菌计数等指标,确定抗生素的效力。
需要注意的是,不同的抗生素和微生物对上述方法的适用性可能有所差异,具体选择方法时需要根据具体实验目的和条件进行判断。
此外,还需要遵循相关实验操作规范和安全操作指南,确保实验的准确性和安全性。
碟法测定硫酸链霉素效价的工作计划下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!本店铺为大家提供各种类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor. I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you! In addition, this shop provides you with various types of practical materials, such as educational essays, diary appreciation, sentence excerpts, ancient poems, classic articles, topic composition, work summary, word parsing, copy excerpts, other materials and so on, want to know different data formats and writing methods, please pay attention!一、背景介绍硫酸链霉素是一种广泛应用于医药和饲料行业的抗生素,其效价的测定对于产品质量的保障至关重要。
链霉素的皮试方法
链霉素的皮试方法
溶液配制
一、取链霉素1克(100万单位)加生理盐水3.5毫升,溶解后即成4毫升(25万单位/毫升)。
二、取上液0.1毫升,加生理盐水0.9毫升成2.5万单位/毫升。
三、取(二)液0.1毫升,加生理盐水
0.9毫升成2500单位/毫升。
四、取(三)液0.2毫升加生理盐水
0.8毫升成500单位/毫升。
皮试方法和结果观察
取皮试液0.1毫升(50单位)做皮内试验。
20分钟后,如局部出现中心晕团、周围红斑,直径大于1厘米,或局部红晕或伴有小水泡者为阳性。
注意事项
一、皮试阴性的患者,注射时也可发生过敏反应,故应做好抢救准备。
二、皮试方法,目前全国尚不统一。
已规定要做皮试的地区,应坚持下来。
链霉素效价测定方案试验目的: 1、设计链霉素效价测定方案2、 熟悉并掌握抗生素效价测定方法试验器材:双碟 陶瓦盖 钢管、钢管放置器、玻璃容器 、毛细滴管 、灭菌刻度吸管 、称量瓶 、恒温培养箱 、万分之一天平、干燥箱、恒温水浴箱 、显微镜、抑菌圈测量仪或游标卡尺 、超净工作台 、冰箱、酒精灯、接种环供试品称量量:50mg缓冲液:磷酸盐缓冲液(ph7.8)取磷酸氢二钾5.59g 与磷酸氢二钾0.41g,加水使成1000ml,摇匀滤过。
121℃蒸汽灭菌30min 备用。
培养基制备数量营养琼脂培养基:100ml,作为菌种活化用。
双碟数量:8套(供试品效价测定)+8套(预试验)。
共16副小钢管:32个(供试品效价测定)+32个(预试验),共64个,每个双碟中放置4个。
1个 供试品效价测定 4个 用于预试验5个每瓶100ml1个 用于预试验 1个供试品效价测定2个 每瓶250ml7个三角瓶操作步骤菌种1)枯燥芽孢杆菌【Bacillus subtilis CMCC(B) 63 501】2)枯燥芽孢杆菌菌悬液的制备菌液制备取枯燥芽孢杆菌的营养琼脂斜面培养物,加灭菌水2ml冲下菌苔,制成悬液,用吸管将此悬液接种于营养琼脂培养基上,均匀摊布,在37℃培养7天,取菌苔少许涂片,用革兰染色镜检,应有芽孢85%以上。
用灭菌水将芽孢洗下,制成芽孢悬液,合并至灭菌大试管内,65℃水浴内加热30min,将菌体杀死,待冷后放冰箱储藏为浓菌液。
供试品溶液的制备供试品估计效价1000000U/g.精密称取样品50.0mg,加水50ml,稀释制成1000U/ml溶液,吸取2ml加入100ml容量瓶中,加pH7.8磷酸盐缓冲液稀释至刻度,制成20U/ml溶液,吸取7ml加入100ml 容量瓶中,制成1.4U/ml溶液, 吸取25ml加入50ml容量瓶中,制成0.7U/ml溶液,作为滴碟用供试品及标准品溶液。
培养基Ⅰ胨5g 牛肉浸出粉3g磷酸氢二钾3g 琼脂20g 水1000ml除琼脂外,混合上述成分,调节ph值使比最总的ph值略高0.2,加入琼脂,加热溶化后滤过,调ph值使灭菌后为7.8~8.0,在115℃灭菌30min。
二氢链霉素,链霉素,壮观霉素和新霉素检测方法1.分析目标化合物农药等成分物质 分析目标化合物二氢链霉素和链霉素 二氢链霉素和链霉素 壮观霉素 壮观霉素新霉素 新霉素2.仪器设备高效液相色谱—质谱仪。
3.试剂除下列试剂外,使用附录2所列试剂。
七氟丁酸:七氟正丁酸庚磺酸钠:1-庚磺酸钠(特级)4.标准品盐酸壮观霉素:本品1.000mg含603µg以上效价的壮观霉素。
硫酸二氢链霉素: 本品1.000mg含720µg以上效价的二氢链霉素。
硫酸链霉素:本品1.000mg含718µg以上效价的链霉素。
硫酸新霉素: 本品1.000mg含680µg以上效价的新霉素。
5.试验溶液的制备a 提取方法①肌肉、脂肪、肝脏和肾脏肌肉:尽可能除去脂肪,搅碎混合均匀后,称取其5.00g。
脂肪:尽可能除去肌肉,搅碎混合均匀后,称取其5.00g。
肝脏和肾脏:搅碎混合均匀后,称取其5.00g。
加入25mL 1%的偏磷酸溶液,搅拌3分钟后,以每分钟3000转离心分离10分钟,脱脂棉过滤。
②奶称取5.00g样品,加入25mL 1%的偏磷酸溶液,搅拌3分钟后,用振荡器激烈振荡5分钟,以每分钟3000转离心分离10分钟,脱脂棉过滤。
③蛋除去蛋壳,充分均匀后,称取其5.00g,加入25mL 1%的偏磷酸溶液,搅拌均匀后,以每分钟3000转离心分离10分钟,脱脂棉过滤。
b、净化方法在十八烷基甲硅烷基化硅胶小柱(500mg)中,依次注入5mL甲醇和10mL水,舍去流出液。
柱中依次注入a 提取方法所得到的溶液和5mL水,流出液中加入2mL 0.1mol /L庚磺酸钠。
柱中再依次注入5ml甲醇和10mL水,舍去流出液。
依次注入前面加入了庚磺酸钠的溶液和5mL水,舍去流出液。
柱中注入10mL甲醇,收集流出液于磨口减压浓缩器中,40℃以下除去甲醇。
残留物中加入1.0mL乙腈:0.005mol/L七氟丁酸溶液(1:9)混合溶液溶解,此为试验溶液。
链霉素效价测定方案
试验目的: 1、设计链霉素效价测定方案
2、 熟悉并掌握抗生素效价测定方法
试验器材:
双碟 陶瓦盖 钢管、钢管放置器、玻璃容器 、毛细滴管 、灭菌刻度吸管 、称量瓶 、恒温培养箱 、万分之一天平、干燥箱、恒温水浴箱 、显微镜、抑菌圈测量仪或游标卡尺 、超净工作台 、冰箱、酒精灯、接种环
供试品称量量:50mg
缓冲液:
磷酸盐缓冲液(ph7.8)取磷酸氢二钾5.59g 与磷酸氢二钾0.41g,加水使成1000ml,摇匀滤过。
121℃蒸汽灭菌30min 备用。
培养基制备数量
营养琼脂培养基:100ml,作为菌种活化用。
双碟数量:8套(供试品效价测定)+8套(预试验)。
共16副
小钢管:32个(供试品效价测定)+32个(预试验),共64个,每个双碟中放置4个。
1个 供试品效价测定 4个 用于预试验
5个每瓶100ml
1个 用于预试验 1个供试品效价测定
2个 每瓶250ml
7个三角瓶
操作步骤
菌种
1)枯燥芽孢杆菌【Bacillus subtilis CMCC(B) 63 501】
2)枯燥芽孢杆菌菌悬液的制备
菌液制备
取枯燥芽孢杆菌的营养琼脂斜面培养物,加灭菌水2ml冲下菌苔,制成悬液,用吸管将此悬液接种于营养琼脂培养基上,均匀摊布,在37℃培养7天,取菌苔少许涂片,用革兰染色镜检,应有芽孢85%以上。
用灭菌水将芽孢洗下,制成芽孢悬液,合并至灭菌大试管内,65℃水浴内加热30min,将菌体杀死,待冷后放冰箱储藏为浓菌液。
供试品溶液的制备
供试品估计效价1000000U/g.精密称取样品50.0mg,加水50ml,稀释制成1000U/ml溶液,吸取2ml加入100ml容量瓶中,加pH7.8磷酸盐缓冲液稀释至刻度,制成20U/ml溶液,吸取7ml加入100ml 容量瓶中,制成1.4U/ml溶液, 吸取25ml加入50ml容量瓶中,制成0.7U/ml溶液,作为滴碟用供试品及标准品溶液。
培养基Ⅰ
胨5g 牛肉浸出粉3g
磷酸氢二钾3g 琼脂20g 水1000ml
除琼脂外,混合上述成分,调节ph值使比最总的ph值略高0.2,加入琼脂,加热溶化后滤过,调ph值使灭菌后为7.8~8.0,在115℃灭菌30min。
检菌为枯燥芽孢杆菌【Bacillus subtilis CMCC(B) 63 501 】双碟的制备
预实验
将培养基用微波炉融化,保温使温度降至60℃左右,取8套已灭菌双碟,每套中加20mlⅠ培养基,作为底层。
将另外四个装量为100ml的培养基,于58℃保温,30min底层凝固后,往100ml培养基中分别加入菌悬液2.0ml,1.5ml,1.0ml,0.5ml,摇匀,于每套双碟中分别加5ml,并迅速摇匀,作为菌层。
30min菌层凝固后,用钢管放置器,每套双碟中放入4只小钢管。
将滴好的双碟放入37℃恒温室中培养18h。
取出双碟,将钢管倒入消毒液中,盖上玻璃盖,用效价抑菌圈测量仪测量抑菌圈大小。
高剂量和低剂量的抑菌圈直径相差大于等于2mm的为最适加菌量。
供试品
将培养基用微波炉融化,保温使温度降至60℃左右,取8套已灭菌双碟,每套中加20mlⅠ培养基,作为底层,另一个100ml培养基,要于58℃保温,30min底层凝固后,往100ml培养基中加入菌悬液1.0ml(由预试验得到),摇匀,于每套双碟中分别加5ml,并迅速摇匀,作为菌层。
30min菌层凝固后,用钢管放置器,每套双碟中放入4只小钢管。
滴碟培养
取上述供试品溶液滴入钢管内,滴加顺序为:顺时
针,SH-TH-SL-TL。
将滴好的双碟放入37℃恒温室中培养18h。
取出双碟,将钢管倒入消毒液中,盖上玻璃盖,用效价抑菌圈测量仪测量结果。