5分子平均动能按自由度均分的统计规律
- 格式:ppt
- 大小:408.50 KB
- 文档页数:2









气体分子的方均根速率μ
RT
m kT v 332=
=
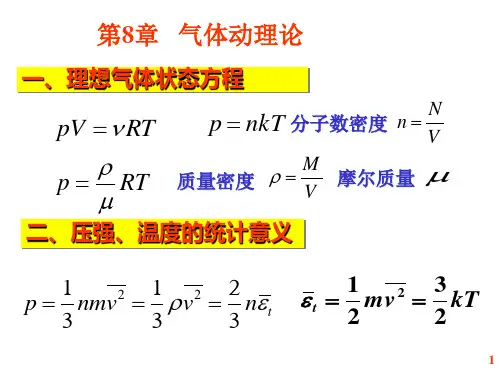
T (273K) 2H 2O 2N 空气 2v (m/s ) 1830 461 493 485 (5)压强的另一个公式
P =K n ε32=kT n 2
3
32⋅=nkT
P =nkT 理想气体状态方程的另一种表达式 比 PV=νRT 适用范围更广泛
例:推导道尔顿分压定律:混合气体压强等于各种气体分压强之和 解:设容器中有几种理想气体组成混合气体
T 相同,K K K εεε=== 21
总分子数密度 ++=21n n n P=K n ε32=K n n ε⋅++)(3221 =K n ε132+K n ε232
+ P = ++21P P
第4节 能量按自由度均分原理 理想气体内能
P =K n ε32,K ε=kT 2
3
考虑到分子结构,分子运动:平动,转动,振动
(注:专业文档是经验性极强的领域,无法思考和涵盖全面,素材和资料部分来自网络,供参考。
可复制、编制,期待你的好评与关注)。
能量按自由度均分定理能量按自由度均分定理能量按自由度均分定理是热力学的基本定理之一,它描述了一个系统中分子所具有的能量如何分布。
该定理表明,系统中每个自由度上的平均能量相等。
1. 能量和自由度在热力学中,一个系统的能量可以被划分为不同类型的能量,例如动能、势能、内能等。
而自由度则指一个分子或者原子可以在空间中运动的方向数。
例如,在三维空间中,一个粒子有三个自由度:x、y和z方向上的运动。
2. 能量按自由度均分定理的表述根据这个定理,一个系统中每个自由度上的平均能量相等。
具体而言,假设一个系统有N个粒子,每个粒子有f个自由度,则该系统总共有Nf个自由度。
如果该系统处于温度为T的热平衡状态下,则每个自由度上平均能量为:E = (1/2)kT其中k是玻尔兹曼常数。
3. 推导过程这个结论可以通过统计力学推导得出。
假设我们考虑一个单原子气体,它处于温度为T的热平衡状态下。
在这种情况下,我们可以将每个原子看作一个简谐振子,它在三个方向上都有能量。
根据统计力学,我们可以得到每个简谐振子的平均能量为:<E> = (1/2)kT因此,对于一个单原子气体而言,它的总能量就是每个原子的平均能量之和。
由于每个原子都有三个自由度(x、y、z方向),因此总共有3N个自由度。
根据能量按自由度均分定理,每个自由度上的平均能量相等,因此该系统中每个自由度上的平均能量为:E = (1/2)kT4. 应用能量按自由度均分定理在热力学中具有广泛的应用。
例如,在化学反应中,该定理可以用来预测反应物和产物之间转移的能量。
在材料科学中,该定理可以用来计算材料内部各种不同类型粒子(如电子、离子等)所占据的位置和状态。
5. 局限性虽然能量按自由度均分定理是热力学中非常重要的一个基本定理,但它也存在一些局限性。
例如,在低温下或者非常小尺寸的系统中,该定理可能不再适用。
此外,在分子之间存在相互作用的情况下,该定理也可能不再适用。
6. 结论能量按自由度均分定理是热力学中非常重要的一个基本定理,它描述了一个系统中分子所具有的能量如何分布。
《物理学》课程标准适用专业:高职电气自动化、生产过程自动化、机电一体化、应用电子技术、焊接自动化技术、检测技术、石化、分析、药分、安全、精细、应用化工技术适用学制:三制《物理学》课程标准课程名称:物理学总学时数: 88/60适用专业:高职电气自动化、生产过程自动化、机电一体化、应用电子技术、焊接自动化技术、检测技术、石化、分析、药分、安全、精细、应用化工技术一、课程定位1、课程性质公共基础课2、课程作用物理学是研究物质的基本结构、基本运动形式、相互作用的自然科学。
它的基本理论渗透在自然科学的各个领域,应用于生产技术的许多部门,是其他自然科学和工程技术的基础。
大学物理课程是高等学校理工科学生的一门重要基础课,它所阐述的物理学基本概念、基本思想、基本规律和基本方法不仅是学生学习后续专业课程的基础,而且也是培养和提高学生综合素质和科技创新能力的重要内容。
作为一名工程应用型技术人员,其物理基础的厚薄、掌握的好坏将影响到他们工作中的适应性、创造性。
二、课程设计(以能力目标指导下,基于职业教育[校企合作、工学结合、基于生产过程等]的课程整体开发设计说明);三、课程目标1、能力目标通过众多的理想模型的建立和应用,培养学生能根据问题的性质和需要,抓住主要因素,略去次要因素,对所研究的复杂问题进行合理简化处理的能力。
注意培养学生抽象思维的能力和理论联系实际的能力.培养学生运用物理的理论、观点和方法以及所掌握的高等数学工具分析、研究、计算或估算一般难度的物理问题的能力,并能把典型数据结果在量级上加以比较,对结果的合理性做出判断。
创造条件使学生多接触各种物理现象,在教学中加强观察和实验有利于激发起学生学习物理的兴趣,而对物理学习的兴趣又能对观察能力的培养起积极作用。
培养学生的自学能力。
在整个教学过程中,应注意有计划地、循序渐进地培养学生独立阅读教材和参考书的能力,并要求学生达到理解其主要内容和写出条理较清楚的笔记、小结和心得体会。