离子反应 2动画
- 格式:ppt
- 大小:1002.00 KB
- 文档页数:21



《离子反应第2课时》教学设计三、教学设计导入新课复习:电解质和电离的概念。
过渡:有上述知识作基础,下面我们学习离子反应和离子方程式。
电解质在溶液里的反应必定有离子的参加,离子间是如何进行反应的呢?反应的本质是什么呢?推进新课师:请同学们阅读课本P31~P32的内容,进行自学。
[思考]什么是离子反应?什么是离子方程式?[板书]二、离子反应和离子方程式。
1.离子反应:有离子参加的反应叫离子反应。
2.离子方程式:用实际参加反应的离子符号来表示反应的式子[问题1]教师演示[实验2-1]后填表,并写出反应的化学方程式。
化学方程式:NaCl+CuSO4(不反应)CuSO4+BaCl2====BaSO4↓(白)+CuCl2设计意图:学生通过操作实验仪器、观察实验现象,培养直觉行动思维。
师生活动::学生观察讨论后填表。
[问题2]从溶液中离子变化的角度,分析上述实验现象。
[分析]当CuSO4溶液与NaCl溶液混合时,没有发生化学反应,只是CuSO4电离出来的Cu2+、2-SO与Na+、Cl-等混合没有发生变化。
当B中CuSO4溶液与BaCl2溶液混合时,CuSO4电离4SO与BaCl2电离出来的Ba2+反应生成难溶的BaSO4白色沉淀。
出来的-24过渡:电解质在水作用下可解离成自由移动的阴、阳离子,这些电解质在溶液中发生的反应实质上是离子间的反应。
[板书]1.离子反应:有离子参加的反应叫离子反应。
过渡:如何表示离子反应呢?[板书]2.离子方程式:用实际参加反应的离子符号来表示反应的式子。
[问题3]通过教师演示[实验2-2]后观察实验现象,写出P32四个化学反应方程式。
设计意图:学生通过操作实验仪器、观察实验现象,培养直觉行动思维。
师生活动:引导学生观察实验现象,完成化学反应方程式。
[问题4]阅读P32回答问题:中和反应的实质是什么?答:酸和碱发生中和反应的实质就是由酸电离出的H+与碱电离出的OH-结合生成弱电解质H2O,其离子方程式:H++OH-====H2O,该电离方程式只表示强酸与强碱发生的中和反应(除去硫酸与氢氧化钡的中和反应)。


第四节离子反应第2课时离子反应的应用一、教学目标证据推理与模型认知:会书写离子方程式,熟知离子反应的应用,建立离子检验与推断的思维模型,学会常见物质的检验方法。
科学精神与社会责任:能从物质检验与含量测定、物质制备与纯化等化学任务角度举例说明离子反应的应用,能理解生活中常见的离子反应。
二、教学重难点离子的检验与推断三、教学过程【课程引入】【复习回顾】✓离子反应发生的条件:、、、;✓检验NH4+的反应;✓酸性条件下MnO4−与Fe2+发生氧化还原反应的离子方程式:。
【过渡】离子反应是多数物质在水溶液中进行的一类常见反应,利用离子的特征反应可以检验一些常见离子以及测定溶液中某些离子的浓度。
【新知讲解】(一)物质检验与含量测定1. 常见离子的检验【思考讨论】实验室有一瓶失去标签的溶液,可能是稀硫酸或稀盐酸中的一种。
如何检验?4们可以通过检验SO 42-或Cl -是否存在做出判断。
SO 42-的检验一般用可溶性钡盐,Cl -检验一般用AgNO 3溶液,但AgNO 3溶液遇到SO 42-会生成Ag 2SO 4微溶物,会干扰到AgCl 沉淀的观察,所以我们选择用BaCl 2溶液检验SO 42-是否存在。
方法:取少量待测液于试管中,加入几滴BaCl 2溶液,若有白色沉淀,则为硫酸;若无明显现象,则为盐酸。
【归纳总结】2. 测定溶液中离子的浓度 (1)沉淀法如溶液中SO 42-的浓度,用Ba 2+将其转化为BaSO 4沉淀,再称量沉淀的质量求得。
(2)酸碱中和滴定法如强酸溶液中H +的浓度可以用已知准确浓度的强碱溶液滴定的方法获得。
(3)氧化还原反应滴定法如溶液中MnO 4−的浓度可以用已知准确浓度的Fe 2+溶液滴定获得。
(二)物质的制备与纯化 1. 物质的制备【思考讨论】哪些常见物质可以通过离子反应制备?写出下列离子方程式。
• 用可溶性铜盐与氢氧化钠反应制备氢氧化铜: • 用铁与稀硫酸反应制备硫酸亚铁:• 用硫化物(如硫化亚铁)与稀硫酸反应制备硫化氢: • 实验室制取CO 2:氯碱工业:2Cl -+2H 2O===2OH -+Cl 2↑+H 2↑ 2. 物质的纯化 ➢ 粗盐提纯【思考讨论】粗盐的主要成分是NaCl ,此外还含有少量的Ca 2+、Mg 2+、SO 42−杂质。
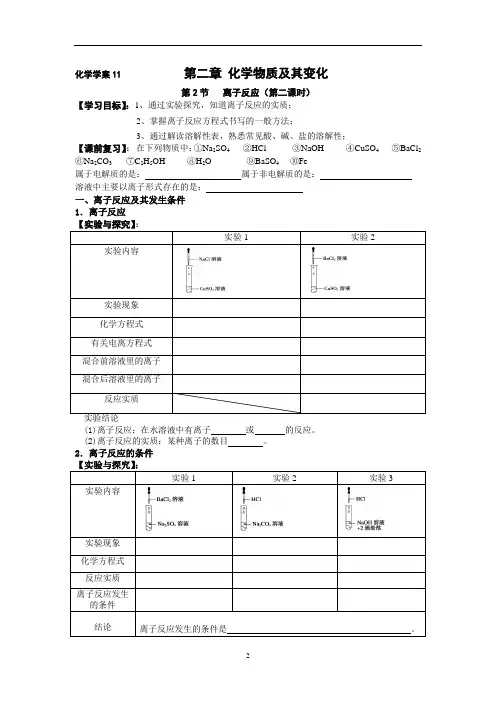
化学学案11第二章化学物质及其变化第2节离子反应(第二课时)【学习目标】:1、通过实验探究,知道离子反应的实质;2、掌握离子反应方程式书写的一般方法;3、通过解读溶解性表,熟悉常见酸、碱、盐的溶解性;【课前复习】:在下列物质中:①Na2SO4②HCl ③NaOH ④CuSO4 ⑤BaCl2⑥Na2CO3 ⑦C2H5OH⑧H2O⑨BaSO4 ⑩Fe属于电解质的是:属于非电解质的是:溶液中主要以离子形式存在的是:一、离子反应及其发生条件1.离子反应实验1 实验2 实验内容实验现象化学方程式有关电离方程式混合前溶液里的离子混合后溶液里的离子反应实质(1)离子反应:在水溶液中有离子或的反应。
(2)离子反应的实质:某种离子的数目。
2.离子反应的条件实验1实验2实验3实验内容实验现象化学方程式反应实质离子反应发生的条件结论离子反应发生的条件是。
【练习1】下列反应属于离子反应的是: ( )A.H2和O2反应生成水 B.锌片投入稀硫酸中C.KClO3加热分解制取O2D.H2还原CuOE. NaOH溶液与盐酸混和 F.盐酸与Na2CO3溶液混和G. CuSO4与NaOH溶液【小结】离子反应发生的条件是。
3、离子方程式(1)定义:用实际参加反应的表示离子反应的式子叫做离子方程式。
(2)离子方程式的书写(重要内容)步骤:四步。
(以盐酸与CaCO3反应为例)“写”:根据实验事实,写出正确的化学方程式;“拆”:反应物和生成物,以其在溶液中的主要存在形态出现。
如:的物质写成离子形式;的物质写成化学式形式。
(微溶物作反应物时,在溶液中就要拆;作生成物时就不拆。
)“删”:删去两边相同的离子,“查”:检查两边原子个数和电荷数是否相等、反应条件、沉淀符号、气体符号等。
(3)过关默写:离子形式:“易溶于水”且“易电离”:包括。
强酸:HCl、H2SO4、HNO3强碱:NaOH、KOH、Ba(OH)2、Ca(OH) 2化学式形式:单质、气体、氧化物。




离子反应第二课时
1.教学目标分析
①知识与技能:
⑴让学生理解离子反应的概念,掌握复分解型离子反应发生的条件;
⑵在学生掌握复分解型离子反应发生条件的基础上,能够分析溶液中离子的共存问题;
②过程与方法:
⑴通过组织学生实验探究的方法,掌握复分解型离子反应发生的条件,并在此基础上掌握溶液中离子共存问题
⑵学会运用观察、实验等多种手段获取信息,并运用比较、分类、归纳、概括等方法对信息进行加工。
③情感态度与价值观:
⑴通过学生自主探究获得知识,让学生体验科学知识获得和形成的过程与方法,体会成功的获得知识的乐趣。
⑵通过实验激发学生学习化学的兴趣和情感,对学生进行透过现象看本质的辩证唯物主义教育;
3.教学重点、难点和关键
重点:离子反应发生的条件的探究和提出问题、解决问题的方法与能力
难点:引导学生设计离子反应发生的条件的探究方案
2.教学过程。