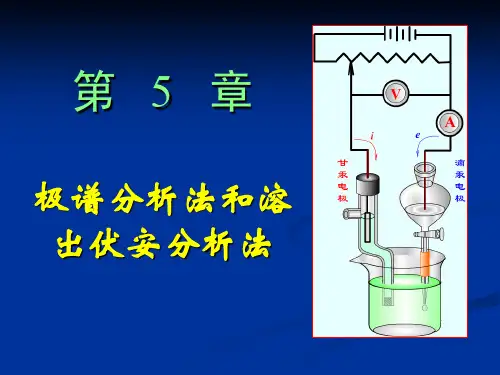
第五章 伏安法和极谱分析法
- 格式:doc
- 大小:94.00 KB
- 文档页数:3



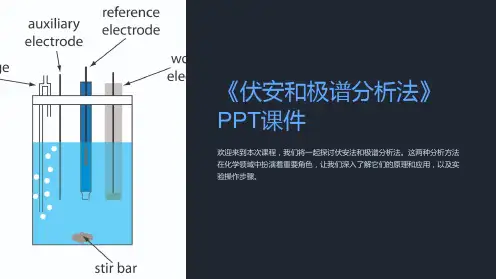
伏安与极谱分析法
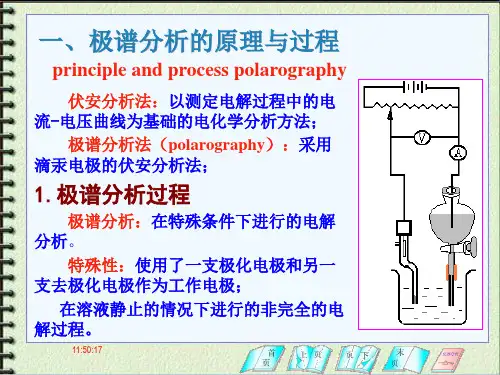
伏安与极谱分析法是根据电解池中所发生的电化学现象,通过记录电流-电压曲线进行分析的方法。
所不同的是伏安法使用固体或固定电极作工作电极而极谱法使用液态汞电极作工作电极,本章的重点、难点与需要掌握的知识要点如下:
1.极谱波的形成。
极谱定量分析的基础是极限扩散电流与溶液中待测离子的浓度呈正比,即i d =kC, 扩散电流方程式c 9nD 607id 6113/2m τ⋅⋅=
极谱定量方法:除标准曲线法之外,常用标准加入法 ;极谱波方程式描述了扩散电流与电位之间的关系,简单金属离子的极谱波方程式:i
i id lg n 059.0E E 21e d -+
=⋅,金属络合物的极谱波方程式: i i id n L n x Kc D D n E E Mc a e d -+--+︒=⋅lg 059.0]lg[059.0lg 2059.0lg 059.02121
i
i id lg n 059.0)E (E c e d 21-+
=⋅ 脉冲极谱法的基本原理和主要特点,单扫描示波极谱法的原理及其特点,循环伏安法的原理及特点,溶出伏安法的原理及其应用。
本章以课堂讲授的方式,学时分配为5。





第五章极谱与伏安分析法一、简答题1.伏安和极谱分析时一种特殊情况下的电解形式,其特殊表观在哪些方面2.极谱分析法采用的滴汞电极具有哪些特点在极谱分析法中为什么常用三电极系统3.什么是极化电极什么是去极电极试结合极谱分析加以说明。
4.何谓半波电位它有何性质和用途5.何谓极谱扩散电流方程式(也称尤考维奇方程式)式中各符号的意义及单位是什么6.影响极谱扩散电流的因素是什么极谱干扰电流有哪些如何消除7.极谱的底液包括哪些物质其作用是什么8.直流极谱法有哪些局限性应从哪些方面来克服这些局限性》9.试比较单扫描极谱法及循环伏安法的原理、特点和应用等方面的异同点。
10.试述脉冲极谱法的基本原理,为什么示差脉冲极谱法的灵敏度较高11.极谱催化波有哪些类型各类催化波产生的过程有何不同12.试述溶出伏安法的基本原理及分析过程,解释溶出伏安法灵敏度比较高的原因。
13.脉冲极谱的主要特点是什么14.单扫描极谱与普通极谱的曲线图形是否有差别为什么15. 在极谱分析中,为什么要使用滴汞电极16. 在极谱分析中,影响扩散电流的主要因素有那些测定中如何注意这些影响因素17.为何说极谱分析是一种特殊的电解分析18.在极谱分析中,为什么要加入大量支持电解质$19.极谱分析的定量依据是什么有哪些定量方法20.影响扩散电流的主要因素有哪些测定时,如何注意这些影响影响因素二、填空题型笔录式极谱仪由三部分组成,即主机、记录仪和。
2.滴汞电极的滴汞面积很,电解时电流密度很,很容易发生极化,是极谱分析的。
3.极谱极大可由在被测电解液中加入少量物质予以抑制,加入可消除迁移电流。
4. 是残余电流的主要部分,这种电流是由于对滴汞电极和待测液的形成的,所以也叫。
5.选择极谱底液应遵循的原则:好;极限扩散电流与物质浓度的关系;干扰少等。
6.我国生产的示波极谱仪采用的滴汞时间间隔一般为7s,在最后s才加上我的以观察i-v曲线。
;7.示波极谱仪采用三电极系统是为了确保工作电极的电位完全受的控制,而参比电极的电位始终保持为的恒电位控制体系,所以i-v即。
第五章 伏安法和极谱分析法
6.用直流极谱法测定某试样中铅的含量。
准确称取1.000g 样品溶解后转移至50mL 容量瓶中,加入5mL1mol ·L -
1KNO 3溶液,数滴饱和Na 2SO 3溶液和3滴0.5%动物胶,稀释
至刻度。
然后移取10.00mL 于电解池中,在-0.2―-1.0V 间记录极谱波。
测得极限扩散电流i d 为9.20μA ,再加入1.0mg ·mL -
1Pb 2+
标准溶液0.50mL ,在同样条件下测得i d 为22.8μA 。
试计算试样中铅的质量分数?扼要说明加入KNO 3、Na 2SO 3和动物胶的作用是什么?
解:由尤考维奇方程:i Kc = 加标前: x x i Kc = 加标后:0()
()
x x s s x s K c V c V i V V +=
+
两式相除得:0-1()1010.522.8()9.2(100.5)(22.810.59.210)9.20.5
0.0312(mg mL )
x x s s x x x s x x
x x i c V c V c i V V c c c c +⨯+⨯=⇒=⇒++⨯-⨯=⨯=
则试样中铅的质量分数30.031250
1.561011000
W -⨯=
=⨯⨯
7.在一定底液中测得1.25×10-
3 mol ·L -
1Zn 2+
的极限扩散电流i d 为7.12μA ,毛细管特性的t=3.47s ,m=1.42mg ·s -
1。
试计算Zn 2+
在该试液中的扩散系数为多少?
解:由尤考维奇方程:2113620607i zD m t c =
将各数值代入得:21136
2
13
2
6217.126072 1.42 3.47 1.25
3.0210
9.1210(cm s )
D D D ---=⨯⨯⨯⨯⨯=⨯=⨯ (注意各参数的单位)
8.在0.1 mol ·L -
1KCl 底液中,5.00×10-
3mol ·L -
1Cd 2+的极限扩散电流i d 为50.0μA ,
若汞在毛细管中的流速为18滴/min ,10滴汞重3.82×10-
2g ,求:
(1) Cd 2+
在KCl 溶液中的扩散系数;
(2) 若使用另一根毛细管,汞滴的滴落时间t 为3.0s ,10滴汞重为4.20×10-
2g ,计算
新的极限扩散电流值。
解:(1)由尤考维奇方程:211
36
2
0607i zD m t c =
得:22136
(
)607i D zm t c =
汞的流速为:2-13.8210181000
1.15mg s 10160
m -⨯⨯⨯=
=⨯⨯ 一滴汞滴落的时间60
3.3318
t s == 则
16
25212123336
3
50.0
(
)[
] 3.7710(cm s )
6076072(1.15)(3.33)(51010)
i D zm t c ---===⨯⨯⨯⨯⨯⨯⨯ (2)使用另一根毛细管后,汞的流速为:
2-14.20101000
1.40mg s 10 3.0
m -⨯⨯==⨯
则新的扩散电流为:
2121115333636
2206076072(3.7710)(1.40)(3.0)(51010)55.9(μA)
d i zD m t c --==⨯⨯⨯⨯⨯⨯⨯⨯= 9.若去极剂在滴汞电极上还原为可逆波。
在汞柱高度为64.7cm 时,测得极限扩散电流为1.71μA 。
当汞柱高度升至时83.1cm ,极限扩散电流为多少?
解:由公式12
d i kh =
当h 为64.7cm 时,有12
1.71(64.7)k = 当h 为83.1cm 时,有12
(83.1)d i k =
两式相除得1212
(83.1) 1.71 1.94(μA)(64.7)
d i =
⨯=
10.在0.10 mol ·L -
1NaClO 4溶液中,Ni 2+的半波电位为-1.02V(vs.SCE)。
在0.10 mol ·L
-1
NaClO 4和0.10 mol ·L
-1
乙二胺(en )溶液中,半波电位为-1.46V 。
试计算Ni(en)的稳定
常数。
解:由1/21/20.05920.0592
()()lg lg[]p c s K X z z
ϕϕ=-
-稳 将已知数据代入,其中p=3
17
0.05920.0592
1.46 1.02lg 3lg[0.10]22
lg 17.8657.3310K K K -=---⨯==⨯稳稳稳
12.在0.5 mol ·L -
1NaOH 溶液中CrO 42-在滴汞电极上还原得一极谱波。
当CrO 42-浓度
为2.00×10-
3mol ·L -
1, 在-1.10V(vs.SCE)时测得的极限扩散电流i d
为23.2μA 。
在-0.84V 时测得的电流i 为4.45μA 。
若CrO 42-在该溶液中的扩散系数为1.00×10-
5cm 2·s -
1,,试求z 和 值。
解:由211
36
20607i zD m t c =
则2111533
36
2
2
23.2
607(1.0010) 2.00 2.0010106073
d
i z D m t c --=
=
⨯⨯⨯⨯⨯⨯≈
由1/21/21/21/20.0592lg 0.059223.2 4.45
lg 3 4.45
0.840.012
0.852V
d d
e i i
z i
ϕϕϕϕϕ-=+
-+
-=+=-代入已知数据,得
-0.84=
15.用单扫描极谱法测定某试液中Ni 2+
的含量。
在含25.00mL 含Ni 2+
的试液(已加支
持电解质,动物胶并除O 2)中测得的峰电流i p 为2.36μA 。
当加入0.50mL2.87×10-
2mol ·L
-1
Ni 2+ 标准溶液后测得i p 为3.79μA ,试求试液中的Ni 2+浓度。
解:由p i kc = 加标前:2.36x kc =
加标后:323
()(0.0250.510 2.8710)
3.79()(0.0250.510)
x x s s x x s k c V c V k c V V ---+⨯+⨯⨯⨯==++⨯ 两式相除得:4
-1
910mol L x c -=⨯
,00.221
326132-
⋅S mg t m 为2
1ϕ。