羧酸衍生物
- 格式:doc
- 大小:1.92 MB
- 文档页数:58

(生物科技行业)第十三章羧酸衍生物第十三章羧酸衍生物学习要求1.掌握酰卤,酸酐,酯,酰胺的化学性质及相互间的转化关系。
2.熟悉酯缩合反应,霍夫曼降级反应等重要人名反应。
3.熟悉酯的水解反应历程。
4.掌握乙酰乙酸乙酯和丙二酸二乙酯在有机合成上的应用。
5.了解油脂的组成和性质;合成表面活性剂的类型及去污原理。
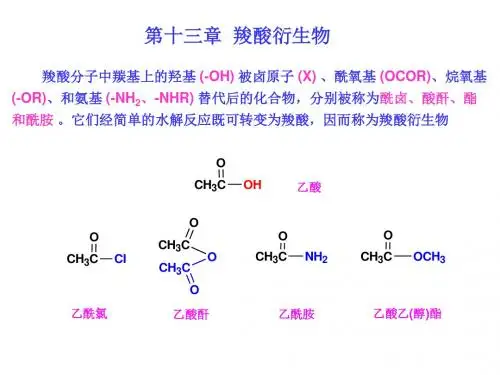
羧酸衍生物是羧酸分子中的羟基被取代后的产物,重要的羧酸衍生物有酰卤,酸酐,酯,酰胺。
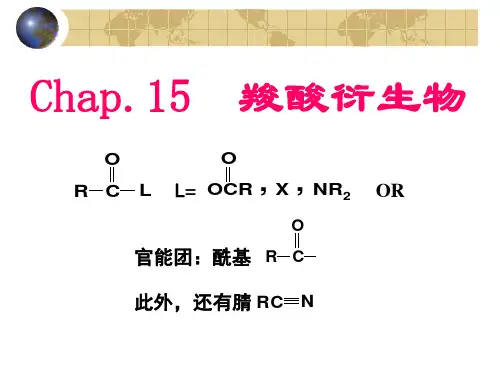
§13.1羧酸衍生物的结构和命名13.1.1羧酸衍生物的结构羧酸衍生物在结构上的共同特点是都含有酰基(),酰基和其所连的基团都能形成P-π共轭体系。
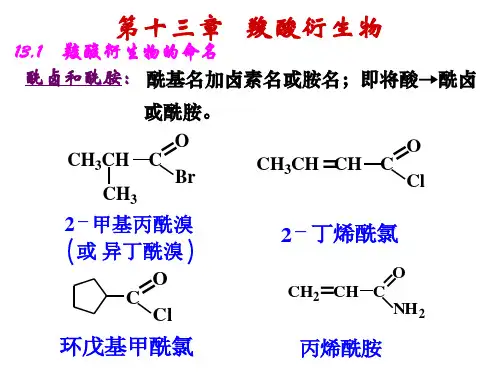
13.1.2羧酸衍生物的命名酰卤和酰胺根据酰基称为某酰某。
例见P386~387。
酸酐的命名是在相应羧酸的名称之后加壹“酐”字。
例如:酯的命名是根据形成它的酸和醇称为某酸某酯。
例如:13.1.3羧酸衍生物的光谱性质见P387~389(略)§13.2酰卤和酸酐13.2.1酰卤1.酰卤的制备酰卤的制取壹般是由羧酸和卤化磷或氯化亚砜作用而得。
2.物理性质无色,有刺激性气味的液体或低熔点固体。
低级酰卤遇水激烈水解。
乙酰氯暴露在空气中即水解放出氯化氢。
3.化学性质(1)水解、醇解、氨解(常温下立即反应)反应结果是在分子中引入酰基,故酰卤是常用的酰基化剂。
(2)和格氏试剂反应酰氯和格氏试剂作用能够得到酮或叔醇。
反应可停留在酮的壹步,但产率不高。
(3)仍原反应罗森蒙德(Rosenmund)仍原法可将酰卤仍原为醛。
13.2.2酸酐1.制备(1)由羧酸脱水而得,可制得单纯酐。
(2)混酐通过酰氯和羧酸盐作用制得。
2.物理性质(略)3.化学性质(1)水解、醇解、氨解(反应需稍加热)见P390。
酸酐也是常用的酰基化剂。
(2)柏琴(Perkin)反应酸酐在羧酸钠催化下和醛作用,再脱水生成烯酸的反应称为柏琴(Perkin)反应。
§13.3羧酸酯13.3.1来源和制法广泛存在于自然界。





羧酸衍生物羧酸衍生物是有机化学中最重要的一类化合物,这类化合物由羧酸和其衍生物组成,它们在医药及其他领域有着广泛的应用,是有机化学研究的主要焦点之一。
羧酸衍生物是由羧酸分子和其他不同化学结构的分子组合形成的有机化合物。
羧酸是一种具有一个羧基及以上的有机酸,按照水溶性的大小分为酒精型,醇型,酸型和碱型。
羧酸衍生物的其他分子可以是碳氢化合物、不饱和烃、烃类、碳氮化合物、醛类、酮类等等。
一般来说,羧酸衍生物具有很强的湿润性、高抗蚀性和良好的抗氧化性,可以用于改善纤维素,提高其物理性能以及防止其被氧化老化。
它也具有解吸性能,能够有效溶解纤维素结构,增强其耐受性和抗水性,从而改善纤维素的物理性质。
羧酸衍生物也可以用于保护植物,制备植物类医药剂,减少植物的损害,如光及抗盐的胁迫,从而促进植物的发育健康。
羧酸衍生物还可以用于制备多种医药产品,具有良好的药性,可以用来治疗各种疾病。
它们可以作为抗生素使用,增强机体免疫力,杀灭病原体,防止病原体的复制,从而有效治疗感染性疾病。
此外,它们还可以作为抗炎药使用,降低炎症的发生,减少肿痛,缓解疼痛,从而抑制肿瘤细胞的生长。
羧酸衍生物还可以用于制备抗癌药,有效抑制癌细胞的增殖,降低肿瘤恶化等。
羧酸衍生物还可以用于制造日常用品,如洗发水、洗衣液等。
由于其良好的抗菌性和卫生性,羧酸衍生物可以有效杀灭污染源,减少细菌的滋生,从而维护卫生,保护人们的健康。
羧酸衍生物的应用由于其独特的性质而受到广泛的重视,在有机化学研究中有着重要的地位,经过长期的研究,学者们发现它们具有多种重要的功能,在不同的领域都能发挥重要作用。
未来,羧酸衍生物将在药物研究中发挥更为重要的作用,为人类的健康和生命贡献更多。
羧酸的四大衍生物
羧酸的四大衍生物
羧酸是一类含有羧基(-COOH)的有机化合物,可作为各种化学反应
的重要中间体。
羧酸有多种衍生物,其中最常见的是如下四种。
一、酰氯(Acyl chloride)
酰氯是羧酸最常见的反应产物,它可以通过将羧酸与氯化物反应制得。
酰氯是一个非常重要的中间体,可用于合成酯、醚、酰胺等多种化合物。
酰氯有弱腐蚀性,可多用于有机合成实验室中。
二、酐(Anhydride)
酐是两个羧酸分子缩合而成的产物,分为内酐和外酐两种。
内酐是指
两个羧基在同一分子内缩合而成的环状产物,外酐则是指两个羧基不
在同一分子内缩合而成的非环状产物。
酐也可作为中间体用于合成酯、酰胺等化合物。
三、酸酐(Acid anhydride)
酸酐是两个不同羧酸分子缩合而成的产物,以其极强的反应性而闻名。
酸酐可用于合成酸酐酯、酸酰胺、酸酐酸等化合物。
但由于其极易水解,因此在使用过程中需要特别注意。
四、酯(Ester)
酯是羧酸的一种重要衍生物,它由羧酸和醇反应而成。
酯具有良好的挥发性和揮發性,并可用于制备香精、香料、油漆等多种化合物。
酯也可作为用于制硝化纤维、炸药等的重要中间体。
在有机合成中,酰氯、酐、酸酐和酯均属于常见的重要中间体。
它们在不同条件下均可相互转化,因此在尝试合成某种化合物时,应根据需要灵活选择相应的羧酸衍生物。
羧酸衍生物的名词解释羧酸衍生物,指的是一类有机化合物,它们是由羧酸经过化学反应生成的衍生物。
羧酸是一类含有一个羧基(-COOH)的有机化合物,常见的例子如乙酸(CH3COOH)和苹果酸(C4H6O5)。
羧酸衍生物在化学和生物学领域中具有广泛的应用和重要的作用。
羧酸衍生物通常可以通过与其他化合物发生反应而形成。
其中一种常见的反应是酯化反应,即羧酸与醇反应生成酯。
酯是一类含有羧酸酯基(-COOR)的化合物,常见的例子如乙酸乙酯(CH3COOCH2CH3)。
酯具有良好的溶解性和挥发性,广泛用于涂料、溶剂和香料等行业。
除了酯化反应,羧酸衍生物还可以通过羧酸的脱羟基反应生成醛或酮。
脱羟基反应是指羧基上的羟基(-OH)被除去,形成含有碳氧双键的化合物。
醛和酮是含有羰基(C=O)的化合物,分别具有一个和两个碳氧双键。
醛和酮在有机合成和医药化学中都有广泛的应用,可用于合成药物、香料和精细化学品等。
此外,羧酸衍生物还可以通过与胺反应生成酰胺。
酰胺是含有羰基和氮原子的化合物,具有良好的稳定性和溶解性。
酰胺在医药化学和材料科学中具有重要的应用,可用于合成抗生素、聚合物和荧光染料等。
另一类羧酸衍生物是酰氯,它们是羧酸与一分子的氯化亚砜(SOCl2)发生反应而形成的。
酰氯具有很高的反应活性,可与许多化合物发生酰化反应。
酰氯在有机合成和材料科学中具有广泛的应用,可用于合成酰胺、酰化反应和聚合物的修饰等。
总的来说,羧酸衍生物是一类重要的有机化合物,它们通过与其他化合物发生反应,形成具有不同功能和性质的衍生物。
羧酸衍生物在化学和生物学领域中起着重要的作用,广泛应用于药物合成、材料科学和化工工艺等领域。
通过深入研究和理解羧酸衍生物的性质和反应机制,我们可以进一步拓展其应用领域,并为新的化学合成和药物研发提供新的思路和方向。
第十三章羧酸衍生物教学目的:掌握酰卤,酸酐,酯,酰胺的化学性质及相互间的转化关系,乙酰乙酸乙酯和丙二酸二乙酯在有机合成上的应用;熟悉酯缩合反应,霍夫曼降级反应等重要人名反应以及酯的水解反应历程。
了解油脂的组成和性质,合成表面活性剂的类型及去污原理。
教学重点:羧酸衍生物中羰基上的亲核取代反应和反应历程(特别是酯的水解反应历程)、羧酸衍生物在有机合成中的应用和几个重要的有机人名反应等。
教学难点:对不同结构的羧酸衍生物中羰基上的亲核取代反应历程的理解。
第一节羧酸衍生物的分类、命名和光谱性质一、羧酸衍生物的分类·1·羧酸衍生物是羧酸分子中的羟基被取代后的产物,重要的羧酸衍生物有酰卤,酸酐,酯,酰胺。
二、羧酸衍生物的命名酰卤和酰胺根据酰基称为某酰某,即将相应的酰基的名称放在前面,卤素或胺放在后面合起来命名。
例如:酸酐的命名是在相应羧酸的名称之后加一“酐”字。
例如:酯的命名是根据形成它的酸和醇称为某酸某酯。
例如:CH 3C O ClCH 2CH C O BrC O N(CH 3)2NH O N,N-=甲基苯甲酰胺戊内酰胺丙烯酰溴乙酰氯CH 3C O O C OCH 3CH 3C O O C OCH 2CH 3C C O O 乙酸酐乙酸丙酸酐1,2环己烯二甲酸酐CH 3C OO CH 2CH=CH 2CH 3O OH CH 2CH OOCH 3乙酸烯丙酯甲酸甲酯丙烯酸甲酯RCOOH RCOX RC RCNH 2RCOCOR 羧酸酯酸酐酰卤酰胺·3·三、羧酸衍生物的物理性质1. 沸点:分子量相近的衍生物比较,酰卤、酸酐和酯,由于它们分子间不能形成氢键,所以沸点一般比分子量相近的羧酸低。
酰氨分子中含有氨基,它们分子间能形成氢键。
由于酰氨分子间缔合能力较强,因此沸点甚至比相应的羧酸还要高。
2. 密度:酸酐的密度 〉1;脂肪族一元羧酸酯的密度均〈 1; 二元羧酸酯和芳酸酯的密度均 〉1。
3.水溶性:酰氯强烈水解,放出大量的HCl 及热量。
低级酰胺可溶于水。
四、羧酸衍生物的光谱性质CHCOOC 2H 5CH 2COOC 2H 5CH 3C O OC OO CH 2甲基丁二酸二乙酯环戊基甲酸环己酯苯甲酸苄酯C ROH NC ROH HH1. 酰氯:C=O伸缩振动吸收峰在1800cm-1区域。
如和不饱和基或芳环共轭,C=O吸收峰下降至1750cm-1~1800cm-1。
2. 酸酐:C=O有两个伸缩振动吸收峰在1800cm-1~1850cm-1区域和1740cm-1~1790cm-1区域。
两个峰相隔约60 cm-1。
C-O的伸缩振动吸收峰在1045cm-1~1310cm-1。
3. 酯的C-O在1050cm-1~1300cm-1区域有两个强的伸缩振动吸收峰。
可区别于酮。
4. 酰氨:C=O伸缩振动吸收峰低于酮,在1630cm-1~1690cm-1区域。
N-H伸缩振动吸收峰在3050cm-1~3550cm-1区域内。
酰胺的核磁共振谱中CONH的质子吸收峰出现在5~8的范围内。
其吸收峰宽而矮。
第二节酰卤和酸酐一、酰卤1.酰卤的制备酰卤的制取一般是由羧酸与卤化磷或氯化亚砜作用而得。
2.物理性质无色,有刺激性气味的液体或低熔点固体。
低级酰卤遇水激烈水解。
乙酰氯暴露在空气中即水解放出氯化氢。
3. 化学性质(1)水解、醇解、氨解(常温下立即反应)H2ONH3RCOCl + ROH'RCOOHRCONH2+++HClHClHCl'反应结果是在分子中引入酰基,故酰卤是常用的酰基化剂。
(2)与格氏试剂反应酰氯与格氏试剂作用可以得到酮或叔醇。
反应可停留在酮的一步,但产率不高。
二、酸酐R CX+ R'MgX R CR'OMg XX R COR'R CR'R'OMg X2R CR'R'OH酮叔醇·5·1.制备(1) 由羧酸脱水而得,可制得单纯酐。
(2) 混酐通过酰氯与羧酸盐作用制得。
2.物理性质 (略) 3.化学性质(1)水解、醇解、氨解(反应需稍加热)。
R C O C R OO+R C O OH R C O OH+NH 2R C OR C O OH R C O OHH 2OR 'NH R C O O R '++酸酐也是常用的酰基化剂。
(2)柏琴(Perkin )反应酸酐在羧酸钠催化下与醛作用,再脱水生成烯酸的反应称为柏琴(Perkin )反应。
第三节 羧 酸 酯一、来源与制法+CHOCH C RHCOOH OH 2RRCH 2CRCH 2C O O·7·广泛存在于自然界,是生命不可缺少的物质。
酯可通过酯化反应、酰卤或酸酐的醇解、羧酸钠盐与卤代烃作用等方法制得。
二、物理性质酯常为液体,低级酯具有芳香气味,存在于花、果中。
例如,香蕉中含乙酸异戊酯,苹果中含戊酸乙酯,菠萝中含丁酸丁酯等等。
酯的比重比水小,在水中的溶解度很小,溶于有机溶剂,也是优良的有机溶剂。
其常见酯的物理常数见P 40表13-2。
三、酯的化学性质 1.水解、醇解和氨解(1)水解 酯的水解没有催化剂存在时反应很慢,一般是在酸或碱催化下进行。
(2)醇解(酯交换反应) 酯的醇解比较困难,要在酸或碱催化下加热进行。
R C OOR' + H 2OR C OOH R C OONa+ R'OH + R'OH酯化的逆反应皂化反应R C OOR'+ R'OH + R''OH H or OHR C OOR''酯醇新的酯新的醇因为酯的醇解生成另一种酯和醇,这种反应称为酯交换反应。
此反应在有机合成中可用与从低级醇酯制取高级醇酯(反应后蒸出低级醇)。
(3)氨解酯能与羟氨反应生成羟肟酸。
羟肟酸与三氯化铁作用生成红色含铁的络合物。
这是鉴定酯的一种很好方法。
酰卤、酸酐也呈正性反应。
2.与格氏试剂反应酯与格氏试剂反应生成酮,由于格氏COOCH 3COOCH 3+ 2HOCH 2CH 2OHHCOOCH 2CH 2OHCOOCH 2CH 2OH+ 2CH 3OHR OOR'+ NH 3R C ONH 2 + R'OHRCOOC 2H 5 + NH 2OH.HCl RCONHOH + C 2H 5OH 羟肟酸RCONHOH + FeCl 3羟肟酸R CN HFe + 3HCl3红色含铁络合物·9·试剂对酮的反应比酯还快,反应很难停留在酮的阶段,故产物是第三醇。
具有位阻的酯可以停留在酮的阶段。
例如:3.还原反应酯比羧酸易还原,可用多种方法(催化氢化、LiAlH 4、Na + C 2H 5OH 等还原剂)还原,还原产物为两分子醇。
见P 41-42。
酯在金属(一般为钠)和非质子溶剂中发生醇酮缩合,生成酮醇。
这是用二元酸酯合成大环化合物很好的方法。
R C OOC 2H 5R'MgXR C O MgX R R'OR'MgX2C OHR'R'(CH 3)3CCOOCH 3 + C 3H 7MgCl(CH 3)33OC 3H 7-C-O-C 2H 5C 3H 7C OOC 2H 5ONaC 3H 7COC 3H 7C O C 3H 2H 53H 7C O 2H 5OC 3H 7COHC 3H 7C O C 3H 7COC 3H 7C O NaHH4.酯缩合反应有α-H 的酯在强碱(一般是用乙醇钠)的作用下与另一分子酯发生缩合反应,失去一分子醇,生成β-羰基酯的反应叫做酯缩合反应。
(1) 克莱森(Claisen )缩合。
例如: 历程:(CH 2)8COOCH 33Na HAc二甲苯(CH 2)8C C OHO CH 3COC 2H 5OCH 3COC 2H 5O+C 2H 5ONaCH 322H 5 + C 2H 5OH O O乙酰乙酸乙酯CH 3CH 2C-OC 2H 5CH 3CH 2C-CH-COOC 2H 5C 2H 5OHOOOCH 32C 2H 5ONa+C 2H 5C 2H 5OHH CH 2COC2H 5OCH 2COC 2H 5OCH 2COC 2H 5OCH 3COC 2H 5O 2COOC 2H 5CH 3COC 2H 5O·11·(2)交叉酯缩合两种不同的有α-H 的酯的酯缩合反应产物复杂,无实用价值。
无α-H 的酯与有α-H 的酯的酯缩合反应产物纯,有合成价值。
例如;酮可与酯进行缩合得到β-羰基酮。
(3)分子内酯缩合——狄克曼(Dieckmann )反应。
己二酸和庚二酸酯在强碱的作用下发生分子内酯缩合,生成环酮衍生物的反应称为狄克曼(Dieckmann )反应。
例如:H O2COOC 2H 525H C OCHCOOC 2H 5CH3C 6H 5225C C OC 2H 5O25C C O 2H 5OC 2H 5OC 6H 5CH 2CH 22COOC 2H 52C--OC H 5OC 2H 5ONaCH 2CH 2CH 2COOC 2H 52COCH 3CCH 2COC 2H 5OOC 2H 5OCH 3COC 2H 5CH 2COOC 2H 5O缩合产物经酸性水解生成β-羰基酸,β-羰基酸受热易脱羧,最后产物是环酮。
狄克曼(Dieckmann )反应是合成五元和六元碳环的重要方法。
第四节 油脂和合成洗涤剂一、油脂油脂普遍存在于动物脂肪组织和植物的种子中,习惯上把室温下成固态的叫酯,成液态的叫油。
油脂是高级脂肪酸甘油酯的通称。
组成甘油酯的脂肪酸绝大多数是含偶数碳原2CH 2C C 25OC 2H 5OOCH 2CHC C OC 2H 5OO C H ONaCOOC 2H 5O2COOH OO +CO 2子的直链羧酸,其中有饱和的,也有不饱和的。
液态油比固态脂肪会有较多量的不饱和脂肪酸甘油酯。
相关概念:1.干性:某些油涂成薄层,在空气中就逐渐变成有韧性的固态薄膜。
油的这种结膜特性叫做干性(或称干化)。
油的干性强弱(即干结成膜的快慢)是和油分子中所含双键数目和双键结构有关系的,含双键数目多的,结膜快,数目少,结膜慢。
有共轭双键结构体系的比孤立双键体系的结膜快。
成膜是由于双键聚合形成高分子聚合物的结果。
桐油结膜快是由于三个双键形成共轭体系。
顺,反,反,—9,11,13—十八三烯酸2.碘值:不饱和脂肪酸甘油酯的碳碳双键也可以和碘发生加成反应。
100g油脂所能吸收的碘的克数称为碘值(又称碘价)。
二.肥皂和合成洗涤剂1.肥皂:肥皂的制造:·13·2.合成系涤剂a.阴离子洗涤剂溶于水时其有效部分是阴离子。