元素周期表的知识点整理(终极版)
- 格式:doc
- 大小:365.67 KB
- 文档页数:12

一、元素周期表的结构(一)编排三原则:1. 按原子序数递增顺序从左到右排列。
2. 将电子层数相同的元素排列成一个横行。
3. 把最外电子层的电子数相同的元素按电子层数递增的顺序由上而下排列成纵行。
(二)周期:具有相同电子层数的元素按照原子序数递增的顺序排列的一行,叫周期。
(1)周期序数= 电子层数。
周期序数用阿拉伯数字表示。
(2)元素周期表目前有7个周期。
第1、2、3周期称为短周期,分别含有2、8、8种元素;第4、5、6、7周期称为长周期,分别含有18、18、32、26种元素;第7周期又称为不完全周期。
(三)族(1)元素周期表有18个纵行,称为族,共16个族。
族序数用罗马数字表示。
(2)元素周期表中含有7个主族(ⅠA族~ⅦA族)、7个副族(ⅢB族~ⅦB族、ⅠB族~ⅡB族)、1个第Ⅷ族(三个纵行)和1个0族(稀有气体)。
(3)主族元素族序数= 最外层电子数。
(4)稀有气体元素化学性质不活泼,很难与其他物质发生化学反应,把它们的化合价定为0,因而叫做0族。
二、元素的性质与元素在周期表中位置的关系(一)元素的金属性和非金属性与元素在周期表中位置1、同周期从左到右,元素的金属性减弱,非金属性增强。
2、同主族从上至下,元素的金属性增强,非金属性减弱。
3、(1(2域;(312、主族元素化合价的判断。
(1)元素最高正化合价的数值=族的序数=最外电子层电子数(即价电子数)(2)非金属元素最低负化合价的绝对值=8-其最高正化合价三、元素周期律和元素周期表的意义1869年,门捷列夫发现了元素周期律,并编制了第一张元素周期表。
元素周期表是学习研究的一种重要工具。
门捷列夫用元素周期律预言了未知元素,为发现新元素提供了线索。
元素周期律与元素周期表可以指导工农业生产。
【典型例题】[例1] 对比下列两组元素性质:(1)下列各组元素最高价氧化物对应的水化物碱性逐渐减弱、酸性逐渐加强的是( )A. NaOH 、2)(OH Mg 、43PO H 、42SO HB. KOH 、NaOH 、42SO H 、4HClOC. 2)(OH Ca 、2)(OH Ba 、4HBrO 、4HClOD. 2)(OH Mg 、2)(OH Ba 、43PO H 、42SO H(2)下列各组气态氢化物稳定性由强到弱的顺序正确的是( )A. 4SiH 、3PH 、S H 2、HClB. HF 、HCl 、HBr 、HIC. 3PH 、S H 2HCl 、HFD. 3NH 、3PH 、3AsH 、HF精析:(1)A 项第三周期的Na 、Mg 、P 、S 四元素最高价氧化物的水化物的碱性逐渐减弱,酸性逐渐增强。

《元素周期律》知识清单一、元素周期律的定义元素周期律是指元素的性质随着原子序数的递增而呈现周期性变化的规律。
这一规律是化学学科中的重要基石,对于理解元素的性质、化合物的形成以及化学反应等方面都具有极其重要的意义。
二、元素周期表的结构1、周期元素周期表共有 7 个周期。
周期的序号等于该周期元素原子具有的电子层数。
第一周期仅有 2 种元素,称为短周期;第二、三周期各有 8 种元素,也属于短周期;第四、五周期各有 18 种元素,称为长周期;第六、七周期包含的元素较多,分别称为长周期和不完全周期。
2、族元素周期表共有 18 个纵行,分为 16 个族。
7 个主族(ⅠA 族至ⅦA 族)、7 个副族(ⅠB 族至ⅦB 族)、1 个第Ⅷ族(包括 3 个纵行)和 1 个 0 族。
主族元素的族序数等于其最外层电子数;副族元素的族序数与最外层电子数和次外层电子数有关。
3、分区根据元素原子的价电子排布,元素周期表可以分为 s 区、p 区、d 区、ds 区和 f 区。
s 区包括第ⅠA 族和第ⅡA 族,价电子排布为 ns1-2;p 区包括第ⅢA 族至第ⅦA 族以及 0 族,价电子排布为 ns2np1-6;d 区包括第ⅢB 族至第ⅦB 族以及第Ⅷ族,价电子排布为(n 1)d1-10ns1-2;ds 区包括第ⅠB 族和第ⅡB 族,价电子排布为(n 1)d10ns1-2;f 区包括镧系和锕系元素。
三、元素性质的周期性变化1、原子半径同一周期,从左到右,原子半径逐渐减小(稀有气体元素除外);同一主族,从上到下,原子半径逐渐增大。
原子半径的大小主要取决于电子层数和核电荷数。
电子层数越多,原子半径越大;核电荷数越大,对核外电子的吸引力越强,原子半径越小。
2、主要化合价同一周期,从左到右,最高正化合价逐渐升高(第一周期除外),最低负化合价的绝对值逐渐减小;同一主族,化合价相似,最高正化合价等于主族序数(O、F 除外)。
3、金属性和非金属性同一周期,从左到右,金属性逐渐减弱,非金属性逐渐增强;同一主族,从上到下,金属性逐渐增强,非金属性逐渐减弱。
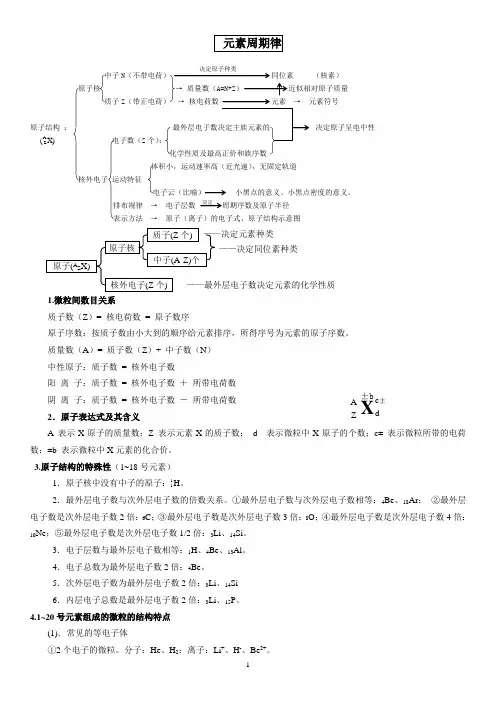
中子N(核素) 原子核质子Z → 元素符号原子结构 : 决定原子呈电中性电子数(Z 个):化学性质及最高正价和族序数 体积小,运动速率高(近光速),无固定轨道核外电子 运动特征电子云(比喻) 小黑点的意义、小黑点密度的意义。
排布规律 → 电子层数 周期序数及原子半径表示方法 → 原子(离子)的电子式、原子结构示意图1.微粒间数目关系质子数(Z )= 核电荷数 = 原子数序原子序数:按质子数由小大到的顺序给元素排序,所得序号为元素的原子序数。
质量数(A )= 质子数(Z )+ 中子数(N )中性原子:质子数 = 核外电子数阳 离 子:质子数 = 核外电子数 + 所带电荷数阴 离 子:质子数 = 核外电子数 - 所带电荷数2.原子表达式及其含义 A 表示X 原子的质量数;Z 表示元素X 的质子数; d 表示微粒中X 原子的个数;c± 表示微粒所带的电荷数;±b 表示微粒中X 元素的化合价。
3.原子结构的特殊性(1~18号元素)1.原子核中没有中子的原子:11H 。
2.最外层电子数与次外层电子数的倍数关系。
①最外层电子数与次外层电子数相等:4Be 、18Ar ; ②最外层电子数是次外层电子数2倍:6C ;③最外层电子数是次外层电子数3倍:8O ;④最外层电子数是次外层电子数4倍:10Ne ;⑤最外层电子数是次外层电子数1/2倍:3Li 、14Si 。
3.电子层数与最外层电子数相等:1H 、4Be 、13Al 。
4.电子总数为最外层电子数2倍:4Be 。
5.次外层电子数为最外层电子数2倍:3Li 、14Si6.内层电子总数是最外层电子数2倍:3Li 、15P 。
4.1~20号元素组成的微粒的结构特点(1).常见的等电子体①2个电子的微粒。
分子:He 、H 2;离子:Li +、H -、Be 2+。
决定 X)(A Z 原子(A Z X) 原子核核外电子(Z 个) 质子(Z 个) 中子(A-Z)个 ——决定元素种类 ——决定同位素种类 ——最外层电子数决定元素的化学性质X A Z c ± d±b②10个电子的微粒。
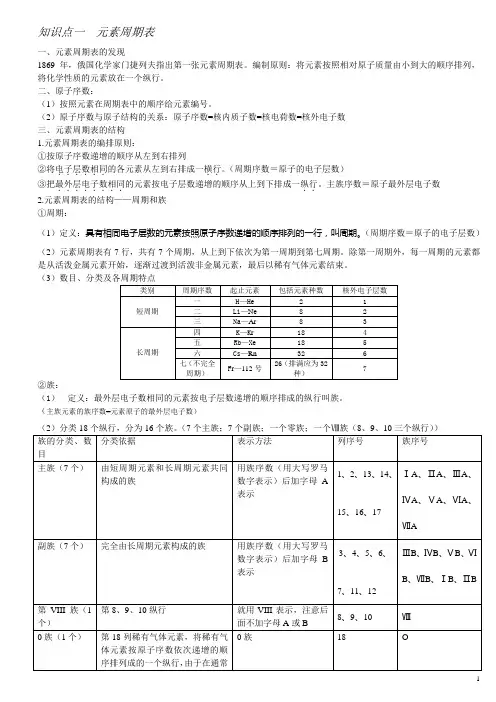
知识点一元素周期表一、元素周期表的发现1869年,俄国化学家门捷列夫指出第一张元素周期表。
编制原则:将元素按照相对原子质量由小到大的顺序排列,将化学性质的元素放在一个纵行。
二、原子序数:(1)按照元素在周期表中的顺序给元素编号。
(2)原子序数与原子结构的关系:原子序数=核内质子数=核电荷数=核外电子数三、元素周期表的结构1.元素周期表的编排原则:①按原子序数递增的顺序从左到右排列②将电子层数相同..。
(周期序数=原子的电子层数)......的各元素从左到右排成一横行③把最外层电子数相同..。
主族序数=原子最外层电子数........的元素按电子层数递增的顺序从上到下排成一纵行2.元素周期表的结构——周期和族①周期:(1)定义:具有相同电子层数的元素按照原子序数递增的顺序排列的一行,叫周期。
(周期序数=原子的电子层数)(2)元素周期表有7行,共有7个周期,从上到下依次为第一周期到第七周期。
除第一周期外,每一周期的元素都是从活泼金属元素开始,逐渐过渡到活泼非金属元素,最后以稀有气体元素结束。
(3②族:(1)定义:最外层电子数相同的元素按电子层数递增的顺序排成的纵行叫族。
(主族元素的族序数=元素原子的最外层电子数)③族的别称:第ⅠA 族称为碱金属元素 第ⅣA 族称为碳族元素 第ⅤA 族称为氮族元素 第ⅥA 族称为氧族元素 第ⅦA 族称为卤素族元素 零族称为稀有气体元素(3)元素周期表中几个特殊区域a.过渡元素:元素周期表中部从第IIIB 族到第II 族共10个纵行为过渡元素,这些元素都是金属,所以又把它们叫过渡金属。
b.镧系元素:第6周期中,57号元素镧(La)到71号元素镥(Lu),共15种元素,它们原子的电子层结构和性质十分相似,总称镧系元素。
c. 锕系元素:第7周期中,89号元素锕(Ac)到103号元素铹(Lr),共15种元素,它们原子的电子层结构和性质也十分相似,总称锕系元素。
为了使表的结构紧凑,将全体镧系元素和锕系元素分别按周期各放在同一个格内,并按原子序数递增的顺序,把它们分两行另列在表的下方。

高中化学元素周期律知识点总结-CAL-FENGHAI.-(YICAI)-Company One1第一节课时1元素周期表的结构一、元素周期表的发展历程二、现行元素周期表的编排与结构1.原子序数(1)含义:按照元素在元素周期表中的顺序给元素编号,得到原子序数。
(2)原子序数与原子结构的关系原子序数=核电荷数=质子数=核外电子数。
2.元素周期表的编排原则(1)原子核外电子层数目相同的元素,按原子序数递增的顺序从左到右排成横行,称为周期。
(2)原子核外最外层电子数相同的元素,按电子层数递增的顺序由上而下排成纵行,称为族。
3.元素周期表的结构(1)周期(横行)①个数:元素周期表中有7个周期。
②特点:每一周期中元素的电子层数相同。
③分类(3短4长)短周期:包括第一、二、三周期(3短)。
长周期:包括第四、五、六、七周期(4长)。
(2)族(纵行)①个数:元素周期表中有18个纵行,但只有16个族。
②特点:元素周期表中主族元素的族序数等于其最外层电子数。
③分类④常见族的特别名称 第ⅠA 族(除H):碱金属元素;第ⅦA 族:卤族元素;0族:稀有气体元素;ⅣA 族:碳族元素;ⅥA 族:氧族元素。
课时2 元素的性质与原子结构一、碱金属元素——锂(Li)、钠(Na)、钾(K)、铷(Rb)、铯(Cs)、钫(Fr) 1.原子结构(1)相似性:最外层电子数都是__1__。
(2)递变性:Li ―→Cs ,核电荷数增加,电子层数增多,原子半径增大。
2.碱金属单质的物理性质3.碱金属元素单质化学性质的相似性和递变性 (1)相似性(用R 表示碱金属元素)单质R —⎩⎪⎨⎪⎧与非金属单质反应:如Cl 2+2R===2RCl 与水反应:如2R +2H 2O===2ROH +H 2↑与酸溶液反应:如2R +2H +===2R ++H 2↑化合物:最高价氧化物对应水化物的化学式为ROH ,且均呈碱性。
(2)递变性具体表现如下(按从Li→Cs 的顺序)①与O 2的反应越来越剧烈,产物越来越复杂,如Li 与O 2反应只能生成Li 2O ,Na 与O 2反应还可以生成Na 2O 2,而K 与O 2反应能够生成KO 2等。
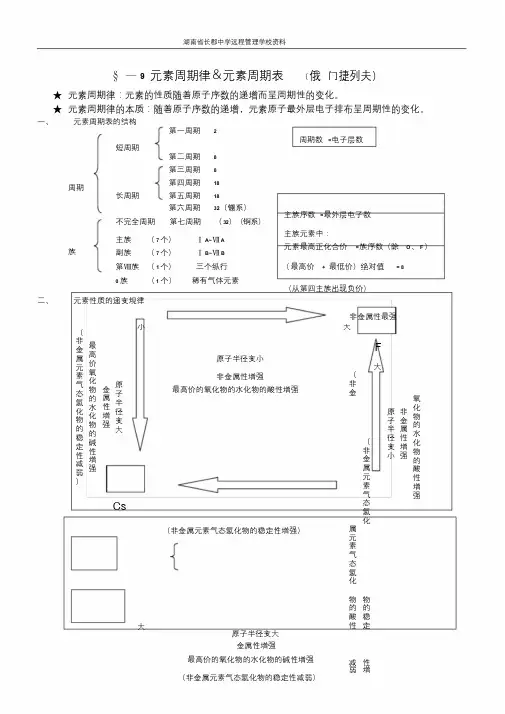
湖南省长郡中学远程管理学校资料§—9 元素周期律&元素周期表(俄门捷列夫)★元素周期律:元素的性质随着原子序数的递增而呈周期性的变化。
★元素周期律的本质:随着原子序数的递增,元素原子最外层电子排布呈周期性的变化。
一、元素周期表的结构第一周期 2周期数=电子层数短周期第二周期8第三周期8周期长周期第四周期18第五周期18第六周期32(镧系)不完全周期第七周期(32)(锕系)主族序数=最外层电子数族主族(7 个)ⅠA~ⅦA副族(7 个)ⅠB~ⅦB主族元素中:元素最高正化合价=族序数(除O、F)第Ⅷ族(1 个)三个纵行(最高价+ 最低价)绝对值= 80 族(1 个)稀有气体元素(从第四主族出现负价)二、元素性质的递变规律非金属性最强(非金属元素气态氢化物的稳定性减弱)最高价氧化物的水化物的碱性增强金属性增强原子半径变大Cs小大F原子半径变小大非金属性增强最高价的氧化物的水化物的酸性增强(非金(非金属元素气态氢化(非金属元素气态氢化物的稳定性增强)属元素气态氢化大物物的的酸稳性定原子半径变大金属性增强最高价的氧化物的水化物的碱性增强减性弱增(非金属元素气态氢化物的稳定性减弱)原子半径变小非金属性增强氧化物的水化物的酸性增强)强大小)最高价金属性最强元素的最高价氧化物的水化物主族元素R →R2O xR金属R(OH) xR 非金属H8-x RO 4元素气态氢化物H6-x RO 3非金属元素R →H x R ( RH x ) X 代表元素最低价的绝对值怀化市长郡湖天中学、怀化市第一中学、怀化市第五中学。



一.元素周期表1.原子序数=核电荷数=核内质子数=核外电子数2.主族元素最外层电子数=主族序数3.电子层数=周期序数4.碱金属元素:密度逐渐增大,熔沸点逐渐变大,自上而下反应越来越剧烈银白色金属,密度小,熔沸点低,导电导热性强5.判断元素金属性强弱的方法:单质与水(酸)反应置换出氢的难易程度最高价氧化物的水化物(氢氧化物)的碱性强弱单质间的置换6.卤族元素:密度逐渐增大,熔沸点逐渐升高与氢气反应剧烈程度越来越弱,生成氢化物稳定性渐弱7.判断元素非金属性强弱的方法:与氢气生成气态氢化物的难易程度以及氢化物的稳定性最高价氧化物的水化物的酸性单质间的置换8.质量数:核内所有质子和中子的相对质量取近似整数相加9.核素:具有一定数目质子和一定数目的中子的一种原子10.同位素:质子数相同而中子数不同的同一元素的不同原子互称为同位素天然稳定存在的同位素,无论是游离态还是化合态各同位素所占的原子个数百分比一般是不变的在相同状况下,各同位素的化学性质基本相同(几乎完全一样),物理性质有所不同12.原子相对原子质量=1个原子的质量/(1/12 C12的原子质量)13.原子的近似相对原子质量=质量数14.元素的相对原子质量=各同位素的相对原子质量的平均值= A·a%+B·b%…15.元素的近似相对原子质量=各同位素质量数的平均值= A·a%+B·b%…二.元素周期律1.K、L、M、N、O、P、Q(1,2,3,4,5,6,7,)层数越大,电子离核越远,其能量越高2.能量最低原理3.各电子层最多容纳电子数:2n^24.最外层不超过8,次外层18,倒数第三层325.原子半径:同周期主族元素,原子半径从左到右逐渐减小同主族元素,元素原子半径从上到下逐渐增大6.元素性质的周期性变化是元素原子的核外电子排布的周期性变化的结果(实质)7.同一周期元素,电子层数相同,从左到右,核电荷数增多,原子半径减小,失电子的能力逐渐减弱,得电子的能力逐渐增强8.同一主族,自上而下,元素的金属性逐渐增强,非金属性逐渐减弱,最外层电子数相同,电子层数增多,原子半径增大9.最高正价=最外层电子数最低负价=8—最外层电子数10.各周期元素种类:2,8,8,18,32,3211.稀有气体原子序数;2,10,18,36,54,8612.同族上下相邻的原子序数差:2,8,18,3213.同周期IIA族与IIIA族原子序数相差:1,1,11,11,2514.电子层数不同,原子序数(核电荷数)均不同时,电子层数越多,半径越大15.电子层数相同,原子序数(核电荷数)不同时,原子序数(核电荷数)越大,半径越小16.电子层数,原子序数(核电荷数)均相同时,核外电子数越多,半径越大17.电子排布相同的离子,离子半径随核电荷数递增而减小选修三.原子结构与性质1.原子轨道(能级即亚层):处于同一电子层的原子核外电子,也可以在不同类型的原子轨道上运动,分别用s、p、d、f表示不同形状的轨道,s轨道呈球形、p轨道呈纺锤形,d轨道和f轨道较复杂.各轨道的伸展方向个数依次为1、3、5、7.2.电子云:用小黑点的疏密来描述电子在原子核外空间出现的机会大小所得的图形叫电子云图.离核越近,电子出现的机会大,电子云密度越大;离核越远,电子出现的机会小,电子云密度越小.3.原子核外电子排布原理.①.能量最低原理:电子先占据能量低的轨道,再依次进入能量高的轨道.②.泡利不相容原理:每个轨道最多容纳两个自旋状态不同的电子.③.洪特规则:在能量相同的轨道上排布时,电子尽可能分占不同的轨道,且自旋状态相同.4.洪特规则的特例:对于一个能级,当电子排布为充满、半充满或全空时,是比较稳定的5.元素电离能:第一电离能:气态电中性基态原子失去1个电子,转化为气态基态正离子所需要的能量叫做第一电离能。

第一章 物质结构 元素周期律第一节 元素周期表一、原子结构1. 原子核的构成核电荷数(Z) == 核内质子数 == 核外电子数 == 原子序数 2、质量数将原子核内所有的质子和中子的相对质量取近似整数值加起来,所得的数值,叫质量数。
质量数(A )= 质子数(Z )+ 中子数(N )==近似原子量 原子 A Z X3、阳离子 aW m+ :核电荷数=质子数>核外电子数,核外电子数=a -m 阴离子 b Y n-:核电荷数=质子数<核外电子数,核外电子数=b +n 二、核素、同位素 1、定义核素:人们把具有一定数目质子和一定数目中子的一种原子称为核素。
同位素:质子数相同而中子数不同的同一元素的不同核素互为同位素。
3、元素的相对原子质量 2、同位素的特点① 化学性质几乎完全相同②天然存在的某种元素,不论是游离态还是化合态,其各种同位素所占的原子个数百分比(即丰度)一般是不变的。
三、核外电子排布1、电子云:我们只能指出它在原子核外空间某处出现的机会大小——几率 电子云密度大小反映电子在该区域(单位体积)出现的机会(几率)大小2、核外电子排布的规律:1.电子是在原子核外距核由近及远、能量由低至高的不同电子层上分层排布;2.每层最多容纳的电子数为2n 2(n 代表电子层数);3.电子一般总是尽先排在能量最低的电子层里,即最先排第一层,当第一层排满后,再排第二层,等等。
4.最外层电子数则不超过8个(第一层为最外层时,电子数不超过2个)。
3、元素性质与元素的原子核外电子排布的关系①稀有气体的不活泼性:稀有气体元素的原子最外层有8个电子(He为2)处于稳定结构,因此化学性质稳定,一般不跟其它物质发生化学反应。
②非金属性与金属性(一般规律)电外层电子数得失电子趋势元素性质金属元素<4 易失金属性非金属元素>4 易得非金属性一、元素周期表的结构1.周期:周期序数=电子层数七个周期(1、2、3短周期;4、5、6长周期;7不完全周期)2.族:主族元素的族序数=元素原子的最外层电子数(或:主族序数=最外层电子数) 18个纵行(7个主族;7个副族;一个零族;一个Ⅷ族(8、9、10三个纵行))二、元素性质与原子结构1、碱金属元素(1) 在结构上:结构异同:异:核电荷数:由小→大;电子层数:由少→多;同:最外层电子数均为1个。
化学元素最全知识点总结
1. 原子结构
- 原子:化学元素的基本粒子,由质子、中子和电子组成。
- 质子:带正电荷的粒子,位于原子核中。
- 中子:位于原子核中,没有电荷。
- 电子:带负电荷的粒子,绕原子核中的电子壳运动。
2. 元素周期表
- 元素周期表:一种按元素的原子序数和元素周期进行排列的
表格。
- 周期:指的是元素周期表中的水平行,代表了原子壳的数量。
- 周数:指的是元素周期表中的垂直列,代表了原子核周围的
电子云的形状和结构。
3. 元素分类
- 金属元素:大多数元素都是金属元素,具有光泽、导电性和
热传导性。
- 非金属元素:相对于金属元素,非金属元素的导电性、热传
导性和光泽较差。
- 过渡元素:在元素周期表中位于主族元素和非金属元素之间。
- 稀有气体:位于元素周期表的最右侧,具有低的化学活性。
4. 原子团与分子
- 原子团:由两个或多个原子结合形成的稳定的结构。
- 分子:一个由两个或多个原子通过共用电子形成的稳定结构。
5. 化合物
- 化合物:由两种或两种以上不同种类的原子通过化学键结合
而成的物质。
- 阴离子:带有负电荷的化学物质。
- 阳离子:带有正电荷的化学物质。
6. 化学反应
- 化学反应:化学物质之间发生的变化。
- 反应物:化学反应中参与的起始物质。
- 生成物:化学反应中形成的新物质。
以上是化学元素最全的知识点总结,希望对您有帮助!。
考纲要求:①了解元素、核素和同位素的含义。
②了解原子的构成。
了解原子序数、核电荷数、质子数、中子数、核外电子数以及它们之间的相互关系。
③了解原子核外电子排布规律。
④掌握元素周期律的实质。
了解元素周期表(长式)的结构(周期、族)及其应用。
⑤以第3周期为例,掌握同一周期内元素性质的递变规律与原子结构的关系。
⑥以ⅠA 和ⅦA 族为例,掌握同一主族内元素性质递变规律与原子结构的关系。
⑦了解金属、非金属元素在周期表中的位置及其性质递变规律。
⑧了解化学键的定义。
了解离子键、共价键的形成。
知识点总结:中子N(核素)原子核质子Z → 元素符号原子结构 : 决定原子呈电中性 电子数(Z 个):化学性质及最高正价和族序数核外电子 运动特征:体积小,运动速率高(近光速)排布规律 → 电子层数 周期序数及原子半径 表示方法 → 原子(离子)的电子式、原子结构示意图1.原子结构[核电荷数、核内质子数及核外电子数的关系]核电荷数=核内质子数=原子核外电子数注意: (1) 阴离子:核外电子数=质子数+所带的电荷数阳离子:核外电子数=质子数-所带的电荷数(2)“核电荷数”与“电荷数”是不同的,Cl -的核电荷数为17,电荷数为1.[质量数] 用符号A 表示.将某元素原子核内的所有质子和中子的相对质量取近似整数决定X)(A Z值相加所得的整数值,叫做该原子的质量数.说明(1)质量数(A)、质子数(Z)、中子数(N)的关系:A=Z + N.(2)符号A Z X的意义:表示元素符号为X,质量数为A,核电荷数(质子数)为Z的一个原子.例如,2311Na中,Na原子的质量数为23、质子数为11、中子数为12.[原子核外电子运动的特征](1)当电子在原子核外很小的空间内作高速运动时,没有确定的轨道,不能同时准确地测定电子在某一时刻所处的位置和运动的速度,也不能描绘出它的运动轨迹.在描述核外电子的运动时,只能指出它在原子核外空间某处出现机会的多少.(2)描述电子在原子核外空间某处出现几率多少的图像,叫做电子云.电子云图中的小黑点不表示电子数,只表示电子在核外空间出现的几率.电子云密度的大小,表明了电子在核外空间单位体积内出现几率的多少.(3)在通常状况下,氢原子的电子云呈球形对称。
元素周期表知识点总结元素周期表知识点总结导语:化学元素周期表是根据原子序数从小至大排序的化学元素列表。
下面是小编收集整理的元素周期表知识点总结,希望对你有帮助!1、原子结构(1).所有元素的原子核都由质子和中子构成。
正例:612C、613C、614C三原子质子数相同都是6,中子数不同,分别为6、7、8。
反例1:只有氕(11H)原子中没有中子,中子数为0。
(2).所有原子的中子数都大于质子数。
正例1:613C、614C、13H等大多数原子的中子数大于质子数。
正例2:绝大多数元素的相对原子质量(近似等于质子数与中子数之和)都大于质子数的2倍。
反例1:氕(11H)没有中子,中子数小于质子数。
反例2:氘(11H)、氦(24He)、硼(510B)、碳(612C)、氮(714N)、氧(816O)、氖(1020Ne)、镁(1224Mg)、硅(1428Si)、硫(1632S)、钙(2040Ca)中子数等于质子数,中子数不大于质子数。
(3).具有相同质子数的微粒一定属于同一种元素。
正例:同一元素的不同微粒质子数相同:H+、H-、H等。
反例1:不同的中性分子可以质子数相同,如:Ne、HF、H2O、NH3、CH4。
反例2:不同的阳离子可以质子数相同,如:Na+、H3O+、NH4+。
反例3:不同的阴离子可以质子数相同,如:NH4+、OH-和F-、Cl和HS。
2、电子云(4).氢原子电子云图中,一个小黑点就表示有一个电子。
含义纠错:小黑点只表示电子在核外该处空间出现的机会。
3、元素周期律(5).元素周期律是指元素的性质随着相对原子质量的递增而呈周期性变化的规律。
概念纠错:元素周期律是指元素的性质随着原子序数的递增而呈周期性变化的规律。
(6).难失电子的元素一定得电子能力强。
反例1:稀有气体元素很少与其它元素反应,即便和氟气反应也生成共价化合物,不会失电子,得电子能力也不强。
反例2:IVA的非金属元素,既不容易失电子,也不容易得电子,主要形成共价化合物,也不会得失电子。
第一节元素周期表一、元素周期表的结构1、原子序数原子序数=核电荷数=质子数=核外电子数2、元素周期表:横竖二、元素的性质与原子结构1、碱金属元素:从上到下原子的电子层数在,原子半径逐渐,所以失电子的能力逐渐,元素金属性逐渐●碱金属元素的化学性质(1)R+2H2O====2ROH+H2(2)4Li+O2====2Li2O(常温或加热) 4Na+O2====2Na2O(缓慢氧化)2Na+O2====Na2O2●碱金属的主要物理性质:颜色:(略带金色光泽)由上至下:密度:(反常)熔点:沸点:2、卤族元素●从上到下电子层数依次,原子半径依次,所以得电子的能力也依次,即非金属性依次●单质溴是唯一在常温常压下呈液态的非金属单质卤素的化学性质(1)X -+Ag +===AgX ↓(AgCl 白色沉淀,AgBr 淡黄色沉淀,AgI 黄色沉淀) (2)X 2+H 2O===HX+HXO (除F 2+H 2O=====HF+O 2 ) (3)2Fe+3Cl 2===2FeCl 3(最高价金属氯化物) Fe+I 2===FeI 2(较低价金属碘化物)三、核素1、 原子的结构:(1)原子的质量集中在原子核上,电子的质量很小,几乎可以忽略不计 (2)一个质子带一个单位的正电荷,一个电子带一个单位的负电荷,中子 不带电,所以原子对外显中性2、质量数:将原子核内所有质子和中子的相对质量取近似整数值相加,所得到 的数值。
质量数(A )=质子数(Z )+中子数(N )3、核素:具有一定数目质子和一定数目中子的一种原子叫做核素4、同位素(1)质子数相同而中子数不同的同一元素的不同原子互为同位素(2)当某种元素具有两种或两种以上天然、稳定的同位素时,无论是在单质 还是在化合物里,任意一种同位素在该元素内所占的原子数目百分比都不变(3)大多数元素都有同位素,所以原子的种类比元素的种类要多。
(4)同一元素的各种核素的,化学性质 。
物理性质 。
(完整版)元素周期表主要知识点元素周期表一、元素周期表概述1、门捷列夫周期表:按相对原子质量由小到大依次排列,将化学性质相似的元素放在一个纵行,通过分类、归纳制出的第一张元素周期表。
2、现行常用元素周期表⑴周期表的编排原则:①按原子序数递增的顺序从左到右排列②将电子层数相同的元素排成一个横行③把最外层电子数相同的元素(个别例外)按电子层数递增的顺序从上到下排成纵行⑵周期表的结构:七个横行;7个周期[三短(2、8、8)、三长(18、18、32)、一不完全]18个纵行(列),16个族:7个主族(ⅠA~ⅦA);(1、2、13~17列);7个副族(ⅠB~ⅦB);(3~12列)Ⅷ族:3个纵行;(8、9、10列); 零族:稀有气体(18列)周期表中有些族有特殊的名称:第ⅠA族:碱金属元素(不包括氢元素);第ⅦA族:卤族元素0族:稀有气体元素3、元素周期表的结构与原子结构的关系原子序数==核电荷数==质子数==核外电子数; 周期序数==原子的电子层数主族序数==最外层电子数==最高正价数(O、F除外)==价电子数非金属的负价的绝对值==8-主族序数(限ⅣA~ⅦA)4、由原子序数确定元素位置的规律⑴主族元素:周期数==核外电子层数;主族的族序数==最外层电子数⑵确定族序数应先确定是主族还是副族,其方法是采用原子序数逐步减去各周期的元素种数,最后的差值即可确定。
基本公式:原子序数-零族元素的序数(或各周期元素总数)== 差值①对于短周期元素:若差值为0,则为相应周期的零族元素;若0<差值≤7,则元素在下一周期,差值即为主族序数。
差值为1~7时,差值即为族序数,位于Ⅷ族左侧;差值为8、9、10时,为Ⅷ族元素。
差值为11~17时,再减去10所得最后差值,即为Ⅷ族右侧的族序数。
若差值>17,再减14,按同上方法处理。
5、同主族元素上、下相邻元素原子序数推导规律:⑴ⅠA、ⅡA族元素:元素的原子序数==上一周期的元素的原子序数+上一周期的元素总数⑵ⅢA~ⅦA、0族元素:元素的原子序数==上一周期的元素的原子序数+本周期的元素总数二、核素1、质量数:将原子核内所有质子和中子的相对质量取近似整数值相加,所得到的数值叫质量数(Li →Cs)质量数(A )=质子数(Z )+中子数(N )2、核素:具有一定数目质子和一定数目中子的一种原子叫做核素3、同位素:● 质子数相同而中子数不同的同一元素的不同原子互为同位素● 当某种元素具有两种或两种以上天然、稳定的同位素时,无论是在单质还是在化合物里,任意一种同位素在该元素内所占的原子数目百分比都不变4、同素异形体指同种元素形成的不同单质,它们之间互称为同素异性体。
第一章 物质结构 元素周期表第一节 元素周期表一、周期表原子序数 = 核电荷数 = 质子数 = 核外电子数1、依据横行:电子层数相同元素按原子序数递增从左到右排列纵行:最外层电子数相同的元素按电子层数递增从上向下排列2、结构周期序数=核外电子层数 主族序数=最外层电子数短周期(第1、2、3周期) 周期:7个(共七个横行)周期表 长周期(第4、5、6、7周期) 主族7个:ⅠA-ⅦA族:16个(共18个纵行)副族7个:IB-ⅦB第Ⅷ族1个(3个纵行) 零族(1个)稀有气体元素二.元素的性质和原子结构(一)碱金属元素:1、原子结构 相似性:最外层电子数相同,都为1个递变性:从上到下,随着核电核数的增大,电子层数增多,原子半径增大2、物理性质的相似性和递变性:(1)相似性:银白色固体、硬度小、密度小(轻金属)、熔点低、易导热、导电、有展性。
(2)递变性(从锂到铯):①密度逐渐增大(K 反常) ②熔点、沸点逐渐降低 结论:碱金属原子结构的相似性和递变性,导致物理性质同样存在相似性和递变性。
3、化学性质(1)相似性:(金属锂只有一种氧化物)4Li + O 2 Li 2O 2Na + O 2 Na 2O 22 Na + 2H 2O = 2NaOH + H 2↑ 2K + 2H 2O = 2KOH + H 2↑ 2R + 2 H 2O = 2 ROH + H 2 ↑产物中,碱金属元素的化合价都为+1价。
点燃 点燃 过渡元素结论:碱金属元素原子的最外层上都只有1个电子,因此,它们的化学性质相似。
(2)递变性:①与氧气反应越来越容易②与水反应越来越剧烈结论:①金属性逐渐增强②原子结构的递变性导致化学性质的递变性。
总结:递变性:从上到下(从Li到Cs),随着核电核数的增加,碱金属原子的电子层数逐渐增多,原子核对最外层电子的引力逐渐减弱,原子失去电子的能力增强,即金属性逐渐增强。
所以从Li到Cs的金属性逐渐增强。
(二)卤族元素:1、原子结构相似性:最外层电子数相同,都为7个递变性:从上到下,随着核电核数的增大,电子层数增多,原子半径增大2.物理性质的递变性:(从F2到I2)(1)卤素单质的颜色逐渐加深;(2)密度逐渐增大;(B r2反常)(3)单质的熔、沸点升高3、化学性质(1)卤素单质与氢气的反应:X2 +H2=2 HXF2Cl2Br2I2卤素单质与H2的剧烈程度:依次增强;生成的氢化物的稳定性:依次增强(HF 最稳定)(2)卤素单质间的置换反应2NaBr +Cl2=2NaCl + Br2氧化性:Cl2________Br2;还原性:Cl-_____Br-2NaI +Cl2=2NaCl + I2氧化性:Cl2_______I2;还原性:Cl-_____I-2NaI +Br2=2NaBr + I2氧化性:Br2_______I2;还原性:Br-______I-结论:F2 F-Cl2 Cl-Br2 Br-I2 I-单质的氧化性:从下到上依次增强(F2氧化性最强),对于阴离子的还原性:从上到下依次增强(I-还原性最强)结论:①非金属性逐渐减弱②原子结构的递变性导致化学性质的递变性。
元素周期表的高中化学问题终极总结一、最外层电子数规律1.最外层电子数为1的元素:主族(IA族)、副族(IB、VIII族部分等)。
2.最外层电子数为2的元素:主族(IIA族)、副族(IIB、IIIB、IVB、VIIB族)、0族(He)、VIII族(26Fe、27Co等)。
3.最外层电子数在3~7之间的元素一定是主族元素。
4.最外层电子数为8的元素:0族(He除外)。
二、数目规律1.元素种类最多的是第IIIB族(32种)。
2.同周期第IIA族与第IIIA族元素的原子序数之差有以下三种情况:(1)第2、3周期(短周期)相差1;(2)第4、5周期相差11;(3)第6、7周期相差25。
3.设n为周期序数,每一周期排布元素的数目为:奇数周期为;偶数周期为。
如第3周期为种,第4周期为种。
4.同主族相邻元素的原子序数:第IA、IIA族,下一周期元素的原子序数=上一周期元素的原子序数+上一周期元素的数目;第IIIA~VIIA族,下一周期元素的原子序数=上一周期元素的原子序数+下一周期元素的数目。
三、化合价规律1.同周期元素主要化合价:最高正价由+1+7(稀有气体为0价)递变、最低负价由-4-1递变。
2.关系式:(1)最高正化合价+|最低负化合价|=8;(2)最高正化合价=主族族序数=最外层电子数=主族价电子数。
3.除第VIII族元素外,原子序数为奇(偶)数的元素,元素所在族的序数及主要化合价也为奇(偶)数。
四、对角线规律金属与非金属分界线对角(左上角与右下角)的两主族元素性质相似,主要表现在第2、3周期(如Li 和Mg、Be和Al、B和Si)。
五、分界线规律位于金属与非金属之间的分界线,右上方的元素为非金属(周期表中的颜色为深绿色),在此可以找到制造农药的元素(如Cl、P等),左下角为金属元素(H除外),分界线两边的元素一般既有金属性,又有非金属性;能与酸和碱反应(如Be、Al等),还可找到制造半导体材料的元素(如Si、Ge等)。
六、金属性、非金属性变化规律1.同一周期,从左到右(0族除外)金属性减弱,非金属性增强;同一主族,从上到下金属性增强,非金属性减弱。
金属性最强的位于左下角的铯,非金属性最强的是位于右上角的氟。
2.金属性越强,单质越容易跟水或酸反应置换出氢,对应的最高价氧化物水化物碱性越强;非金属性越强,跟氢气反应越容易,生成的气态氢化物越稳定,对应的最高价氧化物水化物酸性越强。
七、半径大小规律1.原子半径:同主族--从上到下逐渐增大;同周期--从左到右逐渐减小(0族除外)。
2.离子半径:同主族--同价离子从上到下逐渐增大;同周期--阴离子半径大于阳离子半径;具有相同的电子层结构的离子--核电荷数越大,离子半径越小。
3.同种元素的各种微粒,核外电子数越多,半径越大;反之,核外电子数越少,半径越小(如)。
八、主族族序数与周期序数的规律1.关系式:主族族序数=最外层电子数;周期序数=电子层数。
2.设主族族序数为a,周期数为b,则:时,为金属元素,且比值越小,元素的金属性越强;时,为两性元素(H除外),其最高价氧化物为两性氧化物,最高价氧化物的水化物为两性氢氧化物。
时,为非金属元素,且比值越大,元素的非金属性越强。
九、电子层与电子数的倍比关系(短周期元素)1.若原子的最外层电子数与最内层电子数的比值为a,则有:为第IA族元素;(2)a=1为第IIA族元素或H、He;(3)a=2为第IVA族元素;(4)a=3为第VIA族元素;(5)a=4为0族元素。
2.若原子的最外层电子数与次外层电子数的比值为b,则有:为Na;(2)为Mg;(3)为Li、Si;(4)b=1为Be、Ar;(5)b=2为C;(6)b=3为O;(7)b=4为Ne。
3.若原子的最外层电子数与电子总数的比值为c,则有:(1)为Mg;(2)为Li、P;(3)为Be;(4)c=1为H、He。
4.原子的最外层电子数与核外电子层数相等为H、Be、Al。
知识赠送以下资料英语万能作文(模板型)Along with the advance of the society more and more problems are brought to our attention, one of which is that....随着社会的不断发展,出现了越来越多的问题,其中之一便是____________。
As to whether it is a blessing or a curse, however, people take different attitudes.然而,对于此类问题,人们持不同的看法。
(Hold different attitudes 持不同的看;Come up with different attitudes 有不同的看法)As society develops, people are attaching much importance to....随着社会的发展,人们开始关注............People are attaching more and more importance to the interview during job hunting求职的过程中,人们慢慢意识到面试的重要性。
As to whether it is worthwhile ....., there is a long-running controversial debate. It is quite natural that people from different backgrounds may have divergent attitudes towards it.关于是否值得___________的问题,一直以来争论不休。
当然,不同的人对此可能持不同的观点。
In the process of modern urban development, we often find ourselves in a dilemma.在都市的发展中,我们往往会陷入困境。
Recently the phenomenon has aroused wide concern, some people are in alarm that....最近,这种现象引起了人们的广泛关注,有人开始担心______________。
The human race has entered a completely new stage in its history, with the increasingly rapid economic globalization and urbanization, more problems are brought to our attention.人类进入了一个历史的崭新的阶段,经济全球化、都市化的速度不断加快,随之给我们带来了很多问题。
...... plays such an important role that it undeniably becomes the biggest concern of the present world, there comes a question, is it a blessing or a curse?"_______显得非常重要而成为当今世界所关注的最大的问题,这是无可厚非的。
不过,问题是:"我们该如何抉择?"Now we are entering a new era, full of opportunities and challenges,现在我们正在进入一个充满机会和挑战的新时代。
People from different backgrounds would put different interpretations on the same case.不同行业的人对同一种问题的解释不尽相同。
The controversial issue is often brought into public focus. People from different backgrounds hold different attitudes towards the issue.这中极具争议性的话题往往很受社会的关注。
不同的人对此问题的看法也不尽相同。
When asked ..., some people think..... while some prefer...说到______,有人认为________,而另一些人则认为__________。
Just as the saying goes: "so many people, so many minds". It is quite understandable that views on this issue vary from person to person.俗话说,""。
不同的人对此有不同的看法是可以理解的。
To this issue, different people come up with various attitudes.对于这个问题,不同的人持不同的观点。
There is a good side and a bad side to everything, it goes without saying that...万事万物都有其两面性,所以,勿庸置疑,____________。
When it comes to ..., most people believe that ..., but other people regard ...as ....提到_________问题,很多人认为_________,不过,一些人则认为______是____.When faced with...., quite a few people claim that ...., but other people think as...提到_________问题,仅少数人认为________,但另一些人则认为_________。
There is a public controversy nowadays over the issue of .... There who criticize ...argue that ...., they believe that ...,but people who favor .., on the other hand, argue that...目前,____问题争议较大。
批判_____的人认为_____,他们认为_____,不过,另一方面,赞同_____的人则认为_______。