第二章水分
- 格式:ppt
- 大小:4.41 MB
- 文档页数:70

《食品化学》—打开食品科学之门的钥匙主讲人:李红所在单位:食品与生物工程学院日期:2010.9.17掌握水在食品中的重要作用;了解水和冰的结构及性质;掌握水在食品中的存在状态;掌握水分活度和水分等温吸湿线的概念、意义;掌握水分活度与食品的稳定性之间的关系。
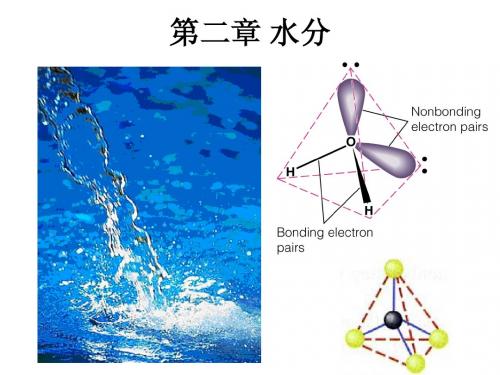
2.2.2 水分子的缔合作用水分子不仅相互之间可以通过氢键缔合,而且可以和其它带有极性基团的有机分子通过氢键相互结合,所以糖类、氨基酸类、蛋白质类、黄酮类、多酚类化合物在水中均有一定的溶解度。
冰的结构疏水水合作用的表现形式:笼形水合物的形成。
笼形水合物是冰状包合物,其中水为“主体”,通过氢键形成了笼状结构,物理截留了另一种称为“客体”的分子。
“主体”水分子与“客体”分子之间的相互作用一般是弱的范德华力。
笼形水合物一般由20~74个水分子形成,具体多少视非极性物质的几何尺寸而定;只有“客体”的大小和形状适合于“主体”的笼才能被截留。
大多数蛋白质分子中,约40%的氨基酸具有非极性侧链,而且约有三分之一的非极性基团暴露在水中,与水之间产生疏水的相互作用,对于保持蛋白质的活性构象具有一定的作用。
水与溶质的结合力非常重要,相互作用如下表:结合水和体相水之间的界限很难定量区分,只能根据其理化性质作定性区分:结合水的量与食品中有机大分子的极性基团的数量有比较固定的比例关系,如100g蛋白质大约可结合50g 的水,100g淀粉的持水能力在30~40g;结合水对食品品质和风味有较大的影响,当结合水被强行与食品分离时,食品质量、风味就会改变;结合水的蒸汽压比自由水低得多,在一定温度(100o C)下结合水不能从食品中分离出来;结合水不易结冰(冰点约-40o C),使得植物的种子和微生物的孢子得以在很低的温度下保持其生命力;而多汁的组织在冰冻后细胞结构往往被体相水的冰晶所破坏,解冻后组织不同程度的崩溃;结合水不能作为溶剂;体相水可被微生物所利用,结合水则不能。
2.4 水分活度长期以来人们就已认识到食品的水分含量和它的易腐性之间存在着一定的关系。















食品化学第二章水分1、名词解释:(1)水分活度:指食品的水分蒸汽压与相同温度下纯水的饱和蒸汽压的比值。
(2)水分的吸湿等温线:在恒定温度下,以食品中水分含量为纵坐标,以水分活度为横坐标绘制而成的曲线称为吸附等温线(MSI)。
(3)等温线的滞后现象:一种食物一般有两条吸附等温线。
一条是水分回吸等温线,是食品在吸湿时的吸附等温线;一条是水分解吸等温线,是食品在干燥时的吸附等温线;往往这两条曲线并不完全重叠,在中低水分含量部分张开了一细长的眼孔,把这种现象称为“滞后”现象。
2、问答题(1)水分活度与食品稳定性的关系。
①食品aw与微生物生长的关系:从微生物活动与食物水分活度的关系来看,各类微生物生长都需要一定的水分活度,一般说来:细菌为Aw>0.9;酵母为Aw>0.87;霉菌为Aw>0.8。
②食品aw与酶促反应的关系:一方面影响酶促反应的底物的可移动性,另一方面影响酶的构象。
食品体系中大多数的酶类物质在Aw<0.85 时,活性大幅度降低,如淀粉酶、酚氧化酶和多酚氧化酶等。
但也有一些酶例外,如酯酶在Aw为0.3甚至0.1时也能引起甘油三酯或甘油二酯的水解。
③食品aw与非酶化学反应的关系:降低食品的Aw ,可以延缓酶促反应和非酶反应的进行,减少食品营养成分的破坏,防止水溶性色素的分解。
但Aw过低,则会加速脂肪的氧化酸败,还能引起非酶褐变。
④食品aw与质地的关系:当水分活度从0.2~0.3增加到0.65时,大多数半干或干燥食品的硬度及黏着性增加。
水分活度为0.4~0.5时,肉干的硬度及耐嚼性最大。
(2)水分的吸附等温线的定义,以及3个区段的水分特性。
①在恒定温度下,以食品中水分含量为纵坐标,以水分活度为横坐标绘制而成的曲线称为吸附等温线。
②I区:为化合水和临近水区。
这部分水是食品中与非水物质结合最为紧密的水,为化合水和构成水,吸湿时最先吸入,干燥时最后排除;这部分水不能使干物质膨润,不能作为溶剂,在- 40℃不结冰。