包装材料检验记录
- 格式:doc
- 大小:57.50 KB
- 文档页数:3
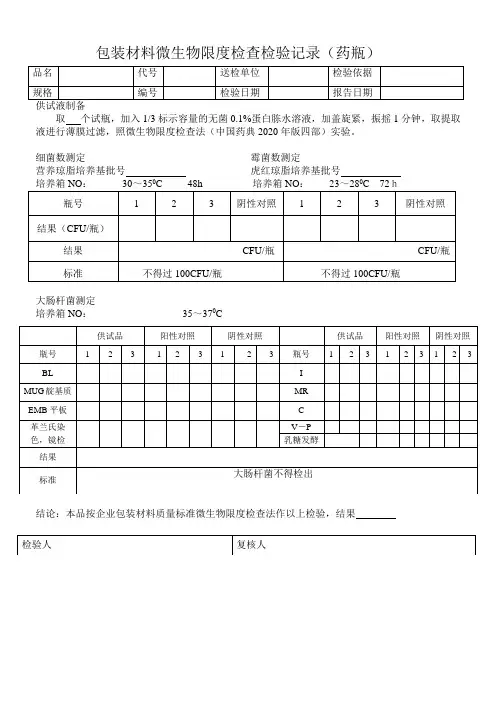
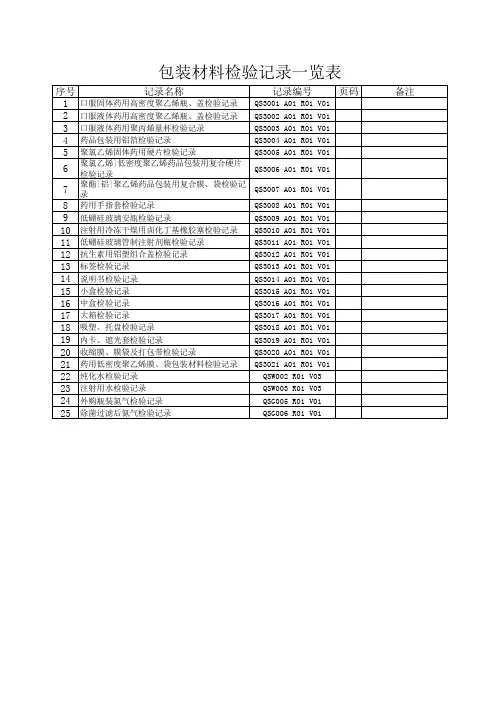
包装材料微生物限度检查检验记录(药瓶)
取个试瓶,加入1/3标示容量的无菌0.1%蛋白胨水溶液,加盖旋紧,振摇1分钟,取提取液进行薄膜过滤,照微生物限度检查法(中国药典2020年版四部)实验。
细菌数测定霉菌数测定
营养琼脂培养基批号虎红琼脂培养基批号
00
大肠杆菌测定
培养箱NO:35~370C
结论:本品按企业包装材料质量标准微生物限度检查法作以上检验,结果
包装材料(复合膜、袋)微生物限度检查检验记录
供试液制备
取试样用开孔面积为20cm2的消毒过的金属模板压在内层面上,将无菌棉签用无菌0.1%蛋白胨水溶液稍沾湿,在板孔范围内擦抹5次,换1支棉签再擦抹5次,每个位置用2支棉签共擦抹10次。
共擦抹5个位置100cm2。
每支棉签擦抹完后立即剪短,投入盛有30ml无菌0.1%蛋白胨水溶液的锥形瓶中,全部擦抹棉签均投入瓶中后。
迅速摇晃1分钟,即得供试液。
细菌数测定:霉菌数测定:
营养琼脂培养基批号玫瑰红纳琼脂培养基批号
培养箱NO:℃48h 培养箱NO:℃72h
大肠杆菌测定:
胆盐乳糖培养基批号:MUG培养基批号:
培养箱NO:36℃±1℃
结论:本品按国家药品监督管理局,国家药品包装容器(材料)标准(试行),药品包装通则,微生物限度检查法检验,结果规定。
文件制修订记录1、抽样方案按GB/T2828.1-2012 (AQL:主0.65 次1.0)抽样标准进行随机抽检。
13 2、检验依据检验卡、包材料检验规范3、检验流程仓库开立送检单至IQC,IQC接送检单后应对产品标识单品名,型号及判定状态进行初步核对,若出现品名,型号或不合格产品直接做退货处理(外购产品除外),并如实对检验状况进行记录,开立品质异常通知单至上级部门进行确认并交送各相关部门进行处理。
4、环保检查若有需要,供方应提供具有权威性检测机构出示的有效期内的环保资料证书。
5、外观检验目视检查是否有如下不良现象:A、主要缺点:材料错误、结构不符、潮湿、油污、裂纹、多料、缺损、偏芯、变形、脱层、加工损坏、印刷错误、压痕、杂色、收缩、瓦绫稀疏、齿状、毛边等不良现象。
B、次要缺点:颜色稍有差异等轻微外观不良现象。
6、尺寸检验参照检验卡抽取数量,对来料厚度尺寸,长、宽、高尺寸进行测量,检查是否符合技术要求,并将测量结果记录于IQC检验记录表。
7、负荷检查A、外包装箱粘贴成型后平面应能够承受75㎏重量不变形,反折90°3次不得出现裂痕、破损。
B、内包装箱粘贴成型后平面应能够承受10㎏重量不变形,反折90°3次不得出现裂痕、破损。
C、包装塑管应能够承受10㎏重量不变形,扳动幅度状不得出现发白、断裂。
D、吸塑盒应能够承受3㎏重量不变形,反折90°3次不得出现裂痕、破损。
8、组装试验抽取相互配合包材进行试装验证(试装必须将所有包材以正常方式进行装配),组装后各相互包装盒/管不得出现挤压变形。
9、判定、处理依据检验卡对检验结果参照主次缺点允收水准接收值进行综合判定,完全符合要求则在产品识别标识单判定为合格并签名确认,若产品状况出现任一条件不相符超过主次缺点允收水准接收值,应判定为不合格处理,描述不合格原因并附不合格样品装订于产品识别标识单左上角,加盖红色NG印章。
随货移至不合格品区域,立即开立品质异常通知单至上级领导进行审批,并将审批后异常通知单分发相关单位办理退货处理、如实对送检单进行判定返送仓库,并对各项检验状况记录于IQC检验记录表报上级审批后存档。

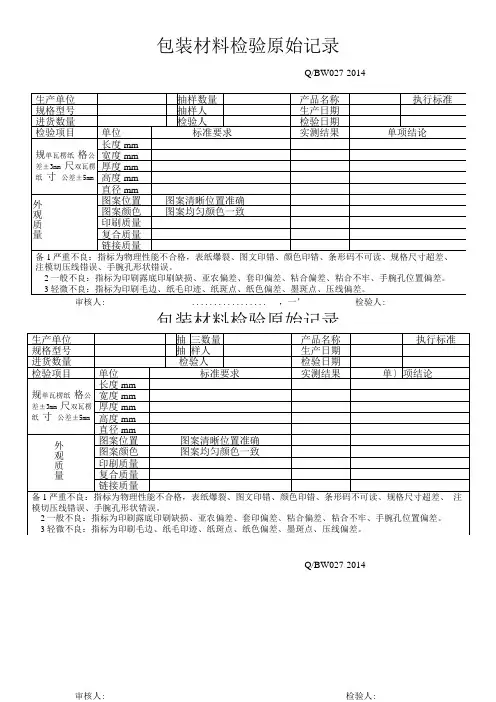

包装材料验证报告拟制****** 日期2007年9月20日审核****** 日期2007年9月20日批准****** 日期2007年9月20日版号 A 生效日期2007年10月1日*************有限公司1 包装材料的要求据EN868-1、YY/T0313-1998标准。
1.1 用作制造******(商品名“******”)的包装材料原料是原始材料,应有原料的来源,明确其历史和可追溯性,并受到控制,以确保成品始终能满足要求。
1.2 包装材料的设计必须在满足原定用途的条件下,把对使用者或患者的安全造成危害的可能性降低到最小程度。
1.2.1 包装材料与******(商品名“******”)的相容性(即包装与医疗器材相互无不良影响):主要考虑的有:拟包装的医疗器械的大小和形状,对物理和其它防护的要求,医疗器械对特殊危险例如辐射、湿气、机械性撞击,静电放射的敏感性。
1.2.3 包装材料与标识方式的相容性:标识方法必须对包装材料与采用的灭菌过程的相容性无不良影响,印刷或书写所采用的油墨不会转移到******(商品名“******”)上,也不会和包装材料起反应而影响包装材料的效用,也不会变色而使标识变的模糊不清,对固定在包装材料表面的标识,其附着方式必须能耐受灭菌过程的使用及制造厂规定的贮存和运输条件。
1.2.4 包装材料能够提供对物理、化学和微生物的防护。
1.2.5 包装材料在使用场所与使用者撕开包装取出使用时的要求相容性(例如无菌的开封)。
1.3 在使用条件下,在灭菌前、中、后,包装材料不可释放已知是有毒的,其数量足以对健康危害的物质。
1.5 无菌状态的保持:(即从其产品灭菌后,成为无菌之时起,直至规定的失效日期或使用时止),包装材料的微生物阻隔特性(见2包装完整性报告)。
2 包装完整性试验2.1 包装完整性试验报告1 试验目的对******(商品名“******”)的包装系统,按照EN868-1:1997“需灭菌的医疗器械的包装材料和方式一”标准中的包装完整性试验方法和“包装完整性试验方案”进行包装完整性验证,来评价包装系统的符合性。
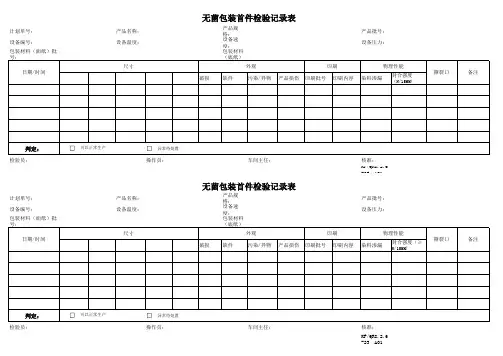
计划单号:产品名称:产品规格:产品批号:设备编号:
设备温度:
设备速度:设备压力:
包装材料(面纸)批号:
包装材料(底纸)
破损
缺件
污染/异物
产品损伤
印刷批号
印刷内容
染料渗漏
封合强度
(N/15MM)
判定:
检验员:
操作员:车间主任:
核准:
KF/QR8.2.6-23 A01
计划单号:产品名称:产品规格:产品批号:设备编号:
设备温度:
设备速度:设备压力:
包装材料(面纸)批号:
包装材料(底纸)
破损
缺件
污染/异物
产品损伤
印刷批号
印刷内容
染料渗漏
封合强度(≥
N/15MM)
判定:
检验员:
操作员:车间主任:核准:KF/QR8.2.6-23 A01
日期/时间
日期/时间
撕裂口撕裂口备注
备注
无菌包装首件检验记录表
尺寸
外观
印刷
物理性能
无菌包装首件检验记录表
尺寸
外观
印刷
物理性能
可以正常生产异常待处置
可以正常生产异常待处置。
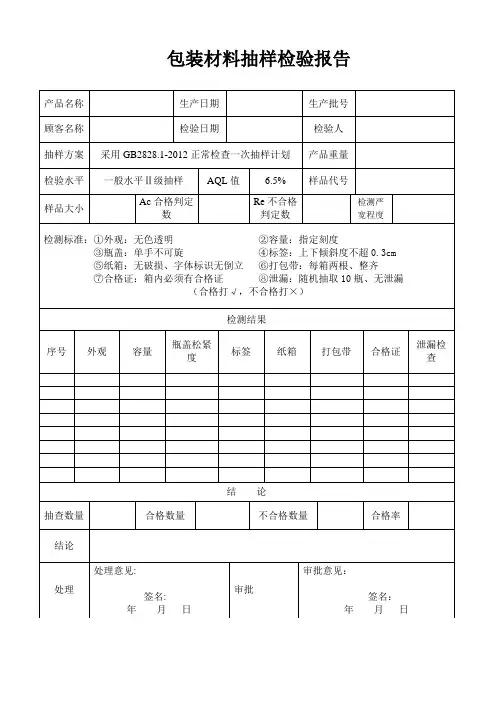

包装检验指导书一、引言包装作为产品质量的重要组成部分,承担着保护产品安全、方便运输和储存的重要职责。
因此,包装的质量和合格性至关重要。
为了确保产品的正常运输和销售过程中不受到损害,我们制定了本《包装检验指导书》。
二、检验目的本指导书的目的是为了规范包装的质量检验流程,确保产品包装符合相关标准和要求,保证产品安全运输和储存,提高客户满意度。
三、检验范围本指导书适用于所有我公司生产的产品的包装检验,包括但不限于以下方面:1. 包装材料的强度和耐久性检验;2. 包装外观检验;3. 包装封装检验;4. 包装标志和说明检验;5. 包装文件和证书检验。
四、检验内容和方法1. 包装材料的强度和耐久性检验我们需要对包装材料的强度和耐久性进行检验,以确保其能够承受正常运输过程中的各种力和压力。
包装材料可以通过拉伸试验、冲击试验、水压试验等多种方法进行检验。
2. 包装外观检验包装外观的检验是为了确保产品包装的完整性和美观性。
我们将对包装盒、包装袋等外观进行检验,检查是否存在划痕、变形、破损等问题。
3. 包装封装检验包装封装的检验是为了确保产品包装的封闭性和防撕裂性。
我们将对包装盒、包装袋的封口进行检验,以确保其能够有效地防止产品的泄漏和损坏。
4. 包装标志和说明检验包装标志和说明的检验是为了确保产品的包装标志和说明与实际产品相符,并且能够为用户提供正确的使用和保养信息。
我们将检查包装上的标志、标签和说明,确保其内容的准确性和清晰度。
5. 包装文件和证书检验包装文件和证书的检验是为了确保产品包装的合法性和规范性。
我们将检查包装文件和证书的齐全性和准确性,并与相关文件进行核对。
五、检验记录和报告在进行包装检验过程中,我们将详细记录检验的结果和过程,包括检验日期、检验人员、检验方法和检验结果等信息。
并可根据需要编制包装检验报告,将检验结果和建议提供给相关部门或客户。
六、质量反馈和改进如发现包装存在质量问题或改进的空间,我们将及时进行反馈并进行改进。
产品包装检验要求
背景
产品包装是保障产品在运输、储存、销售等环节中不受损坏、
变质的重要环节。
因此,对产品包装的检验显得尤为重要,它可以
保证产品的质量和安全,提高客户满意度,降低售后成本。
检验要求
1. 包装完整性检验
检查包装是否完整无损,没有破损、磨损、裂开、变形、漏气、漏水、漏油等现象。
同时检查包装材料是否符合要求,如尺寸、厚度、材质等。
2. 包装标识检验
检查包装标识是否齐全、准确、清晰、不易脱落。
包装标识应
包括产品名称、规格型号、生产日期、保质期、生产企业名称和地
址等信息。
3. 包装质量检验
检查包装质量是否符合国家和行业标准要求,如承重能力、耐压、抗冲击、防潮、防震等。
同时,也要检查包装的美观度和实用性,如易于存储、搬运、打开等。
4. 包装检验记录
对每批次产品的包装进行检验,并及时记录检验结果。
检验记
录应包括产品名称、规格型号、生产日期、检验日期、检验员名称、检验结果等信息。
总结
产品包装检验是保证产品质量和安全的重要环节,需要严格按
照国家和行业标准进行检验。
同时,还需要及时记录检验结果,为
售后服务和质量管理提供参考依据。
只有做到严格检验,才能保证产品的质量和安全,提高客户满意度,增强企业的市场竞争力。
包装材料检验验收规程1.原辅材料及包装材料进厂后,由技术品控部负责全公司各类原辅材料、包装材料的质量抽样、检验、结果判定以及相关原辅材料检验标准的制定工作。
2.原、辅材料及包装材料进厂后,由查验员根据标准要求对原料进行检验,并出具《包装材料检验报告单》。
3.在辅料进厂时,由财务部包材库房管理员持《到货通知单》通知技术品控部查验员,进行取样、检验;4.品控员接到通知单后,按《包装材料验收标准》、合同规定以及相关的国家标准进行感官上的检验,并按抽检数量进行初步使用验证,出具检验报告。
5.技术品控部验完后,并出具《包装材料检验报告单》给库房,库房管理员接到包装材料检验合格证明后,方可办理入库手续。
瓦楞纸箱检验验收规程1.目的:此标准对用瓦楞纸板制成的纸箱的质量要求、检验方法及检验规则作出规定。
2.范围适用于公司产品运输包装所用的个品种规格的瓦楞纸箱3.职责3.1仓库负责包装箱之命名、规格、数量的入库。
3.2行政中心负责各规格包装箱的规格、版面、数量的采购和相关检测报告的索取3.3技术品控部负责包装材料和相关检测报告的验收和审核。
4.技术要求4.1 材质:纸箱材质为国产牛皮纸或瓦楞纸.基重(g/m2)应符合GB/T6544-2008、GB/T13024-2003、GB/T13023-2008.4.2外观、尺寸。
4.2.1纸箱表面应平整、干净无污渍,纸箱应无破损,无裂纹,纸箱切口应齐整。
4.2.2图案、文字印刷要求套印准确,墨色匀实,图案文字清晰,无油污、水化现象、无错位、无重影。
图案、文字边缘齐整、无毛刺。
4.2.3印刷文字正确,图案、文字应与样板一致,套色准确,无颜色过浓或过淡现象。
4.2.4粘合瓦楞纸箱接头粘合搭接舌边宽度不少于30mm,粘合接缝的粘合剂涂布应均匀充分,不得有多余的粘合剂溢出现象。
粘合剂牢固,剥离时至少有70%的粘合面被破坏。
4.2.5瓦楞纸箱压痕宽度不得大于17mm,箱壁不可有多余的压痕线,当纸箱折合时,压痕处不可有破裂、断线的现象。
《材料进场检验记录》材料进场清单及验收记录表鲁jj—022g□□□鲁jj—022g□□□材料/购配件/设备进场检验记录表鲁jj—022g□□□第二篇:材料进场检验制度材料、设备进出场检验制度一、做好进货接收时的联检工作。
在材料、半成品及加工订货进场时,项目部材料室负责组织质检员、材料员参加的联合检查验收。
检查内容包括:产品的规格、型号、数量、外观质量、产品出厂合格证、准用证以及其他应随产品交付的技术资料是否符合要求。
材料室负责填写《材料进场检验》表格,相关人员签字。
二、做好材料进场复试工作。
对于钢材、水泥、砂石料、砼、防水材料等须复试的产品,由项目试验员严格按规定进行,对原材料进行取样,送实验室试验。
同时,做好监理参加的见证取样工作,材料复试合格后方可使用。
专业工程师对材料的抽样复试工作进行检查监督。
三、对于设备的进场验证,由项目各专业技术负责人主持。
专业工程师进行设备的检查和调试,并填写相关记录。
四、在进行材料、设备的检验工作完成后,相关的内业工作(产品合格证、试验报告、准用证等材质证明文件的收集,整理、归档)应及时做到位。
五、在检验过程中发现的不合格材料、设备原则上应做退货处理,并进行记录,按"外埠进入不合格品"进行处置,报项目技术负责人审批。
如可进行降级使用或改用做其它用途,由项目技术负责人签署处理意见。
六、材料、设备进场检验时严格按有关验收规范执行,检验合格后方可使用,出现问题扣发当事人当月奖金,并追究其责任。
七、材料、设备进场检验要做到100%,发现-次未经检验进场或未留下检验记录,分别给予当事人50-100元罚款。
八、材料室做好材料的品种、数量清点,进货检验后要全部人库,及时点验,库管员要做好发放记录。
第三篇:原材料进场抽样检验制度xx工程原材料进场抽样检验制度xx项目部xx年10月原材料进场抽样检验制度1总则为了有效地指导对各种原材料的检验工作,以使原材料的各类要求符合规定,确保新海尚宸家园商业综合体工程的质量,特制定本制度。
定量包装商品净含量计量检验原始记录表编号附表:小学生冬季消防安全主题班会教案安全人人抓,幸福千万家。
安全两天敌,违章和麻痹。
下面聘才小编为大家收集整理的相关资料。
欢迎大家阅读!! 小学生冬季消防安全主题班会教案冬季是火灾多发期和特险期,引发火灾的不安全因素较之平常明显增多。
为确保校园消防安全,吸取xx市“”事件的教训,提高大学生防范火灾意识和技能,普及消防安全知识,推进消防“四个能力”建设,学院将于近期召开冬季消防安全教育主题班会,具体如下:1.召开时间、形式、地点:XX年11月11日起至22日止;各系自行安排时间,以班级为单位开展教育活动,XX级班级在本班教室,XX级班级自行安排教室。
2.班会内容:见后附件“XX年冬季消防安全教育主题班会材料”。
3.班会要求:(1)辅导员老师要亲自到班级主持召开消防安全教育主题班会,同时结合本班存在的消防安全隐患如在宿舍抽烟、乱扔烟头等现象进行教育,尤其要加强对重点对象的教育,如经常出现断电情况的寝室学生、有抽烟行为的学生等。
(2)班会须拍摄相片作为资料存留,相片场景要求:从教室后面往讲台方向,以黑板为背景,拍摄辅导员老师在班级主持召开安全教育主题班会的教室全景照片,黑板上须用粉笔写上班会标题“XX年冬季消防安全教育主题班会”。
(3)班会要做好记录工作,参加班会的学生须在班会记录上签名。
(4)班会记录材料请于11月23日前以系部为单位交给保卫处朱老师(弘商楼一楼保卫处治安科),电子相片(1张)请在12日前发保卫处电子信箱xx;电子相片也可用U盘存储,在交材料时进行拷贝。
相片命名:××班级XX年冬季消防安全教育照片。
因相片存储需要,只收电子版相片,请勿将照片冲印。
(5)XX级毕业班辅导员要克服困难,对留在学校的学生进行教育,确保毕业班宿舍的消防安全。
火灾危害极大,一旦发生火灾,轻则损失财产,重则危及生命,并危及群体,因此消防安全工作责任重大,开展好消防安全教育活动对保障师生的人身安全、财物安全、维护学院和社会的安全稳定有着重要的意义。
包装材料检验记录
编号:RD-5007
[性状]本品为。
一.标准依据:
1.内包装膜、袋:依据YBB00072005《药用低密度聚乙烯膜、袋》及参照《中国药典》2010年版微生物限度检查法
2.瓦楞纸箱:依据中华人民共和国国家标准GB6453-86《瓦楞纸箱》标准。
3.复合塑编袋(三合一):依据GB/T8947-1998《复合塑料编织袋》检查。
二.内包装膜、袋的检查:
1.外观:
取本品适量,在自然光线明亮处,正视目测;表面应光洁、平整、色泽均匀,不得有穿孔、异物、异味、粘连。
袋的热封部位应平整、无虚封。
2.接头数(膜):随机记录,实用时复核,每卷不得多于3个,并在接头处加一标记。
3.卷面和端面:目测,应缠紧、缠齐,端面应平整,不允许有错层、塔层、松层或管芯自由脱落现象,不允许有严重碰伤、压陷。
4.印刷质量:
4.1印刷图案、文字:与标准样张核对,文字应无错漏,文字内容应有批准文号、品名、规格、适应症、用法用量等内容,文字清晰。
手拭,文字应不脱落、不掉色。
4.2印刷错位:与标准样张核对,以分度尺为0.5mm的直尺测量,应在指定位置±2mm 内。
4.3印刷色泽:色泽均匀,与标准样张核对,同批与不同批之间不允许有明显色差。
5.微生物限度检查:取试样,用开孔面积为25cm2的消毒过的金属模板压在内层面上,将湿润的无菌棉签在板孔范围内擦抹5次,换1支棉签再擦抹5次,每个位置用2支棉签共擦抹10次,共擦抹4个位置100cm2。
每支棉签抹完后立即剪断,投入盛有50ml无菌生理水的锥形瓶中,全部擦抹棉签投入瓶中后,将瓶迅速摇晃1分钟,即得供试液,取供试液参照中国药典2005年版附录微生物限度检查法项下规定,按《微生物限度检验操作规程》检验。
细菌:≤800个/g;霉菌(酵母菌):≤80个/g;大肠埃希菌不得检出。
三.复合塑编袋(三合一)的检查:
1.复合塑编袋(三合一)是指以聚乙烯树脂、聚丙烯为主要原料,经挤压、拉伸成扁丝,再经编织成的塑料编织布为基材,经流延法复合制成的用于包装粉状或粒状固体物料的复合编织袋(布/膜/纸复合为三合一,经缝制或粘和缝制成袋称为三合一袋)。
2.本标准规定的复合塑编袋(三合一)型号为A型,允许装载质量为25kg,规格尺寸由供需双方商定。
3
4
5
6.内袋的微生物限度检查:依据内包装膜、袋的微生物限度检查法检查,细菌数不得过1000个/100cm2,霉菌(酵母菌)数不得过100个/100cm2,大肠埃希菌不得检出。
7.检查:
7.1外观检验:在自然光线下目测,应符合要求。
7.2长度和宽度:将袋摊平,用精确至1mm的直尺在中间和离边100mm处各量三处,直尺与袋边平行,以最大偏差作为测试结果。
7.3袋的单位面积质量:将袋摊平,在袋的上下两对角处取面积为100mm2两方块,试样外边线与袋边线相距100mm,用最小分度值为0.01g的天平称取质量。
四.瓦楞纸箱的检查:本公司所用纸箱为双瓦楞纸箱。
1.检查所取样品是否洁净、无污染;印刷文字应有批准文号、品名、规格等内容,文字清晰。
手拭,文字应不脱落,不掉色。
箱面印刷文字清晰、深浅一致,位置准确。
2.尺寸偏差:尺寸偏差为±5mm。
3.箱体方正,表面不允许有明显的损坏和污迹,切断口表面裂损宽度不超过8mm。
4.纸箱接头钉合搭舌边宽度35-50mm,金属钉应沿搭接部分中线钉合,采用斜钉(与纸箱立边成45度角),箱钉应排列整齐,单排钉距不大于80mm,钉距均匀,头尾钉距底面厂压痕边距不大于20mm,钉合接缝应钉牢、钉透,不得有叠钉、翘钉、不转角等缺陷。
5.若纸箱接头为粘合剂粘合,粘合搭接舌边宽度不小于30mm,粘使剂应涂布均匀,以致面纸分离时接缝仍然粘合不分,同时不应有多余的粘合剂溢出接缝。
6.瓦楞纸箱的压痕宽度不大于17mm,折线居中,不得有破裂断线,箱壁不允许有多余的压痕。
7.瓦楞纸箱摇盖经开、合180°往复5次以上,面层和里层都不得有裂缝。
8.纸箱隔挡(俗称隔板)必须采用竖瓦分割,每格间距根据纸箱长度平均分割。
衬垫(垫板)要求厚度为2mm,尺寸如下。
附:
包装材料规格(mm):。