鲁科版化学必修一金属钠与化合物的性质
- 格式:ppt
- 大小:1.91 MB
- 文档页数:7

第三章 金属及其化合物 第一节 钠及其重要化合物一、钠 1、物理性质银白色金属光泽,质软(可用小刀切割),密度比水小比煤油大(保存在煤油中),熔沸点低,具有良好的导热性和导电性。
2、化学性质(1)与非金属反应:如O 2、Cl 2、S 等。
①钠与氧气反应常温下生成Na 2O (白色),化学方程式为: 4Na+O 2=2Na 2O燃烧时生成Na 2O 2(黄色),化学方程式为: 2Na+O 2 Na 2O 2 ②钠与氯气反应化学方程式为:2Na+Cl 2 2NaCl ③钠与硫反应化学方程式为: 2Na+S Na 2S (2)与水、酸反应(反应顺序:先酸后水)①钠与水、酸反应的实质上均是和H +反应,离子方程式分别为: 2Na+2H 2O=2Na ++2OH —+H 2↑、2Na +2H +=2Na ++H 2↑ ②钠与水反应(加酚酞)的实验现象和解释(3)Na 与盐溶液的反应(反应顺序:先与水反应,再考虑NaOH 是否与盐反应) ①钠投入到NH 4Cl 溶液中,有H 2和NH 3逸出,化学方程式为: 2Na+2NH 4Cl=2NaCl+2NH 3↑+H 2↑②投入到CuSO 4溶液中,有气体放出和蓝色沉淀生成,化学方程式: 2Na+2H 2O=2NaOH+H 2↑ 、 CuSO 4+2NaOH =Na 2SO 4+Cu(OH)2↓ 思考:金属钠露置在空气中的变化过程是怎样的?点燃点燃加热切开金属钠,呈银白色(钠的真面目)→变暗(生成Na2O)→变白色固体(生成NaOH)→成液(NaOH 潮解)→结块(吸收CO2成Na2CO3·10H2O)→最后成白色粉末(Na2CO3·10H2O风化为Na2CO3)。
3、钠的保存、制取及用途⑴金属钠的保存及取用少量金属钠可保存在煤油里,大量的金属钠则存入在铁筒中用石蜡密封。
取用时一般先用镊子把钠从煤油中夹出来,并用滤纸把表面的煤油吸干,然后用小刀切下绿豆大小的一块再做有关实验。
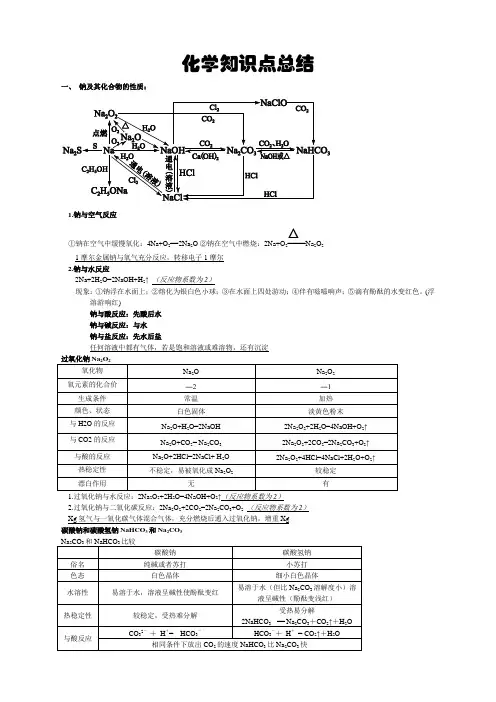
化学知识点总结一、 钠及其化合物的性质:1.钠与空气反应①钠在空气中缓慢氧化:4Na+O 2==2Na 2O ②钠在空气中燃烧:2Na+O 2=====△Na 2O 21摩尔金属钠与氧气充分反应,转移电子1摩尔 2.钠与水反应2Na+2H 2O=2NaOH+H 2↑ (反应物系数为2)现象:①钠浮在水面上;②熔化为银白色小球;③在水面上四处游动;④伴有嗞嗞响声;⑤滴有酚酞的水变红色。
(浮溶游响红)钠与酸反应:先酸后水 钠与碱反应:与水 钠与盐反应:先水后盐任何溶液中都有气体,若是饱和溶液或难溶物,还有沉淀过氧化钠Na 2O 2氧化物 Na 2O Na 2O 2 氧元素的化合价 ―2 ―1 生成条件 常温 加热 颜色、状态 白色固体 淡黄色粉末与H2O 的反应 Na 2O+H 2O=2NaOH 2Na 2O 2+2H 2O=4NaOH+O 2↑ 与CO2的反应 Na 2O+CO 2= Na 2CO 3 2Na 2O 2+2CO 2=2Na 2CO 3+O 2↑ 与酸的反应 Na 2O+2HCl=2NaCl+ H 2O 2Na 2O 2+4HCl=4NaCl+2H 2O+O 2↑热稳定性 不稳定,易被氧化成Na 2O 2较稳定 漂白作用无有1.过氧化钠与水反应:2Na 2O 2+2H 2O=4NaOH+O 2↑(反应物系数为2)2.过氧化钠与二氧化碳反应:2Na 2O 2+2CO 2=2Na 2CO 3+O 2 (反应物系数为2) Xg 氢气与一氧化碳气体混合气体,充分燃烧后通入过氧化钠,增重Xg 碳酸钠和碳酸氢钠NaHCO 3和Na 2CO 3 Na 2CO 3和NaHCO 3比较碳酸钠 碳酸氢钠 俗名 纯碱或者苏打 小苏打 色态 白色晶体细小白色晶体水溶性 易溶于水,溶液呈碱性使酚酞变红易溶于水(但比Na 2CO 3溶解度小)溶液呈碱性(酚酞变浅红)热稳定性 较稳定,受热难分解 受热易分解2NaHCO 3 == Na 2CO 3+CO 2↑+H 2O与酸反应CO 32-+ H += HCO 3-HCO 3-+ H += CO 2↑+H 2O相同条件下放出CO 2的速度NaHCO 3比Na 2CO 3快与碱反应Na 2CO 3+Ca(OH)2= CaCO 3↓+2NaOH CO 32-与金属阳离子的复分解反应 NaHCO3+NaOH =Na2CO3+H2O HCO 3-+OH -= H 2O +CO 32-与H 2O 和CO 2Na 2CO 3+CO 2+H 2O =2NaHCO 3 CO 32-+H 2O +CO 2 =H CO 3-不反应1.在碳酸钠溶液中滴加稀盐酸:Na 2CO 3+ HCl = NaCl+NaHCO 3 NaHCO 3+ HCl = NaCl+H 2O+CO 2↑(过一会有气泡) 在碳酸氢钠中加入稀盐酸:NaHCO 3+ HCl = NaCl+H 2O+CO 2↑(迅速产生大量气体) 在盐酸中加入碳酸钠溶液:Na 2CO 3+ 2HCl = 2NaCl+H 2O+CO 2↑(产生大量气体 较慢)2.在碳酸钠溶液中通入二氧化碳:Na 2CO 3+CO 2+H 2O=2NaHCO 33.碳酸氢钠受热分解:2NaHCO 3=====△Na 2CO 3+H 2O+CO 2↑4.氢氧化钠与碳酸氢钠反应:NaOH+NaHCO 3=Na 2CO 3+H 2O 鉴别碳酸钠与碳酸氢钠的物质可以是酸、盐,不能为碱 二、 氯及其化合物的性质氯元素单质及其化合物间的转化关系1、液氯、新制的氯水和久置的氯水比较2、Cl 2的用途:①自来水杀菌消毒Cl 2+H 2O == HCl +HClO 2HClO ===(光照) 2HCl +O 2 ↑ 其中次氯酸HClO 有强氧化性和漂泊性,起消毒漂白作用。

第1课时 研究物质性质的基本方法自主学习1.研究物质的性质,常常运用□01观察、实验、分类、比较等方法。
(1)观察⎩⎨⎧直接观察:直接用肉眼观察物质的□02颜色、状态以及用鼻子闻物质的气味等间接观察:借助一些仪器来进行观察(2)实验是□03根据科学研究的目的,尽可能排除外界影响,突出主要因素并利用一些专门的仪器设备,人为地变革、控制或模拟研究对象,使某一现象或过程发生或再现的研究方法。
①在研究物质性质的过程中,可通过□04实验来验证对物质性质的预测或探究物质未知的性质。
②利用实验方法研究物质性质时,实验前要□05明确实验目的、实验用品和实验方案等;实验中要□06仔细观察实验现象,并做好实验记录;实验后要□07对实验结果进行分析,并写好实验报告。
实验过程中,要注意控制□08温度、压强、溶液的浓度等条件,这是因为同样的反应物在不同的条件下可能会发生不同的反应。
(3)除了观察和实验外,□09分类和比较也是研究物质性质时的常用方法。
在研究物质的性质时,可以运用分类的方法,总结□10各类物质的一般性质,并根据物质所属的类别对物质及其变化进行预测;可以运用比较的方法,认识□11各类物质性质之间的异同,以及各类物质性质之间的内在联系。
(4)除了研究物质性质的基本方法外,在进行化学研究时还会用到□12假说和模型的方法。
在已有事实和科学理论的基础上,科学工作者往往通过□13提出假说对有关现象或规律的本质以及未知物质或现象进行推测性说明,通过建构模型对物质或物质的变化进行简化模拟。
假说和模型具有□14解释性功能和预见性功能,但是所做的预测或说明是否正确还需要通过□15实验来验证。
在科学研究中,随着研究的深入,往往是旧的假说或模型被推翻,而建立起新的假说或模型。
2.钠的性质、用途及保存 (1)钠的物理性质①钠与水的反应:常温下与冷水剧烈反应,反应的化学方程式为□212Na +2H 2O===2NaOH +H 2↑。

1、Na放置在空气中:4Na+O2=2Na2O2、Na在空气中燃烧:2Na+O2点燃Na2O23、Na和水反应:2Na+2H2O=2NaOH+H2↑离子方程式2Na+2H2O=2Na++2OH—+H2↑4、过氧化钠(Na2O2)与水反应:2Na2O2 + 2H2O = 4NaOH + O2↑离子方程式2 Na2O2+2H2O=4Na++4OH—+O2↑5、过氧化钠(Na2O2)与二氧化碳反应:2Na2O2 + 2CO2 = 2Na2CO3 + O26、NaHCO3加热:2NaHCO3加热Na2CO3+H2O+CO2↑7、用小苏打治疗胃酸过多:NaHCO3+HCl==NaCl+H2O+CO2↑离子方程式HCO3_—+H+== H2O+CO2↑8、碳酸钠与盐酸反应Na2CO3+2HCl==2NaCl+H2O+CO2↑离子方程式CO3_2—+2H+== H2O+CO2↑认识本质(分步反应过程如下):Na2CO3+ HCl==2NaCl + NaHCO3 NaHCO3+HCl==NaCl+H2O+CO2↑9、氢氧化钠中通入少量的二氧化碳:2NaOH+ CO2= Na2CO3 + H2O10、氢氧化钠中通入过量的二氧化碳:2NaOH+ CO2= Na2CO3 + H2O 和Na2CO3 + H2O+ CO2= 2NaHCO3总反应:NaOH+ CO2= NaHCO3二、知识讲解考点1、钠的性质1.物理性质:银白色金属光泽、质软、可以用刀切割、密度小于水大于煤油、熔沸点低。
2.化学性质:(1)钠与非金属单质反应:2Na +Cl 22NaCl (白烟) 2Na +S Na 2S缓慢氧化:4Na+O 22Na 2O (白色固体)剧烈燃烧:2Na+O 22O 2(淡黄色固体)(2)钠与水的反应2Na+2H 2O2NaOH+H 2↑ 2Na+2H 2O2Na ++2OH-+H 2↑(3)与酸(主要指非氧化性酸)的反应:钠不足,则反应为:钠与酸直接反应。

第三章 金属及其化合物知识点3.1 – 钠及其化合物知识点☆(了解)一、钠单质的性质(1)钠的物理性质:钠是银白色金属,密度小(0.97g/cm3),熔点低(97℃),硬度小,质软,可用刀切割。
钠通常保存在煤油中。
是电和热的良导体。
(2)钠的化学性质:从原子结构可知钠是活泼的金属单质。
Na――――――――→O 2、Cl 2、H 2O 、H +等-e-Na +二、钠(Na )与非金属单质反应: ★(掌握)①钠和空气和氧气的反应: 钠和空气的反应: 钠在空气中的变化:银白色的钠→ 变暗(生成了氧化钠)→ 变白(生成氢氧化钠)→ 潮解 变成白色固体(生成碳酸钠)。
钠和氧气的反应: 常温: 4Na + O 2 == 2Na 2O加热: 2Na + O 2 == Na 2O 2; 2Na + Cl 2 == 2NaCl; 2Na + S == Na 2S 等反应实验:A 、实验过程: ①→②→③→④→⑤→⑥→⑦B 、反应原理: 2Na +O 2∆=====Na 2O 2,2Na 2O 2+2H 2O =4NaOH +O 2↑ C 、注意事项:①玻璃管中装的钠不能太大,太大反应太剧烈,会将玻璃管炸裂. ②反应开始时,即钠熔成小球后要稍稍倾斜玻璃管,但是角度不能太大,以防止钠从玻璃管中脱出.并能保证空气疏通从而观察到明显现象.③在取钠时要将其表面的氧化物用小刀除去,用纯钠进行实验.因为表面被氧化的钠在受热熔化后,钠表面会有一层黑色而影响实验现象的观察.④加热时间不能太长,否则钠与O2迅速反应、燃烧起来,现象就不是很明显了.⑤盛Na2O2的小试管要干燥.D、实验现象:钠熔成小球,先变成白色后变成淡黄色固体,淡黄色固体遇水放出使带火星木条复燃的气体.E、实验结论:钠熔点低,与O2加热反应生成Na2O2,Na2O2遇水生成O2.★(掌握)②钠与水反应:钠与水的反应:2Na + 2H2O == 2NaOH + H2↑反应实验:A、反应原理:2Na + 2H2O == 2NaOH + H2↑B、实验现象:①钠与水剧烈反应②钠熔化成小球③钠球在水面上不停地滚动④有气体生成,并发出嘶嘶声⑤因为生成强碱,使得酚酞溶液变红☆(了解)③钠和酸、盐溶液、氢气的反应☆(了解)钠与酸的反应:A、反应原理:2Na + 2HCl == 2NaCl + H2↑B、实验现象:Na放入稀盐酸中,是先与酸反应,酸不足再与水反应。

鲁科版-高中化学必修1知识点总结高中化学必修一知识点总结(鲁科版)一、钠及其化合物的性质:钠(Na)是一种金属元素,具有活泼的化学性质。
1.钠与空气反应钠在空气中会缓慢氧化,生成氧化钠(Na2O),也可以燃烧生成过氧化钠(Na2O2)。
2.钠与水反应钠与水反应会生成氢气和氢氧化钠(NaOH),同时会有剧烈的反应,表现为钠浮在水面上,熔化为银白色小球,在水面上四处游动,并伴有嗞嗞响声。
此外,滴入酚酞的水会变红色。
过氧化钠(Na2O2)是一种强氧化剂,与水和二氧化碳反应会生成氢氧化钠和碳酸钠。
碳酸钠和碳酸氢钠(NaHCO3和Na2CO3)是常见的钠化合物。
在碳酸钠溶液中滴加稀盐酸会生成碳酸氢钠,而在盐酸中加入碳酸钠溶液则会生成二氧化碳气体。
碳酸氢钠受热分解会生成碳酸钠、水和二氧化碳气体。
氢氧化钠与碳酸氢钠反应会生成碳酸钠和水。
二、氯及其化合物的性质氯(Cl)是一种具有强氧化性的非金属元素。
1.氯气(Cl2)与金属单质的反应氯气可以与铁丝和铜丝燃烧生成相应的金属氯化物。
2.氯气与非金属单质的反应氯气可以与氢气燃烧生成氢氯酸。
此外,氯气还可以与硫化氢、二氧化硫等非金属单质反应。
3.氯气与水的反应氯气与水反应会生成次氯酸和盐酸。
4.氯气与氢氧化钠的反应氯气与氢氧化钠反应会生成次氯酸钠和氯化钠,常用于氯气的尾气处理。
5.制取漂白粉氯气能通入石灰浆,生成氯化钙和次氯酸钙,后者经过干燥和粉碎即可得到漂白粉。
2CaCl2和Ca(ClO)2叫做漂白粉。
漂白粉在空气中会变质,变成CaCO3和2HClO。
以物质的量为中心的物理量关系包括三个部分:物理量、物质的量单位和XXX(mol)。
物质的摩尔质量M可以通过n=m/M计算得出。
气体的摩尔体积Vm可以通过n=V/Vm计算得出,其中V为气体体积,单位是升(L),而Vm是气体摩尔体积,标准状况下,1 mol气体为22.4 L。
溶液中溶质的物质的量浓度c可以通过n=cV计算得出,其中C为溶液中溶质的物质的量浓度,单位为mol•L。

第一章第一节1.化学科学的概念:化学是在原子、分子的基础上研究物质的组成、结构、性质、转化及其应用的一门基础科学2.①1661年-英国科学家波义耳提出了元素的概念②1881年-法国化学家拉瓦锡建立了燃烧的氧化学说③1803年-英国科学家道尔顿提出原子学说④1811年-俄国科学家阿伏伽德罗提出分子学说⑤1869年门捷列夫发现元素周期律第二节研究物质性质的基本方法:观察法、实验法、分类法、比较法、模型法、假说法(一)金属钠22常温4Na+O2=2Na2O(白色固体)现象:银白色变为白色加热/点燃2Na+O2=加热/点燃=Na2O2 (淡黄色固体)现象:剧烈燃烧,产生淡黄色火焰,生成淡黄色固体3.与酸反应(钠少量)2Na+2HCl=2NaCl+ H2↑(比钠与水反应更剧烈) 现象:有无色无味气体产生(钠多量:先和酸再和水) 2Na+2HCl=2NaCl+ H2↑2Na+2H2O=2NaOH+H2↑现象:有无色无味气体产生4.与碱反应只和水2Na+2H2O=2NaOH+H2↑5.与盐反应钠和硫酸铜2Na+2H2O=2NaOH+H2↑2NaOH+CuSO4=Cu(OH)2↓+Na2SO4 现象:有气体生成,有蓝色沉淀生成总结:与酸先和酸,与碱只和水,与盐先和水,与氧看条件6.钠的用途:(1)蒸汽钠灯(2)用作还原剂(3)Na-K合金作导热剂222Na→Na2O→NaOH→NaOH溶液→Na2CO3溶液/结晶→Na2CO3粉末Na2O2→NaOH→NaOH溶液→Na2CO3溶液/结晶→Na2CO3粉末9.钠保存在煤油中原因:钠与空气中氧气和水蒸气均反应,因为密度比煤油大沉在煤油瓶底部,从而隔绝空气233别名 纯碱、苏打小苏打 溶解性 Na 2CO 3溶解性> NaHCO 3溶解性 与CO 2反应 Na 2CO 3+ CO 2+H 2O=2 NaHCO 3与HCl 反应Na 2CO 3+HCl= NaHCO 3+ NaClNaHCO 3+ HCl= NaCl+H 2O+ CO 2↑ NaHCO 3+ HCl= NaCl+H 2O+ CO 2↑ 与NaOH 反应 NaHCO 3+NaOH= Na 2CO 3+ H 2O与Ca(OH)2反应 Na 2CO 3+ Ca(OH)2= CaCO 3↓+2NaOH(少)NaHCO 3+ Ca(OH)2= Na 2CO 3+CaCO 3↓+2H 2O (多)NaHCO 3+ Ca(OH)2= CaCO 3↓+NaOH+H 2O 转化 Na 2CO 3 NaHCO 3 用途造纸、化工原料、制玻璃制药、制发酵粉11.比较Na 2CO 3和NaHCO 3热稳定性实验装置B 管是Na 2CO 3 A 管是NaHCO 3现象:右边的澄清石灰水变浑浊(二)研究物质性质的基本程序 1.氯气的物理性质 颜色 状态 密度 味道 溶解性 毒性 黄绿色气体比空气大刺激性气味能溶于水有毒2.氯气的化学性质 ①与H 2O 反应△Cl 2+H 2O ⇄HCl+ HClO△结论:干燥的氯气没有漂白作用,湿润的氯气具有漂白性(氯气和水反应生成HClO )△HClO :能使有色物质褪色,消毒,杀菌作用,不稳定性2HClO=光照=2HCl+ O 2↑△久置氯水:稀盐酸△新制氯水:三分子四离子 分子:Cl 2、H 2O 、HClO 四离子H +、Cl -、OH -、ClO -△实验内容 实验现象实验结论 将镁条投入氯水中 镁条表面有气泡冒出 氯水中含有H +将氯水中滴加硝酸银溶液 产生白色沉淀 氯水中含有Cl -将红色的布条放入氯水中 红色布条褪色 氯水中含有漂白性物质(HClO ) 氯水中滴加紫色石蕊溶液先变红后褪色氯水中含H +和漂白性物质(HClO )△Cl 2和碱反应(NaOH 可吸收多余Cl 2,防止污染空气)制备84消毒液Cl 2+2NaOH=NaClO+NaCl+ H 2O 消毒原理 NaClO+CO 2+H 2O=NaHCO 3 + HClO有效成分 2HClO=光照=2HCl+ O 2↑制备漂白粉2Cl 2+ 2Ca(OH)2= Ca(ClO)2+CaCl 2+ H 2O 漂白原理Ca(ClO)2+CO 2+H 2O= CaCO 3↓+2 HClO用石灰乳 有效成分 2HClO=光照=2HCl+ O 2↑②与Na 反应 Cl 2+2Na=点燃=2NaCl(剧烈燃烧,黄色火焰,产生大量白烟)③与Fe 反应 3Cl 2+2Fe=点燃=2FeCl 3(产生红棕色烟,溶于水,溶液呈黄色) 氯气的强氧化性 ④与Cu 反应 Cl 2+Cu=点燃=CuCl 2(产生黄棕色烟。

高中化学必修一钠及其化合物work Information Technology Company.2020YEAR高中化学必修一钠及其化合物要点一:钠单质的重要性质及其应用1.物理性质 颜色 熔点 硬度 密度导电导热性银白色低小比水的 ,比煤油的 。
良好2.化学性质从钠的结构认识钠的化学性质——还原性。
(1)与非金属单质(如O 2、Cl 2)的反应 与O 2反应⎪⎩⎪⎨⎧==+==+22222a a 2a 2a 4O N O N O N O N :加热时,化学方程式为:常温下,化学方程式为(2)与水的反应①化学方程式为:2Na+2H 2O==2NaOH+H 2↑ ②与滴加酚酞的水反应的现象与解释 浮:钠的密度比水要小;要点诠释:钠在空气中的变化过程分析 过程 现象 反应原理 ① 变暗 4Na+O 2===2Na 2O ② 成液 Na 2O +H 2O===2NaOH③ 结块 2NaOH+9H 2O+CO 2===Na 2CO 3·10H 2O ④变成粉末Na 2CO 3·10H 2O===Na 2CO 3+10H 2O综上,把钠久置在空气中,最终变成Na2CO3粉末。
(3)与酸的反应2Na+2H+=====2Na++H2↑a.若酸过量,则只考虑钠与酸的反应。
b.若钠过量,钠首先与酸反应,剩余的钠再与水反应。
(4)与盐的反应与盐溶液发生反应时先与水反应,生成的碱与盐可能发生复分解反应。
a.与NaCl、Na2SO4、NaNO3溶液反应:实质是与水反应。
b.与CuSO4溶液反应:钠先与水反应,生成的NaOH再与CuSO4反应。
写出Na与CuSO4溶液反应的离子方程式:3.工业制备与保存钠的制取及保存4.钠的重要用途典型例题1、等质量的两块钠,第一块在足量氧气中加热,第二块在足量氧气(常温)中充分反应,则下列说法正确的是()A.第一块钠失去电子多B.两块钠失去电子一样多C.第二块钠的反应产物质量最大D.两块钠的反应产物质量一样大解:A、金属钠失电子均变为+1价的阳离子,等质量的两块钠,失电子是一样的,故A错误;B、金属钠失电子均变为+1价的阳离子,等质量的两块钠,失电子是一样的,故B正确;C、根据4Na+O2=2Na2O,则1mol金属钠获得氧化钠的质量是31g,根据反应2Na+O2Na2O2,则1mol金属钠获得过氧化钠的质量是39g,等质量的两块钠,即金属钠的物质的量是相等的,所以生成过氧化钠的质量大,即第一块钠的反应产物质量最大,故C错误;D、根据C的计算可以知道第一块钠的反应产物质量最大,故D错误。



化合物知识点总结一.金属钠(一)钠1.物性金属钠是一种柔软,银白色、有金属光泽的金属,是热和电的良导体;它的密度比水的密度小,比煤油的密度大,熔点为℃、沸点为℃2.化性(1)跟非金属反应:4Na+O2=2Na2O,(空气中钠的切面变暗 2Na+O2Na2O2(黄色火焰) Na2O2比Na2O 稳定 2Na+Cl2 NaCl(白烟) 钠与水反应:2Na+2H2O =2NaOH +H2↑现象:①浮:钠投入水中并浮在水面上②声:钠立即跟水反应,并放出热量,发出嘶嘶响声,产生气体。
③游:同时钠熔成一个闪亮的小球并在水面上向各方迅速游动最后消失,④红:反应后的水溶液使酚酞变红。
钠与CuSO4溶液反应2Na+2H2O+CuSO4=Na2SO4 +Cu(OH)2↓+H2↑3.钠的制取和存放(1)制备:2NaCl(熔融) 2Na+Cl2↑(2)钠的存放:少量金属钠可保存在煤油里。
(3)用途:强还原剂,工业用它还原金属钛、锆、铌等;如:4Na+TiCl4(熔融)=Ti+4NaCl,钠和钾的合金在常温下呈液态,是原子反应堆的导热剂;钠也可用于制高压钠灯(二).钠的化合物12.碳酸钠与碳酸氢钠3.氢氧化钠(NaOH)是常见的强碱,是一种白色片状晶体,。
极易溶于水(并放出大量热),易吸水而发生潮解,在空气中还易变质,反应为:2NaOH+CO2=Na2CO3+H2O。
俗名:苛性钠、烧碱、火碱,氢氧化钠有很强腐蚀性,具有碱的通性。
保存:密封保存。
试剂瓶不能用玻璃塞,应用橡皮塞。
因为烧碱能与玻璃成分中的SiO2发生反应:SiO2+2NaOH=Na2SiO3+H2O,生成的Na2SiO3使玻璃塞与瓶口粘结。
二、镁的性质(1)物理性质:镁是一种银白色金属,密度小,只有铝密度2/3,熔点较低,硬度较小,镁合金的强度高、机械性能好。
金属镁有“国防金属”的美誉。
在冶金工业上,金属镁常做脱氧剂和还原剂。
(2)化学性质(还原性)①与非金属单质反应 2Mg + O2点燃2MgO3Mg + N2点燃Mg3N2 Mg + Cl2点燃MgCl2②与酸反应与镁与非氧化性酸如稀硫酸、盐酸等反应生成氢气:Mg + 2H+=Mg2+ + H2↑与镁与氧化性酸,如浓硫酸、硝酸等反应,但不生成氢气:Mg + 2 H2SO4(浓) = MgSO4 + SO2↑+ 2H2O③与某些氧化物反应2Mg + CO2点燃2MgO + C现象:燃着的镁条在CO2中继续燃烧,发出耀眼的白光,生成白色固体,在集气瓶的内壁有黑色固体附着。
鲁科版化学必修一知识点总结一、钠及其化合物的性质:氯元素单质及其化合物间的转化关系氯气Cl 21.与金属单质铁丝在氯气中燃烧:2Fe+3Cl 22FeCl 3 (剧烈燃烧=====点燃 铜丝在氯气中燃烧:Cu+Cl 2CuCl 2(剧烈燃烧=====点燃 2.与非金属单质1.物质的量n 单位-摩尔(mol )①n= N/N AN :微粒个数N A :阿伏加德罗常数 N A =6.02×1023 mol -11.定义:分散质粒子直径介于1-100nm2.胶体性质:①丁达尔现象②聚沉3.胶体提纯:渗析五、电解质和非电解质1.电解质定义:①条件:水溶液或熔融状态;②性质:能否导电;③物质类别:化合物。
2.强电解质:强酸、强碱、大多数盐、金属氧化物;弱电解质:弱酸、弱碱、水等。
3.离子方程式的书写:①写:写出化学方程式②拆:将易溶、易电离的物质改写成离子形式,其它以化学式形式出现。
下列情况不拆:难溶物质、难电离物质(弱酸、弱碱、水等)、氧化物、③删:将反应前后没有变化的离子符号删去。
六、氧化还原反应1.氧化还原反应的两条线:还原剂(所含某元素)价升高—失电子—被氧化——产物为氧化产物氧化剂(所含某元素)价降低—得电子—被还原——产物为还原产物3.氧化性:氧化剂>氧化产物1.Fe2+及Fe3+离子的检验:① Fe2+的检验:(浅绿色溶液)a) 加氢氧化钠溶液,产生白色沉淀Fe(OH)2,继而变灰绿色,最后变红褐色b) 加KSCN溶液,不显红色,再滴加氯水,溶液显血红色。
② Fe3+的检验:(黄色溶液)a) 加氢氧化钠溶液,产生红褐色沉淀Fe(OH)3。
b) 加KSCN溶液,溶液显血红色。
2.主要反应的化学方程式:氮及其重要化合物的转化关系1.“雷雨发庄稼”涉及反应原理: ① N 2+O 2放电2NO ② 2NO+O 2=2NO 2 ③ 3NO 2+H 2O=2HNO 3+NO =====放电2.氨的工业制法:N 2+3H 22NH 33.氨的实验室制法:① 原理:2NH 4Cl+Ca(OH)22NH 3↑+CaCl 2+2H 2O=====△② 装置:与制O 2相同 ③ 收集方法:向下排空气法 ④ 检验方法:a) 用湿润的红色石蕊试纸试验,会变蓝色。
第二节研究物质性质的方法和程序【教学目标】1.知识与技能目标:⏹使学生了解金属钠的物理性质及主要的化学性质(钠跟水、氯气的反应),认识钠是一种很活泼的金属。
⏹使学生了解氯气的物理性质和主要的化学性质(氯气跟金属单质、非金属单质及水的反应)。
⏹进一步熟练药品的取用,加热等基础实验操作。
2.过程与方法目标:⏹通过引导学生观察、分析实验现象,让他们体会怎样科学、合理地运用观察方法。
⏹通过对钠跟氧气的反应及氯气性质的实验探究,让学生体会实验方法在化学研究中的作用,并认识到实验过程中控制实验条件的重要性。
⏹在归纳金属钠的性质及预测氯气性质的过程中,让学生体验分类、比较等研究方法在学习和研究物质性质过程中的应用。
3.情感态度与价值观目的:⏹通过对金属钠和氯气性质的探究,激发学生学习化学的兴趣,让他们乐于探究物质变化的奥秘;⏹利用阅读材料《含氯化合物的漂白与消毒作用》培养学生将化学知识与生产、生活实践相结合的意识。
【教学重点、难点】1.知识上重点、难点:金属钠和氯气的化学性质2.方法上重点、难点:使学生初步学会以观察、实验、比较、分类等方法在研究物质性质中的运用,初步掌握研究物质的一般程序。
【教学准备】1.课堂活动记录及报告(详见教学过程)⏹活动1.2.1.1 交流·研讨:⏹活动1.2.1.2 观察·思考:观察金属钠的物理性质及钠与水反应的现象⏹活动1.2.1.3 活动·探究金属钠与氧气反应的实验⏹活动1.2.1.4交流·研讨⏹活动1.2.2.1 研究氯气的性质2.将学生为4-6人小组3.试验试剂和仪器:见课堂活动记录及报告【教学方法】观察、实验探究、对比法【教学过程】〖发放课堂活动记录及报告〗〖引言〗在前面的学习中我们知道,化学科学是在原子、分子水平上研究物质的组成、结构、性质、变化、制备和应用的一门自然科学。
认识物质的性质是化学研究的一项重要任务,且只有深入地研究物质的性质,才能更好地利用物质为人类生产、生活服务。
2020-2021学年高中化学新教材鲁科版必修第1册学案:第1章第2节第1课时研究物质性质的基本方法第2节研究物质性质的方法和程序第1课时研究物质性质的基本方法发展目标体系构建1.通过对金属钠的性质研究等一系列科学探究活动,认识钠是一种非常活泼的金属单质,了解钠的物理性质、主要化学性质.2。
通过观察、分析实验现象,体会怎样科学合理地运用观察方法。
3.通过对钠与氧气反应的实验探究,体会实验方法在化学研究中的作用,并认识实验过程中控制实验条件的重要性。
4.在归纳金属钠的性质过程中,体验分类、比较等研究方法在研究和学习物质性质过程中的重要应用。
5.激发学习的化学兴趣,乐于探究物质变化的奥秘,同时树立安全意识和环保意识。
一、研究物质性质的基本方法研究物质的性质,常常运用观察、实验、分类、比较等方法。
1.观察法(1)含义:观察是一种有计划、有目的地运用感官考察研究对象的方法。
(2)内容观察错误!(3)运用观察法时的注意事项①不能用手直接接触化学药品。
②严禁品尝化学药品的味道.③闻气体气味时要用“扇闻法”.操作如图所示.(4)实施观察的程序错误!―→错误!―→错误!2.实验法(1)含义:通过实验来验证对物质性质的预测或探究物质未知的性质的方法。
(2)注意的问题:在进行实验时,要注意控制温度、压强、溶液的浓度等条件。
(3)实验的步骤3.分类法在研究物质性质时,可以运用分类的方法总结各类物质的一般性质,并根据物质所属的类别对物质及其变化进行预测.4.比较法运用比较的方法,认识各种物质性质之间的异同与内在联系。
二、基本方法的应用——金属钠及性质1.观察法认识钠的物理性质(1)观察目的:认识金属钠的状态、颜色、硬度以及密度的相对大小及熔点的相对高低。
(2)观察内容:试剂瓶中的金属钠及钠块切面。
(3)观察记录:状态颜色光泽硬度密度熔点固体银白色有金属光泽小,可切割比水的小,比煤油的大熔点较低2.实验法、观察法、推理法的应用--金属钠与水的反应实验步骤实验现象现象分析钠浮在水面上钠的密度比水小钠熔化成闪亮的小球钠的熔点低,反应放出热量小球在水面上四处游动,最后完全消失反应产生的气体推动小球运动与水反应发出嘶嘶响声钠与水反应产生气体反应后溶液变为红色反应生成碱性物质实验结论常温下,钠与水剧烈反应,生成NaOH和H2。
1、Na放置在空气中:4Na+O2=2Na2O2、Na在空气中燃烧:2Na+O点燃Na2O23、Na和水反应:2Na+2H2O=2NaOH+H2↑离子方程式2Na+2H2O=2Na++2OH—+H2↑4、过氧化钠(Na2O2)与水反应:2Na2O2 + 2H2O = 4NaOH + O2↑离子方程式2 Na2O2+2H2O=4Na++4OH—+O2↑5、过氧化钠(Na2O2)与二氧化碳反应:2Na2O2 + 2CO2 = 2Na2CO3 + O26、NaHCO3加热:2NaHCO3加热Na2CO3+H2O+CO2↑7、用小苏打治疗胃酸过多:NaHCO3+HCl==NaCl+H2O+CO2↑离子方程式HCO3_—+H+== H2O+CO2↑8、碳酸钠与盐酸反应Na2CO3+2HCl==2NaCl+H2O+CO2↑离子方程式CO3_2—+2H+== H2O+CO2↑认识本质(分步反应过程如下):Na2CO3+ HCl==2NaCl + NaHCO3 NaHCO3+HCl==NaCl+H2O+CO2↑9、氢氧化钠中通入少量的二氧化碳:2NaOH+ CO2= Na2CO3 + H2O10、氢氧化钠中通入过量的二氧化碳:2NaOH+CO2= Na2CO3+H2O 和Na2CO3+H2O+ CO2= 2NaHCO3总反应:NaOH+ CO2= NaHCO3二、知识讲解考点1、钠的性质1.物理性质:银白色金属光泽、质软、可以用刀切割、密度小于水大于煤油、熔沸点低。
2.化学性质:(1)钠与非金属单质反应:2Na +Cl 22NaCl (白烟) 2Na +S Na 2S缓慢氧化:4Na+O 22Na 2O (白色固体) 剧烈燃烧:2Na+O 22O 2(淡黄色固体)(2)钠与水的反应2Na+2H 2O2NaOH+H 2↑ 2Na+2H 2O2Na ++2OH -+H 2↑(3)与酸(主要指非氧化性酸)的反应:钠不足,则反应为:钠与酸直接反应。
第1章认识化学科学第2节研究物质的方法和程序(第一课时)本节是位于鲁科版化学必修第一册第1章第2节第一课时:研究物质性质的基本方法,教材通过探究金属钠的性质让学生体会如何运用研究物质性质的一般方法。
教材介绍了四种方法:观察法、实验法、分类法和比较法。
教材安排观察金属钠及金属钠与水的反应和金属钠与氧气的实验对金属钠性质的研究,掌握金属单质的基本性质,激发他们学习化学的兴趣,让他们乐于探究物质变化的奥秘,培养他们将化学知识与生产、生活实践相结合的意识,为今后将化学知识应用于生产、生活中做好准备。
宏观辨识与微观探析根据金属单质的结构和性质,预测金属钠的性质并进行探究。
科学探究与创新意识1、观察金属钠及金属钠与水反应的现象。
2、探究金属钠和氧气反应的实验。
科学态度与社会责任1、了解一些物质对生活的作用。
2、初步学会研究物质性质的基本方法——观察法、实验法、分类法和比较法。
1、知道钠的保存,了解钠的用途。
2、钠与非金属单质,水、盐溶液等的反应。
3、过氧化钠与二氧化碳和水的反应。
实验药品:金属钠、玻璃片、小刀、滤纸、坩埚、铁三脚、泥三角、酒精灯、硫酸铜、水等多媒体【引入】通过溴化银感光性的研究,制成了感光胶卷。
通过叠氮化钠的性质,制成了汽车安全气囊;通过对燃料性质的研究,制成了火箭推进剂。
【提问】怎样才能更科学地研究物质的性质呢?【设计意图】利用身边常见物质的用途,引起学生极大的学习热情。
让学生知道只有深入了解物质的性质,才能更好的利用物质,提出本节课的教学目的。
【联想·质疑】1、在初中化学的学习中,你认识了哪些物质?你是通过什么方法来研究他们的性质的?观察颜色和状态;观察法将化合物分为酸、碱、盐;分类法化学是以实验为基础的一门自然科学。
实验法【板书】研究物质性质的基本方法【过渡】这节课主要学习观察法,请同学们打开课本第10页,一起朗读第二、三自然段。
从这里我们知道,要想正确使用观察法,首先要明确观察的目的;然后在实验中用眼睛、耳朵、鼻子这些感官来观察,在实验室中仪器观察不常用;并在观察中记录实验现象;最后对观察现象进行分析、思考和综合。