5羧酸及其衍生物取代羧酸胺及其它含氮物
- 格式:doc
- 大小:284.50 KB
- 文档页数:5

RCOOH..第九章 羧酸及其衍生物和取代酸(一COOH )官能团的化合物,一元饱和脂肪羧酸的通式为C n H 2n O 2 。
羧基中的羟基被其它原子或基团取代的产物称为羧酸衍生物(如酰卤、酸酐、酯、酰胺等),羧酸烃基上的氢原子被其他原子或基团取代的产物称为取代酸(如卤代酸、羟基酸、羰基酸、氨基酸等)。
羧酸是许多有机化合物氧化的最终产物,常以盐和酯的形式广泛存在于自然界,许多羧酸在生物体的代谢过程中起着重要作用。
羧酸对于人们的日常生活非常重要,也是重要的化工原料和有机合成中间体。
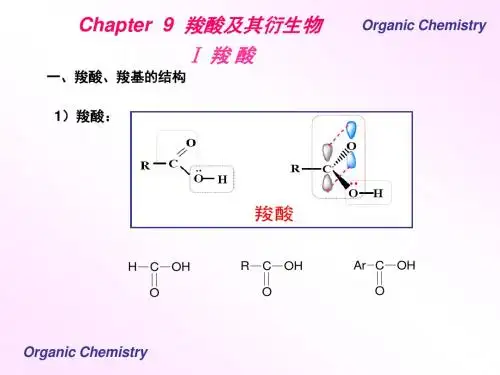
§9-1 羧酸一、羧酸的结构、分类和命名 1、羧酸的结构在羧酸分子中,羧基碳原子是sp 2杂化的,其未参与杂化的p 轨道与一个氧原子的p 轨道形成C=O 中的π键,而羧基中羟基氧原子上的未共用电子对与羧基中的C=O 形成p -π共轭体系,从而使羟基氧原子上的电子向C=O 转移,结果使C=O 和C —O 的键长趋于平均化。
X 光衍射测定结果表明:甲酸分子中C=O 的键长(0.123 nm )比醛、酮分子中C=O 的键长(0.120nm )略长,而C —O 的键长(0.136nm )比醇分子中C —O 的键长(0.143nm )稍短。
RCOOH羧基上的p -π共轭示意图2、羧酸的分类和命名 2.1.羧酸的分类根据分子中烃基的结构,可把羧酸分为脂肪羧酸(饱和脂肪羧酸和不饱和脂肪羧酸)、脂环羧酸(饱和脂环羧酸和不饱和脂环羧酸)、芳香羧酸等;根据分子中羧基的数目,又可把羧酸分为一元羧酸、二元羧酸、多元羧酸等。
例如:或OOCOOcCOOHHOOC HOOC CH 2COOHCH 2COOHCH 2HOOC CH 3CH C H C OOHCOOH HOOC脂肪羧酸 一元羧酸 脂环羧酸 芳香羧酸二元羧酸多元羧酸2.2.羧酸的命名羧酸的命名方法有俗名和系统命名两种。
俗名是根据羧酸的最初来源的命名。
在下面的举例中,括号中的名称即为该羧酸的俗名。

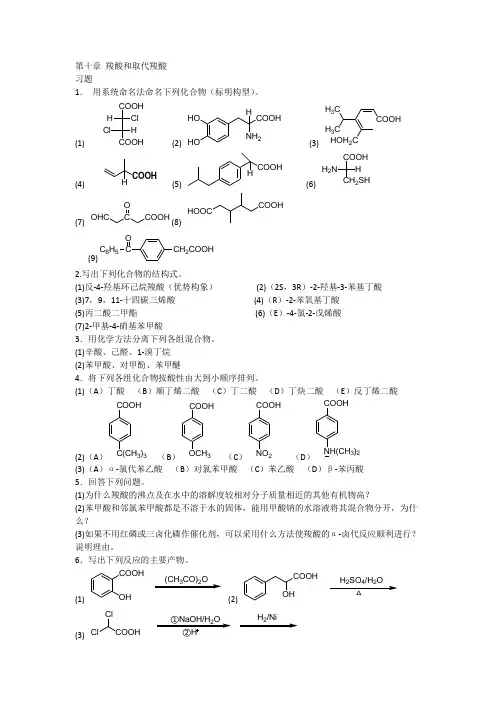
第十章 羧酸和取代羧酸 习题1. 用系统命名法命名下列化合物(标明构型)。
(1)COOHCOOH Cl H HCl (2) HO HO COOHNH 2H(3) COOHHOH 2CH 3CH 3C(4)H(5)COOH H(6)COOHCH 2SH H H 2N (7)OHC C O (8)COOHHOOC(9)CH 2COOHCC 6H 5O2.写出下列化合物的结构式。
(1)反-4-羟基环己烷羧酸(优势构象) (2)(2S ,3R )-2-羟基-3-苯基丁酸 (3)7,9,11-十四碳三烯酸 (4)(R )-2-苯氧基丁酸 (5)丙二酸二甲酯 (6)(E )-4-氯-2-戊烯酸 (7)2-甲基-4-硝基苯甲酸3.用化学方法分离下列各组混合物。
(1)辛酸、己醛、1-溴丁烷 (2)苯甲酸、对甲酚、苯甲醚4.将下列各组化合物按酸性由大到小顺序排列。
(1)(A )丁酸 (B )顺丁烯二酸 (C )丁二酸 (D )丁炔二酸 (E )反丁烯二酸(2)(A )COOH C(CH 3)3 (B )COOHOCH 3 (C )NO 2COOH (D )COOH NH(CH 3)2(3)(A )α-氯代苯乙酸 (B )对氯苯甲酸 (C )苯乙酸 (D )β-苯丙酸 5.回答下列问题。
(1)为什么羧酸的沸点及在水中的溶解度较相对分子质量相近的其他有机物高?(2)苯甲酸和邻氯苯甲酸都是不溶于水的固体,能用甲酸钠的水溶液将其混合物分开,为什么?(3)如果不用红磷或三卤化磷作催化剂,可以采用什么方法使羧酸的α-卤代反应顺利进行?说明理由。
6.写出下列反应的主要产物。
(1)COOHOH(CH 3CO)2O(2)COOHOH△242(3) ClCl2(4)ClC 6H 5NaOH/H 2O△4H(5)COOHOH OH+(6)COOH ONaBH 4(7)COOH①LiAlH 4②H 3O(8)COOH2(9) COOH25H(10) COOHSOCl 27.下列化合物在加热条件下发生什么反应?写出主要产物。


云南大学硕士招生考试916-《制药工艺学》考试大纲(研究生招生考试属于择优选拔性考试,考试大纲及书目仅供参考,考试内容及题型可包括但不仅限于以上范围,主要考察考生分析和解决问题的能力。
)《制药工艺学》专业课程考试大纲适用于云南大学制药工程专业的硕士研究生入学考试,涉及两大部分内容:(1)制药工艺学课程,(2)有机化学课程。
考题总分为150分,其中第一部分制药工艺学课程考试内容约占70分,第二部分有机化学课程考试内容约占80分。
要求学生全面掌握制药工艺学的基本概念、基本原理和基本技能,熟悉代表性产品的工艺研究、工艺过程与控制原理等,具有应用所学知识进行分析和解决工艺过程中存在问题的初步能力。
一、考试的内容(一)制药工艺学部分考试内容:1、绪论制药工艺学研究的对象与内容、化学合成药物的生产特点、GLP、GMP、GSP、GCP、实验室工艺研究过程、中试放大研究过程、我国现阶段制药工业主要发展战略、创新药的概念及研究开发过程、仿制药的概念及研究开发过程、药品注册管理和生产管理法律法规2、药物合成工艺路线的设计与选择工艺路线的概念、工艺路线设计与选择的研究对象、合成路线设计的相关概念、逆合成分析方法、追溯求源法、分子对称法、模拟类推法、药物合成工艺路线的评价标准、药物合成工艺路线的选择、收率的计算3、化学合成药物的工艺研究影响化学反应的因素、工艺研究的基本思路和方法、反应试剂的选择、催化剂的选择、反应溶剂的选择、配料比与反应浓度、加料顺序与投料方法、反应温度、反应压力、搅拌与搅拌方式、反应时间、优化催化反应、反应后处理方法、产物纯化与精制方法、重结晶技术、工艺过程控制的研究内容和方法、利用实验设计优化工艺4、手性药物的制备技术手性药物与生物活性、手性药物的制备技术、影响手性药物生产成本的主要因素、结晶法拆分外消旋混合物、结晶法拆分非对映异构体、对映异构体的动力学拆分、手性合成子与手性辅剂、手性源的组成和应用、不对称合成的定义和发展、不对称合成反应类型。

羧酸及其衍生物的分类结构和物理性质羧酸是一类具有羧基(-COOH)的有机化合物,它是碳链上的一个碳原子与一个羧基团相连形成的化合物。
羧基团由一个碳原子与一个氧原子以及一个氢原子组成。
根据羧基的位置不同,羧酸可以分为两类:取代羧酸和芳香羧酸。
取代羧酸是指羧基连接在碳链上,而芳香羧酸则是指羧基连接在芳香环上。
在取代羧酸中,根据羧基所连接到的碳原子的取代原子(或基团)的不同,可以进一步分为单取代羧酸、二取代羧酸和多取代羧酸。
单取代羧酸是指羧基所连接的碳原子上只有一个取代原子(或基团),如乙酸(CH3COOH)。
二取代羧酸是指羧基所连接的碳原子上有两个取代原子(或基团),如丙酸(CH3CH2COOH)。
多取代羧酸是指羧基所连接的碳原子上有多个取代原子(或基团),如苯甲酸(C6H5COOH)。
芳香羧酸是指羧基连接在芳香环上的羧酸化合物。
芳香羧酸通常以其常见的名称命名,如苯甲酸(C6H5COOH)和苯乙酸(C6H5CH2COOH)等。
羧酸及其衍生物通常具有一些共同的物理性质。
首先,羧酸具有高沸点和高熔点,这是因为羧酸分子之间通过氢键形成二聚体或多聚体结构。
其次,由于羧酸中的羧基是极性官能团,因此羧酸具有很强的溶解性。
它们可以与水中的氢氧根离子形成氢键,也可以通过与有机溶剂(如醇、醚和酯)的酯化反应溶解。
此外,羧酸还具有一定的酸性,可以在水中与碱进行中和反应。
羧酸的反应性与羧基的酸性和碳原子的电子密度有关。
具有更高电子密度的碳原子上的羧基更容易释放负电荷,在水溶液中呈现更强的酸性。
此外,羧基的芳香羧酸比取代羧酸更酸。
总之,羧酸及其衍生物是一类具有羧基的有机化合物。
根据羧基的位置和取代原子的不同,羧酸可以分为取代羧酸和芳香羧酸。
羧酸具有高沸点、高熔点、良好的溶解性和一定的酸性。
这些属性使得羧酸在许多领域都有广泛的应用,如有机合成、染料工业、食品添加剂等。



羧酸及其衍生物羧酸及其衍生物Ⅰ 目的要求羧酸是含有羧基(―COOH)的含氧有机化合物,我们平常所说的有机酸就是指的这类化合物。
所谓羧酸衍生物,包括的化合物种类很多,诸如羧酸盐类、酰卤类、酯类(包括内酯、交酯、聚酯等)、酸酐类、酰胺类(包括酰亚胺、内酰胺)等都是羧酸衍生物,有人甚至把腈类也包括在羧酸衍生物的范围之内。
其实,比较常见的而又比较重要的是酰卤、酸酐、酯和酰胺这四类化合物。
羧酸盐与一般无机酸盐在键价类型上没大区别,不作专门介绍。
至于腈类,将放在含氮化合物中加以介绍。
这四类化合物都是羧酸分子中,因酰基转移而产生的衍生物,所以又叫羧酸的酰基衍生物。
羧酸及其衍生物RCOL(L:-OH、-X、-OOCR′、-OR′、-NH2)在许多重要天然产物的构成以及在生物代谢过程中均占有重要地位。
本章将以饱和一元脂肪酸为重点,讨论羧酸及其衍生物的结构和性质。
鉴于乙酰乙酸乙酯和丙二酸二乙酯在有机合成上的重要地位,本章作概括介绍。
希望学生在此基础上,探讨设计合成路线的一般方法。
本章学习的具体要求1、掌握羧酸的结构与性质之间的关系。
2、掌握羧酸衍生物的主要化学性质。
3、了解羧酸衍生物的亲核取代反应机理。
4、掌握羧酸与羧酸衍生物之间相互转变条件。
5、了解卤代酸、羟基酸的特性。
6、掌握乙酰乙酸乙酯和丙二酸二乙酯的制法、性质和在有机合成上的应用。
这也是本章的重点之一。
Ⅱ 学习提要(一)羧酸一、概述羧酸往往有俗名,希望学生有所了解,尽可能记忆一些,脂肪酸的系统命名原则和醛相β α同。
γCH3-CH-CH2-COOH2 14 3 OH 芳香酸命名是把芳环视作取代基。
76羧酸的沸点比分子量相近的其它有机物高,这是由于羧酸能以氢键缔合。
同时,即使在气态时,羧酸也是双分子缔合的,所以羧酸的沸点比分子量相近的醇还要高。
二、羧酸结构和化学性质亲核取代O 还原R-C-C-O-H α-H反应H 脱羧酸性1、酸性?E O O O +?R-C H + R-C R-C E EO-H O OO O NaOH/Na2CO3/ NaHCO3H2O + R-C E R-C EH+ O-Na O-H应用:①鉴别:与酚不同,与非酸性物质不同。

羧酸及其衍生物学习指南羧酸是分子中含有羧基的有机化合物。
羧基是由羰基和羟基组成的官能团,羧酸的化学反应主要发生在羧基及受羰基影响的—氢原子上。
羧酸分子中的羟基被其他原子或基团取代后生成羧酸衍生物。
它们都是含有酰基的化合物,由于结构相似,所以具有许多相似的化学性质。
本章重点介绍羧酸及其衍生物的特征反应、官能团间的相互转化规律及其在实际中的应用。
学习本章内容应在了解羧酸及其衍生物结构特点的基础上做到: 1.了解羧酸的分类,掌握羧酸及其衍生物的命名方法;2.了解羧酸及其衍生物的物理性质和变化规律,熟悉重要羧酸及其衍生物的化学反应及应用;3.掌握羧酸及其衍生物官能团的特征反应及鉴别方法.掌握羧酸及其衍生物间的相互转化关系;4.熟悉重要羧酸及其衍生物的工业制法以及在生产、生活中的实际应用。
任务1 羧酸一、羧酸的结构、分类和命名1. 羧酸的结构由羰基和羟基组成的基团叫做羧基。
羧基的构造式为(),(也可简写为)羧酸就是分子中含有羧基的一类有机化合物,常用通式()来表示。
在羧基中,由于羰基和羟基互相影响,使它们不同于醛酮分子中的羰和醇分子中的羟基,而表现出一些特殊的性质。
2.羧酸的分类根据分子中烃基的结构不同可将羧酸分为脂肪族羧酸、脂环族羧酸和芳香族羧酸;根据烃基是否饱和,又可分为饱和羧酸和不饱和羧酸;还可以根据分子中所含羧基数目分为一元羧酸、二元羧酸和三元羧酸等,二元及二元以上的羧酸统称为多元羧酸。
例如:异丁酸丙烯酸丙二酸(脂肪族饱和一元羧酸) (脂肪族不饱和一元羧酸) (脂肪族饱和二元羧酸)环己基甲酸 苯甲酸 对苯二甲酸 (脂环族一元羧酸) (芳香族一元羧酸) (芳香族二元羧酸) 3.羧酸的命名 (1)俗名羧酸广泛存在于自然界中,而且早已被人们所认识,因此,许多羧酸有俗名,这些俗名一般是α C OH OCOOH RCOOH CH 3HOOCCH 2COOHCH 3 CH COOHCH 2 CH COOH COOH COOHCOOHHOOC根据他们最初来源命名的。
大学化学实验-(取代)羧酸及其衍生物、胺的性质大学化学实验-(取代)羧酸及其衍生物、胺的性质实验二十五(取代)羧酸及其衍生物、胺的性质【实验目的】1. 熟悉羧酸、羧酸衍生物和取代羧酸的化学性质;2. 掌握胺类化合物的性质及其鉴别方法;3. 了解酰化反应和缩二脲反应的应用。
【实验原理】羧酸一般为弱酸性(但酸性比碳酸强)。
羧酸能发生脱羧反应,而且不同各种羧酸的脱羧的条件各有不同,如草酸、丙二酸经加热即易脱羧,放出CO2;羧酸与醇在酸的催化下,加热可以发生酯化反应。
甲酸含有醛基,故能还原托伦试剂。
羧酸除能生成酯外,也能生成酰卤、酸酐和酰胺(四者统称为羧酸衍生物)。
它们的化学性质相似,能发生水解机、醇解和氨解。
活泼顺序为:酰卤酸酐酯酰胺。
取代羧酸中重要的有羟基酸和酮酸。
羟基酸中的羟基比醇分子中的羟基易被氧化,如乳酸能被托伦试剂氧化成丙酮酸;,在碱性高锰酸钾溶液中,则因高锰酸钾被乳酸还原而使紫色褪去。
乙酰乙酸乙酯是酮型和烯醇型两种互变异构体的平衡混合物,这两种异构体借分子中氢原子的移位而互变转换,所以它既具有酮的性质(如与2,4-二硝基苯肼反应生成2,4-二硝基苯腙),又具有烯醇的性质(如能使溴水褪色并能与FeCl3溶液作用呈现紫色)。
胺可以看做是氨分子中的氢原子被羟基取代的衍生物。
胺类化合物有碱性,能与酸反应生成盐。
芳香胺由于氨基的存在使苯环活化,易发生取代反应。
在酰化反应中,伯胺和仲胺由于氮上有氢原子可被酰基取代,生成相应的酰胺类化合物,叔氨氮上无氢原子则无此反应。
大多数酰胺为结晶固体,故可利用酰化反应鉴别胺类化合物。
胺类容易被氧化,氧化产物往往很复杂。
将尿素缓慢加热至熔点以上,则二分子尿素可脱去一分子氨生成缩二脲。
缩二脲在碱性溶液中与稀的硫酸铜溶液反应能产生紫红色,这种反应叫做缩二脲反应。
【仪器材料】小试管10支,烧杯(100 mL)2个,玻璃棒1根,小橡皮塞1个,酒精灯1个,温度计1个,石棉网1个,铁架台1个,铁圈1个,铁夹1个,大试管1个,带孔橡皮塞1个,导管1个,药匙1个。
羧酸及其衍生物第一节羧酸由烃基(或氢原子)与羧基相连所组成的化合物称为羧酸,其通式为RCOOH,羧基(-COOH)是羧酸的官能团.一,分类和命名按羧酸分子中烃基的种类将羧酸分为脂肪族羧酸和芳香族羧酸.按羧酸分子中所含的羧基数目不同将羧酸分为一元酸和多元酸.一些常见的羧酸多用俗名,这是根据它们的来源命名的.如:HCOOH 蚁酸CH3COOH 醋酸HOOC—COOH 草酸脂肪族羧酸的系统命名原则与醛相同,即选择含有羧基的最长的碳链作主链,从羧基中的碳原子开始给主链上的碳原子编号.取代基的位次用阿拉伯数字表明.有时也用希腊字母来表示取代基的位次,从与羧基相邻的碳原子开始,依次为α,β,γ等.例如:CH3CH═CHCOOH2-丁烯酸2,3-二甲基戊酸α-丁烯酸(巴豆酸)芳香族羧酸和脂环族羧酸,可把芳环和脂环作为取代基来命名.例如:对甲基环已基乙酸3-苯丙烯酸(肉桂酸) 4-甲基-3-(2-萘)丙酸命名脂肪族二元羧酸时,则应选择包含两个羧基的最长碳链作主链,叫某二酸.如:邻-苯二甲酸正丙基丙二酸二,羧酸的制法1,氧化法高级脂肪烃(如石蜡)在加热至120℃-150℃和催化剂存在的条件下通入空气,可被氧化生成多种脂肪酸的混合物.RCH2CH2R1 RCOOH + R1COOH伯醇氧化成醛,醛易氧化成羧酸,因此伯醇可作为氧化法制羧酸的原料.含α-氢的烷基苯用高锰酸钾氧化时,产物均为苯甲酸.例如:2,格氏试剂合成法格氏试剂与二氧化碳反应,再将产物用酸水解可制得相应的羧酸.例如:RMgX + CO2 RCOOMgX RCOOH腈水解法在酸或碱的催化下,腈水解可制得羧酸.RCN + H2O + HCl RCOOH + NH4ClRCN + H2O + NaOH RCOONa + NH3三,物理性质1,状态甲酸,乙酸,丙酸是具有刺激性气味的液体,含4-9个碳原子的羧酸是有腐败恶臭气味的油状液体,含10个碳原子以上的羧酸为无味石蜡状固体.脂肪族二元酸和芳香酸都是结晶形固体.2,沸点羧酸的沸点比分子量相近的醇还高.这是由于羧酸分子间可以形成两个氢键而缔合成较稳定的二聚体.3,水溶性羧酸分子可与水形成氢键,所以低级羧酸能与水混溶,随着分子量的增加,非极性的烃基愈来愈大,使羧酸的溶解度逐渐减小,6个碳原子以上的羧酸则难溶于水而易溶于有机溶剂.化学性质1,酸性羧酸具有酸性,因为羧基能离解出氢离子.RCOOH RCOO- + H+因此,羧酸能与氢氧化钠反应生成羧酸盐和水.RCOOH + NaOH RCOONa + H2O羧酸的酸性比苯酚和碳酸的酸性强,因此羧酸能与碳酸钠,碳酸氢钠反应生成羧酸盐.RCOOH + NaHCO3(Na2CO3) RCOONa + H2O + CO2↑但羧酸的酸性比无机酸弱,所以在羧酸盐中加入无机酸时,羧酸又游离出来.利用这一性质,不仅可以鉴别羧酸和苯酚,还可以用来分离提纯有关化合物.例如:欲鉴别苯甲酸,苯甲醇和对-甲苯酚,可按如下步骤进行,在这三者中加入碳酸氢钠溶液,能溶解并有气体产生的是苯甲酸;再在剩下的二个中加入氢氧化钠溶液,溶解的是对-甲苯酚,不溶解的是苯甲醇.当羧酸的烃基上(特别是α-碳原子上)连有电负性大的基团时,由于它们的吸电子诱导效应,使氢氧间电子云偏向氧原子,氢氧键的极性增强,促进解离,使酸性增大.基团的电负性愈大,取代基的数目愈多,距羧基的位置愈近,吸电子诱导效应愈强,则使羧酸的酸性更强.如:三氯乙酸二氯乙酸氯乙酸pKa 0.028 1.29 2.81因此,低级的二元酸的酸性比饱和一元酸强,特别是乙二酸,它是由两个电负性大的羧基直接相连而成的,由于两个羧基的相互影响,使酸性显著增强,乙二酸的pKa1=1.46,其酸性比磷酸的pKa1=1.59还强.取代基对芳香酸酸性的影响也有同样的规律.当羧基的对位连有硝基,卤素原子等吸电子基时,酸性增强;而对位连有甲基,甲氧基等斥电子基时,则酸性减弱.至于邻位取代基的影响,因受位阻影响比较复杂,间位取代基的影响不能在共轭体系内传递,影响较小.对硝基苯甲酸对氯苯甲酸对甲氧基苯甲酸对甲基苯甲酸pKa 3.42 3.97 4.47 4.382,羧基中的羟基被取代羧酸分子中羧基上的羟基可以被卤素原子(-X),酰氧基(-OOCR),烷氧基(-OR),氨基(-NH2)取代,生成一系列的羧酸衍生物.①酰卤的生成羧酸与三氯化磷,五氯化磷,氯化亚砜等作用,生成酰氯.RCOOH + PCl3(PCl5 SOCl2) RCOCl②酸酐的生成在脱水剂的作用下,羧酸加热脱水,生成酸酐.常用的脱水剂有五氧化二磷等.RCOOH + RCOOH RCOOOCR③酯化反应羧酸与醇在酸的催化作用下生成酯的反应,称为酯化反应.酯化反应是可逆反应,为了提高酯的产率,可增加某种反应物的浓度,或及时蒸出反应生成的酯或水,使平衡向生成物方向移动.RCOOH + R1OH RCOOR1 + H2O酯化反应可按两种方式进行:RCOOH + HOR1 RCOOR1 + H2O (1)RCOOH + HOR1 RCOOR1 + H2O (2)实验证明,大多数情况下,酯化反应是按(1)的方式进行的.如用含有示踪原子18O的甲醇与苯甲酸反应,结果发现18O在生成的酯中.④酰胺的生成在羧酸中通入氨气或加入碳酸铵,首先生成羧酸的铵盐,铵盐胺热脱水生成酰胺.RCOOH + NH3 RCOONH4 RCONH23,α-氢被取代羧基和羰基一样,能使α-H活化.但羧基的致活作用比羰基小,所以羧酸的α-H卤代反应需用在红磷等催化剂存在下才能顺利进行.CH3COOH + Cl2 CH2ClCOOH CHCl2COOH CCl3COOH还原反应羧酸在一般情况下,和大多数还原剂不反应,但能被强还原剂—氢化锂铝还原成醇.用氢化铝锂还原羧酸时,不但产率高,而且分子中的碳碳不饱和键不受影响,只还原羧基而生成不饱和醇.例如: RCH2CH═CHCOOH RCH2CH═CHCH2OH5,脱羧反应羧酸分子脱去羧基放出二氧化碳的反应叫脱羧反应.例如,低级羧酸的钠盐及芳香族羧酸的钠盐在碱石灰(NaOH-CaO)存在下加热,可脱羧生成烃.CH3COONa CH4 + Na2CO3这是实验室用来制取纯甲烷的方法.一元羧酸的脱羧反应比较困难,把羧酸盐蒸气通过加热至400-500℃的钍,锰或镁的氧化物,则脱羧生成酮.2CH3COOH CH3COCH3 + CO2 + H2O当一元羧酸的α-碳上连有吸电子基时,脱羧较容易进行,如:CCl3COOH CHCl3 + CO2↑五,重要的羧酸1,甲酸俗称蚁酸,是具有刺激性气味的无色液体,有腐蚀性,可溶于水,乙醇和甘油.甲酸的结构比较特殊,分子中羧基和氢原子直接相连,它既有羧基结构,又具有醛基结构,因此,它既有羧酸的性质,又具有醛类的性质.如能与托伦试剂,斐林试剂发生银境反应和生成砖红色的沉淀,也能被高锰酸钾氧化.2,乙酸俗称醋酸,是食醋的主要成分,一般食醋中含乙酸6℅-8℅.乙酸为无色具有刺激性气味的液体.当室温低于16.6℃时,无水乙酸很容易凝结成冰状固体,故常把无水乙酸称为冰醋酸.乙酸能与水按任何比例混溶,也可溶于乙醇,乙醚和其它有机溶剂.3,苯甲酸俗名安息香酸,是无色晶体,微溶于水.苯甲酸钠常用作食品的防腐剂.4,乙二酸俗称草酸,是无色晶体,通常含有两分子的结晶水,可溶于水和乙醇,不溶于乙醚.草酸具有还原性,容易被高锰酸钾溶液氧化.利用草酸的还原性,还可将其用作漂白剂和除锈剂.5,已二酸为白色电晶体,溶于乙醇,微溶于水和乙醚.已二酸和已二胺发生聚合反应,生成聚酰胺(尼龙-66).羧酸衍生物一,分类和命名重要的羧酸衍生物有酰卤,酸酐,酯和酰胺.1,酰卤和酰胺酰卤和酰胺的命名由酰基名称加卤素原子或胺.酰基:羧酸分子从形式上去掉一个氢原子以后所乘余的部分.某酸所形成的酰基叫某酰基.例如:某酰基乙酰氯乙酰胺N-甲基乙酰胺2,酸酐某酸所形成的酸酐叫\"某酸酐\".如:乙酐(醋酐) 乙丙酐丁二酸酐邻-苯二甲酸酐酯酯的命名为\"某酸某酯\".如:CH3CH2COOCH3 丙酸甲酯(CH3)2C═CHCH2COOCH2CH3 4-甲基-3-戊烯酸乙酯苯甲酸甲酯苯甲酸苄酯HOOC—COOCH2CH3 乙二酸氢乙酯CH3CH2OOC—CH2—COOCH2CH3 丙二酸二乙酯二,物理性质酰氯大多数是具有强烈刺激性气味的无色液体或低熔点固体.低级酸酐是具有刺激性气味的无色液体,高级酸酐为无色无味的固体.酸酐难溶于水而溶于有机溶剂.低级酯是具有水果香味的无色液体.酯的相对密度比水小,难溶于水而易溶于乙醇和乙醚等有机溶剂.三,化学性质1,水解四种羧酸衍生物化学性质相似,主要表现在它们都能水解,生成相应的羧酸.RCOCl HClRCOOOCR1 R1COOHRCOOR1 + H2O RCOOH + R1OHRCONH2 NH3水解反应进行的难易次序为:酰氯> 酸酐> 酯> 酰胺例如,乙酰氯与水发生猛烈的放热反应;乙酐易与热水反应;酯的水解在没有催化剂存在时进行得很慢;而酰胺的水解常常要在酸或碱的催化下,经长时间的回流才以完成.2,醇解和氨解酰氯,酸酐和酯都能与醇作用生成酯.RCOCl HClRCOOOR1 + HOR2 RCOOR2 + R1COOHRCOOR1 R1OH酰氯,酸酐和酯都能与氨作用,生成酰胺.RCOCl HClRCOOOR1 + NH3 RCONH2 + R1COOHRCOOR1 R1OH四,重要的羧酸衍生物1,乙酰氯:是一种在空气中发烟的无色液体,有窒息性的刺鼻气味.能与乙醚,氯仿,冰醋酸,苯和汽油混溶.2,乙酐:又名醋(酸)酐,为无色有极强醋酸气味的液体,溶于乙醚,苯和氯仿.3,顺丁烯二酸酐:又称马来酸酐和失水苹果酸酐.为无色结晶性粉末,有强烈的刺激性气味,易升华,溶于乙醇,乙醚和丙酮,难溶于石油醚和四氯化碳.4,乙酸乙酯:为无色可燃性的液体,有水果香味,微溶于水,溶于乙醇,乙醚和氯仿等有机溶剂.5,甲基丙烯酸甲酯:为无色液体,其在引发剂存在下,聚合成无色透明的化合物,俗称有机玻璃.6,丙二酸二乙酯及其在有机合成中的应用:丙二酸二乙酯,简称丙二酸酯,为无色有香味的液体,微溶于水,易溶于乙醇,乙醚等有机溶剂.常用下面的方法来制取丙二酸酯:CH2ClCOONa CH2CNCOONa + C2H5OH C2H5OOCCH2COOC2H5由于丙二酸酯分子中亚甲基上的氢原子受相邻两个酯基的影响,比较活泼,其能在乙醇化钠的催化下与卤代烃或酰氯反应,生成一元取代丙二酸酯和二元取代丙二酸酯.烃基或酰基取代两二酸酯经碱性水解,酸化和脱羧后,可制得相应的羧酸.这是合成各种类型羧酸的重要方法,称为丙二酯酯合成法.取代羧酸羧酸分子中烃基上的氢原子被其它原子或原子团取代后生成的化合物称为取代羧酸.常见的取代羧酸有卤代酸,羟基酸,羰基酸(氧代酸)和氨基酸等.第一节羟基酸一,分类和命名羟基酸可以分为醇酸和酚酸两类.羟基酸的命名是以相应的羧酸作为母体,把羟基作为取代基来命名的.自然界存在的羟基酸常按其来源而采用俗名.如:CH3CHOHCOOH 2-羟基丙酸(乳酸)HOOCCH2CHOHCOOH 羟基丁二酸(苹果酸)HOOCCHOHCHOHCOOH 2,3-二羟基丁二酸(洒石酸)2-羟基苯甲酸(水杨酸)3,4,5-三羟基苯甲酸(没食子酸)二,醇酸的性质1,物理性质醇酸一般为结晶的固体或粘稠的液体.由于羟基和羧基都以且慢水形成氢键,所以醇酸在水中的溶解度比相应的醇或羧酸都大,低级的醇酸可与水混溶.2,化学性质醇酸既具有醇和羧酸的一般性质,如醇羟基可以氧化,酰化,酯化;羧基可以成盐,成酯等,又由于羟基和羧基的相互影响,而具有一些特殊的性质.(1)酸性在醇酸分子中,由于羟基的吸电子诱导效应沿着碳链传递到羧基上,而降低了羧基碳的电子云密度,使羧基中氧氢键的电子云偏向于氧原子,促进了氢原子解离成质子.由于诱导效应随传递距离的增长而减弱,因此醇酸的酸性随着羟基与羧基距离的增加而减弱.如:CH3CHOHCOOH OHCH2CH2COOH CH3CH2COOHpKa 3.87 4.51 4.882,α-醇酸的分解反应由于羟基和羧基都有吸电子诱导效应,使羧基与α-碳原子之间的电子云密度降低,有利于二者之间键的断裂,所以当α-醇酸与稀硫酸共热时,分解成比原来少一个碳原子的醛或酮和甲酸.RCHOHCOH RCHO + HCOOH此反应常用于由高级羧酸经α-溴代酸制备少一个碳原子的高级醛.RCH2COOH RCHBrCOOH RCHOHCOOH RCHO + HCOOH3,脱水反应脱水产物因羟基与羧基的相对位置不同而有所区别.①α-醇酸生成交酯:α-醇酸受热时,一分子α-醇酸的羟基与另一分子α-醇酸的羟基相互脱水,生成六元环的交酯.RCHOHCOOH + RCHOHCOOH 交酯②β-醇酸生成α,β-不饱和羧酸:β-醇酸中的α-氢原子同时受到羟基和羧基的影响,比较活泼,受热时容易与β-碳原子上的羟基结合,发生分子内脱水生成α,β-不饱和羧酸.RCHOHCH2COOH RCH═CHCOOH + H2O③γ-和δ-醇酸生成物内酯:γ-和δ-醇酸在室温时分子内的羟基和羧基就自动脱去一分子水,生成稳定的γ-和δ-内酯.④羟基与羧基相隔5个或5个以上碳原子的醇酸受热,发生多分子间的脱水,生成链状的聚酯.三,酚酸的性质(1)物理性质酚酸大多数为晶体,有的微溶于水(如水杨酸),有的易溶于水(如没食子酸).(2)化学性质羟基处于邻或对位的酚酸,对热不稳定,当加热至熔点以上时,则脱去羧基生成相应的酚.+ CO2↑+ CO2↑四,重要的羟基酸1,乳酸:为无色粘稠液体,有很强的吸湿性和酸味,溶于水,乙醇,甘油和乙醚,不溶于氯仿和油脂.2,β-羟基丁酸:是吸湿性很强的无色晶体,一般为糖浆状粘稠液体,易溶于水,乙醇及乙醚,不溶于苯.3,苹果酸:为针状结晶,易溶于水和乙醇,微溶于乙醚.苹果酸在酶的催化下生成草酰乙酸.苹果酸在食品工业中用作酸味剂.4,洒石酸:是透明棱形晶体,有很强的酸味,易溶于水.洒石酸常用于配制饮料,洒石酸钾钠用于配制斐林试剂.5,柠檬酸:为无色结晶,含一分子结晶水,易溶于水,乙醇和乙醚,有强酸味.柠檬酸常用于配制清凉饮料和作糖果的调味剂,也是制药工业的重要原料.6,水杨酸:为无色针状结晶,微溶于冷水,易溶于乙醇,乙醚和热水.它具有酚和羧酸的一般性质,如易被氧化,遇三氯化铁显紫红色,酸性比苯甲酸强等.7,乙酰水杨酸:俗称\"阿司匹林\",为白色针状晶体.它可用水杨酸和乙酐在少量浓硫酸存在下制得.乙酰水杨酸具有解热镇痛作用,是常用的解热镇痛药.乙酰水杨酸分子中中无游离的酚羟基,故其纯品与三氯化铁不显色,但在潮湿的空气中,其易水解为水杨酸和乙酸,因此应密闭于干燥处贮存.8,没食子酸:又称五倍子酸.纯粹的没食子酸为白色结晶性粉末,能溶于水,乙醇和乙醚.没食子酸有较强还原性,极易被氧化,露置在空气中能迅速氧化呈暗褐色,可用作抗氧剂的影像显影剂.没食子酸与三氯化铁产生蓝黑色沉淀,可用来制造墨水.第二节羰基酸一,分类和命名分子中既含有羰基又含有羧基的化合物称为羰基酸.根据所含的是醛基还是酮基,将其分为醛酸和酮酸.羰基酸的命名与醇酸相似,也是以羧酸为母体,羰基的位次用阿拉伯数字或用希腊字母表示.如:OHC—COOH CH3COCOOH CH3COCH2COOH乙醛酸丙酮酸3-丁酮酸(β-丁酮酸)二,化学性质酮酸具有酮和羧酸的一般性质,如与氢或亚硫酸氢钠加成,与羟胺生成肟,成盐和酰化等.由于两种官能团的相互影响,α-酮酸和β-酮酸又有一些特殊的性质.(一)α-酮酸的性质1,脱羧和脱羰反应在α-酮酸分子中,羰基与羧基直接相连,由于羰基和羧基的氧原子都具有较强的吸电子能力,使羰基碳与羧基碳原子之间的电子云密度降低,所以碳碳键容易断裂,在一定条件下可发生脱羧和脱羰反应.α-酮酸与稀硫酸或浓硫酸共热,分别发生脱羧和脱羰反应生成醛或羧酸.RCOCOOH + 稀H2SO4 RCHO + CO2↑RCOCOOH + 浓H2SO4 RCOOH + CO↑2,氧化反应α-酮酸很容易被氧化,托伦试剂就能其氧化成羧酸和二氧化碳.RCOCOOH + *Ag(NH3)2++ RCOONH4 + Ag↓(二)β-酮酸的性质在β-酮酸分子中,由于羰基和羧基的吸电子诱导效应的影响,使α-位的亚甲基碳原子电子云密度降低.因此亚甲基与相邻两个碳原子间的键容易断裂,在不同的反应条件下,能发生酮式和酸式分解反应.1,酮式分解β-酮酸在高于室温的情况下,即脱去羧基生成酮.称为酮式分解.RCOCH2COOH RCOCH3 + CO2↑2,酸式分解β-酮酸与浓碱共热时,α-和β-碳原子间的键发生断裂,生成两分子羧酸盐.称为酸式分解.RCOCH2COOH + 40℅NaOH RCOONa + CH3COONa三,乙酰乙酸乙酯及酮式-烯醇式互变异构现象1,乙酰乙酸乙酯的制备在醇钠的催化作用下,两分子乙酸乙酯脱去一分子乙醇生成乙酰乙酸乙酯,此反应称为克莱森酯缩合反应.2CH3COOC2H5 CH3COCH2COOC2H5 + C2H5OH2,酮式-烯醇式互变异构现象乙酰乙酸乙酯能与羰基试剂如羟按,苯肼反应生成肟,苯腙等,能与氢氰酸,亚硫酸氢钠等发生加成反应.由此,证明它具有酮的结构.另外,乙酰乙酸乙酯还能与金属钠作用放出氢气,能使溴的四氯化碳溶液褪色,与三氯化铁作用产生紫红色.由此,又证明它也具有烯醇式的结构.这种现象的产生是因为乙酰乙酸乙酯室温下通常是由酮式和烯醇式两种异构体共同组成的混合物,它们之间在不断地相互转变,并以一定比例呈动态平衡.像这样两种异构体之间所发生的一种可逆异构化现象,叫做互变异构现象.乙酰乙酸乙酯分子中烯醇式异构体存在的比例较一般羰基化合物要高的原因,是由于其分子中的亚甲基氢受羰基和酯基的吸电子诱导效应的影响酸性较强,容易以质子形式解离.形成的碳负离子与羰基和酯基共轭,发生电子离域而比较稳定.当H+与羰基氧结合时,就形成烯醇式异构体.此外,还由于烯醇式异构体能形成六元环的分子内氢键,以及其分子中共轭体系的存在,更加强了它稳定性. 3,分解反应(1)酮式分解乙酰乙酸乙酯在稀碱溶液中加热,可发生水解反应,经酸化后,生成β-丁酮酸.β-丁酮酸不稳定,失去二氧化碳生成丙酮.(2)酸式分解乙酰乙酸乙酯与浓碱共热时,生成两分子乙酸盐,经酸化后得到两分子乙酸.4,在合成上的应用乙酰乙酸乙酯亚甲基上的氢原子很活泼,与醇钠等强碱作用时,生成乙酰乙酸乙酯的钠盐,再与活泼的卤烃或酰卤作用,生成乙酰乙酸乙酯的一烃基,二烃基或酰基衍生物.+ RCOX乙酰乙酸乙酯的钠盐还可与卤代酸酯,卤代丙酮等反应,引入相应的酯基和羰基.乙酰乙酸乙酯的一烃基,二烃基或酰基衍生物,再进行酮式分解或酸式分解反应,可以制取甲基酮,二酮,一元羧酸,二元羧酸,酮酸等化合物.四,重要的羰基酸1,乙醛酸:为无色糖浆状液体,易溶于水.2,丙酮酸:为无色有刺激性气味的液体,可与水混溶,酸性比丙酮和乳酸都强.3,β-丁酮酸:又称乙酰乙酸,是无色粘稠液体,酸性比丁酸和β-羟基丁酸强,可与水或乙醇混溶.临床上把β-丁酮酸,β-羟基丁酸和丙酮三者总称为酮体.酮体是脂肪酸在人体内不能完全氧化成二氧化碳和水的中间产物,大量存在于糖化酶尿病患者的血液和尿中,使血液的酸度增加,发生酸中毒,严重时引起患者昏迷或死亡.4,α-酮丁二酸:又称草酰乙酸,为晶体,能溶于水,在水溶液中产生互变异构,生成α-羟基丁烯二酸,其水溶液与三氯化铁反应显红色.α-酮丁二酸具有二元羧酸和酮的一般反应.如能成盐,成酯,成酰胺,与2,4-二硝基苯肼作用生成2,4-二硝基苯腙等.立体化学基础按结构不同,同分异构现象分为两大类.一类是由于分子中原子或原子团的连接次序不同而产生的异构,称为构造异构.构造异构包括碳链异构,官能团异构,位置异构及互变异构等.另一类是由于分子中原子或原子团在空间的排列位置不同而引起的异构,称为立体异构.立体异构包括顺反异构,对映异构和构象异构.。
第13章 羧酸及其衍生物和取代羧酸一、学习基本要求·掌握羧酸及其衍生物、取代羧酸的分类和命名。
·了解羧酸及其衍生物的结构特点,熟悉结构对羧酸及其衍生物的物理性质影响;掌握羧酸及其衍生物的化学性质。
·了解取代酸的结构特点,熟悉取代酸化学性质。
二、重点和难点·重点:羧酸及其衍生物的重要性质,如酯缩合反应、Hoffmann 降解反应等。
·难点:结构对羧酸及其衍生物性质的影响,以及各类羧酸酸性强弱的比较。
13.1 羧酸(一)基本概念1.羧酸:羧基与烃基或氢原子连接而成的化合物叫做羧酸。
2. 酰基:羧酸分子中去掉羟基留下的部分称为酰基,羧酸中羧基去掉氢留下的部分称为酰氧基,羧酸电离出氢离子留下的部分称为羧酸根。
(二)基本知识1、羧酸的结构羧基是羧酸的官能团,一元羧酸的通式为R -COOH 。
羧基中的碳原子是sp 2杂化,羧基中羟基氧原子上的未共用电子对与羰基的π键形成 p-π共轭体系。
羧基不是羰基和羟基的简单加合,所以羧基中不存在典型的羰基和羟基的性质,而是两者互相影响的统一体。
羧酸分子间可以形成氢键,缔合成较稳定的二聚体和多聚体,羧酸的沸点比分子量相近的醇还高。
2、羧酸的命名羧酸的系统命名与醛的命名相似,选择包括羧基碳原子在内的最长碳链为主链,根据主链碳原子数目称为某酸,由羧基碳原子开始给主链编号,或用希腊字母α、β等从与羧基相邻碳原子开始编号。
二元脂肪酸的命名,主链两端必须是羧基。
许多羧酸都根据其来源或生理功能有俗名。
3.羧酸化学性质 (1)羧酸的酸性羧基p-π共轭体系的存在,使羟基氧原子的电子云密度降低,增强了O -H 键的极性,有利于离解H +;而酸根的p-π共轭更为显著,实验证明在酸根离子中2个C -O 键长是完全相等的,这说明羧基碳与2个氧间的电子密度是完全平均化的,其负电荷分散在两个氧与一个碳上,故酸根负离子比较稳定,易生成。
因此羧酸的酸性比水和醇要强得多。
有机化学综合练习五
一、命名或写出结构式 1、己二胺 2、二乙胺
3、DMF
4、硬脂酸
5、
C O O H
O
C C H 3
O
6、3-羟基-3-羧基戊二酸
7、
O
C C H 2C O O H
C H 3
8、N,N-二甲基苯胺 9、邻苯二甲酰亚胺 10、联苯胺
二、根据题意回答
1、比较下列物质的水解速率顺序( )
A.O
CH 3 C
O CH 3
O
C Cl
O
C NH 2
B. CH 3
C. CH
3CH
3
C
O 2O
D.
2、比较酸性次序( )
A. C 2H 5OH
B.CH 2CO O H Cl
C. CH 3COO H
D. F CH 2CO OH
3、比较下列化合物的碱性顺序( )
C H 3NH
C H 3
B. N H 3
C. C H 3O
C N H 2
D.
N H 2
A.
4、下列化合物中烯醇式含量最高的是( )
C C H 2 C O OC 2H 5
O
C C H 2O
C C H 3
O
C 2H 5C
O
C O C C 2H 5H 2
A. C H 3
B. C H 3
C.
5、下列化合物中最难还原的是( ) A. 酮 B. 羧酸 C. 酯
6、下列人名反应是( )
C
O
R R
+
R
Cl
CO OE t
N aO Et
C
C
R R
CO O Et H
A. Knovengel 反应
B. Perkin 反应
C. Darzen 反应
D. Wolff 反应 7、下列化合物中可用于制备重氮盐的是( ) A. α-萘胺 B. 苯肼 C. N-甲基苯胺 D. 苯甲醛腙 8、下列化合物加热既脱水又脱羧的是( ) A. 丙二酸 B. 丁二酸 C. 己二酸 D. 癸二酸
9、比较下列化合物与苯甲酸酯化时的难易顺序( ) A. 正丁醇 B. 异丁醇 C. 仲丁醇
10、α-羟基酸OH
CHCO OH CH 3在稀H 2SO 4中加热主产物是( )
A.CH 2
CH
COOH
B. CH 3CHO + HCOOH
C. CH 3COOH + HCOOH
三、用化学方法鉴别下列各物物质
1.
C CH 3
O CO O Et
B
A
2.
NH 2
N HCH 3
B A N
C
CH 3CH 3
3.CO OH
COO H B
A O H
四、完成下列反应
1.
O 1) H N O 3
25+
N aO C 2H
5
2.
1) 2C 2H
5M gB r
2
3. C H 31) N aO C 2H 525C C H 2C
OO C 2H 5
O
-4.
1) K O H 2-N H O
O
5. CH 3COO H Br 2大量N H 3
6. CH 3CHO
BrCH 2CO OE t
H 2O +
O
7.-
H 2O 2
8.
C H 3
C H 3
N aN O 29.
NH 2
PH
- 5
H 2N-N H 2 R u/c 10.
NO 2
H +
1) H C N 11.
2) LiA lH 4
NaNO 2O
+
1) 2 CH 3I 12.
N
H
22
H C l 13.
NO 2
1) NaNO 2/HC l
C H 3N H 2
14.
C
B r 2-2
C l
O
H 2O 15. CH
3-
CH CO OH
Cl
16.
O
C H 3
C O OC 2H 5C O OC 2H 525C 2H 5O
H
+
17.
CH 2Cl
CO OH 18.
H
O C C l
C H 3
五、写出下列反应机理
1. 2CH3CO O C2H N aO C2H5HO A c
CH3
O
C CH2
O
C O C2H5 + C2H5OH
2.P hC O OO H
C O O C2H
C O O C2H5N aO C2H5
25
H O C O O C2H5
C O O C2H5
3.
B r2
C N H2
O
-
C H3O H
N H C O OH3
O
4.
O
CH3 C OH + C2H5O H
H
O
CH3 C OC2H5 + H2O
**
六、合成
1、以甲苯为原料,合戌
C H3
C N
B r B r
2、从丙酮及丙二酸二乙酯合成
O
O
3、从甲苯及必要试剂合成CH2C
C2H5
H CO OH
4、从O
C H3
合成
C H C H2C H2C H2C H2C O OH
O H
C H3
5、从O
出发合成N
N
O
Ph
七、推测结构
1、某化合物A(C7H6O3)能溶于NaOH及NaHCO3,与FeCl3有颜色反应,A与乙酐反应生成化合物B(C9H8O4),化合B可被水汽带馏出来。
A与CH3OH作用,生成香料物质C(C8H8O3)。
推出A、B、C的结构。
2、化合物A的分子式为C6H13N与2molCH3I反应,生成季铵盐,后经温湿氧化银处理后,得季铵碱B,B加热得化合物C:C8H17N,化合物C与1molCH3I和AgOH 反应,加热得化合物D(C6H10)和N(CH3)3,D用KMnO4氧化得CH3CH(COOH)2。
推出A、B、C、D结构。
3、化合物A(C5H8O),IR谱中3400~2400cm-1有宽散峰,1760 cm-1和1710 cm-1有强吸收。
A发生碘仿反应后得化合物B(C4H6O4),B的1HNMR:δ2.3(4H,S), 12(2H,S)。
A与过量甲醇在干燥HCl作用下,得化合物C (C8H16O4),化合物C经LiAlH4还原得化合物D(C7H16O3),D的IR:3400 cm-1、1100 cm-1、1050 cm-1有吸收峰。
D 经加热得化合物E和甲醇。
E的IR:1120 cm-1、1070 cm-1有吸收峰,Ms: m/z=116(M+),主要碎片离子m/z=101。
推测化合物A、B、C、D、E的结构。