实验二 缓冲溶液的配制和性质
- 格式:doc
- 大小:41.50 KB
- 文档页数:2

一、实验目的1. 学习并掌握缓冲溶液的配制方法。
2. 了解缓冲溶液的性质及其在化学实验中的应用。
3. 熟悉酸碱指示剂的使用方法。
4. 提高实验操作技能。
二、实验原理缓冲溶液是由弱酸及其共轭碱或弱碱及其共轭酸组成的溶液,具有一定的pH值稳定性。
在加入少量强酸或强碱时,缓冲溶液的pH值变化较小,因此常用于调节溶液的pH值。
缓冲溶液的pH值可用Henderson-Hasselbalch方程计算:pH = pKa + log([A-]/[HA])其中,pKa为弱酸的酸解离常数,[A-]为共轭碱的浓度,[HA]为弱酸的浓度。
三、实验材料与仪器材料:1. 0.1 mol/L HCl溶液2. 0.1 mol/L NaOH溶液3. 0.1 mol/L CH3COOH溶液4. 0.1 mol/L NaCH3COO溶液5. 甲基橙指示剂6. 酚酞指示剂7. pH计仪器:1. 烧杯2. 移液管3. 滴定管4. 电子天平5. 恒温水浴锅四、实验步骤1. 配制醋酸-醋酸钠缓冲溶液:a. 用移液管准确量取25.0 mL 0.1 mol/L CH3COOH溶液,转移至烧杯中。
b. 用移液管准确量取25.0 mL 0.1 mol/L NaCH3COO溶液,转移至烧杯中。
c. 将混合溶液用蒸馏水定容至100 mL,搅拌均匀。
2. 测定缓冲溶液的pH值:a. 将缓冲溶液用pH计测定pH值。
b. 重复测定三次,取平均值。
3. 测定缓冲溶液的缓冲容量:a. 在另一支烧杯中加入25.0 mL 0.1 mol/L CH3COOH溶液。
b. 加入2-3滴甲基橙指示剂,观察颜色变化。
c. 用0.1 mol/L NaOH溶液滴定至溶液颜色由黄色变为橙色,记录消耗的NaOH 体积。
d. 重复滴定三次,取平均值。
五、实验结果与讨论1. 缓冲溶液的pH值:通过实验测定,醋酸-醋酸钠缓冲溶液的pH值为4.75,与理论计算值4.74基本相符。
2. 缓冲溶液的缓冲容量:通过实验测定,醋酸-醋酸钠缓冲溶液的缓冲容量为6.7 mmol。


实验二 缓冲溶液的配制和性质、溶液pH 值测定一、实验目的1. 学习缓冲溶液及常用缓冲溶液的配制方法。
2. 加深对缓冲溶液性质的理解。
3. 学习吸量管的使用方法。
二、实验原理普通溶液不具备抗酸、抗碱、抗稀释作用。
缓冲溶液通常是由足够浓度的弱酸及其共轭碱、弱碱及其共轭酸或多元酸的酸式盐及其次级盐组成的,具有抵抗外加的少量强酸或强碱、或适当稀释而保持溶液pH 值基本不变的作用。
本实验通过将普通溶液和配制成的缓冲溶液对加入酸、碱或适当稀释前后pH 数值的变化来探讨缓冲溶液的性质。
根据缓冲溶液中共轭酸碱对所存在的质子转移平衡:HB ⇌ H ++B -缓冲溶液pH 值的计算公式为:缓冲比lg a p ]共轭酸[]共轭碱[lg a p [HB]][B lg p pH -+=+=+=K K K a式中p K a 为共轭酸解离常数的负对数。
此式表明:缓冲溶液的pH 值主要取决于弱酸的p K a 值,其次决定于其缓冲比。
需注意的是,由上述公式算得的pH 值是近似的,准确的计算应该用活度而不应该用浓度。
要配制准确pH 值的缓冲溶液,可参考有关手册和参考书上的配方,它们的pH 值是由精确的实验方法确定的。
缓冲容量(β)是衡量缓冲能力大小的尺度。
缓冲容量(β)的大小与缓冲溶液总浓度、缓冲组分的比值有关。
][B [HB]][B ×[HB]×2.303β--+=1、缓冲溶液总浓度越大则缓冲容量β越大:缓冲比一定时, c 总([HB]+ [B -])增大时,[HB]、 [B -]以相同的倍数增加,分式的值也以相同倍数增大,所以缓冲溶液的c 总越大,缓冲容量β越大。
2、缓冲比越接近于1,缓冲容量β越大:当c 总([HB]+ [B -])一定时, [HB]与 [B -]的值越接近,即缓冲比越接近于1, [HB] [B -] 的值越大,β越大。
当缓冲比为1时,β达极大值。
实验室中最简单的测定缓冲容量的方法是利用酸碱指示剂变色来进行判断的。

缓冲溶液的配制实验报告缓冲溶液的配制实验报告一、引言缓冲溶液是一种能够维持溶液pH值相对稳定的溶液,它在许多化学和生物学实验中起着重要的作用。
本实验旨在通过配制缓冲溶液的实验操作,探究缓冲溶液的原理和应用。
二、实验目的1. 了解缓冲溶液的基本原理;2. 学会配制不同pH值的缓冲溶液;3. 掌握使用pH计测定溶液pH值的方法。
三、实验原理缓冲溶液的原理基于酸碱中和反应。
当酸和碱的物质摩尔比例为1:1时,溶液的pH值相对稳定。
这是因为当酸性物质向溶液中释放H+离子时,碱性物质会捕获这些H+离子,从而保持溶液pH值的稳定。
四、实验步骤1. 准备所需实验器材和试剂:烧杯、移液管、搅拌棒、pH计、酸和碱溶液;2. 根据实验要求,选择合适的酸和碱溶液,准备不同浓度的缓冲溶液;3. 在烧杯中加入适量的酸溶液,并使用pH计测定其初始pH值;4. 慢慢滴加碱溶液到酸溶液中,同时用搅拌棒搅拌均匀;5. 每滴加一滴碱溶液后,使用pH计测定溶液的pH值,直到达到目标pH值;6. 记录实验数据,并进行分析。
五、实验结果与分析通过实验操作,我们成功地配制出了pH值为4、6和8的缓冲溶液。
在实验过程中,我们观察到随着碱溶液的滴加,溶液的pH值逐渐升高,直到达到目标pH值。
这表明缓冲溶液能够在一定范围内维持溶液的酸碱度。
六、实验讨论在实验中,我们选择了醋酸和氢氧化钠作为酸和碱溶液。
醋酸是一种弱酸,能够释放少量的H+离子,而氢氧化钠是一种强碱,能够捕获这些H+离子。
通过调整酸和碱的摩尔比例,我们能够控制缓冲溶液的pH值。
在实验过程中,我们使用了pH计来测定溶液的pH值。
pH计是一种能够测量溶液酸碱度的仪器,它通过测量溶液中的H+离子浓度来确定pH值。
在实验中,我们注意到pH计的测量结果可能会受到其他因素的干扰,如温度和电极的质量。
因此,在实验中我们需要保持一定的实验条件,以确保测量结果的准确性。
七、实验总结通过本次实验,我们深入了解了缓冲溶液的原理和应用。

竭诚为您提供优质文档/双击可除缓冲溶液配置实验报告篇一:缓冲溶液配制实验实验报告(二)缓冲溶液的配制和ph的测定区县____________学号____________姓名___________ 成绩_________实验内容:1.hAc-naAc缓冲溶液的配制注意:百里酚蓝指示剂的变色范围如下:在试管中加入3mL0.1mol·L的hAc和3mL0.1mol·L的naAc溶液就配制成了该缓冲溶液.加百里酚蓝指示剂5滴,显示___________色.计算此缓冲溶液的ph将配制的缓冲溶液为为3份.(1)取一份,加入5滴0.1mol·L的盐酸,则颜色变化是__________________________________________.再加入过量的0.1mol·L的盐酸,则颜色的变化是_________________________________.(2)取一份,加入5滴0.1mol·L的naoh溶液,则颜色变化是_____________________________________.再加入过量的0.1mol·L的naoh溶液,则颜色的变化是_________________________________.(3)取一份,加入5滴水,则溶液的颜色变化是_________________.2.nh3·h2o-nh4cl缓冲溶液的配制将25mL0.1mol·L的nh3·h2o和25mL0.1mol·L的nh4cl 溶液混合在烧杯中,即成缓冲溶液.测定ph值后,分成2分,分别加入0.5mL0.1mol·Lhcl溶液和0.5mL0.1mol·Lnaoh溶液.填写下表:思考题:什么是缓冲溶液?答:-1-1-1-1-1-1-1-1篇二:4缓冲溶液的配制与ph值的测定实验三缓冲溶液的配制与ph值的测定1.实验目的(1)掌握缓冲溶液的配制原理和方法;(2)熟悉有关缓冲溶液配制的计算公式;(3)了解缓冲溶液的有关性质;(4)学习用ph计测定溶液的ph值;2.实验原理在一定程度上能抵抗外加少量酸、碱或稀释,而保持溶液ph值基本不变的作用称为缓冲作用。

竭诚为您提供优质文档/双击可除缓冲溶液配置实验报告篇一:缓冲溶液配制实验实验报告(二)缓冲溶液的配制和ph的测定区县____________学号____________姓名___________ 成绩_________实验内容:1.hAc-naAc缓冲溶液的配制注意:百里酚蓝指示剂的变色范围如下:在试管中加入3mL0.1mol·L的hAc和3mL0.1mol·L的naAc溶液就配制成了该缓冲溶液.加百里酚蓝指示剂5滴,显示___________色.计算此缓冲溶液的ph将配制的缓冲溶液为为3份.(1)取一份,加入5滴0.1mol·L的盐酸,则颜色变化是__________________________________________.再加入过量的0.1mol·L的盐酸,则颜色的变化是_________________________________.(2)取一份,加入5滴0.1mol·L的naoh溶液,则颜色变化是_____________________________________.再加入过量的0.1mol·L的naoh溶液,则颜色的变化是_________________________________.(3)取一份,加入5滴水,则溶液的颜色变化是_________________.2.nh3·h2o-nh4cl缓冲溶液的配制将25mL0.1mol·L的nh3·h2o和25mL0.1mol·L的nh4cl 溶液混合在烧杯中,即成缓冲溶液.测定ph值后,分成2分,分别加入0.5mL0.1mol·Lhcl溶液和0.5mL0.1mol·Lnaoh溶液.填写下表:思考题:什么是缓冲溶液?答:-1-1-1-1-1-1-1-1篇二:4缓冲溶液的配制与ph值的测定实验三缓冲溶液的配制与ph值的测定1.实验目的(1)掌握缓冲溶液的配制原理和方法;(2)熟悉有关缓冲溶液配制的计算公式;(3)了解缓冲溶液的有关性质;(4)学习用ph计测定溶液的ph值;2.实验原理在一定程度上能抵抗外加少量酸、碱或稀释,而保持溶液ph值基本不变的作用称为缓冲作用。

缓冲溶液的配制和检测一、实验目的:了解缓冲溶液的性质和作用,熟悉掌握缓冲溶液的配制方法及原则二、实验原理:缓冲溶液:由弱酸及其共轭碱或弱碱及其共轭酸组成,具有一定的PH值,不因稀释或加入少量的强酸或强碱而改变PH值(明显改变)的溶液称为缓冲溶液。
由于缓冲溶液具有抗酸和抗碱成分,因此加入少量强酸或强碱,PH值不会受到影响,但是所有的缓冲溶液缓冲能力都有一定限度,即都有一定的缓冲容量,如果超过了这个缓冲容量,即可引起缓冲溶液PH值的急剧改变,失去作用。
三、实验器材:试管、移液枪、比色卡、玻璃棒、容量瓶、小烧杯、天平。
四、实验步骤:1.试剂的配制①1/15 mol/LNa2HPO4:取5.938g Na2HPO4·2H2O溶于500ml蒸馏水中,混匀备用②1/15mol/L KH2PO4:取4.532g KH2PO4溶于500ml蒸馏水中,混匀并在500ml容量瓶中定容。
③精密试纸④蒸馏水⑤0.01 mol/LHcl:取12 mol/L的浓Hcl0.208ml,并稀释至250ml容量瓶中,定容⑥0.01 mol/LNaOH:称取0.1gNaOH固体溶解,并加入250ml蒸馏水定容⑦0.01mol/LNacl:称取0.585gNacl溶解,并在100ml容量瓶中定容2.步骤①缓冲溶液的配制:取3支试管且按顺序标上号①②③,放在试管架上,用移液管按一下要求移取试剂,并使用精密PH试纸测缓冲溶液的PH值②对缓冲溶液进行稀释,按以下要求加入试剂,并观察③④颜色与②是否相同,并解释原因。
经实验验证:③④的颜色与②颜色相一致,即没有颜色的变化,原因是缓冲溶液的PH值取决于[B-][HB]的值,因此稀释缓冲溶液,PH值不应该变化。
③检测缓冲溶液的抗酸抗碱作用:比较①和②,③和④,⑤和⑥,⑦和⑧的颜色是否相一致,并解释其原因。
验证:③和④、⑤和⑥颜色相一致,原因:自制1号缓冲溶液,3号缓冲溶液具有抗酸和抗碱作用。
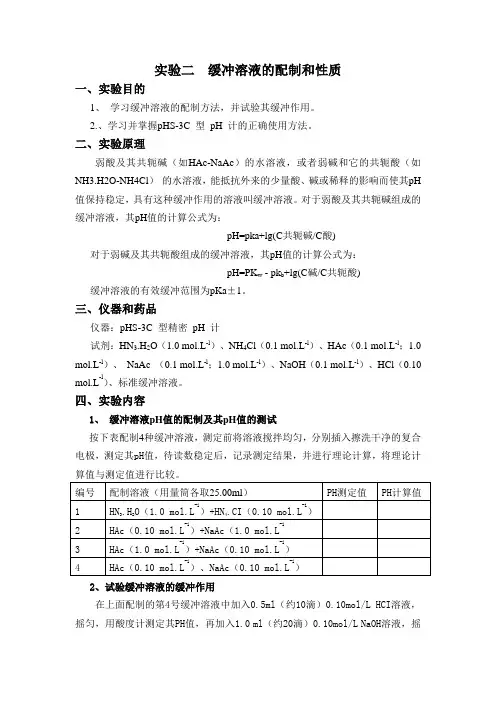
实验二缓冲溶液的配制和性质一、实验目的1、学习缓冲溶液的配制方法,并试验其缓冲作用。
2.、学习并掌握pHS-3C 型pH 计的正确使用方法。
二、实验原理弱酸及其共轭碱(如HAc-NaAc)的水溶液,或者弱碱和它的共轭酸(如NH3.H2O-NH4Cl)的水溶液,能抵抗外来的少量酸、碱或稀释的影响而使其pH 值保持稳定,具有这种缓冲作用的溶液叫缓冲溶液。
对于弱酸及其共轭碱组成的缓冲溶液,其pH值的计算公式为:pH=pka+lg(C共轭碱/C酸)对于弱碱及其共轭酸组成的缓冲溶液,其pH值的计算公式为:pH=PK w - pk b+lg(C碱/C共轭酸) 缓冲溶液的有效缓冲范围为pKa±1。
三、仪器和药品仪器:pHS-3C 型精密pH 计试剂:HN3.H2O(1.0 mol.L-l)、NH4Cl(0.1 mol.L-l)、HAc(0.1 mol.L-l;1.0 mol.L-l)、NaAc (0.1 mol.L-l;1.0 mol.L-l)、NaOH(0.1 mol.L-l)、HCl(0.10 mol.L-l)、标准缓冲溶液。
四、实验内容1、缓冲溶液pH值的配制及其pH值的测试按下表配制4种缓冲溶液,测定前将溶液搅拌均匀,分别插入擦洗干净的复合电极,测定其pH值,待读数稳定后,记录测定结果,并进行理论计算,将理论计算值与测定值进行比较。
2、试验缓冲溶液的缓冲作用在上面配制的第4号缓冲溶液中加入0.5ml(约10滴)0.10mol/L HCI溶液,摇匀,用酸度计测定其PH值,再加入1.0 ml(约20滴)0.10mol/L NaOH溶液,摇实验完成后,清洗电极,整理仪器。
三、设计和配制PH=3.9、PH=6.0的磷酸盐缓冲溶液和PBS缓冲溶液PH=3.9,配一个磷酸溶液(pH应该在1.8左右),用NaOH调到想要的pH即可PH=6.0,0.2 Mol/L Na2HPO4(12.2ml) 0.2Mol/L KH2PO4(87.8ml)五、思考题1、怎样根据缓冲溶液的PH值选定缓冲物质?2、为什么在通常情况下配制的缓冲溶液中酸(或碱)的浓度与其共轭碱(或共轭酸)的浓度接近?这种缓冲溶液的PH值主要决定于什么?3、将10mL0.2mol.L-1 HAc和10mL0.1mol.L-1 NaOH混合,问所得到溶液是否有缓冲作用?这个溶液的pH值在什么范围内?。

一、实验目的1. 理解缓冲溶液的概念、作用和配制原理;2. 掌握缓冲溶液的配制方法;3. 通过实验验证缓冲溶液的pH值和缓冲能力。
二、实验原理缓冲溶液是一种能够抵抗外界酸碱物质加入而使溶液pH值发生较大变化的溶液。
缓冲溶液的原理是:在溶液中存在一定量的弱酸及其共轭碱或弱碱及其共轭酸,当外界酸碱物质加入时,它们会与缓冲溶液中的酸碱物质发生中和反应,使溶液的pH值保持相对稳定。
缓冲溶液的pH值可通过Henderson-Hasselbalch方程计算:pH = pKa + log([A-]/[HA]),其中pKa为弱酸的酸解离常数,[A-]为共轭碱的浓度,[HA]为弱酸的浓度。
三、实验材料与仪器1. 实验材料:- 0.1mol/L的醋酸溶液;- 0.1mol/L的醋酸钠溶液;- 0.1mol/L的氢氧化钠溶液;- 0.1mol/L的盐酸溶液;- pH试纸;- 烧杯;- 移液管;- 容量瓶;- 玻璃棒。
2. 实验仪器:- pH计;- 电子天平;- 移液器。
四、实验步骤1. 配制醋酸-醋酸钠缓冲溶液:- 用移液管准确量取25.0mL的0.1mol/L醋酸溶液,转移至容量瓶中;- 用移液管准确量取25.0mL的0.1mol/L醋酸钠溶液,转移至容量瓶中;- 用去离子水定容至100.0mL,摇匀;- 将配制好的缓冲溶液用pH计测定pH值。
2. 配制醋酸-盐酸缓冲溶液:- 用移液管准确量取25.0mL的0.1mol/L醋酸溶液,转移至容量瓶中;- 用移液管准确量取25.0mL的0.1mol/L盐酸溶液,转移至容量瓶中;- 用去离子水定容至100.0mL,摇匀;- 将配制好的缓冲溶液用pH计测定pH值。
3. 测定缓冲溶液的缓冲能力:- 分别取5.0mL的醋酸-醋酸钠缓冲溶液和醋酸-盐酸缓冲溶液于烧杯中;- 向两个烧杯中分别加入1.0mL的0.1mol/L氢氧化钠溶液,摇匀;- 分别用pH试纸测定加入氢氧化钠溶液后的pH值。


缓冲溶液的配制与性质实验报告缓冲溶液的配制与性质实验报告引言:缓冲溶液是一种能够稳定溶液pH值的溶液,其在生物学、化学和医学等领域中具有重要的应用价值。
本实验旨在通过配制不同浓度的缓冲溶液,并研究其性质,以增进对缓冲溶液的理解。
实验一:醋酸-醋酸钠缓冲溶液的配制与性质研究材料与方法:1. 醋酸(CH3COOH)2. 醋酸钠(CH3COONa)3. 蒸馏水4. pH计5. 烧杯、移液管、试管等实验器材步骤:1. 准备不同浓度的醋酸-醋酸钠缓冲溶液,如0.1M、0.5M和1M。
2. 分别称取适量的醋酸和醋酸钠,加入不同容量的蒸馏水中,制备所需浓度的缓冲溶液。
3. 使用pH计测量各缓冲溶液的pH值,并记录。
结果与讨论:通过实验,我们成功配制了不同浓度的醋酸-醋酸钠缓冲溶液,并测量了其pH 值。
实验结果表明,随着醋酸-醋酸钠浓度的增加,溶液的pH值逐渐降低。
这是因为醋酸是弱酸,醋酸钠是其盐,当两者在适当比例下混合时,可以形成缓冲溶液。
实验二:磷酸盐缓冲溶液的配制与性质研究材料与方法:1. 磷酸二氢钠(NaH2PO4)2. 磷酸二钠(Na2HPO4)3. 蒸馏水4. pH计5. 烧杯、移液管、试管等实验器材步骤:1. 准备不同浓度的磷酸盐缓冲溶液,如0.1M、0.5M和1M。
2. 分别称取适量的磷酸二氢钠和磷酸二钠,加入不同容量的蒸馏水中,制备所需浓度的缓冲溶液。
3. 使用pH计测量各缓冲溶液的pH值,并记录。
结果与讨论:实验结果显示,磷酸盐缓冲溶液的pH值随着磷酸二氢钠和磷酸二钠的浓度变化而变化。
当两者的浓度相等时,溶液的pH值接近中性。
当磷酸二氢钠的浓度大于磷酸二钠时,溶液呈酸性;反之,则呈碱性。
这是因为磷酸二氢钠和磷酸二钠分别是一元酸和二元酸,它们在适当比例下混合时,可以形成缓冲溶液。
实验三:缓冲溶液的稳定性研究材料与方法:1. 醋酸-醋酸钠缓冲溶液(0.1M)2. pH计3. 烧杯、移液管、试管等实验器材步骤:1. 准备0.1M的醋酸-醋酸钠缓冲溶液。
《药用基础化学》缓冲溶液的配制和性质实验【实验目的】1.掌握缓冲溶液的配制方法。
2.深入理解缓冲溶液的性质。
3.了解缓冲容量与缓冲剂浓度和缓冲组分比值的关系。
【实验原理】缓冲溶液是由足够浓度的一对共轭酸碱组成的溶液。
它的pH 值可用下式表示:][][lgpK pH a 共轭酸共轭碱+=因此,缓冲溶液pH 值除了主要取决于pK a 外,还随共轭酸碱的浓度比而变。
若配制缓冲溶液所用的共轭酸、碱的原始浓度相同,上式可改写为:共轭酸共轭碱V V lgpK pH a +=这样,只要按共轭酸、碱溶液体积的不同比值配制溶液,就可得不同pH 值的缓冲溶液。
必须指出,由上述两个公式计算所得到的pH 值,没有考虑离子强度及弱酸离解所产生的影响,其值只是近似值。
准确计算应该用活度来代替量浓度。
要配制准确pH 值的缓冲溶液,可参考有关手册和参考书上的配方,它们的pH 值是由精确的实验方法确定的。
缓冲溶液中具有抗酸成分和抗碱成分,所以加少量强酸或强碱于缓冲溶液中,其pH 值不易改变。
稀释也不影响溶液的pH 值。
缓冲容量是衡量缓冲能力大小的尺度。
它的大小与缓冲剂浓度、缓冲组分的比值有关,缓冲剂浓度越大,缓冲容量越大,缓冲组分比值为1:1时,缓冲容量最大。
【仪器与试剂】仪器:烧杯,试管,量筒。
试剂:1 mol/LNaAc,0.1 mol/L NaAc,1 mol/LHAc,0.1 mol/L HAc,0.1 mol/LNaH2PO4,0.1 mol/LNa2HPO4,0.1 mol/LNH4Cl,0.1 mol/LNH3·H2O,2 mol/LNaOH,01 mol/L NaOH,0.1 mol/LHCl,pH=10的NaOH溶液,pH=4的HCl溶液,甲基红指示剂,广泛pH试纸,精密pH试纸。
【实验内容】(一)缓冲溶液的配制配制总体积为20ml的缓冲溶液。
通过计算,把配制下列3种缓冲溶液所需各组分的毫升数填入表。
一、实验目的1. 掌握缓冲溶液的配制方法;2. 了解缓冲溶液的性质和用途;3. 培养实验操作技能和实验报告撰写能力。
二、实验原理缓冲溶液是由弱酸及其共轭碱或弱碱及其共轭酸组成的溶液,具有抵抗外加少量酸、碱或稀释而保持溶液pH值基本不变的性质。
缓冲溶液的pH值由Henderson-Hasselbalch方程计算:pH = pKa + log([A-]/[HA])其中,pKa为弱酸的解离常数,[A-]为共轭碱的浓度,[HA]为弱酸的浓度。
三、实验材料1. 仪器:容量瓶、移液管、烧杯、玻璃棒、pH计、电子天平、滤纸等;2. 药品:盐酸、氢氧化钠、醋酸、醋酸钠、硼砂、硼酸等。
四、实验步骤1. 配制醋酸-醋酸钠缓冲溶液(1)称取3.75g醋酸钠(NaAc)和5.5ml浓醋酸(CH3COOH),置于100ml容量瓶中;(2)加入少量蒸馏水,用玻璃棒搅拌溶解;(3)加入约80ml蒸馏水,继续搅拌;(4)用pH计测定溶液的pH值,如不符合要求,可适量添加醋酸或醋酸钠进行调节;(5)加入剩余的蒸馏水,定容至100ml;(6)摇匀,待溶液稳定后,用移液管取10ml溶液于烧杯中,加入少量滤纸,进行干燥;(7)将干燥后的溶液用pH计再次测定pH值,确认溶液的pH值符合要求。
2. 配制硼砂-硼酸缓冲溶液(1)称取3.8g硼砂(Na2B4O7·10H2O)和5.5ml浓硼酸(H3BO3),置于100ml容量瓶中;(2)加入少量蒸馏水,用玻璃棒搅拌溶解;(3)加入约80ml蒸馏水,继续搅拌;(4)用pH计测定溶液的pH值,如不符合要求,可适量添加硼砂或硼酸进行调节;(5)加入剩余的蒸馏水,定容至100ml;(6)摇匀,待溶液稳定后,用移液管取10ml溶液于烧杯中,加入少量滤纸,进行干燥;(7)将干燥后的溶液用pH计再次测定pH值,确认溶液的pH值符合要求。
五、实验结果与分析1. 醋酸-醋酸钠缓冲溶液的pH值为4.75,符合实验要求;2. 硼砂-硼酸缓冲溶液的pH值为9.25,符合实验要求。
缓冲溶液的配制与性质的实验报告缓冲溶液的配制与性质的实验报告引言:缓冲溶液是化学实验中常用的一种溶液,它能够在一定范围内维持溶液的pH 值稳定。
本实验旨在通过实验操作,了解缓冲溶液的配制方法以及其性质。
实验一:醋酸-醋酸钠缓冲溶液的配制与性质1. 实验目的:掌握醋酸-醋酸钠缓冲溶液的配制方法,并研究其pH值变化规律。
2. 实验步骤:(1)取一定质量的醋酸固体溶解于蒸馏水中,得到一定浓度的醋酸溶液。
(2)取一定质量的醋酸钠固体溶解于蒸馏水中,得到一定浓度的醋酸钠溶液。
(3)将醋酸溶液和醋酸钠溶液按一定比例混合,得到醋酸-醋酸钠缓冲溶液。
3. 实验结果:通过实验操作,我们成功配制了一定浓度的醋酸-醋酸钠缓冲溶液。
利用pH计测得溶液的pH值为4.8。
4. 实验讨论:醋酸-醋酸钠缓冲溶液的pH值在4.8左右,说明该缓冲溶液能够在一定范围内维持溶液的酸碱度稳定。
这是由于醋酸和醋酸钠之间存在酸碱中和反应,使得溶液中的酸碱物质浓度保持相对稳定。
实验二:磷酸盐缓冲溶液的配制与性质1. 实验目的:了解磷酸盐缓冲溶液的配制方法,并研究其pH值变化规律。
2. 实验步骤:(1)取一定质量的磷酸二氢盐固体溶解于蒸馏水中,得到一定浓度的磷酸二氢盐溶液。
(2)取一定质量的磷酸氢二钠固体溶解于蒸馏水中,得到一定浓度的磷酸氢二钠溶液。
(3)将磷酸二氢盐溶液和磷酸氢二钠溶液按一定比例混合,得到磷酸盐缓冲溶液。
3. 实验结果:通过实验操作,我们成功配制了一定浓度的磷酸盐缓冲溶液。
利用pH计测得溶液的pH值为7.4。
4. 实验讨论:磷酸盐缓冲溶液的pH值在7.4左右,说明该缓冲溶液能够在一定范围内维持溶液的酸碱度稳定。
这是由于磷酸二氢盐和磷酸氢二钠之间存在酸碱中和反应,使得溶液中的酸碱物质浓度保持相对稳定。
实验三:缓冲溶液的应用1. 实验目的:探究缓冲溶液在生物学实验中的应用。
2. 实验步骤:(1)取一定浓度的醋酸-醋酸钠缓冲溶液。
(2)将醋酸-醋酸钠缓冲溶液加入到一定浓度的酸或碱溶液中。
竭诚为您提供优质文档/双击可除缓冲溶液的配制与性质实验报告篇一:《缓冲溶液的配制与性质》实验一缓冲溶液的配制和性质、溶液ph值测定【实验目的】1.2.3.4.5.学习缓冲溶液及常用等渗磷酸盐缓冲溶液的配制方法。
加深对缓冲溶液性质的理解。
强化吸量管的使用方法。
学习使用phs-2c型酸度计。
培养环境保护意识。
【预习作业】1.一般性溶液与缓冲溶液有什么不同?2.缓冲溶液的性质有哪些?3.如何衡量缓冲溶液的缓冲能力大小?缓冲溶液的缓冲能力与什么因素有关?4.实验是如何设计以验证缓冲溶液所具有的性质及缓冲容量的影响因素的,设计时有哪些注意事项?5.该如何检测缓冲溶液的ph值是否发生改变?是否均需要用ph计?6.本实验属定量测定还是定性测定或半定量测定?【实验原理】普通溶液不具备抗酸、抗碱、抗稀释作用。
缓冲溶液通常是由足够浓度的弱酸及其共轭碱、弱碱及其共轭酸或多元酸的酸式盐及其次级盐组成的,具有抵抗外加的少量强酸或强碱、或适当稀释而保持溶液ph值基本不变的作用。
本实验通过将普通溶液和配制成的缓冲溶液对加入酸、碱或适当稀释前后ph数值的变化来探讨缓冲溶液的性质。
根据缓冲溶液中共轭酸碱对所存在的质子转移平衡:-hb?b+h3o+缓冲溶液ph值的计算公式为:ph?pKa?lg[b][hb]-?pKa?lg[共轭碱][共轭酸]?pKa?lg缓冲比式中pKa为共轭酸解离常数的负对数。
此式表明:缓冲溶液的ph值主要取决于弱酸的pKa值,其次决定于其缓冲比。
需注意的是,由上述公式算得的ph值是近似的,准确的计算应该用活度而不应该用浓度。
要配制准确ph值的缓冲溶液,可参考有关手册和参考书上的配方,它们的ph值是由精确的实验方法确定的。
缓冲容量(β)是衡量缓冲能力大小的尺度。
缓冲容量(β)的大小与缓冲溶液总浓度、缓冲组分的比值有关。
β=2.303[hb]×[b][b]×=2.303×-1+缓冲比[hb]+[b]--缓冲溶液总浓度越大则β越大;缓冲比越趋向于1,则β越大,当缓冲比为1时,β达极大值。
缓冲溶液的配制和性质实验目的1.掌握缓冲溶液的配制方法,加深对其性质的理解。
2.掌握刻度吸管、滴管的使用方法。
3.了解pH 计测定溶液pH 的原理,学会使用pH 计。
实验原理缓冲溶液是由弱酸及其盐或弱碱及其盐组成。
对于由弱酸及其盐组成的缓冲体系,其的浓度比配制溶液,就可得到不同pH 的缓冲溶液。
必须指出,由上述公式算得的pH 是近似值,精确的计算应用活度而不应用浓度。
缓冲溶液中具有抗酸及抗碱成分,所以加入少量酸或碱其pH 变化不大。
当稀释缓冲溶液时,酸和盐的浓度比不变,故适当稀释对pH 影响不大。
缓冲容量是衡量缓冲能力大小的尺度。
它的大小与缓冲剂浓度、缓冲组分比值有关。
缓冲剂浓度越大,缓冲容量越大;缓冲组分比值为1∶1 时,缓冲容量最大。
pH 计测定溶液的pH 值是一种比较精确而又快速的方法(电位法)。
pH 计的指示电极( 常用玻璃电级)和参比电极( 常用甘汞电极)与待测溶液组成一原电池:玻璃电极∣待测溶液(pHx)‖甘汞电极甘汞电极的电极电势稳定不变,而玻璃电极的电极电势与待测液的pH 有关,因此通过测定电池的电动势便可求得待测液的pH。
E x = 甘-( 玻- 0.059pH x)因玻不确定,故先用已知pH 的标准液代替待测液测定电池电动势以求算玻,这称为定位或校正。
E s = 甘-( 玻- 0.059pH s)两式相减便可求得pH x 。
RT0.059 由 2.303 F 换算所得,该数值随温度而变。
在pH 计上可通过温度补偿器加以校准。
器材和药品1.器材pH 计、刻度吸管、50mL 烧杯、试管。
2.药品HAc( 0.1mol·L -1),NaAc(0.1mol·L-1),NH 3·H2O(0.1mol·L-1),pH=10 的NaOH,NaOH(0.1mol·L-1),NH4Cl(0.1mol·L-1),HCl(0.1mol·L-1),pH=5 的HCl ,pH 广泛试纸,邻苯二甲酸氢钾(0.05mol · L -1,pH=4.01) ,硼酸(0.01mol·L-1,pH=9.18) 。
实验二缓冲溶液的配制和性质
一、实验目的
1、学习缓冲溶液的配制方法,并试验其缓冲作用。
2.、学习并掌握pHS-3C 型pH 计的正确使用方法。
二、实验原理
弱酸及其共轭碱(如HAc-NaAc)的水溶液,或者弱碱和它的共轭酸(如NH3.H2O-NH4Cl)的水溶液,能抵抗外来的少量酸、碱或稀释的影响而使其pH 值保持稳定,具有这种缓冲作用的溶液叫缓冲溶液。
对于弱酸及其共轭碱组成的缓冲溶液,其pH值的计算公式为:
pH=pka+lg(C共轭碱/C酸)
对于弱碱及其共轭酸组成的缓冲溶液,其pH值的计算公式为:
pH=PK w - pk b+lg(C碱/C共轭酸) 缓冲溶液的有效缓冲范围为pKa±1。
三、仪器和药品
仪器:pHS-3C 型精密pH 计
试剂:HN3.H2O(1.0 mol.L-l)、NH4Cl(0.1 mol.L-l)、HAc(0.1 mol.L-l;1.0 mol.L-l)、NaAc (0.1 mol.L-l;1.0 mol.L-l)、NaOH(0.1 mol.L-l)、HCl(0.10 mol.L-l)、标准缓冲溶液。
四、实验内容
1、缓冲溶液pH值的配制及其pH值的测试
按下表配制4种缓冲溶液,测定前将溶液搅拌均匀,分别插入擦洗干净的复合电极,测定其pH值,待读数稳定后,记录测定结果,并进行理论计算,将理论计算值与测定值进行比较。
2、试验缓冲溶液的缓冲作用
在上面配制的第4号缓冲溶液中加入0.5ml(约10滴)0.10mol/L HCI溶液,摇匀,用酸度计测定其PH值,再加入1.0 ml(约20滴)0.10mol/L NaOH溶液,摇
实验完成后,清洗电极,整理仪器。
三、设计和配制PH=3.9、PH=6.0的磷酸盐缓冲溶液和PBS缓冲溶液PH=3.9,配一个磷酸溶液(pH应该在1.8左右),用NaOH调到想要的pH即可
PH=6.0,0.2 Mol/L Na2HPO4(12.2ml) 0.2Mol/L KH2PO4(87.8ml)
五、思考题
1、怎样根据缓冲溶液的PH值选定缓冲物质?
2、为什么在通常情况下配制的缓冲溶液中酸(或碱)的浓度与其共轭碱(或共轭酸)的浓度接近?这种缓冲溶液的PH值主要决定于什么?
3、将10mL0.2mol.L-1 HAc和10mL0.1mol.L-1 NaOH混合,问所得到溶液是否有缓冲作用?这个溶液的pH值在什么范围内?。