离子推断专题复习
- 格式:ppt
- 大小:730.50 KB
- 文档页数:1


离子推断题汇总(一)1.对某酸性溶液(可能含有Br-、SO42—、H2SO3、NH4+ )分别进行如下实验:①加热时放出的气体可以使品红溶液褪色②加碱调至碱性后,加热时放出的气体可以使润湿的红色石蕊试纸变蓝③加入氯水时,溶液略显黄色,再加入BaCl2溶液时,产生的白色沉淀不溶于稀硝酸对于下列物质不能确认其在溶液中是否存在的是A.Br-B.SO42— C.H2SO3 D.NH4+2.(2010·浙江)某钠盐溶液中可能含有 NO2—、SO42—、SO32—、CO32—、Cl—、I—等阴离子。
某同学取5份此溶液样品,分别进行了如下实验:①用pH计测得溶液的pH大于7②加入盐酸,产生有色刺激性气体③加入硝酸酸化的AgNO3溶液产生白色沉淀,且放出有色刺激性气体④加足量BaCl2溶液,产生白色沉淀,该沉淀溶于稀硝酸且放出气体,将气体通入品红溶液,溶液不褪色⑤加足量BaCl2溶液,产生白色沉淀,在滤液中加入酸化的(NH4)2Fe(SO4)2溶液,再滴加KSCN 溶液,显红色该同学最终确定在上述六种离子中仅含CO32—、NO2—、Cl—三种阴离子。
请分析,该同学只需要完成上述哪几个实验,即可得出此结论。
A.①②④⑤B.③④ C.③④⑤ D.②③⑤3.某无色溶液中含有K+、Cl—、OH—、SO32—、SO42—,为检验溶液中所含的各阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液、溴水和酚酞试液。
检验其中OH-的实验方法从略,检验其他阴离子的过程如下图所示。
(1)图中试剂①~⑤溶质的化学式分别是①_____ ___,②_____ ___,③______ __,④____ ____,⑤_____ ___。
(2)图中现象a、b、c表明检验出的离子分别是a._____ 、b.____ _、c.____ _。
(3)白色沉淀A加试剂②反应的离子方程式是。
(4)无色溶液A加试剂③的主要目的是(5)白色沉淀A若加试剂③而不加试剂②,对实验的影响是。

⾼考复习离⼦的检验、鉴别及推断复习知识点离⼦的检验、鉴别及推断基础盘点⼀、常见阳离⼦的检验1.常规检验法(1)⽤NaOH溶液能检验出Cu2+、Fe3+、Fe2+、Al3+、NH+4Cu2+:产⽣Fe3+产⽣Fe2++先产⽣,然后迅速变为.最终变为Al3+:产⽣⽩⾊沉淀,继续加⼊氢氧化钠溶液,⽩⾊沉淀⼜会_________NH4+:共热,⽣成能使湿润的红⾊⽯蕊试纸变_____的⽓体(2)焰⾊反应⽤焰⾊反应可检验出溶液中的钾离⼦和钠离⼦K+:⽕焰成________⾊(透过蓝⾊钴玻璃)Na+:⽕焰成_____⾊2、特殊检验法Fe3+:加⼊KSCN溶液呈_____⾊Fe2+:加⼊KSCN溶液⽆现象,滴加新制氯⽔后溶液呈_______⾊。
⼆、常见阴离⼦的检验1.利⽤酸碱指⽰剂检验OH-:滴⼊酚酞试液,溶液变⾊, 滴⼊紫⾊⽯蕊试液,溶液变⾊2.利⽤盐酸和其他试剂进⾏检验CO32-:加⼊BaCl2溶液后⽣成,再加⼊稀盐酸,并放出的⽓体SO42-→加⼊稀盐酸⽆沉淀⽣成,⽆⽓体放出,再加⼊BaCl2溶液有产⽣SO32-―→加⼊BaCl2溶液后⽣成,再加⼊稀盐酸,并放出有的⽓体3.利⽤AgNO3(HNO3酸化)溶液检验Cl-→⽣成不溶于稀硝酸的沉淀三、H+和OH-的检验四、熟练掌握在溶液中有特征颜⾊的离⼦4——呈,常见的溶液中有颜⾊的离⼦有:MnO-Cu2+——呈,Fe2+——呈,Fe3+——呈。
沉淀的颜⾊:Cu(OH)2——蓝⾊沉淀,Fe(OH)3——红褐⾊沉淀。
解题中特别注意题⼲条件是“⽆⾊透明”还是“澄清透明”。
考点精讲考点⼀检验常见物质的⼀般程序与思路1.⽆⾊溶液的检验例1 根据下列实验内容得出的结论正确的是()即时巩固1 关于某⽆⾊溶液中所含离⼦的鉴别,下列判断正确的是()A.加⼊AgNO3溶液,⽣成⽩⾊沉淀,加稀盐酸沉淀不溶解时,可确定有Cl-存在B.通⼊Cl2后,溶液变为深黄⾊,加⼊淀粉溶液后溶液变蓝,可确定有I-存在4存在C.加⼊Ba(NO3)2溶液,⽣成⽩⾊沉淀,加稀盐酸后沉淀不溶解时,可确定有SO2-3存在D.加⼊稀盐酸,⽣成的⽓体能使澄清⽯灰⽔变浑浊,可确定有CO2-考点⼆物质的鉴定、鉴别物质的检验通常有鉴定、鉴别。

质对市爱慕阳光实验学校高三第一轮复习离子共存推断专题1.〔10分〕某无色溶液,其中有可能存在的离子如下:Na+、Ag+、Ba2+、Al3+、AlO2-、S2-、CO32-、SO32-、SO42-,现取该溶液进行有关,结果如以下图所示:试答复以下问题:〔1〕沉淀甲是:___________________________,〔2〕沉淀乙是:_________________,由溶液甲生成沉淀乙的离子方程式为:_____________ ___.〔3〕沉淀丙是:__________________.〔4〕气体甲成分可能有哪几种?〔可以不填满也可以补充〕〔5〕综合上述信息,可以肯存在的离子:____ ___________.2.在含有Na+、Mg2+、HCO3—、SO42—的稀溶液中,它们的物质的量之比为2:1:2:1。
〔1〕向该溶液中滴加酚酞试液数滴,溶液呈淡粉,有关反的离子方程式为_____________________。
〔2〕充分加热〔1〕步所得的溶液,加热的过程中观察到的现象有___________;完全反后,溶液呈___________色,有关反的离子方程式为_______________________。
3.有A、B、C、D、E、F、G 7瓶不同物质的溶液,它们各是Na2CO3、Na2SO4、KCl、AgNO3、MgCl2、Ca(NO3)2和Ba (OH )2溶液中的一种。
为了鉴别,各取少量溶液进行两两混合,结果如表所示。
表中“↓〞表示生成沉淀或微溶化合物,“—〞表示观察不到明显变化。
试答复下面问题:〔1〕A的化学式是,G的化学式是。
判断理由是。
〔2〕写出其余几种物质的化学式。
B C D E F 。
4.A、B、C、D是四种可溶的化合物,分别由阳离子K+、Ba2+、Al3+、Fe3+和阴离子OHˉ、-23CO、-3NO、-24SO两两组合而成,它们的溶液发生如下反:A与B反生成白色沉淀,再加过量A,沉淀量减少,但不会完全消失。
离子推断专题一、解题策略:1、关注溶液颜色(Fe2+ Fe3+ Cu2+Mn04- )2、遵循三个原则。
互斥性原则:不能共存(生成弱电解质、挥发物质、难溶物、络合物、发生氧还反应)进出性原则:进出守恒。
电中性原则:电荷守恒。
3、关注特殊物质或特殊变化。
(找准题眼)二、知识点:知识点1、常见阳离子的检验方法:知识点2、常见阴离子的检验方法:离子检验试剂实验现象OH-①酚酞试液②石蕊试液或试纸①呈红色②呈蓝色Cl-AgNO3,稀HNO3白色沉淀Ag++Cl-=AgCl↓Br-AgNO3,稀HNO3淡黄色沉淀Ag++Br-=AgBr↓I-AgNO3,稀HNO3黄色沉淀Ag++I-=AgI↓SO42-HCl,BaCl2溶液加HCl无沉淀,再加Ba2++SO42-=BaSO4↓BaCl2有白色沉淀SO32-稀硫酸,品红溶液无色刺激性气味的气体,能使品红溶液退色SO32-+2H+=SO2↑+H2OCO32-HCl,澄清石灰水白色沉淀CO32-+2H+=CO2↑+H2OCO2+Ca(OH)2=CaCO3+2H2O一、选择题和填空1.某无色透明溶液,可能含有下面离子中的几种:阳离子组:Cu2+、Ba2+、Mg2+、H+;阴离子组:Cl—、OH—、NO3—、CO32—;已知该溶液能和铝粉反应放出氢气,如果确定该溶液中含有Mg2+,试推断溶液中一定含有离子,可能含有离子,一定没有离子。
2.有一瓶无色溶液,可能含有Na+、K+、Al3+、Mg2+、NH4+、Cl—、SO42—、HCO3—、MnO4—离子中的几种。
为确定其成分,进行如下实验:①取少许溶液,逐渐加入过量的Na2O2固体,产生无色无味的气体和白色沉淀且白色沉淀逐渐增多后又部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生;③用洁净的铂丝蘸取原溶液在酒精灯火焰上灼烧,观察到黄色火焰。
下列推断正确的是( )A.肯定有Na+、Al3+、Mg2+、SO42—B.肯定有Na+、Mg2+、Al3+、Cl—C.肯定没有K+、HCO3—、MnO4—D.肯定没有K+、NH4+、Cl—3.某无色溶液子宫可能含有K+、NO3-、NH4+、SO42-、Al3+、Cl-、Al02-、Cu2+、Fe3+、CO32-离子,用pH 试纸检验呈蓝色,该溶液中不可能含有的离子是。

1、一种酸性较强的溶液中,可能存在NO3-、I-、Cl-、Fe3+中的一种或几种。
向该溶液中加入溴水后,溴被还原,由此可推断该溶液中A、含NO3-B、含有NO3-、I-、Cl-C、含I-,但不能确定是否含Cl-D、含有Fe3+2.甲、乙、丙是三种不含相同离子的可溶性强电解质。
它们所含离子如下表所示:甲)>c(乙)>c(丙),则乙物质可能是①MgSO4②NaOH ③(NH4)2SO4④Mg(NO3)2⑤NH4NO3A.①②B.③④C.③⑤D.①⑤3.某溶液中含有SO32-、SiO32-、Br-、CO32-、Na+,向该溶液中通入过量的Cl2,下列判断正确的是①反应前后,溶液中离子浓度基本保持不变的只有Na+②有沉淀生成③有气体产生④溶液颜色发生变化⑤溶液中共发生了3个氧化还原反应A.①③⑤ B.①②③④ C.②④⑤D.①②③④⑤4.有一无色溶液,可能含有K+、Al3+、NH4+、Mg2+、Cl-、SO42-、HCO3-、MnO4-中的一种或几种。
为确定其成分,做如下实验:(1)取部分溶液,加入适量Na2O2固体、产生无色无味的气体并生成白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;(2)另取部分原溶液,加入HNO3酸化的Ba(NO3)2有白色沉淀产生。
下列推断正确的是A.肯定有K+、HCO3-、MnO4- B.肯定有Al3+、Mg2+、HCO3-C.肯定有Al3+、Mg2+、SO42-、Cl- D.肯定有Al3+、Mg2+、SO42-5. 某无色溶液,由Na+、Ag+、Ba2+、Al3+、AlO2—、MnO4—、CO32—、SO42—中的若干组成,取一定溶液进行如下实验:(1)取适量溶液,加入过量盐酸,有气体生成,并得到溶液A(2)在所得溶液A中加入过量碳酸氢铵溶液得到溶液B,同时有气体生成,并析出白色沉淀甲(3)在所得溶液B中加入过量Ba(OH)2溶液,也有气体生成,并析出白色沉淀乙。
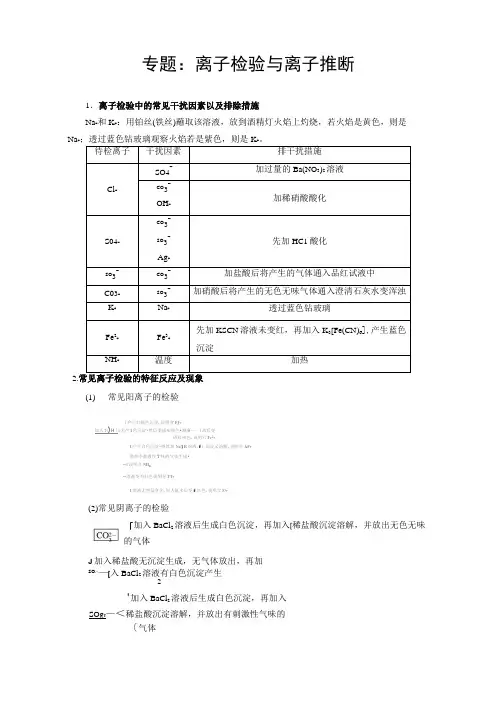
专题:离子检验与离子推断1.离子检验中的常见干扰因素以及排除措施Na+和K+:用铂丝(铁丝)蘸取该溶液,放到酒精灯火焰上灼烧,若火焰是黄色,则是Na+;透过蓝色钻玻璃观察火焰若是紫色,则是K +。
待检离子干扰因素排干扰措施Cl-SO4-加过量的Ba(NO3)2溶液CO3-OH-加稀硝酸酸化S04-CO3-SO3-Ag+先加HC1酸化SO3-CO3-加盐酸后将产生的气体通入品红试液中C03-SO3-加硝酸后将产生的无色无味气体通入澄清石灰水变浑浊K+Na+透过蓝色钻玻璃Fe2+Fe3+先加KSCN溶液未变红,再加入K3[Fe(CN)6],产生蓝色沉淀NH+温度加热2.常见离子检验的特征反应及现象(1)常见阳离子的检验「产①红隔色沉淀.说明會FJ+加人7()H「I尤产'I色沉淀•然后变成灰绿色•濬廉…—I战后变成红褂色.说明六Fe2+I产生白色沉淀•继续加Na()H溶液.f〕沉淀乂溶解.说叫介AF+微热令刺澈性Y味的气体生成•〜I说明介NH:〜溶液变为红色说明存FT+I溶液尤明显变化.加人氟水后变f红色.说明含F/+(2)常见阴离子的检验「加入BaCl2溶液后生成白色沉淀,再加入[稀盐酸沉淀溶解,并放出无色无味的气体J加入稀盐酸无沉淀生成,无气体放出,再加SO^—[入BaCl2溶液有白色沉淀产生2'加入BaCl2溶液后生成白色沉淀,再加入SO g T—<稀盐酸沉淀溶解,并放出有刺激性气味的〔气体叵T一加入AgNO3生成不溶于稀硝酸的白色沉淀[探高考•真题鉴赏]1.(2016・全国高考卷II)某白色粉末由两种物质组成,为鉴别其成分进行如下实验:①取少量样品加入足量水仍有部分固体未溶解;再加入足量稀盐酸,有气泡产生,固体全部溶解;②取少量样品加入足量稀硫酸有气泡产生,振荡后仍有固体存在。
该白色粉末可能为()A.NaHCO3、A1(OH)3B.AgCl、NaHCO gC.NaSO、BaCOD.NaCO、CuSO233234解析:A项中,NaHCO3、A1(OH)3加入足量水中,NaHCO g溶解,Al(OH)3不溶解;加入稀盐酸,固体全部溶解,且有气泡产生;NaHCO3、A1(OH)3均能与H2SO4反应,最后不会有固体剩余。

化学离子推断知识点总结一、化学离子的性质1. 化学离子的定义化学离子是指在溶液中或熔融状态下,由于分子内部电荷平衡的破坏,产生带电离子的物质。
最常见的离子有正离子(阳离子)和负离子(阴离子)两种。
正离子是指失去了一个或多个电子的原子或分子,带有正电荷;而负离子则是指获得了一个或多个电子的原子或分子,带有负电荷。
2. 化学离子的性质(1)离子的生成与溶解特性一些化合物在溶液中可以自发的分解成离子,这种化合物叫做电解质。
电解质的分解通常是不可逆的,也就是不能反应逆过程的生成原始化合物。
比如,NaCl在水中可以分解成Na+和Cl-离子。
(2)离子的化学性质离子之间的结合是靠电离子键、共价键、金属键等方式进行相互结合的,而离子之间的相互作用更具有特点和普遍性,例如NaCl溶解在水中产生Na+和Cl-离子,表示溶液中的Na+和Cl-离子能够自由的游离。
同时,离子在溶液中还具有导电性,溶液中的离子由于能够在电场的作用下向两极迁移,因此导电的现象。
3. 离子的检测方法化学离子的检测主要是通过化学方法来进行,包括有沉淀法、置换法、气体检测法、荧光法等。
其中最常用的方法是沉淀法,利用化学反应生成的沉淀对离子进行检测的方法。
此外,还可以通过分光光度计、电化学方法等仪器化的检测方法进行。
二、化学离子推断方法在化学实验中,根据化学反应原理通过化学反应的结果来推断出物质中所含的化学离子种类和成分,这就是化学离子推断。
1. 双离子反应法双离子反应法是指利用反应过程及结果,通过化学反应的平衡来推断物质中的离子成分。
它的具体方法是观察试剂的加入和反应的结果,根据反应不同的结果,推断出溶液中所含的离子类型。
比如,当加入氯化银试剂,能够产生白色沉淀,表示溶液中含有氯离子。
2. 离子吸附法离子吸附法通过溶液中的离子与固体吸附剂的吸附作用来推断溶液中离子的种类和浓度。
根据吸附剂上的沉淀形状、颜色等来判断溶液中的离子成分。
比如,加入钠石灰试剂,能够吸附溶液中的Ca2+离子,并形成白色沉淀。

高考化学总复习《离子检验与推断》专项复习1.(2020·天津高考真题)检验下列物所选用的试剂正确的是2.(2018·浙江高考真题)通过实验得出的结论正确的是A .将某固体试样完全溶于盐酸,再滴加BaCl 2溶液,出现白色沉淀,则该固体试样中存在SO 42-B .将某固体试样完全溶于盐酸,再滴加KSCN 溶液,没有出现血红色,则该固体试样中不存在Fe 3+C .在某固体试样加水后的溶液中,滴加NaOH 溶液,没有产生使湿润红色石蕊试纸变蓝的气体,该固体试样中仍可能存在NH 4+D .在某固体试样加水后的上层清液中,滴加盐酸出现白色沉淀,再加NaOH 溶液沉淀溶解,则该固体试样中存在SiO 32-3.(2018·浙江高考真题)通过实验得出的结论正确的是A .将某固体试样完全溶于盐酸,再滴加Ba(NO 3)2溶液,出现白色沉淀,则该固体试样中存在SO 42-B .将某固体试样完全溶于盐酸,再滴加KSCN 溶液,没有出现血红色,则该固体试样中不存在Fe 3+C .在某固体试样加水后的溶液中,滴加NaOH 溶液,没有产生使湿润红色石蕊试纸变蓝的气体,该固体试样中仍可能存在NH 4+D .在某固体试样加水后的上层清液中,滴加盐酸出现白色沉淀,再加NaOH 溶液沉淀溶解,则该固体试样中存在SiO 32-4.(2017·浙江高考真题)已知:24Ag SO 微溶于水,可溶于硝酸。
溶液X 中可能含有22222334Na Ca Fe Cl Br CO SiO SO +++-----、、、、、、、中的几种离子。
为了确定其组成,某同学进行了如下实验:下列说法正确的是( )A .溶液X 中一定含有Na +、Cl -和23SiO -B .溶液X 中一定不含2Ca +、Br -C .为确定溶液X 中是否含有24SO -,可取溶液2,加入2BaCl 溶液D .在溶液X 中依次滴入盐酸、双氧水和硫氰化钾溶液后,溶液将变为红色5.(2016·浙江高考真题)某固体可能含有NH 4+、Cu 2+、Na +、Cl -、CO 32-、SO 42-中的几种离子,取等质量的两份该固体,进行如下实验(不考虑盐类的水解及水的电离);(1)一份固体溶于水得无色透明溶液,加入足量BaCl 2溶液,得沉淀6.63g ,在沉淀中加入过量稀盐酸,仍有4.66g 沉淀。

专题五离子推断和检验问题解题方法:解此类试题时首先应关注溶液是无色透明还是澄清透明,确定是否要排除有色离子。
常见的溶液中有颜色的离子有:Fe2+、Fe3+、MnO4-、Cu2+等。
如加入稀盐酸无现象,再加氯化钡溶液,产生白色沉淀,证明含有氯离子;加入硫氰化钾显红色,有Fe3+等等。
更重要的是能够掌握解这类试题的正确思维方法,这就必须遵循以下几个原则:1、互斥性原则所谓互斥性原则就是当我们利用题给实验现象判断出一定有某中离子时,应立即运用已有的知识,当机立断,马上排除与之不能共存的离子。
2、进出性原则所谓进出性原则就是在进行离子检验时,往往要加入试剂,这样就会引进新的离子,那么原溶液中是否存在该种离子就无法判断,从而对后续的实验造成影响。
3、电中性原则所谓电中性原则溶液中阳离子所带正电荷与阴离子所带的负电荷总数相等。
这个隐含条件往往不被人注意,从而造成在离子推断中漏选或错选。
在判断混合体系中某些离子存在与否时,有的离子并未通过实验验证,但我们仍可运用溶液中电荷守恒理论来判断其是否存在。
对点练习一、选择题1.在自来水的生产中,常通入适量氯气进行杀菌消毒,氯气与水反应的产物之一是盐酸。
市场上有些不法商贩为牟取暴利,利用自来水冒充纯净水桶装出售。
为辨别真伪,可用以鉴别的一种试剂是() A.酚酞试液B.氯化钡溶液C.氢氧化钠溶液D.硝酸银溶液2.在甲、乙两烧杯溶液中,共含有Cu2+、K+、H+、Cl-、CO2-3、OH-6种离子。
已知甲烧杯的溶液含其中3种离子并呈蓝绿色,则乙烧杯的溶液中含有的另3种离子是() A.Cu2+、H+、Cl-B.K+、CO2-3、Cl-C.K+、OH-、CO2-3D.K+、H+、Cl-3、某工厂排放的工业废水中可能含有K+、Ag+、NH4+、Mg2+、SO42-、Cl-、NO3-、HCO3-等离子。
经检测废水呈明的碱性,则可确定该厂废水中肯定不含有的离子组合是()A.Ag+、K+、NO3-、HCO3-B.K+、NH4+、NO3-、SO42-C.Ag+、NH4+、Mg2+、HCO3-D.K+、Mg2+、SO42-、Cl-4、向含有下列离子的溶液中分别加入烧碱固体(溶液体积变化可忽略),能引起离子浓度减小的是()A、HCO3-B、Cl-C、OH-D、Cu2+5、溶液中可能有下列阴离子中的一种或几种:Cl-、OH-、CO32-、SO42-。
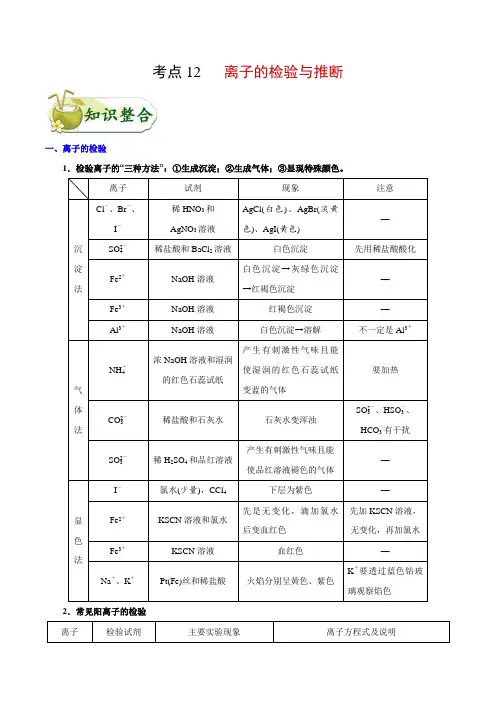
考点12 离子的检验与推断一、离子的检验1.检验离子的“三种方法”:①生成沉淀;②生成气体;③显现特殊颜色。
离子试剂现象注意沉淀法Cl-、Br-、I-稀HNO3和AgNO3溶液AgCl(白色)、AgBr(淡黄色)、AgI(黄色)—SO2-4稀盐酸和BaCl2溶液白色沉淀先用稀盐酸酸化Fe2+NaOH溶液白色沉淀→灰绿色沉淀→红褐色沉淀—Fe3+NaOH溶液红褐色沉淀—Al3+NaOH溶液白色沉淀→溶解不一定是Al3+气体法NH+4浓NaOH溶液和湿润的红色石蕊试纸产生有刺激性气味且能使湿润的红色石蕊试纸变蓝的气体要加热CO2-3稀盐酸和石灰水石灰水变浑浊SO2-3、HSO-3、HCO-3有干扰SO2-3稀H2SO4和品红溶液产生有刺激性气味且能使品红溶液褪色的气体—显色法I-氯水(少量),CCl4下层为紫色—Fe2+KSCN溶液和氯水先是无变化,滴加氯水后变血红色先加KSCN溶液,无变化,再加氯水Fe3+KSCN溶液血红色—Na+、K+Pt(Fe)丝和稀盐酸火焰分别呈黄色、紫色K+要透过蓝色钴玻璃观察焰色2.常见阳离子的检验离子检验试剂主要实验现象离子方程式及说明Ba2+稀硫酸或可溶性硫酸盐溶液先加稀盐酸,不产生沉淀,然后加稀硫酸或可溶性硫酸盐溶液生成白色沉淀Ba2++24SO-BaSO4↓ (白色)Mg2+NaOH溶液生成白色沉淀,NaOH过量时沉淀不溶解Mg2++2OH−Mg(OH)2↓(白色)Al3+NaOH溶液或氨水加氨水或适量NaOH溶液,有絮状白色沉淀生成,沉淀能溶于NaOH溶液,但不溶于氨水Al3++3OH−Al(OH)3↓(白色)Al(OH)3↓+OH−2AlO-+2H2OFe3+ (黄色) NaOH溶液生成红褐色沉淀Fe3++3OH−Fe(OH)3↓(红褐色) KSCN溶液溶液呈红色Fe3++3SCN−Fe(SCN)3(红色)Fe2+ (浅绿色)NaOH溶液加NaOH溶液生成白色沉淀,在空气中迅速变为灰绿色,最后变为红褐色Fe2++2OH−Fe(OH)2↓(白色)4Fe(OH)2+O2+2H2O4Fe(OH)3↓(红褐色) KSCN溶液,新制氯水加KSCN溶液,无明显现象,加新制氯水后溶液呈红色2Fe2++Cl22Cl−+2Fe3+Fe3++3SCN−Fe(SCN)3(红色)H+紫色石蕊溶液变红色H+表现酸性甲基橙溶液变红色pH试纸变红色锌粒生成无色气体Zn+2H+Zn2++H2↑Cu2+ (蓝色)NaOH溶液加NaOH溶液,有蓝色沉淀生成,若加热则沉淀变黑Cu2++2OH−Cu(OH)2↓(蓝色)Cu(OH)2CuO(黑色)+H2O H2S(或Na2S溶液)生成黑色沉淀Cu2++H2S2H++CuS↓(黑色)Ag+稀盐酸或氯化物溶液,稀硝酸生成白色沉淀,不溶于稀硝酸Ag++Cl−AgCl↓ (白色)+4NHNaOH 溶液加NaOH 溶液,加热并用湿润的红色石蕊试纸检验产生的气体,试纸变蓝+4NH +OH −NH 3↑+H 2ONa +焰色反应火焰呈黄色焰色反应属于物理现象K +火焰呈紫色(透过蓝色钴玻璃片)3.常见阴离子的检验 离子检验试剂或方法实验现象 反应方程式及说明OH −①取少量试液于试管中,向其中滴加紫色石蕊溶液(或酚酞试液); ②用玻璃棒蘸取少量试液滴于红色石蕊试纸上①紫色石蕊溶液变蓝(或酚酞试液变红); ②红色石蕊试纸变蓝Cl −取少量试液于试管中,向其中滴加少量AgNO 3溶液,再加入稀硝酸 生成白色沉淀,且不溶于稀硝酸Ag ++Cl −AgCl↓Br −取少量试液于试管中,向其中滴加少量AgNO 3溶液,再加入稀硝酸 生成浅黄色沉淀,且不溶于稀硝酸Ag ++Br −AgBr↓ I −①取少量试液于试管中,向其中滴加少量AgNO 3溶液,再加入稀硝酸; ②滴入淀粉溶液后再滴入氯水①生成黄色沉淀,且不溶于稀硝酸; ②溶液显蓝色①Ag ++I −AgI↓②2I −+Cl 22Cl −+I 2,淀粉遇碘变蓝色23CO -氯化钡溶液、稀硝酸生成白色沉淀,加稀硝酸后白色沉淀溶解,产生无色无味气体Ba 2++23CO -BaCO 3↓ BaCO 3+2H + Ba 2++CO 2↑+H 2O3HCO -氯化钡溶液、稀盐酸不生成沉淀,加稀盐酸,产生无色无味气体3HCO -+H +CO 2↑+H 2O23SO -氯化钡溶液、盐酸、品红溶液先生成白色沉淀,加盐酸后白色沉淀溶解,将生成的气体通入品红溶液中,溶液褪色Ba 2++23SO -BaSO 3↓ BaSO 3+2H + Ba 2++SO 2↑+H 2O24SO-取少量试液于试管中,向其中加入足量稀盐酸后,再加入BaCl2溶液加入盐酸不产生沉淀,加入BaCl2溶液后生成白色沉淀Ba2++24SO-BaSO4↓3NO-加热浓缩溶液,加入浓硫酸和铜片有红棕色的气体产生,溶液变蓝色Cu+4H++23NO-Cu2++2NO2↑+2H2OS2−①稀硫酸或盐酸;②Pb(NO3)2溶液、稀硝酸①生成无色有臭鸡蛋气味的气体;②生成黑色沉淀,且不溶于稀硝酸①S2−+2H+H2S↑②S2−+Pb2+PbS↓(黑色)二、离子的推断1.离子推断题的解题思路该考点主要以选择题及填空题的形式出现,离子推断可以把实验操作、离子反应、离子共存、离子检验、电荷守恒等知识综合起来考查,是综合性较强的题目。
学考专题复习-离子推断姓名 班级1.某100mL 溶液可能含有Na +、NH 4+、Fe 3+、CO 32-、SO 42-、Cl -中的若干种,取该溶液进行连续实验,实验过程如下:(所加试剂均过量,气体全部逸出)下列说法不正确...的是 A .原溶液一定存在CO 32-和SO 42-,一定不存在Fe 3+B .原溶液一定存在Cl -,可能存在Na +C .原溶液中c (Cl -) ≥0.1mol ·L-1D .若原溶液中不存在Na +,则c (Cl -)<0.1mol ·L -12.已知:Ag 2SO 4微溶于水,可溶于硝酸。
溶液X 中可能含有Na +、Ca 2+、Fe 2+、Cl —、Br —、CO32-、SiO 32-、SO 42-中的几种离子。
为了确定其组成,某同学进行了如下实验:下列说法正确的是A .溶液X 中一定含有Na +、Cl —和SiO 32-B .溶液X 中一定不含Ca 2+、Br —C .为确定溶液X 中是否含有SO 42-,可取溶液2,加入BaCl 2溶液D .在溶液X 中依次滴入盐酸、双氧水和硫氰化钾溶液后,溶液将变为红色3.甲、乙、丙、丁四种易溶于水的物质 分别由NH 4+、Ba 2+、Mg 2+、H +、OH -、Cl -、HCO 3-、SO 42-中的不同阳离子和阴离子各一种组成。
已知:①将甲溶液分别与其他三种物质的溶液混合,均有白色沉淀生成;②0.1 mol/L 乙溶液中c (H +)>0.1 mol/L ;③向丙溶液中滴入AgNO 3溶液有不溶于稀HNO 3的白色沉淀生成。
下列结论不正确的是( )A .甲溶液含有Ba 2+B .乙溶液含有SOC .丙溶液含有Cl -D .丁溶液含有Mg2+4.某无色溶液中只可能含有:①Na +、②Ba 2+、③C1—、④Br —、⑤SO 32—、⑥SO 42—离子中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下操作步骤现象(1)用pH 试纸检验溶液的pH 大于7 (2)向溶液中滴中氯水,再加入CC14振荡,静置 CC14层呈橙色 (3)向所得溶液中加入Ba(NO)2溶液和稀HNO 3 有白色沉淀产生 (4)过滤,向滤液中加入AgNO 3溶液和稀HNO 3的白色沉淀产生下列结论正确的是 ( ) A .肯定含有离子的①④⑤ B .肯定没有的离子是②⑤ C .可能含有的离子是①⑥ D .不能确定的离子是①③⑥5.在一含Na +的澄清溶液中,可能还存在NH 4+.Fe 2+.I -.Br -.CO 32-.SO 32-六种离子中的几种:①在原来溶液中滴加足量的饱和氯水,有气泡生成,溶液呈现橙黄色 ②向呈橙黄色的溶液中加入BaCl 2溶液时无沉淀生成 ③橙黄色溶液不能使淀粉溶液变蓝色。
离子共存、离子的检验和推断【知识梳理】一、离子共存1.实质:几种离子在同一溶液中能大量共存,就是指离子之间不发生任何反应;若离子之间能发生反应,则不能大量共存。
2.离子间通常进行的四类反应(1)复分解反应:生成沉淀、气体、弱电解质等思考:试总结因发生复分解反应不能共存的离子(2)氧化还原反应:常见氧化性离子:常见还原性离子:(3)双水解反应:常见的因发生相互促进的水解反应而不能大量共存的离子如下:①Al3+与、、、、AlO2-、SiO32-;②Fe3+与、、AlO2-、SiO32-;③NH4+与AlO2-、SiO32-。
(4)形成配合物:Fe3+与形成、Ag+与NH3·H2O形成而不能大量共存注意:还应注意题干中的限制性条件(详见“知识探究”)A.在溶液中加KSCN,溶液显红色,证明原溶液中有Fe3+,无Fe2+B.气体通过无水CuSO4,粉末变蓝,证明原气体中含有水蒸气C.灼烧白色粉末,火焰呈黄色,证明原粉末中有Na+,无K+D.将气体通入澄清石灰水,溶液变浑浊,证明原气体是CO2【知识探究】一、离子共存问题中的常见“陷阱”例1 下列各溶液中一定能大量共存的离子组是()A.加入铝粉有氢气生成的溶液中:Mg2+、Cu2+、SO42-、K+B.使pH试纸呈红色的溶液中:Fe2+、I-、NO3-、Cl-C.常温下,c(H+)=10-13mol·L-1的溶液中:Na+、AlO2-、S2-、SO32-+--28的溶液中:K+、Na+、HCO-、Ca2+有色离子不能大量存在,例如:Cu2+( )、Fe3+( )、Fe2+( )、MnO4-( )、[Fe SCN2]+( )“因发生氧化还原反应而不能大量共存”只能是氧化性离子和还原性离子不能大量共存,不包括其他类型反应的离子常见的易错点“透明”“透明”也可“有色”“与Al反应放出H2”溶液既可能显酸性也可能显碱性“由水电离出的c(H+)=1×10-12 mol·L-1”溶液既可能显酸性也可能显碱性“通入足量的NH3”与NH3·H2O反应的离子不能大量存在常见题干要求(1)“一定大量共存”(2)“可能大量共存”(3)“不能大量共存”审清关键字二、离子推断例2某钠盐溶液可能含有阴离子NO3-、CO32-、SO32-、SO42-、Cl-、Br-、I-。