新人教版必修1第4章第2节元素周期律第1课时课件
- 格式:pptx
- 大小:1.15 MB
- 文档页数:1

可编辑修改精选全文完整版(新教材)人教版高中化学必修1第四章第2节《元素周期律》优质说课稿(新教材)人教版高中化学必修一第四章第2节《元素周期律》优质说课稿今天我说课的内容是部编人教版(新教材)高中化学必修1第四章第2节《元素周期律》。
丰富多彩的物质世界是由一百多种元素组成的。
那么,这些元素之间有什么内在联系吗?它们是如何相互结合形成多种多样的物质呢?最初,人们是通过分类整理的方法对元素之间的联系进行研究的。
随着元素周期表的建立和元素周期律的发现,特别是原子结构的奥秘被揭示,人们从微观角度探索元素之间的内在联系,进一步认识了元素性质及其递变规律,并通过研究粒子间的相互作用,认识化学反应的本质;逐步建立了结构决定性质的观念。
通过第四章学习,从宏观辨识与微观探析、变化观念与平衡思想、证据推理与模型认知、科学探究与创新意识、科学态度与社会责任5个方面培养学生化学学科核心素养。
本章共有三节,本课是第二节,主要讲述元素周期律,承载着实现本章教学目标的任务。
为了更好地教学,下面我将从课程标准、教材分析、教学目的和核心素养、教学重难点、学情分析、教学准备、教学方法、教学过程等方面进行说课。
一、说课程标准。
普通高中化学课程标准(2017版2020年修订):【内容要求】“ 3.1 原子结构与元素周期律:结合有关数据和实验事实认识原子结构、元素性质呈周期性变化的规律,建构元素周期律。
知道元素周期表的结构,以第三周期的钠、镁、铝、硅、硫、氯,以及碱金属和卤族元素为例,了解同周期和主族元素性质的递变规律。
体会元素周期律(表)在学习元素化合物知识与科学研究中的重要作用。
”二、说教材。
本课是人教版化学必修1第四章《物质结构元素周期律》第二节内容,“元素周期律”是高中化学必修课程中的核心内容之一,是高中一年级学习的重点内容。
本节要在初中知识的基础上进一步加深学习周期表中同周期元素的性质变化规律。
人们从微观角度探索元素之间的内。
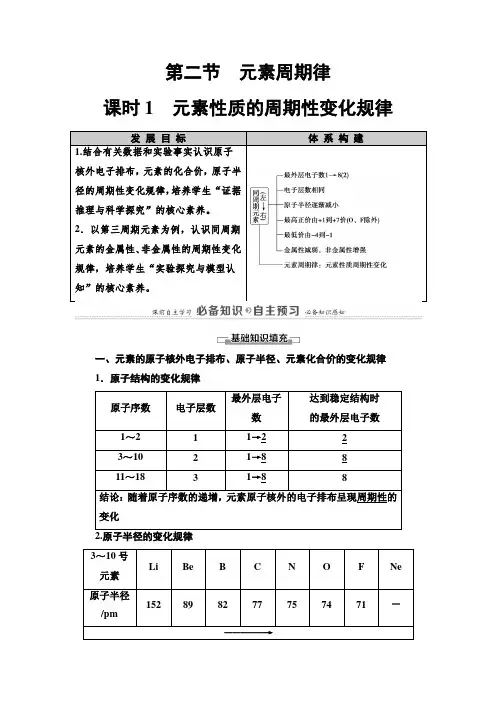
第二节元素周期律课时1元素性质的周期性变化规律发展目标体系构建1.结合有关数据和实验事实认识原子核外电子排布,元素的化合价,原子半径的周期性变化规律,培养学生“证据推理与科学探究”的核心素养。
2.以第三周期元素为例,认识同周期元素的金属性、非金属性的周期性变化规律,培养学生“实验探究与模型认知”的核心素养。
一、元素的原子核外电子排布、原子半径、元素化合价的变化规律1.原子结构的变化规律原子序数电子层数最外层电子数达到稳定结构时的最外层电子数1~2 1 1→2 23~10 2 1→8 811~18 3 1→8 8结论:随着原子序数的递增,元素原子核外的电子排布呈现周期性的变化3~10号元素Li Be B C N O F Ne 原子半径/pm152 89 82 77 75 74 71 -―――――→逐渐减小11~18号元素Na Mg Al Si P S Cl Ar 原子半径/pm186 160 143 117 110 102 99 -变化趋势―――――→逐渐减小结论:随着原子序数的递增,元素原子的半径呈现周期性变化原子序数主要化合价的变化1~2 +1―→03~10+1―→+5-4―→-1―→011~18+1―→+7-4―→-1―→0结论:随着原子序数的递增,元素的主要化合价呈周期性变化二、第三周期元素性质的递变1.钠、镁与水的反应钠镁实验操作实验现象钠熔成小球,浮于水面,四处游动,有“嘶嘶”的响声,反应后溶液加酚酞变红加热前,镁条表面附着了少量无色气泡,加热至沸腾后,有较多的无色气泡冒出,滴加酚酞溶液变为粉红色反应原理2Na+2H2O===2NaOH+H2↑Mg+2H2O=====△Mg(OH)2↓+3(1)实验探究:①向AlCl3溶液中加入足量氨水,现象为产生白色沉淀,反应的离子方程式为Al3++3NH3·H2O===Al(OH)3↓+3NH+4。
②将①实验得到的沉淀分装两支试管中,一支试管中加入盐酸,现象为白色沉淀逐渐溶解,离子方程式为Al(OH)3+3H+===Al3++3H2O;另一支试管中加入NaOH溶液,现象为白色沉淀逐渐溶解,离子方程式为Al(OH)3+OH-===AlO-2+2H2O。








