烷烃和环烷烃
- 格式:docx
- 大小:10.86 KB
- 文档页数:1


鉴别烷烃和环烷烃的方法一、前言烷烃和环烷烃是有机化合物中的两个重要类别,它们在实际应用中具有不同的特性和用途。
因此,正确鉴别烷烃和环烷烃对于化学工作者来说非常重要。
本文将介绍一些常见的鉴别方法。
二、外观1. 环状结构环状结构是环烷烃的一个显著特征。
环状结构使得环烷烃分子相对于线性分子更加紧密,因此其密度更大。
此外,在光学显微镜下观察样品时,环状结构会表现出圆形或椭圆形的形态。
2. 分子大小由于分子量不同,同样数量的分子量下,环状分子比线性分子更大。
因此,在实验中可以通过测量样品的密度或比表面积来区分两者。
三、物理性质1. 沸点由于环形结构使得其相互作用力增强,因此在相同条件下,环形化合物沸点通常较高。
2. 溶解度由于环形结构使得其相互作用力增强,在某些溶剂中(如水),环形化合物的溶解度可能会降低。
四、化学性质1. 氧化反应由于环状结构相对于线性结构更加稳定,因此在氧化反应中,环状分子通常比线性分子更难被氧化。
2. 反应活性由于环状结构使得其相互作用力增强,因此环状分子通常比线性分子具有更高的反应活性。
例如,环烷烃可以通过加氢反应转化为相应的烷基化合物。
五、色谱法色谱法是一种常用的鉴别方法。
在气相色谱中,可以通过样品在某些固定条件下从某个固定位置到达检测器的时间来区分两种不同类型的分子。
由于两者具有不同的物理和化学特征,因此它们在某些条件下会表现出不同的行为。
六、核磁共振法核磁共振是一种非常灵敏和精确的方法。
通过观察样品中不同原子核所发射出来的信号来确定样品中不同类型分子所占比例。
由于两种类型的分子具有不同的原子排列方式,因此它们会表现出不同的核磁共振信号。
七、总结鉴别烷烃和环烷烃的方法有很多种。
在实际应用中,我们可以根据不同的需要选择不同的方法。
总体来说,通过观察样品的外观、物理性质和化学性质,以及使用色谱法和核磁共振法等高级方法,我们可以准确地区分两种不同类型的分子。

烷烃烷烃即饱和烃(saturated group),是只有碳碳单键的链烃,是最简单的一类有机化合物。
烷烃分子里的碳原子之间以单键结合成链状(直链或含支链)外,其余化合价全部为氢原子所饱和。
烷烃分子中,氢原子的数目达到最大值,它的通式为CnH2 n+2。
分子中每个碳原子都是sp3杂化。
最简单的烷烃是甲烷。
烷烃中,每个碳原子都是四价的,采用sp3杂化轨道,与周围的4个碳或氢原子形成牢固的σ键。
连接了1、2、3、4个碳的碳原子分别叫做伯、仲、叔、季碳;伯、仲、叔碳上的氢原子分别叫做伯、仲、叔氢。
为了使键的排斥力最小,连接在同一个碳上的四个原子形成四面体(tetrahedro n)。
甲烷是标准的正四面体形态,其键角为109°28′(准确值:arccos(-1/3))。
理论上说,由于烷烃的稳定结构,所有的烷烃都能稳定存在。
但自然界中存在的烷烃最多不超过50个碳,最丰富的烷烃还是甲烷。
由于烷烃中的碳原子可以按规律随意排列,所以烷烃的结构可以写出无数种。
直链烷烃是最基本的结构,理论上这个链可以无限延长。
在直链上有可能生出支链,这无疑增加了烷烃的种类。
所以,从4个碳的烷烃开始,同一种烷烃的分子式能代表多种结构,这种现象叫同分异构现象。
随着碳数的增多,异构体的数目会迅速增长烷烃还可能发生光学异构现象。
当一个碳原子连接的四个原子团各不相同时,这个碳就叫做手性碳,这种物质就具有光学活性。
烷烃失去一个氢原子剩下的部分叫烷基[1],一般用R-表示。
因此烷烃也可以用通式RH来表示。
烷烃最早是使用习惯命名法来命名的。
但是这种命名法对于碳数多,异构体多的烷烃很难使用。
于是有人提出衍生命名法,将所有的烷烃看作是甲烷的衍生物,例如异丁烷叫做2-一甲基丙烷。
现在的命名法使用IUPAC命名法,烷烃的系统命名规则如下:找出最长的碳链当主链,依碳数命名主链,前十个以天干(甲、乙、丙、丁、戊、己、庚、辛、壬、癸)代表碳数,碳数多于十个时,以中文数字命名,如:十一烷。


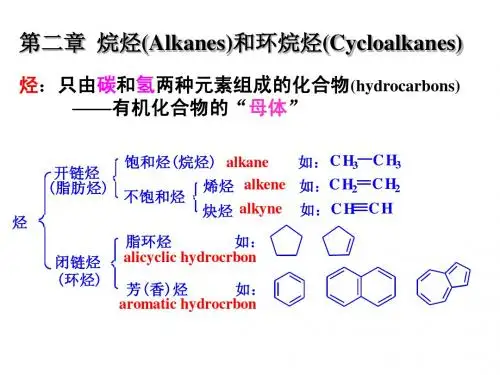
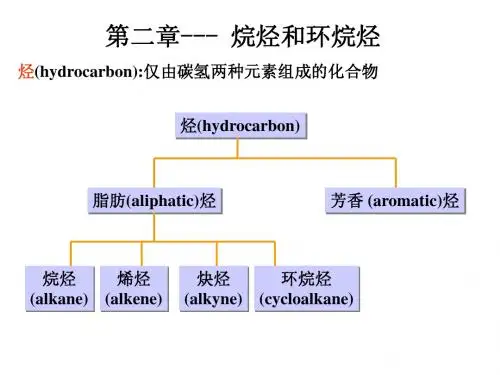


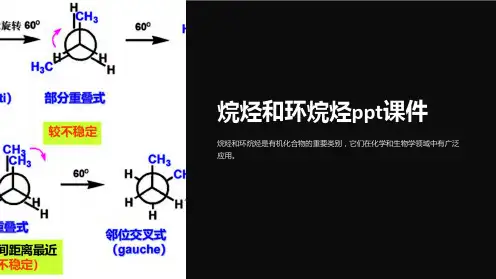
烷烃、环烷烃烷烃烷烃即饱和烃(saturated group),是只有碳碳单键的链烃,是最简单的⼀类有机化合物。
烷烃分⼦⾥的碳原⼦之间以单键结合成链状(直链或含⽀链)外,其余化合价全部为氢原⼦所饱和。
烷烃分⼦中,氢原⼦的数⽬达到最⼤值,它的通式为CnH2n+2。
分⼦中每个碳原⼦都是sp3杂化。
最简单的烷烃是甲烷。
烷烃中,每个碳原⼦都是四价的,采⽤sp3杂化轨道,与周围的4个碳或氢原⼦形成牢固的σ键。
连接了1、2、3、4个碳的碳原⼦分别叫做伯、仲、叔、季碳;伯、仲、叔碳上的氢原⼦分别叫做伯、仲、叔氢。
为了使键的排斥⼒最⼩,连接在同⼀个碳上的四个原⼦形成四⾯体(tetrahedro n)。
甲烷是标准的正四⾯体形态,其键⾓为109°28′(准确值:arccos(-1/3))。
理论上说,由于烷烃的稳定结构,所有的烷烃都能稳定存在。
但⾃然界中存在的烷烃最多不超过50个碳,最丰富的烷烃还是甲烷。
由于烷烃中的碳原⼦可以按规律随意排列,所以烷烃的结构可以写出⽆数种。
直链烷烃是最基本的结构,理论上这个链可以⽆限延长。
在直链上有可能⽣出⽀链,这⽆疑增加了烷烃的种类。
所以,从4个碳的烷烃开始,同⼀种烷烃的分⼦式能代表多种结构,这种现象叫同分异构现象。
随着碳数的增多,异构体的数⽬会迅速增长烷烃还可能发⽣光学异构现象。
当⼀个碳原⼦连接的四个原⼦团各不相同时,这个碳就叫做⼿性碳,这种物质就具有光学活性。
烷烃失去⼀个氢原⼦剩下的部分叫烷基[1],⼀般⽤R-表⽰。
因此烷烃也可以⽤通式RH来表⽰。
烷烃最早是使⽤习惯命名法来命名的。
但是这种命名法对于碳数多,异构体多的烷烃很难使⽤。
于是有⼈提出衍⽣命名法,将所有的烷烃看作是甲烷的衍⽣物,例如异丁烷叫做2-⼀甲基丙烷。
现在的命名法使⽤IUPAC命名法,烷烃的系统命名规则如下:找出最长的碳链当主链,依碳数命名主链,前⼗个以天⼲(甲、⼄、丙、丁、戊、⼰、庚、⾟、壬、癸)代表碳数,碳数多于⼗个时,以中⽂数字命名,如:⼗⼀烷。
烷烃与环烷烃的鉴别
烷烃和环烷烃是有机化合物中最简单的两种结构类型,但在实验
室中常常需要通过一系列的方法来鉴别它们。
首先,我们可以通过它们的化学式来区分。
烷烃的化学式为
CnH2n+2,而环烷烃的化学式为CnH2n。
也就是说,环烷烃相对于烷烃
来说少了两个氢原子。
其次,我们可以通过它们的物理性质来鉴别。
例如,烷烃的沸点
随碳数上升而增加,而环烷烃的沸点与其分子中的环数及分子量有关。
此外,环烷烃的密度比烷烃的密度更高,因为环状分子形成更紧密的
排列,分子间的吸引力更强。
另外,我们还可以通过光谱分析来鉴别烷烃和环烷烃。
一般来说,环烷烃的红外光谱中会出现环张缩模式、-CH2-吸收峰和骨架伸缩模式
等特征性吸收峰。
而烷烃的红外光谱中则没有这些峰。
此外,环烷烃
的质谱图中也会出现环张缩子离子的分子峰。
最后,我们还可以通过化学反应来鉴别烷烃和环烷烃。
例如,环
烷烃和烯烃经过裂解反应后会生成相应的烷烃。
此外,环烷烃和烷基
锂反应时,通常会发生开环反应,生成亚烷基锂和烷基锂等中间体。
总之,烷烃和环烷烃的鉴别需要综合运用多种方法,进行分析对比,才能得出准确的结论。
因此,在实验操作中需要谨慎认真,以确
保实验结果的准确性。
烷烃与环烷烃区别
一、结构不同
1、烷烃:是开链的饱和链烃(saturated group),分子中的碳原子都以单键相连,其余的价键都与氢结合而成的化合物。
2、环烷烃:含有脂环结构的饱和烃。
有单环脂环和稠环脂环。
含有1个脂环且环上无取代烷基的环烷烃,分子通式为CnH₂n。
二、范围不同
烷烃包括环烷烃,环烷烃是烷烃的一种。
三、性质不同
1、烷烃:低沸点(boiling point)的烷烃为无色液体,有特殊气味;高沸点烷烃为黏稠油状液体,无味;烷烃的物理性质随分子中碳原子数的增加,呈现规律性的变化;烷烃中的氢原子被卤原子(即第七主族元素)取代的反应称为卤化反应(halogenation)。
2、环烷烃:环烷烃有很高的发热量,凝固点低,抗爆性介于正构烃和异构烃之间。
化学性质和烷烃相似。
其中以五碳脂环和六碳脂环的性质较稳定。