小儿补液配制
- 格式:wps
- 大小:12.50 KB
- 文档页数:2

儿补液总量是由三部分组成的:1、一般需按累积损失量、继续损失量和生理需要量计算。
①累积损失量:指病后(如急性脱水)减轻之体重数量,这部分液体最主要。
这部分液量可根据脱水程度加以估计。
累积损失量也可按体表面积计算,轻度脱水为30-50ml/kg ,中度脱水为50-100ml/kg,重度脱水为100-150ml/kg。
②继续损失量:按实际损失补充,一般在禁食条件下为40ml/kg﹒d,非禁食状态是30ml/kg。
电解质包括钠、氯及碳酸氢离子各40mmol/L。
继续损失量也可以用口服补液盐(ORS)补充。
③生理需要量:生理需要量,即基础代谢:60-80ml/kg/day。
但是,小儿若小于10kg,通常给以补充100ml/kg/day。
2、量知道了,那么给补什么样的液体呢?累计损失量的补充:根据脱水性质来给予低渗性脱水:2/3张液体等渗性脱水:1/2张液体高渗性托说:1/3-1/5张液体注:渗透压越高,就应该给以张力越小的,以此来稀释至等渗水平,而渗透性越低,则就给以张力大的液体。
继续损失量的补充:通常给予1/3-1/2张液体生理需要量:通常给予1/4-1/5张液体补液1、轻度脱水轻度脱水的患儿,一般在给以调节饮食、药物控制外,只给予ORS,即口服补液盐补充水分,轻度脱水口服补液量约是50-80ml/kg,在8-12小时内把累积损失量补足。
脱水纠正后,将ORS等量稀释后,根据需要随意口服。
注意:ORS是2/3张液,故新生儿及有明显的呕吐、腹胀、休克、心肾功能不全的患儿不宜使用。
2、中度及重度脱水中度及重度的患儿一般采用静脉补液。
⑴第一天的补液:补液量及补液种类,在课本里已经说过了。
在这里需要强调的是:如果患儿中度脱水,出现明显的循环障碍了,那么必须先扩容,方法如下:1)用2:1等张含钠液 20ml/kg,30~60分内静脉推注或快速滴注。
2)以补充累积丢失量为主的阶段:若无微循环障碍,补液从此阶段开始,如以扩容,累积丢失量应减去扩容量。
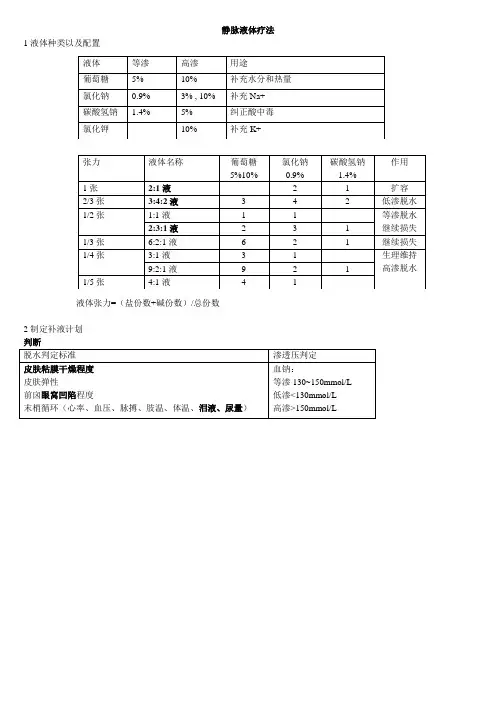
静脉液体疗法1液体种类以及配置液体张力=(盐份数+碱份数)/总份数2制定补液计划判断脱水判定标准渗透压判定皮肤粘膜干燥程度皮肤弹性前囟眼窝凹陷程度末梢循环(心率、血压、脉搏、肢温、体温、泪液、尿量)血钠:等渗130~150mmol/L 低渗<130mmol/L高渗>150mmol/L液体等渗高渗用途葡萄糖5% 10% 补充水分和热量氯化钠0.9% 3% , 10% 补充Na+碳酸氢钠 1.4% 5% 纠正酸中毒氯化钾10% 补充K+张力液体名称葡萄糖5%10% 氯化钠0.9%碳酸氢钠1.4%作用1张2:1液 2 1 扩容2/3张3:4:2液 3 4 2 低渗脱水1/2张1:1液 1 1 等渗脱水继续损失2:3:1液 2 3 11/3张6:2:1液 6 2 1 继续损失1/4张3:1液 3 1 生理维持高渗脱水9:2:1液9 2 11/5张4:1液 4 1方法一个计划:一个24小时计划二个阶段:1.补累积损失快!2.维持补液阶段(继续丢失+生理需要)慢!三个确定:定量、定性、定速四个方向:先快后慢,先盐后糖,见尿补钾,随时调整。
第一天补液累积损失量(ml/kg) 继续损失量(ml/kg)生理维持量(ml/kg)定义自发病以来累计损失的液体量继续腹泻、呕吐、脱水量排尿排便含水,出汗、皮肤不感蒸泄、肺呼吸丢失定量轻度脱水30~50 10~30(40)"丢多少补多少" 60~80发热>38°,1度增加10~15%中度脱水50~100重度脱水100~120(150)定性等渗性脱水:1/2张(1:1液,3:2:1液)低渗性脱水:2/3张(4:3:2液)高渗性脱水:1/5~1/3张(生理维持液) 1/3~1/2张(1:1液,3:2:1液)1/4~1/5张(生理维持液,1:4液)定速原则:先快后慢有循环障碍:先扩容!!!20ml/kg 2:1液30’~1h或者1.4% 氢氧化钠其余:8~12h内完成补完累积损失后,14~16h内均匀滴入A计划补液过程中,先输入1/2看情况随时调整输液后3-4小时排尿表明血容量开始恢复,故要观察和记录输液后首次排尿时间,尿量.于补液24小时皮肤弹性恢复和眼窝凹陷,说明脱水已被纠正。

儿科补液tianya×iayi一、先记住几个重要的公式:1gNaCl=17mmolNa 1mmolNa=6ml %NaCl⑴5% NaHCO3ml=22 –测得的HCO3ˉ体重kg 有写=22 –测得的HCO3ˉ体重kg 5%SB 1ml=补碱的mmol数=-BE W kg即5%SB ml=-BEWkg先给1/2量机体有代偿调节功能,一般无需补足全量碱性液即可纠正酸中毒,故首次可先补1/2计算量,以后根据病情调整用量,注意“宁酸勿碱”.估算法:暂按提高血浆HCO3ˉ5mmol/L,计算给5%SB 5ml/kg次乳酸钠3ml/kg;⑵25%盐酸精氨酸ml=测得HCO3ˉ-27mmol/LWkg⑶需补钾量mmol=4-测得血钾体重kg 1mmol K= %KCl⑷需补钠量mmol=140-测得血钠体重kg女性为⑸需补水量ml=测得血钠值-140体重4kg⑹渗透压公式:mOsm/L=2Na++GLU+BUN单位均为mmol/L或 2 Na++10 式中的10代表血浆中未测定的阳离子大约数,“×2”表示血浆中另一半未测定的阴离子;这里顺便说一下:GLUmg/dl/18=GLUmmol/L BUNmg/dl/=BUNmmol/L二、需要注意和记住的基本问题1、张力与渗透压的概念要分清:渗透压指溶质对水的吸引能力;张力指溶液在体内维持渗透压的能力;一般情况下,张力与渗透压相等,溶液的分子浓度在正常的渗透压范围内为一个张力等张力,如正常渗透压的1/2则为1/2张力;5%GS可认为接近等渗和10%GS高渗,由于Glucose在体内很快被氧化成H2O和CO2,供给机体水和热量,而不能维持渗透压,故是无张力的溶液;判断某溶液的张力,是以它的渗透压与血浆渗透压正常值280~320 mOsm/L,计算时取平均值300mOsm/L相比所得的比值,它是一个没有单位但却能够反映物质浓度的一个数值;稀释定律:稀释前浓度×稀释前体积=稀释后浓度×稀释后体积;即:C1×V1=C2×V2;并且强调但凡涉及物质浓度的换算,均遵循此定律;2、计算补液总量:轻度脱水:90~120ml/kg;中度脱水:120~150ml/kg;重度脱水:150~180ml/kg.3、补充低渗性脱水累积损失量:用2/3张的 4:3:2液4份盐:3份糖:2份碱4、补充等渗性脱水累积损失量、补充各种脱水继续损失量:用1/2张的3:2:1液3份糖:2份盐:1份碱5、记住——盐:碱始终为2:1这里“碱”指的是%SB这样一来才与血浆中的钠氯之比相近,以免输注过多使血氯过高,造成高氯性酸中毒;糖为5%~10%的GS,盐为NS%NaCl,碱为5%NaHCO3稀释为%NaHCO3方法:5%碱量除以4,剩下的用糖补足;例如:100ml5%碱稀释为%碱:100/4=25,100-25=75,即为25ml5%碱+75ml糖注意:应扣除补液中所用的碱性液量;6、补钾:每100ml液体量中10%KCl总量不超过3ml,使钾浓度小于千分之三;7、扩容:2:1等张含钠液2份盐:1份碱按20ml/kg计算,30min内滴完;注:重度脱水患儿首批输液应按20ml/kg-原因是:因重度脱水如失水100ml/kg,血浆水便占1/5,即20ml/kg现代儿科液体疗法2002 邓静主编8、累积损失量在第一个8小时补足,为1/2总量;9、体温每升高10C,应增加液量约10ml/kg;10、5%GNS 是指此溶液中每100ml中含有5g葡萄糖和0.9g氯化钠;其实5%GNS是高渗溶液,但是它却是等张溶液,应用时一定要注意这一点啊许多人可能都忽略了这一点啊5%GS是等渗液,但葡萄糖输入人体后,很快被代谢,供给能量,分解成水和CO2,失去了渗透压的性质,所以一般不计算其张力;只有生理盐水能维持此溶液的渗透压作用;三、液体疗法用于脱水要注意的问题液体疗法多用于脱水,儿科的特点就是小儿易脱水,所以从某种意义上说,液体疗法就是针对脱水而言的;脱水分轻中重,有等渗,低渗,高渗之别;具体标准书中都有,这里只是明确实际中10个问题;1. 判断脱水以及其程度是根据临床症状和体征而不是体重减少的程度;脱水性质依靠的是血钠浓度;2. 儿科查看脱水:精神、囟门、眼眶、眼泪、口干程度、口腔津液、尿量、皮肤粘膜情况、呼吸心率;这些是重点对象;3. 不要把肥胖儿的脱水程度估计过轻,也不要把营养不良的病儿估计过重;4. 低渗脱水,血钠<120mmol/L,不论原因,均要迅速提高血钠水平,常用3%氯化钠,12ml/kg可提高血钠10 mmol/L;5.高渗性脱水是没有循环血量不足的情况出现的,对此的补液,不能急于求成而直接使用低渗溶液,这样做反而会使细胞内水肿;正确的做法是仍给于等张的2:1溶液扩容,而后再渐渐下降张力,使其过程有个梯度;6. 扩容一定要及时足量;特别是伴有休克的小儿,扩容是液体治疗的关键,第一步不成功,那补液方案全盘皆输;2:1溶液是经典扩容液、10~20ml/kg是标准量、20ml/是速度、~1小时扩容成功是生命关;扩容就像抢救农药中毒一样,力求快速阿托品化;那么达到扩容化的指标是什么呢面部转红、呼吸平稳、心率较前下降或至正常、皮肤弹性上升干燥度减轻、哭声有力、出现小便、血压上升;这些就是指标;对于一次扩容不成功的,不要拘于20ml/kg的量,再次评估后再次扩容,所有这一切都是为了一个目标:扩容成功;7. 补液计划要制定;做到定量、定性、定速;一般情况下可以先制定计划的前半部,就是扩容和补充累积损失量;因为这前半部补充成功,后面的补钾才能进行;补液计划不是定下来就不变的,随时要根据病情发展情况进行修改;累积损失量:轻度脱水 30~50ml/kg 中度 50~100ml/kg 重度 100~120 ml/kg,可以先给2/3的量;液体性质:低渗脱水 2/3张~等张、等渗脱水 1/2~2/3张、高渗 1/3~1/5张;暂难明确性质的,先按等渗脱水处理;速度:在8~12小时内给予,先快后慢,开始半小时20ml/kgh,以后8~10 ml/kgh;低渗脱水可稍快,高渗脱水要稍慢;8. 及时补充钾和钙;见尿补钾谁也不能违反;不要忽视了补钙,特别是原来就有缺钙指征的小儿,在扩容纠酸后,低钙就会明显表现出来,所以要早期补充,并不一定要见尿补钙;9. 纠酸:脱水肯定伴有酸中毒;轻度脱水有轻度酸中毒,重度脱水就有重度酸中毒;纠酸的依据是血气分析,所需5% SB 的量,依据的是血气分析中的BE值;计算方法:所需5%SB的ml数=BE-3××体重×;然后配成%,先给予半量,得查血气分析后再作余量的定夺;没有血气分析的可根据酸中毒症状的轻重,给予5%SB 3~5ml/kg;这种方法现已淘汰了,只是不得已而为之;在治疗脱水时,血气分析和快速血电解质分析,这两项检查是必须的,可惜的是基层几乎没有这两项;10. 不要忽视口服补液的重要性;能口服就口服,口服补液是最安全的四、液体疗法基本原则“一、二、三、四”一个计划一个24小时计划二个步骤补充累积损失量,维持补液;三个确定定量,定性,定速度和步骤;四句话先快后慢,先盐后糖 ,见尿补钾,随时调整;静脉输液适用于中重度脱水及呕吐者;轻度至中度失水,无呕吐者可以口服补液;中度至重度脱水必须静脉补液;输液双三原则三定:定输液量、定输液种类、定输液速度;三先:先快后慢,先盐后糖、先浓后淡;第一个24h ml/kg不同脱水程度的输液量轻度中度重度累积损失量 50 50-100 100-120继续损失量 10-20 10-30 10-30生理需要量 60-80 60-80 60-80总输液量 90-120 120-150 180-200三定原则“一”定补液量轻30-50m l/k g累积损失量脱水程度中50-100m l/k g重100-120m l/k g继续损失量丢多少补多少腹泻病10-40m l/k g/d生理需要量基础代谢60-80m l/k g/d a y三定原则“二”定液体性质等渗:2:3:1溶液1/2张累积损失量脱水性质低渗:4:3:2溶液2/3张高渗:2:6:1溶液1/3张继续损失量丢什么补什么腹泻1/3-1/2张生理需要量生理需要1/4-1/5张溶液三定原则“三”定补液速度和步骤第一步:补充累积损失量8-12小时内,8-10m l/k g/h 轻中度脱水分二步第二步:维持补液继续损失量+生理需要量12-16小时内,5m l/k g/h脱水程度第一步:扩容阶段2:1等张含钠液%碳酸钠液20m l/k g总量<300m l,30-60分钟内滴完重度脱水分三步第二步:补充累积损失量应减去扩容量,余同上第三步:维持补液同上电解质的补充1、钠2、钾3、钙纠正酸碱平衡紊乱补充碱剂纠正酸中毒1、按公式计算2、按提高5m m o l/L C O2C P计算四、熟悉常用液体的种类、成分及配制注射用水是禁忌直接由静脉输入的,因其无渗透张力,输入静脉可使RBC膨胀、破裂,引起急性溶血;1非电解质溶液:常用的有5%GS和10%GS,主要供给水分由呼吸、皮肤所蒸发的不显性丢失及排尿丢失的和供应部分热量,并可纠正体液高渗状态,但不能用其补充体液丢失;5%GS为等渗溶液,10%GS为高渗溶液,但输入体内后不久葡萄糖被氧化成二氧化碳和水,同时供给能量,或转变成糖原储存于肝、肌细胞内,不起到维持血浆渗透压作用;注:10%GS 比5%GS供给更多热量,虽其渗透压比5%GS高1倍,如由静脉缓慢滴入,Glucose迅速被血液稀释,并被代谢,其效果基本与5%GS类似;Glucose 输入速度应保持在-0.85gkgh,即8-14mg/kgmin;2电解质溶液:种类较多,主要用于补充损失的液体体液丢失、电解质和纠正酸、碱失衡,但不能用其补充不显性丢失及排稀释尿时所需的水;1生理盐水%氯化钠溶液:为等渗溶液,常与其他液体混合后使用,其含钠和氯量各为154mmol/L,很接近于血浆浓度142mmol/L,而氯比血浆浓度103mmol/L高;输入过多可使血氯过高,尤其在严重脱水酸中毒或肾功能不佳时,有加重酸中毒的危险,故临床常以2份生理盐水和1份%NaHCO3混合,使其钠与氯之比为3:2,与血浆中钠氯之比相近;生理盐水主要用于补充电解质,纠正体液中的低渗状态;2:1等张液与生理盐水功用相同,但无NS之弊,临床常用于严重脱水或休克时扩张血容量;2高渗氯化钠溶液:常用的有3%NaCl和10%NaCl,均为高浓度电解质溶液,3%NaCl 主要用以纠正低钠血症,10%NaCl多用以配制各种混合液;3碳酸氢钠溶液:可直接增加缓冲碱,纠正酸中毒作用迅速,是治疗代谢性酸中毒的首选药物但有呼吸功能障碍及CO2潴留倾向者应慎用,%溶液为等渗液,5%溶液为高渗液;在紧急抢救酸中毒时,亦可不稀释而静脉推注;但多次使用后可使细胞外液渗透压增高;4氯化钾溶液:常用的有10%氯化钾和15%氯化钾溶液两种;均不能直接应用,须稀释成%~%溶液静脉点滴,含钾溶液不可静脉推注,注入速度过快可发生心肌抑制而死亡;5林格氏液等张液:含%NaCl,%KCl,%CaCl2,% NaHCO3;3混合溶液:为适应临床不同情况的需要,将几种溶液按一定比例配成不同的混合液,以互补其不足,常用混合液的组成及配制见以下几种常用混合液的简易配制:几种混合液的简便配制 ml溶液种类 5%10%GS 10%NaCl 5%SB1:1液 500 201:4液 500 102:1液 500 30 472:6:1液 500 10 162:3:1液 500 15 254:3:2液 500 20 33注:为了配制简便,加入的各液量均用整数,配成的是近似的液;2:6:1液 500 10 162:3:1液 500 15 254:3:2液 500 20 332:6:1液 100 2 32:3:1液 100 3 54:3:2液 100 4 7液体 G S 盐 5%SB 张力2∶3∶1 100 3 5 1/24∶3∶2 100 4 6 2/32∶1 100 7 9 等张1∶1 100 5 1/21∶4 100 2 1/51/3张液 100 3 1/31/4张液 100 1/4混合液组成及用途5%GS %NaCl %SB 渗透压用途2:1含钠液 2 1 等张重度脱水扩容酸2:3:1溶液 3 2 1 1/2张等渗性脱水4:3:2溶液 3 4 2 2/3张低渗性脱水2:6:1溶液 6 2 1 1/3张高渗性脱水混合液配制举例手写1:1液指N S及G S各1份,为1/2张液,用于没有明显碱中毒及酸中毒的呕吐脱水;1:4液指N S1份,G S4份,为1/5张液,用于补充生理需要量;举例患儿,男,1岁,发育正常,诊断秋季腹泻;PE:眼凹深陷,皮肤干燥,哭时无泪,尿少脉速;根据病史,眼凹,皮肤弹性、循环情况、尿量等指标判断:重度低渗性脱水;1岁发育正常估计体重10kg输液总量:18010=1800ml,其中扩容2010=200ml,累积损失量1800/2-200=700补1/2总量在9-10h内输入总量的1/2,其余1/2量在13-14h内输入;输液步骤:第一步扩容210/3=70ml,702=140ml盐,70ml碱%NaHCO3相当于70/4= 5%NaHCO3和= GS第二步补累积损失量700ml的4:3:2液,700/9=,804=320ml盐,803=240糖,802=160碱%NaHCO3相当于160/4=40ml 5%NaHCO3和160-40=120mlGS 第三步补继续损失量和生理需要量=890-900ml的3:2:1液,900/6=150,1503=450糖,1502=300ml盐,150ml碱%NaHCO3相当于150/4= 5%NaHCO3和= GS +450= GS 第四步见尿补钾:10%KCl 15ml.五、小儿补液目的1 调节循环系统液体量生理需要量,累积损失量, 额外损失量2 纠正电解质酸碱平衡紊乱 PH,K+,Na+ ,Clˉ,Ca2+, HCO3ˉ胶体渗透压静脉输液的目的液体疗法的目的是纠正体内已经存在的水及电解质紊乱,恢复和维持血容量,渗透压,酸碱平衡和电解质成分的稳定,使机体进行正常的生理功能;关键一、液体量:影响因素:修复,生长发育;术后低蛋白血症;新陈代谢旺盛,需水量多;体温每升高10C----------液体量增多10%日需量:10kg 10kg 10kg100ml 50ml 20ml每100ml液体: 10%glucose 80ml % 20ml 10%KCl术后当天液体量为需要量的70% ,应包含止血,抗感染,维生素等若术中检查或术后钾低则可立即补钾,否则……一般术后第一天开始补钾禁饮食者术后第一天补全量累积损失量:脱水程度及脱水性质相关如:轻度中度重度5%体重 5-10 10-15新生儿因为其血液中H+ Cl- Na+ K+ P均高HCO3ˉ低,7天后K+才趋于正常;所以:1 24小时内不需补液,除外外科疾病2 3天内代谢较低,补液量为60-100ml/kg3 7天后补液量可增至100-120ml/kg4 4天内不补Na+ Cl- 可补NaHCO3 和、7天内不补K+5 1-2天内不补电解质二、能量:0~1岁 100kcal/kg 以后每增加三岁能量需要量低减10kcal/kg三、电解质1. 应该补充的等渗含钠液量=正常值-测量值体重4一般而言,开始只补充一半量, 再酌情继续补充2. 低钾时应该补充的等渗含钾液量=正常值-测量值体重一般而言,开始只补充一半量, 再酌情继续补充3. 10%葡萄糖酸钙 kgd输血后常规要补钙 10%葡萄糖酸钙 1ml/100ml血4. 25%硫酸镁次成人4~10ml/次1~2次/周用5% %GS稀释成1%浓度后缓慢静滴;四输液速度婴幼儿7~9ml/kgh2gtt/min心衰<6ml/kgh休克约18~20ml/kgh成分,输液速度重度或中度脱水伴外周循环不良者,先用等张2:1液2份%氯化钠:1份%碳酸氢钠或1/6M乳酸钠20 ml /kg,于30min至1h静脉输入;扩容后根据脱水性质采用不同液体80~100ml/kg,继续静脉输液纠正累积损失;等渗与低渗脱水,速度可快些按8~10ml/kgh,一般8~12h补足累积损失量;高渗脱水则需要慢些,于48h补足累积损失量,防止补液过快出现脑水肿;六、介绍常用的静脉补液方法“4:3:2”补液法4份%生理盐水:3份10%葡萄糖:2份%碳酸氢钠或1/6M乳酸钠;1.等渗脱水补充累积损失:轻度 4:3:2溶液30~50ml/kg,于8~12h静滴;中度 4:3:2溶液50~100ml/kg,于8~12h静滴;重度先给2:1液20ml/kg,于30分钟~1h内静脉输入,以扩充血容量;继以4:3:2溶液80~100ml/kg,于8~12h输入2.低渗脱水纠正累积损失:多见于合并营养不良Ⅱ0~Ⅲ0的患儿,这类患儿体弱心功能差,因此纠正累积损失总量要少、浓度要高、速度要慢;轻度 4:3:2溶液30~50ml/kg,8~12h输入;重度及中度先给2:1液20ml/kg,于30分钟~1h输入,以便快速恢复血容量;继给2:1液20ml/kg4:3:2液40ml/kg 10~12h输入;3. 纠正低钠血症水中毒:不伴脱水,血钠低于130mmol/L;症状表现:细胞内水肿,可有惊厥,昏迷,颅压增高,肌肉松弛,腱反射降低,腹胀,尿少或无尿;可按下述方法纠正:用3%氯化钠12ml/kg能把血钠提高10mmol/L,宜缓慢VD,在1h以上,将血钠提高>120mmol/L,症状缓解后,病人出现大量利尿,可继续输入2/3-等张含钠液,直至累积损失被纠正,脱水症状消失;仍不好再加6ml/kg;如用%氯化钠40ml/kg,能把血钠提高10mmol/L4.高渗性脱水纠正累积损失:高渗脱水,脱水征表现较轻,一般显示轻~中度脱水;高渗脱水不能用单纯葡萄糖液纠正,否则会引起脑细胞水肿,诱发颅内高压,发生惊厥,甚至死亡;因此,所输液体张力不能过低,速度不能过快,要供给适量钾,既可适当提高所输液体的渗透压,又不增如钠负荷,而且钾还可进入细胞内,有利于细胞内脱水的纠正;采用1/3~1/4张液,一般用1/3张“2:6:1”2份%氯化钠:6份5%葡萄糖:1份%碳酸氢钠或1/6M克分子浓度乳酸钠,于48h纠正累积损失;具体按每日1/2的累积损失量加当日生理需要量补充:笫一日2:6:1溶液40~50ml/kg + 含钾维持液90ml/kg,速度5~7ml/kgh;第二日2:6:1溶液40~50ml/kg + 含钾维持液90ml/kg,速度5~7ml/kgh;5.高钠血症盐中毒的治疗:此类病儿体内水不少,钠显着增多,钾减少,钙也减少;治疗重点在补充水分和利尿,以清除钠,并要适量补充钾和钙;可用速尿1mg/kg次,po,im or. VD,1~2次/d,促进体内钠的排出;可口服补充水分,150ml/100cal/kgd,KC1 3~4mmol/kgd;如需输液,可将口服不足之量以5%葡萄糖稀释3~4倍的“2:1”液,以4~6ml/kgh的速度缓慢静脉输入,并按上述方法补充氯化钾;为了纠正低钙血症,可口服乳酸钙0.5g.Tid,输液期间可加用10%葡萄糖酸钙 10ml/次,稀释1倍静脉滴入,同时服用适量VitD;输液过程中要密切观察患儿的脉搏、呼吸,必要时测血压;如脉搏增快、血压增高,反映输液过快,导致脑水肿;应减慢速度,防止惊厥,如已惊厥立即注射镇静剂;6.纠正酸中毒:纠正代谢性酸中毒按以公式计算:50- 现测得的二氧化碳结合力容积%××体重kg=5%碳酸氢钠ml或50 –现测得的二氧化碳结合力容积%××体重kg=1/6M乳酸钠ml腹泻所引起的代谢性酸中毒一般经以上液体疗法即能与脱水同时纠正;对有些重度酸中毒,可考虑另加5%碳酸氢钠5ml/kg,提高二氧化碳结合力10容积% ;七、如何纠正电解质及酸碱平衡紊乱静脉补钾的原则10%kcl 1ml= 1mmol K= %KCl一、尿量时机要求尿量每小时在30ml以上;也就是医学上常说的见尿补钾即有尿或来院前6h 内有尿,就开始补钾;二、浓度静脉滴注液含钾浓度一般不超过%,即500ml加入10%氯化钾不能超过15ml即每升输液中含钾量不宜超过40mmol;浓度高可抑制心肌,且对静脉刺激甚大,病人不能忍受,并有引起血栓性静脉炎的危险.氯化钾禁止静脉推注;三、速度氯化钾进入血液,须经15h左右方可建立细胞内外平衡,成人静脉滴入速度每分钟不宜超过60滴;缓慢滴注,成人:输入钾量应控制在20mmol/h以下;小儿<kgh 四、总量每天补钾总量要正确估计;补钾总量:婴儿3~4mmol/kgd~0.3g./kgd儿童2~3mmol/~0.2g/ 1/2静脉 1/2口服.静脉滴注时间不应短于6~8小时;补钾量一般为200~300mg /kgd;对一般禁食而无其他额外损失者可给10%氯化钾溶液20~30ml/d;不严重缺钾时,24h补钾也不宜超过6~8g10%氯化钾10ml为1g,但特殊情况例外;五、时间:每日静脉补钾量应分在整日的静脉输液中滴入,时间不得短于8h;不得静脉推注;六、疗程:补钾应持续4~6天,不需静脉者可改用口服补充注:当低钾伴有碱中毒时,常伴有低氯,故采用氯化钾液补充可能是最佳策略;现代儿科液体疗法中讲述:补钾应本着“四不宜”原则,即:①不宜过早,应“见尿补钾”;②不宜过多,氯化钾一般不超过每日0.3g/kg,一日总量不超过6g;③不宜过浓,一般不超过%;④不宜过快,每日补钾量的静滴时间最好为12~24h,如果病情危急,必须快速输入,年长儿每日补钾量的静滴时间也不应短于8h,而且应用心电图和测定血钾进行监护;在一般情况下,最好将每日补钾量的一部分口服给药,一部分由静脉补充;钙和镁的补充:■在补液过程中如出现惊厥等低钙症状时,可给10%葡萄糖酸钙5~10ml/次,用5~10%葡萄糖溶液稀释后静滴,疗程5天;■若用钙剂无效应考虑低镁可给25%硫酸镁kg/次,深部肌肉注射,每6小时1次,每日3~4次,症状缓解后停用;静脉补钙时注意事项 :①推注速度不能快,边推边听心率,过快可引起呕吐、心率减慢;甚至心脏停搏;②钙剂不能漏到血管外,否则会引起局部组织坏死,留下疤痕;③不能与碳酸氢钠同时使用,因其可使血中钙离子浓度降低;④不能与洋地黄同时使用,必须使用时两药需间隔至少4h 以上;⑤不能与输血浆及输全血同时进行,因血浆蛋白越高,则血中可弥散钙越少,钙离子亦相应减少而加重惊厥;代谢性碱中毒:用盐酸精氨酸静滴,剂量取决于碱中毒严重情况、年龄、体重和临床状况等因素;可下列公式计算剂量:即25%盐酸精氨酸ml=测得HCO3ˉ-27mmol/L 体重kg,加入葡萄糖中稀释后缓慢静滴;每支5g:20ml1份SB+2-3份GS5% NaHCO3 4张 %NaHCO3 1张,书上写张5/=17mmol Na+相当于1g钠盐;成人每天正常需要量4.5g代谢性酸中毒:纠正1使用混合液2重度酸中毒可按以下公式计算5% NaHCO3ml=22 –测得的CO2CP 体重kg 有写=22 –测得的CO2CP体重kg 5%SB 1ml=补碱的mmol数=-BE W kg即5%SB ml=-BEWkg先给1/2量机体有代偿调节功能,一般无需补足全量碱性液即可纠正酸中毒,故首次可先补1/2计算量,以后根据病情调整用量,注意“宁酸勿碱”.3估算法:无条件测定血酸碱情况,可先暂按提高血浆HCO3ˉ5mmol/L,计算给5% SB 5ml/kg次乳酸钠3ml/kg次;注意:补碱时应扣除补液中所用的碱性液量;代谢性酸中毒用碱性液的指征有二:实用儿科学7版1.HCO3ˉ丢失过多或肾小管排酸障碍,不能产生新的HCO3ˉ所致的代酸;2.无论何种病因,只要酸中毒严重,适当用碱性液纠正,可争取抢救时间,以便弄清病因,进一步进行治疗;一般主张PH<时,才是应用碱性液的指征,使PH纠正到为宜;多数情况下碱性液剂量可按每次1-2mmol/kg相当于%NaHCO3 or. 1/6mol乳酸钠溶液6-12ml/kg计算,此量约提高血HCO3ˉ3-6mmol/L,以1/2-等渗碱性液配方数小时内由静脉滴注;根据病情需要,可重复给药;备注以腹泻所引起的脱水、代谢性酸中毒为例,酸中毒并非单纯由粪便丢失HCO3ˉ所致,脱水时,肾及组织循环不良可引起酸性代谢产物堆积及高乳酸血症,饥锇可致酮症,均是引起代谢性酸中毒的原因,因此病人的AG值可正常也可增高,病儿用3:2:1或3:4:2等纠正脱水,代谢性酸中毒可同时被纠正;因上述液体可补充粪便中HCO3ˉ丢失;可扩充血容量,改善肾循环,使体内堆积的酸性代谢产物从尿排出,组织循环恢复,溶液含有葡萄糖能供给热卡,使体内酮体及乳酸能进一步被代谢,根据血HCO3ˉ或CO2-CP 用上述公式计算出所需的NaHCO3予以补充,有可能会引起高钠血症或代谢性碱中毒;纠正酸中毒的同时,应注意同时纠正水、电解质紊乱;如纠正低血钾和低血钙,如严重腹泻造成的酸中毒时由于细胞内K+内流,往往掩盖了低血钾,补碱纠正酸中毒后,K+又返回细胞内,可明显地出现低血钾;酸中毒时游离钙增多,酸中毒纠正后,游离钙明显减少,有时可出现手脚抽搐,因为Ca2+与血浆蛋白在碱性条件下可生成结合钙,使游离钙减少,而在酸性条件下,结合钙又可离解为Ca2+与血浆蛋白,使游离钙增多;H+Ca2++血浆蛋白结合钙OH-高血钾的治疗:快速静脉用NaHCO1-3mmol/kg, +RI-1g Glucose/kg,每3g3Glucose+1u RI多用10%GS沙丁胺醇5ug/kg,经15min静脉应用or. 雾化吸入常能有效地降低血钾,并能持续2-4h;10%葡萄糖酸钙缓慢IV2-10min以上;摘自六版儿科学七、脱水的处理脱水时的液体疗法:小儿易发生脱水;注意观察精神、眼泪、尿量、口渴、皮肤粘膜、眼窝、前囟、皮温及休克征;尿少、皮肤苍白弹性差、明显口渴为中度脱水;出现淡漠、昏迷、休克表现为重度脱水;补液总量:轻度失水:90-120ml/kgd中度失水:120-150 ml/kgd重度失水:150-180 ml/kgd第一阶段:扩容头8小时,补1/2总量速度为:10ml/kg hr等渗性脱水用1/2张2 : 3 : 1液NS : 5%GS : %SBSB为NaHCO3低渗性脱水用2/3张4 : 3 : 2液NS : 5%GS : %SB高渗性脱水用1/3张2 : 6 : 1液NS : 5%GS : %SB重度脱水者用2 : 1液NS : %SB 等张液10-20 ml/kg于半小时内快速扩容第二阶段:补累积损失量后16小时,补1/2总量补1/3张2 : 6 : 1速度为:5 ml/kghr重度酸中毒HCO3ˉ<9mmol/L时,需要的5% NaHCO3ml=22 –测得的HCO3ˉ体重kg 给需要量的一半,滴注约4hr见尿补钾:10%KCl 3-4ml/kgd100ml溶液中10%KCl的加入量不得大于3ml 抽搐补钙:10%葡萄糖酸钙5-10ml加入等量10%GS稀释后慢推心率下降超过20次/min以上者停用;不能与西地兰同用iv or. VD,5y以上5-10ml/次,新生儿低钙血症1-2ml/kg,最大量不超过10ml/次,成人10-20ml/次,以等量25%GS稀释后IV or. +5%-10%GS 250-500ml VD 慢个别无效者考虑补镁:25%MgSO4 次 im深部肌肉注射Bid-Tid可加VitB1 50-100mg im Qd第二天补继续损失量+生理需要量生理需要量用1/4-1/5张含钠液补总原则:三定定量,定性,定速,三先先盐后糖,先浓后淡,先快后慢,见尿补钾,抽搐补钙见上举例注:先盐后糖,先浓后淡这两句是指先应用含钠液、张力高些,然后含钠液逐减,液体的张力也逐减;列始的速度可快些,然后逐步减慢;不见尿而补钾以防产生高钾血症,见尿而不补钾,可出现低钾血症;呼吸增快时,不显性失水增加 4~5倍;体温每升高1o C,不显性失水每小时增加0.5ml/kg;环境湿度大小可分别减少或增加不显性失水;体力活动增多时,不显性失水增加 30%;补液过程中,计算并记录24小时液体出入量,是液体疗法护理的重要工作内容;当然脱水的程度判断是最重要的,如果是重度丢失水分>体重的10%,则不管是高渗,低渗,还是等渗,首先按20ml/kg补充2:1等张抢救液是不变的真理,迅速扩容;另外我上面说的液体中都有钾的成分,那么补钾也要按照金标准:见尿补钾;各程度脱水的补充量同教科书;最后送个补液十六字口诀给各位同行:先快后慢,先盐后糖,先晶后胶,见尿补钾;血浆等胶体的东西一定要靠后用哦丁香园。

quote][/quote]2:3:1液—等渗性脱水—1/2张(2份生理盐水,3份5%GS,1份1.4%的碳酸氢钠)1:4液—生理维持液—1/5张(一份生理盐水,四份5%GS)此组液体加0.15%氯化钾变为1/3张液2:6:1液—低渗性脱水—1/3张(2份生理盐水,6份5%GS,1份1.4%碳酸氢钠)4:3:2液—高渗性脱水—2/3张(4份5%GS,3份生理盐水,2份1.4%碳酸氢钠)1:1液—等渗性脱水—1/2张(1份生理盐水,1份5%GS)2:1等张含钠液—脱水循环衰竭的时候用—等张液(2份生理盐水,1份1.4%碳酸氢钠)1:2液—1/3(一份生理盐水,3份5%GS)关键词:作为一个儿科医师不会补液是半个儿科医生,刚开始我不相信此话,现在体会了才觉得是对的,因为小儿的生理特点,特别是在体液分布上和成人是有很大的区别的,年龄愈小机体需水两愈大,相反年龄愈大需要水两是愈少的。
还有年龄愈小肾脏功能愈发育不完善,所以排酸排钠的能力就愈差,所以新生儿在一般输液治疗是是不输生理盐水的,原因就在这,此外由于10天以内的新生儿RBC破坏增多释放钾增多,所以不能输注钾的。
现在我将我在临床上儿科工作当中的学习经验总结如下:1.补液有“三定”即定量,定性,定速。
2.原则:先盐后糖,先浓后淡(指含钠液的张力而言),先快后慢,见尿补钾,见惊不钙,如果不理想效果要考虑缺镁。
<1>定量方面这里现在临床上的观点和理论有冲突,因为现在生活条件以及营养的不断改善,小儿体质均较好,所以在补液时比理论中定的量要偏少:比如现在临床上对于轻度脱水补液总量定在50—90毫升,中度90—120毫升,重度120—150毫升。
那么这里的总量包括累计丢量(相当于补液总量的1/2),(继续丢失量,生理需要量)也是第一天的补液量。
一般第二天脱水已基本补足,只需补充继续丢失量和生理需要量即可。
在这里要提一点特殊的情况,对于中重度脱水患儿伴有周围循环衰竭的时候我们可以静脉滴注或者推注生理盐水或者2:1等张含钠液,以每公斤体重20毫升计算,最多不超国300毫升,在半小时内输完。

儿科补液?一、先记住几个重要的公式:⑴5%NaHCO3(ml)=(22–测得的HCO3ˉ)*0.5*1.7*体重(kg)(有写0.6)=(22–测得的HCO3ˉ)*体重(kg)(5%SB1ml=0.6mmol)补碱的mmol数=(-BE)*0.3*W(kg)即5%SB(ml)=(-BE)*0.5*W(kg)先给1/2量估算法:暂按提高血浆HCO3ˉ5mmol/L,计算给5%SB5ml/kg*次OR.11.2%乳酸钠3ml/kg。
⑵25%盐酸精氨酸(ml)=[(测得HCO3ˉ-27)mmol/L]*0.5*0.84*W(kg)⑶需补钾量(mmol)=(4-测得血钾)*体重(kg)*0.6(1mmolK=0.8mlInj.10%KCl)⑷需补钠量(mmol)=(140-测得血钠)*体重(kg)*0.6(女性为0.5)⑸需补水量(ml)=(测得血钠值-140)*体重*4(kg)⑹二、需要注意和记住的问题1、计算补液总量:轻度脱水:90-120ml/kg;中度脱水:120-150ml/kg;重度脱水:150-180ml/kg.2、补充低渗性脱水累积损失量:用2/3张的4:3:2液(4份盐:3份糖:2份碱)3、补充等渗性脱水累积损失量、补充各种脱水继续损失量与生理需要量:用1/2张的3:2:1液(3份糖:2份盐:1份碱)4、记住——盐:碱始终为2:1(这里“碱”指的是1.4%SB)这样一来才与血浆中的钠氯之比相近,以免输注过多使血氯过高。
糖为5%-10%的GS,盐为NS(0.9%NaCl),碱为5%NaHCO3(稀释为1.4%NaHCO3方法:5%碱量除以4,剩下的用糖补足。
例如:100ml5%碱稀释为1.4%碱:100/4=25,100-25=75,即为25ml5%碱+75ml糖)5、补钾:每100ml液体量中10%KCl总量不超过3ml,使钾浓度小于千分之三。
6、扩容:2:1等张含钠液(2份盐:1份碱)按20ml/kg计算,30分钟内滴完。

小儿补液三部曲来源:穆欢喜的日志一、首先,我们必须先判断孩子的病情到底如何,属于哪种脱水程度,以知道我们下一步的补液计划。
1、程度性脱水判断:轻度脱水:由于身体内水分减少,患儿会稍感到口渴,有尿排出,检查见患儿一般情况良好,两眼窝稍有陷,捏起腹部或大腿内侧皮肤后回缩尚快。
(轻度脱水最重要的判断标准就是:有尿排出,一般情况可,哭时有泪)中度脱水:患儿的出烦躁,易激惹;口渴想喝水,婴儿四处找奶头,如果得到奶瓶,会拼命吸吮;医学教育网原创啼哭时泪少,尿量及次数也减少;检查见患儿两眼窝下陷,口舌干燥,捏起腹壁及大腿内侧皮肤后回缩慢。
(中度脱水主要的判断标准:开始烦躁,易激惹,哭时泪少,眼窝下陷)重度脱水:患儿现为精神极度萎缩、昏睡,甚至昏迷;口喝非常严重,啼哭时无泪流出,尿量及尿次数明显数少。
检查见患儿两眼窝明显下陷,口舌非常干燥;捏起腹壁及大腿内侧皮肤后回缩很慢。
(重度脱水判断标准:精神萎靡,甚至昏睡。
皮肤相当的干燥,甚至出现了花纹,哭时无泪,无尿排出。
)2、渗透性的判断:低渗:血清钠<130mmol/L;(初期并未有口渴症状,但是极易发生脑水肿)等渗:血清钠130-150mmol/L;高渗:血清钠>150mmol/L。
(口渴症状相当的明显,高热,烦躁、肌张力增高.小儿补液三部曲之二先前,我们已经了解判断了小儿脱水的基本判断方法了,那么接下来,我们就应该了解,补什么,补多少,怎么补的问题了。
一、补什么、补多少1、补液总量:轻度失水:90-120ml/kg*d中度失水:120-150 ml/kg*d重度失水:150-180 ml/kg*d补液总量是由三部分组成的:一般需按累积损失量、继续损失量和生理需要量计算。
①累积损失量:指病后(如急性脱水)减轻之体重数量,这部分液体最主要。
这部分液量可根据脱水程度加以估计。
累积损失量也可按体表面积计算,轻度脱水为30-50ml/kg ,中度脱水为50-100ml/kg,重度脱水为100-150ml/kg。

临床常用小儿补液方法等渗性缺水——1/2张含钠液(2:3:1) 低渗性缺水——2/3张含钠液(4:3:2)高渗性缺水—-1/3张含钠液(2:6:1) 定速三个阶段(先盐后糖,先浓后淡,先快后慢)1)扩容阶段: 重度脱水伴循环障碍者,用2:1等张含钠液20ml/kg,30~60分内静脉推注或快速滴注。
2)以补充累积丢失量为主得阶段:若无微循环障碍,补液从此阶段开始,如以扩容,累积丢失量应减去扩容量。
累积量=总量÷2-扩容量8~12小时滴入,8~10ml/kg、h 3)维持补液阶段: 余量于16~18小时或5ml/kg.h输注④纠正酸中毒: 重度酸中毒可用5%NaHCO3:3-5ml/kg,提高HCO3—5mmol/L粗略计算。
血气测定计算:5%NaHCO3(ml)=(-BE)×0。
5×体重;稀释成1.4%得溶液(1ml 5%NaHCO3=3。
5ml1、4%)。
以上均半量给予。
两补1)补钾:见尿补钾, 浓度低于0、3%,0。
15~0.3g/kg.日。
需4~6天。
2)补钙,补镁:补液中出现抽风,先补钙,若无效,再补镁。
补钙:10%葡萄糖酸钙1—2ml /kg;补镁:25%硫酸镁0.1mg/kg/次,q6h第二天及以后得补液一、脱水及电解质已纠正1)溶液得定量:生理需要量,继续丢失量,补钾及供给热量、一般为口服,病重或不能口服者静脉补液。
2)溶液得定性:生理需要量: 60~80ml/kg, 用1/5张;继续丢失量:丢多少补多少,用1/2~1/3张。
二者加起来1/3~1/4张,12~24小时均匀静滴。
儿科常用液体得组成及张力1:1液1/2张0。
9%氯化钠50ml;5%或10%葡萄糖50ml 1:2液1/3张0。
9%氯化钠35ml;5%或10%葡萄糖65ml 1:4液1/5张0.9%氯化钠20ml;5%或10%葡萄糖80ml 2:3:1液1/2张0。
9%氯化钠33ml;5%或10%葡萄糖50ml;1、4%碳酸氢钠/1、87%乳酸钠17ml4:3:2液2/3张0、9%氯化钠45ml;5%或10%葡萄糖33ml;1。

小儿补液何估计小儿应该补几张的液体?因人而宜,因病而宜。
总体来说,年龄越小张力越小。
新生儿一般用无张或四一到五一张,小婴儿四一到五一张,幼儿儿童三一张左右。
一般感染疾病带药进去三四一张都可,腹泻补液讲究量速度张力根据脱水情况而定。
介绍一下儿科几种液体的简易配置方法:5%GS(ml)10%NS(ml)5%SB(ml)2:1 100 6 102:3:1 100 3 54:3:2 100 4 7大家只要记住1/2张1、3、5;2/3张1、4、7;1张1、6、10。
例如:欲配制300ml2:1液体则是300 ml5%GS+18ml10%NS+30ml5%SB。
(系数是300/100=3)欲配制200ml2:1液体则是200 ml5%GS+12ml10%NS+20ml5%SB。
(系数是200/100=2)欲配制400ml4:3:2液体则是400ml5%GS+16ml10%NS+28ml5%SB。
(系数是400/100=4)欲配制250ml2:3:1液体则是250ml5%GS+7.5ml10%NS+12.5ml5%SB。
(系数是250/100=2.5)余此按比例类推,信手拈来。
如果大家把这理解了,基本上已经达到主治医师水平!!!!!!!!!!!!!!!小儿补液是儿科医生的基本功,尤其是基层医院,腹泻的小儿特别多,更是要熟练掌握。
要和临床紧密结合的,不要太教条。
别人介绍的一个实用的方案:(天津方案)⑴4:5:12:7液体,在这组液体里,4为1.2%的氯化钾,5为1.4%的SB,12为糖水,7为0.9%的生理盐水。
4:5:12:7是他们之间的配比关系。
这组液体的张力大约在1/2张到1/3张之间,是一组比较安全的液体,适用于各种性质的脱水。
⑵4:5:6:7液体,各成分同上,只是糖水减半,大约1/2张。
适用于高渗脱水。
有的同仁会问我,为什么高渗脱水不补低张液?问的好,其实如果是高渗脱水,血浆比较粘稠,细胞处于皱缩状态,这个时候骤然补低张液体,会让皱缩的细胞骤然水肿膨胀,甚至破裂,会形成脑水肿的危险,所以建议高渗脱水一来不要补低渗液体,1/2张最安全。

临床常用小儿补液方法等渗性缺水——1/2X含钠液〔2:3:1〕低渗性缺水——2/3X含钠液〔4:3:2〕高渗性缺水——1/3X含钠液〔2:6:1〕定速三个阶段〔先盐后糖,先浓后淡,先快后慢〕1〕扩容阶段:重度脱水伴循环障碍者,用2:1等X含钠液20ml/kg,30~60分内静脉推注或快速滴注。
2〕以补充累积丧失量为主的阶段:假设无微循环障碍,补液从此阶段开场,如以扩容,累积丧失量应减去扩容量。
累积量=总量÷2-扩容量8~12小时滴入,8~10ml/kg.h3〕维持补液阶段:余量于16~18小时或5ml/kg.h输注④纠正酸中毒:重度酸中毒可用5%NaHCO3:3-5ml/kg,提高HCO3- 5mmol/L粗略计算。
血气测定计算:5%NaHCO3 〔ml〕=〔-BE〕×0.5×体重;稀释成1.4%的溶液〔1ml 5%NaHCO3 =3.5ml 1.4%〕。
以上均半量给予。
两补1〕补钾:见尿补钾,浓度低于0.3%,0.15~0.3g/kg.日。
需4~6天。
2〕补钙,补镁:补液中出现抽风,先补钙,假设无效,再补镁。
补钙:10%葡萄糖酸钙1-2ml/kg;补镁:25%硫酸镁0.1mg/kg/次,q6h第二天及以后的补液一、脱水及电解质已纠正1〕溶液的定量:生理需要量,继续丧失量,补钾及供应热量。
一般为口服,病重或不能口服者静脉补液。
2〕溶液的定性:生理需要量:60~80ml/kg,用1/5X;继续丧失量:丢多少补多少,用1/2~1/3X。
二者加起来1/3~1/4X,12~24小时均匀静滴。
儿科常用液体的组成及X力1:1液1/2X 0.9%氯化钠50ml;5%或10%葡萄糖50ml1:2液1/3X 0.9%氯化钠35ml;5%或10%葡萄糖65ml1:4液1/5X 0.9%氯化钠20ml;5%或10%葡萄糖80ml2:3:1液1/2X 0.9%氯化钠33ml;5%或10%葡萄糖50ml;1.4%碳酸氢钠/1.87%乳酸钠17ml4:3:2液2/3X 0.9%氯化钠45ml;5%或10%葡萄糖33ml;1.4%碳酸氢钠/1.87%乳酸钠22ml2:1液1X 0.9%氯化钠65ml;1.4%碳酸氢钠/1.87%乳酸钠35ml0.9%的溶液内参加尿素〔尿素可**********通过细胞膜〕,渗透压会增高但是X力不变X力:等渗的电解质溶液占总液量的百分比1:1液就是1/2X 3:2:1液就是3/〈3+2+1〉还是1/2X粗略算法:10%氯化钠3.3ML参加100ML10%GS就是1/3X10%氯化钠5ML参加100ML10%GS就是1/2X10%氯化钠6.6ML参加100ML10%GS就是2/3X以250ml,1/2X,3:2:1液举例为糖:等渗0.9%Nacl :等渗1.4%NaHCO3,〔钾为细胞内离子,不算X力,糖也不算X力〕1.用等渗液配法为:5%或10%糖:250ml×1/2(即3/3+2+1)=125ml0.9%Nacl:250ml×1/3=83ml1.4%NaHCO3:250ml×1/6=41ml三者混合就是3:2:1,250ml算一下,350ml,4:2:1怎么配制?2.临床上我们都用10%Nacl和5%NaHCO3 来配制,10%Nacl为11X,5%NaHCO3为3.5X,为了应用方便,10%Nacl简记为10X,5%NaHCO3简记为4X。


临床常用小儿补液方法等渗性缺水——1/2张含钠液(2:3:1)低渗性缺水——2/3张含钠液(4:3:2)高渗性缺水——1/3张含钠液(2:6:1)定速三个阶段(先盐后糖,先浓后淡,先快后慢)1)扩容阶段:重度脱水伴循环障碍者,用2:1等张含钠液20ml/kg,30~60分内静脉推注或快速滴注。
2)以补充累积丢失量为主的阶段:若无微循环障碍,补液从此阶段开始,如以扩容,累积丢失量应减去扩容量。
累积量=总量÷2-扩容量8~12小时滴入,8~10ml/kg.h3)维持补液阶段:余量于16~18小时或5ml/kg.h输注④纠正酸中毒:重度酸中毒可用5%NaHCO3:3-5ml/kg,提高HCO3- 5mmol/L粗略计算。
血气测定计算:5%NaHCO3 (ml)=(-BE)×0.5×体重;稀释成1.4%的溶液(1ml 5%NaHCO3 =3.5ml 1.4%)。
以上均半量给予。
两补1)补钾:见尿补钾,浓度低于0.3%,0.15~0.3g/kg.日。
需4~6天。
2)补钙,补镁:补液中出现抽风,先补钙,若无效,再补镁。
补钙:10%葡萄糖酸钙1-2ml/kg;补镁:25%硫酸镁0.1mg/kg/次,q6h第二天及以后的补液一、脱水及电解质已纠正1)溶液的定量:生理需要量,继续丢失量,补钾及供给热量。
一般为口服,病重或不能口服者静脉补液。
2)溶液的定性:生理需要量: 60~80ml/kg,用1/5张;继续丢失量:丢多少补多少,用1/2~1/3张。
二者加起来1/3~1/4张,12~24小时均匀静滴。
儿科常用液体的组成及张力1:1液1/2张0.9%氯化钠50ml;5%或10%葡萄糖50ml 1:2液1/3张0.9%氯化钠35ml;5%或10%葡萄糖65ml 1:4液1/5张0.9%氯化钠20ml;5%或10%葡萄糖80ml 2:3:1液1/2张0.9%氯化钠33ml;5%或10%葡萄糖50ml;1.4%碳酸氢钠/1.87%乳酸钠17ml4:3:2液2/3张0.9%氯化钠45ml;5%或10%葡萄糖33ml;1.4%碳酸氢钠/1.87%乳酸钠22ml2:1液1张0.9%氯化钠65ml;1.4%碳酸氢钠/1.87%乳酸钠35ml0.9%的溶液内加入尿素(尿素可**********通过细胞膜),渗透压会增高但是张力不变张力:等渗的电解质溶液占总液量的百分比1:1液就是1/2张 3:2:1液就是3/〈3+2+1〉还是1/2张粗略算法:10%氯化钠3.3ML加入100ML10%GS就是1/3张10%氯化钠5ML加入100ML10%GS就是1/2张10%氯化钠6.6ML加入100ML10%GS就是2/3张以250ml,1/2张,3:2:1液举例为糖:等渗0.9%Nacl :等渗1.4%NaHCO3,(钾为细胞内离子,不算张力,糖也不算张力)1.用等渗液配法为:5%或10%糖:250ml×1/2(即3/3+2+1)=125ml0.9%Nacl:250ml×1/3=83ml1.4%NaHCO3:250ml×1/6=41ml三者混合就是3:2:1,250ml算一下,350ml,4:2:1怎么配制?2.临床上我们都用10%Nacl和5%NaHCO3 来配制,10%Nacl为11张,5%NaHCO3为3.5张,为了应用方便,10%Nacl简记为10张,5%NaHCO3简记为4张。
小儿补液计算方法
小儿补液计算方法根据患儿的体重、年龄和病情确定。
以下是一种常用的计算方法:
1. 首先确定患儿的体重(单位可以是千克或磅)。
2. 然后根据患儿的体重和年龄确定液体输注速率。
根据患儿的具体情况,可以使用不同的计算公式。
以下是一种常用的公式:
- 对于体重在10千克以下的患儿,常规液体输注速率为100
毫升/千克/24小时。
- 对于体重超过10千克的患儿,常规输注速率为1000毫升/
千克/24小时的前10千克,加上50毫升/千克/24小时超过10
千克的部分。
3. 根据患儿的病情需要,可能需要调整液体输注速率。
常见的调整包括:
- 如果患儿有发热或呕吐,可增加液体输注速率。
- 如果患儿有腹泻或大量呕吐,可能需要根据丢失的液体量
进行补液。
4. 定期监测患儿的输注速率和液体摄入量,根据患儿的病情需要进行调整。
请注意,这只是一种常用的小儿补液计算方法,具体的计算方
法还需要根据医生的指导和患儿的具体情况进行确定。
在给患儿补液时务必遵循医生的建议,切勿自行决定液体输注速率。
医学计算公式大全1.小儿体重的计算1~6个月:出生体重+月龄X0.77~12个月:体重=6+月龄X0.252~12岁:年龄X2+8注:出生体重平均为3kg,生后3~4个月时体重约为出生时的2倍。
一岁时约为3倍,2岁时约为4倍。
2.小儿身高的计算:出生时约为50cm,半岁时约为65cm,一岁时75cm,2岁时87cm。
2~12岁身高=年龄X7+70(或75)。
注:身高低于正常的百分之三十即为异常。
3.头围:出生时约为33~34,一岁以内增长最快。
1岁时46cm,2岁时48cm,5岁时50cm。
15岁接近成人54~58cm 注:头围测量在2岁前最有价值。
4.胸围:出生时平均32cm。
一岁时头围与胸围大致相等。
约46cm。
5.牙齿:乳牙计算公式:月龄—4(或6)注:出生后4~10个月乳牙开始萌出,12个月未萌出者为出牙延迟。
6.囟门:出生时为1.5~2.0cm,1~1.5岁(12~18个月)应闭合7.全脂奶粉按重量配置时,其比例1:8;按容积1:4小儿每日每千克体重需要8%的糖牛乳100~110ml 例如:小儿,3个月,5kg,每日需要8%的糖牛乳的量为多少?即 5X(100~110)=500~5508.小儿药物的剂量计算(1)按体重:每日(次)剂量=患儿体重kgX每日(次)每公斤体重所需药量(2)按体表面积:体重小于等于30kg,小儿体表面积=体重X0.035+0.1体重>30,小儿体表面积=【体重—30】X0.02+1.05(3)按成人剂量折算:小儿剂量=成人剂量X小儿体重/509.血压:2岁以后收缩公式收缩压=年龄X2+80mmhg(年龄X0.27+10.67kpa)舒张压=收缩压X2/3注:新生儿收缩压平均为60~70mmhg,1岁以内70~80mmhg,测血压时,袖带宽度约为上臂长度的三分之二为宜。
10.烧伤面积的计算:烧伤面积是以烧伤部位与全身体表面积百分比计算的。
第一个24小时补液计算=体重(KG)X 烧伤面积(%)X1.5(ml)加2000ml生理需要量(1)新九分法:头、颈、面各占3%,共占9%;双上肢(双上臂7%、双前臂6%、双手5%)共占18%;躯干(前13%、后13%、会阴1%)共占27%;双下肢(两大腿21%、两小腿13%、双臀5%、足7%)共占46%。
介绍常用的静脉补液方法―4:3:2‖补液法(4份0.9%生理盐水:3份10%葡萄糖:2份1.4%碳酸氢钠或1/6M 乳酸钠)。
1.等渗脱水补充累积损失:轻度4:3:2溶液30~50ml/kg,于8~12h静滴。
中度4:3:2溶液50~100ml/kg,于8~12h静滴。
重度先给2:1液20ml/kg,于30分钟~1h内静脉输入,以扩充血容量。
继以4:3:2溶液80~100ml/kg,于8~12h输入2.低渗脱水纠正累积损失:多见于合并营养不良Ⅱ0~Ⅲ0的患儿,这类患儿体弱心功能差,因此纠正累积损失总量要少、浓度要高、速度要慢。
轻度4:3:2溶液30~50ml/kg,8~12h 输入。
重度及中度先给2:1液20ml/kg,于30分钟~1h输入,以便快速恢复血容量。
继给2:1液20ml/kg4:3:2液40ml/kg 10~12h输入。
3. 纠正低钠血症(水中毒):不伴脱水,血钠低于130mmol/L。
症状表现:细胞内水肿,可有惊厥,昏迷,颅压增高,肌肉松弛,腱反射降低,腹胀,尿少或无尿。
可按下述方法纠正:用3%氯化钠12ml/kg能把血钠提高10mmol/L,(宜缓慢VD,在1h以上,将血钠提高>120mmol/L,症状缓解后,病人出现大量利尿,可继续输入2/3-等张含钠液,直至累积损失被纠正,脱水症状消失)。
仍不好再加6ml/kg。
如用0.9%氯化钠40ml/kg,能把血钠提高10mmol/L4.高渗性脱水纠正累积损失:高渗脱水,脱水征表现较轻,一般显示轻~中度脱水。
高渗脱水不能用单纯葡萄糖液纠正,否则会引起脑细胞水肿,诱发颅内高压,发生惊厥,甚至死亡。
因此,所输液体张力不能过低,速度不能过快,要供给适量钾,既可适当提高所输液体的渗透压,又不增如钠负荷,而且钾还可进入细胞内,有利于细胞内脱水的纠正。
采用1/3~1/4张液,一般用1/3张―2:6:1‖(2份0.9%氯化钠:6份5%葡萄糖:1份1.4%碳酸氢钠或1/6M克分子浓度乳酸钠),于48h纠正累积损失。
小儿腹泻补液计算方法低渗性脱水以缺Na>缺水血清Na<130mmol/L 补2/3张液体等渗性脱水血清Na 130-150mmol/L之间补1/2张液体高渗性脱水血清Na>150mmol/L 补1/3张液体以250ml,1/2张,3:2:1液举例为糖:等渗0.9%Nacl :等渗1.4%NaHCO3,(钾为细胞内离子,不算张力,糖也不算张力)1.用等渗液配法为:5%或10%糖:250ml×1/2(即3/3+2+1)=125ml0.9%Nacl:250ml×1/3=83ml1.4%NaHCO3:250ml×1/6=41ml三者混合就是3:2:1,250ml算一下,350ml,4:2:1怎么配制?2.临床上我们都用10%Nacl和5%NaHCO3 来配制,10%Nacl为11张,5%NaHCO3为3.5张,为了应用方便,10%Nacl简记为10张,5%NaHCO3简记为4张。
250ml,3:2:1的粗略配制:先定总量:5%或10%糖250ml内加10%Nacl:250×1/3×1/10=8.3ml内加5%NaHCO3 :250×1/6×1/4=11ml混合就是粗略的3:2:1液了。
注:按此简易算法,实际溶液总量为250+8.3+11=260ml,而且与精确的配制相比,Nacl略多,NaHCO3略少,但实际应用中,这种差异可以忽略,要追求精确的话,可适当减少10%Nacl或增加5%NaHCO3的量,但实际上都在1ml的范围内。
用得多了,根本不必去死记书本上配制比例小儿腹泻病静脉补液的原则及方法常见的静脉溶液①等张液:2:I液=0.9%氯化钠液:1.4%NaHC03(或1/6M乳酸钠);②2/3张液:4:3:2液=0.9%氯化钠液:10%葡萄糖:1.4%NaHC03(或1/6M乳酸钠);l:1加碱液=0.9%氯化钠液lOOml+1O%葡萄糖100m1+5%NaHCOa10ml;③1/2张液:2:3:1液二0.9%氯化钠液:10%葡萄糖:l.4%NaHC03(或1/6M乳酸钠);④1/3张液:2份0.9%氯化钠液:6份10%葡萄糖:1份1.4%NaHCO3;⑤维持液:10%葡萄糖100ml+5%NaHC035m1+10%KCl2ml。
小儿补液液体配制
1、将10%NaCl10ml稀释至100ml,请问稀释后溶液百分比浓度。
10%×10=X×100,X=1%。
稀释定律:稀释前浓度×稀释前体积=稀释后浓度×稀释后体积。
即:C1×V1=C2×V1。
并且强调但凡涉及物质浓度的换算,均遵循此定律。
2、能够用来表达物质浓度的有(ABC)A.百分比浓度B.摩尔浓度C.张力
3、阐述溶液张力的概念及计算
张力是指溶液溶质的微粒对水的吸引力,溶液的浓度越大,对水的吸引力越大。
某溶液的张力=它的渗透压与血浆渗透压正常值(280~320mosm/L,计算时取平均值300mosm/L)相比所得的比值,它是一个没有单位但却能够反映物质浓度的一个数值。
溶液渗透压=(百分比浓度×10×1000×每个分子所能离解的离子数)/分子量
如0.9%NaCl溶液渗透压=(0.9×10×1000×2)/58.5=308mOsm/L(794.2kPa)该渗透压与血浆正常渗透压相比,比值约为1,故该溶液张力为1张。
又如5%NaHCO3溶液渗透压=(5×10×1000×2)/84=1190.4mOsm/L(3069.7kPa)该渗透压与血浆正常渗透压相比,比值约为4,故该溶液张力为4张。
记住张力是物质浓度的一种表达方式,其换算自然亦遵循稀释定律:C1×V1=C2×V2。
然后列出课本上已标明相应张力的几种常用溶液:
10%(NaCl)11张(临床上可按10张计算)
5%(NaHCO3)4张
10%(KCl)9张
10%(GS)0张(无张力,相当于水)
4、举例说明混合溶液张力的计算
例1、10%NaCl(10ml)+10%GS(90ml),请问该组溶液张力。
同学们很快能够根据C1×V1=C2×V2列出算式:10×10=X×100,X=1张
例2、10%NaCl(20ml)+5%NaHCO3(25ml)+10%GS(255ml),请问该组溶液张力。
10×20+4×25=X×300,X=1张。
例3、欲配制一组300ml,2/3张液体,现已使用5%NaHCO3(15ml),还需10%NaCl多少毫升。
10×X+4×15=2/3×300,X=14ml
那么,再加入10%GS271(270)ml后即可配制成所需液体(300-15-14=271ml,GS为0张)
5、2∶1等张液是抢救休克时扩容的首选溶液,其有固定组份,由2份等渗盐溶液+1份等渗碱溶液配制而成。
给出一个简单的计算公式配制2∶1液Mml,则需
10%NaCl=M/15ml————a
5%NaHCO3=M/12ml———b
10%GS=M-a-bml
例5、配制2∶1液300ml,需10%NaCl、5%NaHCO3、10%GS各多少毫升。
10%NaCl=300/15=20ml
5%NaHCO3=300/12=25ml
10%GS=300-20-25=255ml。