醇的催化氧化ppt课件
- 格式:ppt
- 大小:187.50 KB
- 文档页数:8


醇的催化氧化规律可以根据不同的醇类和催化剂进行研究和描述。
一般而言,醇的催化氧化规律包括以下几个方面:
催化剂选择:不同的催化剂对醇的氧化反应具有不同的催化活性和选择性。
常见的催化剂包括过渡金属催化剂如铂、钯、钌等,以及非金属催化剂如氧化铁、二氧化锰等。
选择合适的催化剂对于实现高效催化氧化具有重要意义。
氧化剂选择:氧化剂是促使醇氧化反应进行的重要组成部分。
常见的氧化剂包括氧气、过氧化氢、过氧化苯甲酰等。
氧化剂的选择和使用方式会影响醇的氧化反应速率和产物选择性。
反应条件:反应温度、压力、溶剂选择等反应条件对醇的催化氧化具有影响。
适当的反应条件可以提高反应速率和选择性,同时确保反应的安全性和高效性。
催化氧化机制:不同醇的催化氧化反应机制可能存在差异。
一般而言,催化氧化反应涉及醇分子的活化、氧化剂和催化剂之间的相互作用,以及反应中间体的生成和转化等过程。




醇的氧化反应原理和现象
醇的氧化反应是指醇分子中的氢原子转移给氧气,形成水和相应的醛或酮的反应过程。
这样的氧化反应通常需要催化剂的存在,常见的催化剂有氧化剂如二氧化铬(CrO2)、高价铜氯(CuCl2)、酸性高锰酸钾(KMnO4)等。
醇的氧化反应是一种氧化还原反应,即醇的氧化态提高,同时氧化剂的还原态降低。
在反应过程中,醇中的氢原子被氧化剂的氧原子取代,形成水分子,同时产生相应的醛或酮。
例如,乙醇(CH3CH2OH)可以氧化为乙醛(CH3CHO)或乙酸(CH3COOH)。
氧化反应可由如下反应式表示:
乙醇+ 氧气→乙醛+ 水
乙醇+ 氧气→乙酸+ 水
氧化反应通常在一定的温度和压力条件下进行。
反应的速率和产物的选择取决于氧化剂的性质和反应条件的控制。
此外,氧化反应还可能伴随着其他反应,如分解、重排等。
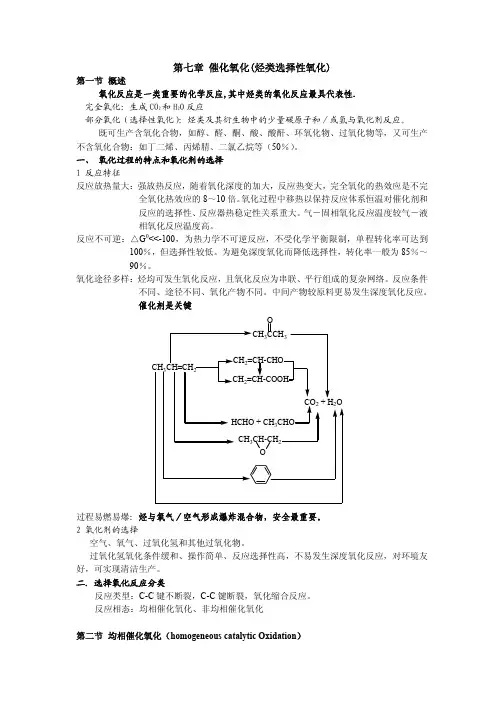

醇的催化氧化的机理
醇的催化氧化机理可以分为两步骤:首先是醇的氧化步骤,其次是产物的分解和重新组合步骤。
1. 醇的氧化步骤:
在催化剂的作用下,醇分子首先与氧气发生氧化反应。
对于一般的醇分子,其氧化反应可以分为两种类型:
a) 亲氧性氧化(alcohol dehydrogenation):醇中的氢原子被去除,生成相应的醛或酮。
这一步骤可以通过醇分子在催化剂表面上的吸附形成活化中间体来实现。
在活化中间体的形成过程中,醛基或酮基与催化剂通过化学键相连。
b) 氧辅助氧化(oxygen-assisted oxidation):醇中的氧原子被氧气的氧原子取代,生成相应的酮或醛。
该反应可以通过醇分子在催化剂表面上的吸附形成活化中间体来实现。
2. 产物分解和重新组合步骤:
在醇经历氧化步骤后,生成的酮或醛可能会进一步发生分解和重新组合反应,生成更多的副产物。
这些反应通常发生在醇的氧化反应的副产物和催化剂表面的氧而不是醇分子之间。
总体来说,醇的催化氧化机理涉及醇的氧化反应和产物的分解和重新组合反应两个主要步骤。
具体的反应机制可能受到催化剂的种类、反应条件和醇分子的结构等多种因素的影响。


乙醇和铜的催化氧化醇氧化催化是一种反应,它能将一种有机物质如乙醇,氧化成另一种物质,并且在这个反应过程中会使用铜作为催化剂。
乙醇氧化催化具有很多优势,包括低能耗、高效率以及不受外界影响的稳定性,使得这种反应被广泛应用于化学和药物行业。
一、乙醇氧化催化的基本原理乙醇氧化催化反应的基本原理是,当原料中的乙醇经过铜催化剂的作用,它的反应单位——羟基可以和氧分子形成羟基氧化物(乙醇氧化物),从而在反应传递过程中有效地生成了乙醇氧化物。
二、乙醇氧化催化反应的原料1. 乙醇:乙醇是醇氧化反应的基本原料,几乎所有乙醇氧化反应都以乙醇为主要输入原料,乙醇氧化反应中乙醇会和氧分子发生反应并产生乙醇氧化物,从而达到乙醇氧化反应的目的。
2. 铜:铜是乙醇氧化催化反应的关键催化剂,铜能够使乙醇的羟基发生亲和作用,从而促进氧化反应的发生。
而且,铜在乙醇氧化催化反应中具有抑制反应中间产物的功能,有效地降低了反应中的化学耗能。
三、乙醇氧化催化反应的应用1. 工业应用:乙醇氧化催化反应在工业中有着广泛的应用,它能够有效把乙醇氧化为一种醇类化合物,并应用于制造医药行业,生产羟乙基溴化钠等产品。
2. 生物学应用:乙醇氧化反应在生物学中有着重要的应用,它可以帮助有机生物体分解乙醇,使其得到更多的能量,并分解出更多的物质,达到更好的代谢效果。
四、乙醇氧化催化反应的优势1. 低能耗:乙醇氧化催化反应比起普通的氧化反应能耗更低,因为乙醇氧化催化反应可以有效减少反应过程中的化学耗能。
2. 高效:乙醇氧化催化反应反应速度比普通的氧化反应要快,因为催化剂可以促进反应速度,从而大大提高氧化反应的效率。
3. 稳定性:乙醇氧化催化反应具有比较稳定的反应性,反应过程不受外界因素的影响,这使得乙醇氧化催化反应能够更好地被应用于工业生产中。
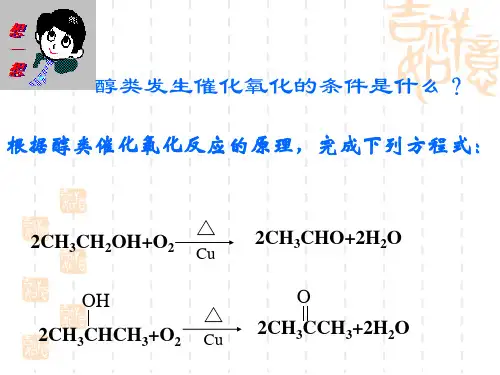
醇催化氧化的条件
醇催化氧化的条件是,Cu或Ag等过渡金属做催化剂和加热;与羟基相连接的碳原子即α碳原子上有氢原子。
同时还要有催化剂,并且在加热的条件下发生催化氧化。
因为醇有α-H,也就是与C-OH相连的C上的H,就比如CH3CH2OH 可以发生催化氧化,而(CH3)3COH却不能够发生催化氧化。
醇要发生催化氧化,与羟基相连的碳原子上就必须要有氢,有一个氢就会生成酮,有两个氢就会生成醛。
因为催化氧化是要脱去羟基上的一个氢,并且跟与羟基相连的碳原子上的一个氢发生反应,如果没有氢是没有办法完成脱氢的。
醇氧化产物是由羟基所连接的碳原子种类来决定的。
醇,有机化合物的一大类,是脂肪烃、脂环烃或芳香烃侧链中的氢原子被羟基取代而成的化合物。
醇类化合物受羟基的影响,存在分子间的氢键,在水中还有醇分子和水分子间的氢键。
所以,它们的物理性质与相应的烃差异较大。
主要表现在熔沸点比较高,在水中有一定的溶解度等。