麦克斯韦速率分布
- 格式:pdf
- 大小:174.88 KB
- 文档页数:12
![§2[1].3麦克斯韦速率分布](https://uimg.taocdn.com/b635b63887c24028915fc3b6.webp)


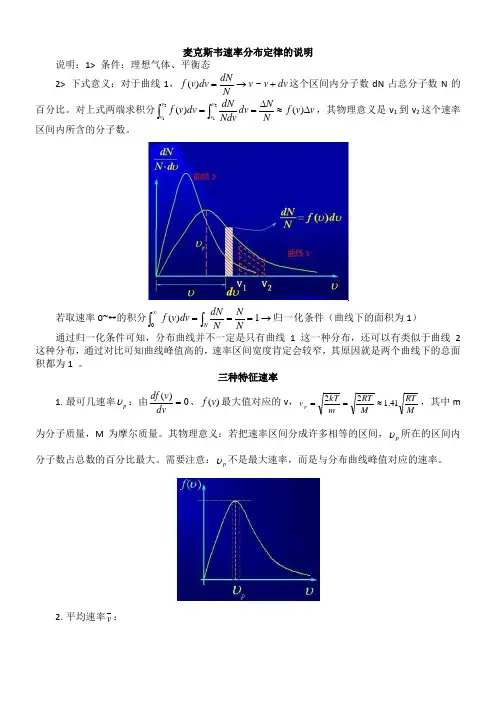
麦克斯韦速率分布定律的说明说明:1> 条件:理想气体、平衡态2> 下式意义:对于曲线1,dv v v N dN dv v f +→=~)(这个区间内分子数dN 占总分子数N 的百分比。
对上式两端求积分v v f NN dv Ndv dN dv v f v v v v ∆≈∆==⎰⎰)()(2121,其物理意义是v 1到v 2这个速率区间内所含的分子数。
若取速率0~∞的积分归一化条件→===⎰⎰∞1)(0NN N dN dv v f N (曲线下的面积为1) 通过归一化条件可知,分布曲线并不一定是只有曲线1这一种分布,还可以有类似于曲线2这种分布,通过对比可知曲线峰值高的,速率区间宽度肯定会较窄,其原因就是两个曲线下的总面积都为1 。
三种特征速率1. 最可几速率p υ:由0)(=dv v df 、)(v f 最大值对应的v ,MRT M RT m kT v p 41.122≈==,其中m 为分子质量,M 为摩尔质量。
其物理意义:若把速率区间分成许多相等的区间,p υ所在的区间内分子数占总数的百分比最大。
需要注意:p υ不是最大速率,而是与分布曲线峰值对应的速率。
2. 平均速率v :M RT M RT dv v vf N dN v N N v N N v N v v Niii 60.18)(02211≈===∆=+∆+∆=⎰⎰∑∞π , 物理意义:在平衡状态下,气体分子速率的算术平均值,注意:平均速率不是平均速度。
因为分子都是作物规则的运动,所以其平均速度0=v 。
3. 方均根速率2v :MRT M RT v 73.132≈=,物理意义:在平衡状态下,气体分子热运动速率的另一种统计平均值。
注意:22v v v v =∙≠,方均根速率是每个分子的速率平方后再累加求平均值。
4. 说明:1> 三种速率均由麦氏速率 分布率求得(理想气体 平衡态),2> 具有统计意义——属于大量分子整体,均正比与MRT ,且2v v v p <<。







麦克斯韦速率分布
麦克斯韦速率分布是描述气体分子速度分布的概率分布函数之一。
它由麦克斯韦速度分布定律提出,该定律认为在一定温度下,分子速度的分布服从麦克斯韦速率分布。
麦克斯韦速率分布的表达式为:
f(v) = (m / (2 * π * k * T))^(3/2) * 4 * π * v^2 * exp(-(m * v^2) / (2 * k * T))
其中,f(v)是速度为v的气体分子出现的概率密度,m是分子的质量,k是玻尔兹曼常数,T是温度。
麦克斯韦速率分布描述了速率在不同范围内的分子数的相对比例。
麦克斯韦速率分布具有以下特点:
1. 最概然速率:在麦克斯韦速率分布曲线上,存在一个速度值,使得该速度值对应的气体分子出现的概率最高,这个速度就是最概然速率。
2. 平均速率:麦克斯韦速率分布曲线的面积下的整数倍等于总分子数,因此可以通过平均积分得到平均速率。
3. 方均根速率:方均根速率是指速率的平方取平均后开根号的值,它与麦克斯韦速率分布曲线的宽度有关。
麦克斯韦速率分布在解释气体的物理性质和进行气体动力学研究中起着重要的作用,尤其在理解气体温度、分子碰撞等方面具有较高的应用价值。