合成酰胺键的方法
- 格式:doc
- 大小:178.50 KB
- 文档页数:3

肽键酰胺键酰胺基
肽键、酰胺键和酰胺基是生物化学中常见的概念,它们在蛋白质的结构和功能中起着重要的作用。
下面将以人类的视角,以生动的方式来描述它们。
肽键是连接氨基酸的一种特殊化学键。
当两个氨基酸分子相遇时,它们中的一个氨基酸中的氨基团和另一个氨基酸中的羧基团发生反应,形成肽键。
这个过程就像两个人之间的握手,它们通过肽键紧密地连接在一起。
酰胺键是连接多个氨基酸形成肽链的键。
当多个氨基酸相互作用时,它们的氨基团和羧基团依次反应,形成一个又一个的酰胺键,将它们连接在一起,形成了蛋白质的主链。
这就像人们手拉手形成一个长队伍,每个人都与前后的人紧密相连。
而酰胺基则是指连接在酰胺键上的原子或原子团。
在蛋白质中,酰胺基既可以是氨基酸的侧链,也可以是其他分子的一部分。
它们通过酰胺键与主链连接在一起,共同构建了蛋白质的三维结构。
肽键、酰胺键和酰胺基的形成是蛋白质合成和折叠的基础。
它们的稳定性和特殊性质使得蛋白质能够在复杂的生物环境中发挥各种生物学功能。
正是由于肽键、酰胺键和酰胺基的存在,我们才能拥有如此多样化的蛋白质结构和功能。
总结起来,肽键、酰胺键和酰胺基是生物化学中非常重要的概念。
它们通过连接氨基酸和形成酰胺链,构建了蛋白质的主链和侧链,从而赋予蛋白质以特殊的结构和功能。
它们在生命的起源和进化中发挥着重要的作用,是生物化学研究的核心内容之一。

形成酰胺键酶法
形成酰胺键的酶法是通过酶催化的反应来实现。
酶是一种特殊的蛋白质,可以加速化学反应的进行,而不会改变反应的平衡态。
在形成酰胺键的酶法中,通常使用一种酰胺合成酶作为催化剂。
酰胺合成酶可以将一个酰基转移至氨基上,形成酰胺键。
具体的反应机理通常包括以下步骤:
1. 酰胺合成酶与底物(通常是酰胺的前体)结合,形成酶底物复合物。
2. 酶底物复合物发生一系列反应,包括酶催化的亲电攻击、质子化等步骤,形成一个酰胺中间体。
3. 酰胺中间体重新排列,并进一步反应,使底物中的酰基转移到氨基上,形成稳定的酰胺产物。
4. 酰胺产物解离出酶,完成反应。
需要注意的是,不同的酰胺合成酶对于底物的结构和反应条件有不同的特异性,因此选择合适的酶催化剂对于实现特定的酰胺键形成反应是至关重要的。

合成酰胺键的方法1、酰卤法最常用的是酰氯,一般的操作方法是将羧酸与SOCl2或者(COCl)2反应生成酰氯,然后与游离的氨基反应生成酰胺键。
催化量的DMF可以促进酰氯的生成,而DMAP可以促进酰氯和氨基的反应。
该方法的优点是活性高,可以与大位阻的氨基反应;缺点是在酸性条件下形成酰氯,很多对酸敏感的基团承受不了,还有就是产物比较容易消旋。
为了克服第一个缺点,人们发展了用氰脲酰氯(2, 4, 6-三氯-1, 3, 5-三嗪)/TEA或者PPh3/CCl4条件形成酰氯,第二个缺点可用酰氟代替酰氯加以克服。
2、混合酸酐法氯甲酸乙酯或氯甲酸异丁酯是最常用的生成混酐的试剂。
它是利用羧酸羰基的亲电性高于碳酸羰基,从而使氨基选择性的进攻羧酸羰基形成酰胺键。
混酐法具有反应速度快,产物纯度较高等优点,但由于混酐的活性很高,极不稳定,要求反应在低温无水条件下进行,产品也容易出现消旋现象。
3、活化酯法常见的活化酯有硝基苯酯,2, 4, 6-三氯苯酯,五氯苯酯,五氟苯酯(PfOH),N-羟基琥珀酰亚胺(HOSu)酯和N-羟基苯并三唑酯(HOBt)等。
一般的操作步骤是先制备并分离得到活化酯,再与氨基反应生成酰胺键。
由于活化酯活性较酰氯和酸酐低,可以极大地抑制消旋现象,并能在加热的条件下反应。
4、酰基迭氮法一般是用酰肼与亚硝酸钠反应制成酰基迭氮,然后与氨基反应形成酰胺键。
优点是迭氮法引起的消旋程度较小,比活化酯法效率更高,但是,酰基迭氮中间体不稳定,产生的迭氮酸有毒,而且制备步骤繁琐。
Shioiri等人发展的DPPA可以与羧酸现场生成酰基迭氮,很好地解决了酰基迭氮制备的问题,得到广泛的运用。
5、缩合试剂法该方法是目前应用最广的形成酰胺键的方法,同时也广泛地应用于酯键、大环内酰胺和内酯的构建。
这种方法通常是将羧基组份和氨基组份混合,在缩合试剂作用下,中间体不经分离直接进行反应形成酰胺键。
这样就无需预先制备酰卤、酸酐和活化酯等羧基被活化的中间体,不仅简捷高效,而且可以有效地避免在活化中间体分离提纯以及存放过程中产生的一些副反应。

两种药物通过酰胺键连接的方法
两种药物通过酰胺键连接的方法主要有以下两种:
1.化学合成法:此方法一般涉及将两种药物通过酰胺键连接起来。
具体来说,首先需要将第一种药物的羧基转化为胺,然后与第二种药物的氨基进行缩合反应,生成酰胺键。
此方法需要精确控制反应条件,包括温度、pH值、反应时间等,以确保生成的酰胺键结构正确,且不会有其他副产物生成。
2.生物合成法:此方法主要利用微生物或细胞来生产目标药物。
在
生物体内,酰胺键的合成通常涉及到一系列的生物化学反应。
这些反应一般由特定的酶催化,而且在生物体的适宜环境下,反应效率较高,能大规模地生产目标药物。

酰胺键形成能全文共四篇示例,供读者参考第一篇示例:酰胺键形成能是一种重要的化学反应,在有机化学领域中有着广泛的应用。
酰胺键是一种酯类和胺类发生缩烷反应后生成的共价键,其中酰基和胺基之间通过一个碳-氮键连接。
由于酰胺键的特殊性质和结构,使得它具有很高的热力学稳定性和结构稳定性,因此在生物体系中广泛存在,如蛋白质、多肽、核酸等生物大分子。
酰胺键形成能的大小主要取决于酯类和胺类的反应性及反应条件。
一般而言,酯类和胺类反应生成酰胺键需要消耗一定的能量,这个过程即为酰胺键形成能。
酰胺键形成能的大小对于化学反应的进行和反应速率有着重要的影响,它决定了反应是否会进行和反应的进行程度。
在有机合成中,酰胺键的形成能常常被用于探讨不同反应物之间的反应性和反应条件的选择。
一般来说,酰胺键形成能较小的反应对于生成酰胺键会更有利,而酰胺键形成能较大的反应则需要更高的温度、催化剂或其他条件来促进反应的进行。
通过研究和测定不同反应的酰胺键形成能,可以为有机合成提供理论上的指导和实验上的依据。
除了在有机合成中的应用外,酰胺键形成能在生物化学和药物化学领域也有着重要的意义。
许多药物分子中含有酰胺键,酰胺键的形成能直接影响了药物的结构稳定性和生物活性,因此研究和探讨药物分子中酰胺键的形成能对于药物的设计和研发具有重要意义。
许多生物大分子如蛋白质和多肽中也含有大量的酰胺键,酰胺键的形成能对于这些生物大分子的结构和功能有着重要的影响。
酰胺键形成能是一项重要的化学参数,它在有机反应、药物设计和生物化学领域都有着重要的应用价值。
通过研究和测定酰胺键形成能,可以更好地理解和探讨化学反应的机制和规律,为化学和生物化学领域的发展和应用提供理论和实践上的支持。
第二篇示例:酰胺键形成能,是指将一个酸和一个胺分子结合形成酰胺键所需要的能量。
酰胺键是一种常见的共价键,通常存在于蛋白质、多肽等生物大分子中。
在生物体内,酰胺键的形成在很多生物过程中起着关键作用,因此了解酰胺键形成能对于生物化学领域的研究是非常重要的。


天然产物酰胺键
酰胺键是一种化学键,属于酰胺(amide)官能团的一部分。
酰胺是由羧基(carboxyl group)和胺基(amino group)通过酰胺键结合而成的。
这种键的形成涉及羧基的羰基碳和胺基的氮之间的共价键连接。
天然产物中存在大量含有酰胺键的分子,其中一些常见的包括:
蛋白质:蛋白质是由氨基酸组成的生物分子,氨基酸之间的肽键就是一种酰胺键。
蛋白质在生物体内起着关键的结构和功能作用。
多肽:类似于蛋白质,多肽也是由氨基酸通过酰胺键连接而成,但相对较短。
核酸:RNA(核糖核酸)和DNA(脱氧核糖核酸)中的磷酸二酯键和磷酸三酯键也包含酰胺键。
酰胺类化合物:天然产物中还包括许多酰胺类化合物,例如荷尔蒙、抗生素和天然产生的一些药物。
酰胺键的形成通常是通过羧基上的羰基和胺基上的氮之间的缩
合反应,释放一分子水。
在这个缩合反应中,羧基中的氧与胺基中的
氢结合形成酰胺键。
这种缩合反应是多肽链和蛋白质的合成中的基本步骤。
总体而言,酰胺键在生物体内的分子结构和生物活性中发挥着重要的角色,是天然产物中的重要结构基元。

合成酰胺键的一般方法刚才浏览帖子,看到有人问如何合成酰胺键。
由于本人博士论文是做多肽合成的,所以有一些经验。
现将我的博士论文关于如何合成酰胺键的一段贴过来,希望能对即将从事多肽合成的人有些用。
本帖原创,转载请注明出处。
在这里我们简单介绍一下多肽化学合成的方法以及常用的多肽缩合试剂。
1、酰卤法最常用的是酰氯,一般的操作方法是将羧酸与SOCl2或者(COCl)2反应生成酰氯,然后与游离的氨基反应生成酰胺键。
催化量的DMF可以促进酰氯的生成,而DMAP可以促进酰氯和氨基的反应。
该方法的优点是活性高,可以与大位阻的氨基反应;缺点是在酸性条件下形成酰氯,很多对酸敏感的基团承受不了,还有就是产物比较容易消旋。
为了克服第一个缺点,人们发展了用氰脲酰氯(2, 4, 6-三氯-1, 3, 5-三嗪)/TEA或者PPh3/CCl4条件形成酰氯,第二个缺点可用酰氟代替酰氯加以克服。
2、混合酸酐法氯甲酸乙酯或氯甲酸异丁酯是最常用的生成混酐的试剂。
它是利用羧酸羰基的亲电性高于碳酸羰基,从而使氨基选择性的进攻羧酸羰基形成酰胺键。
混酐法具有反应速度快,产物纯度较高等优点,但由于混酐的活性很高,极不稳定,要求反应在低温无水条件下进行,产品也容易出现消旋现象。
3、活化酯法常见的活化酯有硝基苯酯,2, 4, 6-三氯苯酯,五氯苯酯,五氟苯酯(PfOH),N-羟基琥珀酰亚胺(HOSu)酯和N-羟基苯并三唑酯(HOBt)等。
一般的操作步骤是先制备并分离得到活化酯,再与氨基反应生成酰胺键。
由于活化酯活性较酰氯和酸酐低,可以极大地抑制消旋现象,并能在加热的条件下反应。
4、酰基迭氮法一般是用酰肼与亚硝酸钠反应制成酰基迭氮,然后与氨基反应形成酰胺键。
优点是迭氮法引起的消旋程度较小,比活化酯法效率更高,但是,酰基迭氮中间体不稳定,产生的迭氮酸有毒,而且制备步骤繁琐。
Shioiri 等人发展的DPPA可以与羧酸现场生成酰基迭氮,很好地解决了酰基迭氮制备的问题,得到广泛的运用。

酰胺(R—CONH—R')的合成反应主要有以下几种:
1. 羧酸与氨或胺的缩合反应,生成酰胺。
这是合成酰胺的最主要方法,可以在温和的条件下进行,不需要高温或高压等条件。
2. 羧酸铵盐与醇的反应也可以生成酰胺。
这是由于醇有可能被水替代,进而形成酰胺键。
这种反应是在酸或碱的存在下进行的,生成物通常为水溶性的。
3. 羧酸与有机酸的酐化反应也可以生成酰胺。
但是这种反应条件要求比较高,需要高温或高压等条件。
在酰胺合成反应中,需要关注酰胺合成中产物的纯度和收率问题。
纯度和收率取决于反应条件、试剂和底物的性质等因素。
如果反应条件过于苛刻,或者底物容易发生副反应,那么产物的纯度和收率就会降低,从而影响最终的合成效果。
因此,在合成酰胺时,需要仔细选择反应条件和试剂,并进行充分的实验设计和实验操作,以确保得到预期的产物。
此外,酰胺合成反应中还需要关注环境保护问题。
由于酰胺合成过程中可能会产生一些有害物质,因此需要采取有效的环保措施,确保实验室和生产过程中的环境保护。
总的来说,酰胺合成反应是一种重要的有机合成方法,可以用于合成各种酰胺类化合物。
在实践中,需要根据具体情况选择合适的合成方法,并注意产物的纯度和收率、环境保护等问题,以确保合成的成功和顺利进行。

pybrop反应机理PyBOP反应机理PyBOP是一种常用的活化剂,用于合成肽和蛋白质。
它是一种非对称活化剂,可以在室温下快速反应,并且可以在水溶液中使用。
PyBOP 的反应机理是通过活化羧基,使其与氨基酸或肽链中的氨基反应,形成酰胺键。
PyBOP的反应机理可以分为三个步骤:活化、缩合和去保护基。
1. 活化PyBOP的活化是通过与N-羟基苯并咪唑(HOBt)和二甲基氨(DMAP)反应来完成的。
HOBt和DMAP可以增加反应速率和选择性。
在活化过程中,PyBOP的氯离子会被HOBt取代,形成一个中间体,该中间体可以与氨基酸或肽链中的氨基反应。
2. 缩合在活化过程中,中间体与氨基酸或肽链中的氨基反应,形成酰胺键。
这个过程被称为缩合。
缩合反应是一个亲核取代反应,其中氨基酸或肽链中的氨基攻击中间体,形成酰胺键。
缩合反应是一个快速的反应,可以在室温下完成。
3. 去保护基在缩合反应完成后,需要去除保护基。
保护基是在合成肽和蛋白质时使用的一种化学保护基,可以保护氨基酸中的侧链官能团。
去除保护基的方法是使用强酸或碱,例如三氟乙酸或氢氧化钠。
去除保护基后,可以得到纯净的肽或蛋白质。
总结PyBOP是一种常用的活化剂,用于合成肽和蛋白质。
它的反应机理是通过活化羧基,使其与氨基酸或肽链中的氨基反应,形成酰胺键。
PyBOP的反应机理可以分为三个步骤:活化、缩合和去保护基。
在活化过程中,PyBOP的氯离子会被HOBt取代,形成一个中间体,该中间体可以与氨基酸或肽链中的氨基反应。
在缩合反应完成后,需要去除保护基。
去除保护基的方法是使用强酸或碱。
通过PyBOP的反应机理,可以高效地合成肽和蛋白质。
缩合剂在合成制药工业酰胺化反应中的大规模应用酰胺键的形成是药物化学研究中应用最广泛的一类化学反应。
与以往的文章不同,本文主要评价各类酰胺缩合剂在候选药物合成中由酸和胺缩合成酰胺的大规模应用,突出了每个缩合剂在工业规模上应用的优点及不足。
酰胺键常常存在于活性药物成分(API)结构中。
实际上,酰胺键的形成在制药工业中是最普遍的反应之一,在所有药物化学实验室开展的化学反应中占16%。
然而,酰胺合成最理想的方法,如,羧酸和胺直接缩合成酰胺,同时生成一当量的水,这是唯一的副产物,也是最理想的方法。
这个理想的方法不可行是因为在缩合反应物之间会发生质子交换而形成羧酸铵盐,只有在较强反应条件下(如,高温和微波照射)才能发生缩合反应,显然这和目前候选药物的化学复杂性是不相适应的。
酸活化能促进其与胺的缩合,因此发展在工业规模上活化酸并进而与胺缩合的安全、有效的方法是至关重要的。
在工业生产上选择酰胺缩合剂需要考虑许多方面,理想的试剂应该是价廉、无毒、安全、处理简单、广泛使用、易从反应混合物中除去、仅导致最小量的废水,而且在生产路线快结束形成酰胺键的同时,副产物的检测和清除在监管限制内是优先考虑的事项。
当然,对于一个给定的酸和胺而言,不是所有的缩合剂都表现得一样好,上述过程及酰胺反应条件要同时考虑,以获得高的收率和选择性,好的重复性,在底物有手性中心的情况下,产生较低的差向异构化。
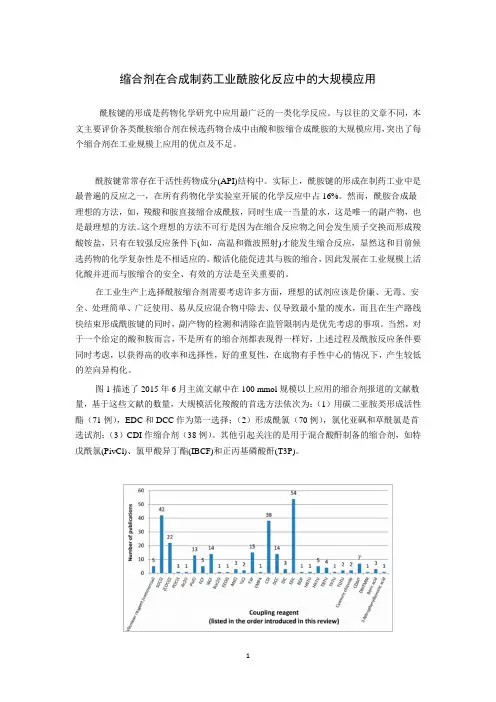
图1描述了2015年6月主流文献中在100 mmol规模以上应用的缩合剂报道的文献数量,基于这些文献的数量,大规模活化羧酸的首选方法依次为:(1)用碳二亚胺类形成活性酯(71例),EDC和DCC作为第一选择;(2)形成酰氯(70例),氯化亚砜和草酰氯是首选试剂;(3)CDI作缩合剂(38例)。
其他引起关注的是用于混合酸酐制备的缩合剂,如特戊酰氯(PivCl)、氯甲酸异丁酯(IBCF)和正丙基磷酸酐(T3P)。
图1. 2015年6月缩合剂应用的参考文献数量,酰胺键生成规模在100 mmol以上后续将对酰胺化反应中缩合剂的应用作一个系列报道,每期介绍一类酰胺键形成所用试剂的情况、作用机理及其大规模应用实例。
酰胺键的n无h全文共四篇示例,供读者参考第一篇示例:酰胺键是有机化学中一种重要的官能团,它是一种由羧基和氨基之间形成的特殊键。
在生物大分子中,酰胺键扮演着至关重要的角色,如蛋白质、核酸等大分子中都包含大量的酰胺键。
但在本文中我们将要探讨的是“无H的酰胺键”。
首先我们来了解一下普通的酰胺键。
一般来说,普通的酰胺键中,氨基上的氢原子和羧基上的羟基氧原子可以发生氢键作用,从而使得酰胺键具有稳定的构象。
而无H的酰胺键,是指在酰胺键中氨基上的氢原子被其他原子所取代,无法出现氢键。
这种酰胺键的存在对于生物大分子的稳定性和结构产生了一定的影响。
事实上,无H的酰胺键可以被认为是一种非正常的结构,但在某些特定情况下却可以发挥重要的作用。
无H的酰胺键最常见的情况是在环状肽类化合物中。
环状肽是一种特殊的多肽类化合物,由多个氨基酸残基组成,通过酰胺键连接在一起形成环状结构。
而在一些环状肽中,一些氨基上的氢原子被其他原子所取代,导致形成无H的酰胺键。
这种无H的酰胺键使得环状肽在结构上更加紧凑稳定,同时也增加了其在生物体内的生物活性和生物稳定性。
无H的酰胺键在药物设计和药物研发领域也有着重要的应用。
由于无H的酰胺键使得化合物在空间结构上更加复杂,因此可以通过合理设计无H的酰胺键来调控化合物的药效和生物利用度。
一些抗癌药物和免疫调节剂中就包含了无H的酰胺键结构。
无H的酰胺键虽然在自然界中较为罕见,但在一些特定的生物大分子和药物化合物中具有重要的作用。
通过深入研究无H的酰胺键的结构和性质,可以为药物设计和新型生物大分子的研究开拓新的方向和途径。
希望未来能够更加深入地探讨无H的酰胺键在生物化学领域中的应用,为人类的健康和生命科学研究做出更大的贡献。
第二篇示例:酰胺键是有机化合物中常见的键,它是连接酰胺基团和酰胺基团的键。
酰胺键通常是通过在碳原子上形成一个双键的方式形成的,这个双键与氮原子上的一个孤对电子形成共轭。
酰胺键的性质与双键和孤对电子的性质有关。
缩合剂在合成制药工业酰胺化反应中的大规模应用酰胺键的形成是药物化学研究中应用最广泛的一类化学反应。
与以往的文章不同,本文主要评价各类酰胺缩合剂在候选药物合成中由酸和胺缩合成酰胺的大规模应用,突出了每个缩合剂在工业规模上应用的优点及不足。
酰胺键常常存在于活性药物成分(API)结构中。
实际上,酰胺键的形成在制药工业中是最普遍的反应之一,在所有药物化学实验室开展的化学反应中占16%。
然而,酰胺合成最理想的方法,如,羧酸和胺直接缩合成酰胺,同时生成一当量的水,这是唯一的副产物,也是最理想的方法。
这个理想的方法不可行是因为在缩合反应物之间会发生质子交换而形成羧酸铵盐,只有在较强反应条件下(如,高温和微波照射)才能发生缩合反应,显然这和目前候选药物的化学复杂性是不相适应的。
酸活化能促进其与胺的缩合,因此发展在工业规模上活化酸并进而与胺缩合的安全、有效的方法是至关重要的。
在工业生产上选择酰胺缩合剂需要考虑许多方面,理想的试剂应该是价廉、无毒、安全、处理简单、广泛使用、易从反应混合物中除去、仅导致最小量的废水,而且在生产路线快结束形成酰胺键的同时,副产物的检测和清除在监管限制内是优先考虑的事项。
当然,对于一个给定的酸和胺而言,不是所有的缩合剂都表现得一样好,上述过程及酰胺反应条件要同时考虑,以获得高的收率和选择性,好的重复性,在底物有手性中心的情况下,产生较低的差向异构化。
图1描述了2015年6月主流文献中在100 mmol规模以上应用的缩合剂报道的文献数量,基于这些文献的数量,大规模活化羧酸的首选方法依次为:(1)用碳二亚胺类形成活性酯(71例),EDC和DCC作为第一选择;(2)形成酰氯(70例),氯化亚砜和草酰氯是首选试剂;(3)CDI作缩合剂(38例)。
其他引起关注的是用于混合酸酐制备的缩合剂,如特戊酰氯(PivCl)、氯甲酸异丁酯(IBCF)和正丙基磷酸酐(T3P)。
图1. 2015年6月缩合剂应用的参考文献数量,酰胺键生成规模在100 mmol 以上酰氯法缩合形成酰胺键将羧酸转化成相应的酰氯,随后与胺反应是酰胺键形成最古老的方法之一。
酰胺合成的研究进展孙健;王吉洋;金朝辉;高华晶【摘要】酰胺官能团是自然界中最基本的化学结构单元之一,并且广泛存在于精细化学品结构中.目前,合成酰胺的方法已被国内外所报道,包括羧酸与胺的偶联反应、醛和胺的缩合反应、以芳基卤化物和胺和CO为底物的氨基羰基化反应.随着环保的理念深入人心,酰胺的制备也逐渐趋于绿色、环保的合成方法.本文从原料的角度综述了各种合成酰胺的方法.【期刊名称】《广州化工》【年(卷),期】2019(047)007【总页数】3页(P14-16)【关键词】酰胺;偶联反应;缩合反应;氨基羰基化反应【作者】孙健;王吉洋;金朝辉;高华晶【作者单位】吉林化工学院石油化工学院, 吉林吉林 132022;吉林化工学院石油化工学院, 吉林吉林 132022;吉林化工学院研究生学院, 吉林吉林 132022;吉林化工学院石油化工学院, 吉林吉林 132022【正文语种】中文【中图分类】O621.3酰胺是药物化学中重要的组成部分,在药物化学分析数据库中有超过25%的已知药物中含有酰胺类化合物[1]。
同时,含有酰胺结构的聚合物也有重要应用。
如尼龙,是重要的工程和医用材料,不仅可以替代铜、铁等金属,还可以用于医用缝线。
目前,合成酰胺的主要方法有两种。
一种是羧酸与胺的缩合酰化反应[2],由于该方法需要用到缩合剂,因此,研究人员开发了多种缩合剂应用于这种酰化反应,但是该方法需要增加成本处理反应中产生的大量副产物。
另外一种是酶催化法合成酰胺[3],虽然反应生成单一产物,但是酶催化剂的使用条件非常苛刻,并且这种方法的底物范围受到限制。
基于酰胺化合物的重要性以及合成酰胺方法的局限性,Allen等[4]从催化剂的角度,对合成酰胺的方法进行过总结。
而本文从原料的角度出发,总结了国内外近年来使用不同底物合成酰胺的反应类型。
1 以羧酸和胺为底物合成酰胺由于偶联试剂的多样化,使得金属催化剂在以羧酸和胺为原料合成酰胺的反应领域研究较少,同时羧酸和胺可以生成季胺盐,因此用羧酸和胺合成的酰胺具有挑战性。
标准酰胺偶联技术
"标准酰胺偶联技术" 可能指的是一种用于有机合成的常见偶联反应,通常用于连接两个分子并形成酰胺键的方法。
酰胺是一类含有酰胺基团(-CONH-)的有机化合物,是许多生物活性分子和药物的结构中的常见元素。
在有机合成中,标准的酰胺偶联技术通常涉及以下步骤:
1.底物准备:两个底物,通常是胺和酸,被选中以进行偶联反应。
2.激活酸:酸通常需要被激活,以提高其反应活性。
这可以通过
使用活化剂(如活化的酸氯化物或酸酐)来实现。
3.反应条件:通常在室温至室温以上的温度下进行反应,时间取
决于具体的底物和反应条件。
4.产物形成:底物中的胺和酸发生反应,形成酰胺键,产生酰胺。
这种偶联反应通常在有机合成中用于构建酰胺骨架,可以在多种合成场景中找到应用,包括药物合成、聚合物化学、材料科学等。
这是一种常见、有效的化学合成方法,为构建复杂有机分子提供了一种途径。
常用的激活剂包括有机酸氯化物(如DCC、DIC)和活化酸酐(如NHS酯)等。
第1篇一、实验目的1. 熟悉酰胺缩合反应的基本原理和实验操作。
2. 掌握酰胺缩合反应的实验步骤和注意事项。
3. 通过实验,了解实验结果与理论计算结果的差异,提高实验操作技能。
二、实验原理酰胺缩合反应是指羧酸或其衍生物与胺类化合物在催化剂或特定条件下发生缩合反应,生成酰胺化合物的过程。
本实验采用活性酯法,利用氯甲酸乙酯或异丁酯活化羧基,与胺反应得到相应的酰胺。
三、实验仪器与试剂1. 仪器:反应瓶、磁力搅拌器、分液漏斗、旋转蒸发仪、真空泵、红外光谱仪、核磁共振波谱仪等。
2. 试剂:羧酸(如苯甲酸)、胺(如苄胺)、氯甲酸乙酯、异丁酯、活性炭、无水乙醇、无水硫酸钠、碳酸钠、苯、甲苯、氢氧化钠、盐酸等。
四、实验步骤1. 准备反应物:称取一定量的羧酸和胺,置于反应瓶中。
2. 活化羧基:向反应瓶中加入适量的氯甲酸乙酯或异丁酯,搅拌混合。
3. 缩合反应:在搅拌下,将活化后的羧酸与胺反应,控制反应温度和时间。
4. 后处理:反应完成后,将反应液倒入分液漏斗中,加入适量的碳酸钠溶液,萃取有机层。
5. 干燥:将有机层进行干燥处理,去除水分。
6. 纯化:通过旋转蒸发仪去除溶剂,得到粗产物。
7. 分析:对产物进行红外光谱和核磁共振波谱分析,确定产物的结构。
五、实验结果与讨论1. 实验结果:通过实验,成功合成了目标酰胺化合物,产率较高。
2. 结果讨论:实验结果表明,活性酯法在酰胺缩合反应中具有较好的效果。
在实验过程中,应注意以下事项:(1)反应温度和时间:反应温度和时间对产率有较大影响,应根据具体情况进行调整。
(2)反应物比例:羧酸与胺的比例对产率有较大影响,应根据具体情况进行调整。
(3)溶剂选择:选择合适的溶剂有利于提高产率,本实验中选用无水乙醇作为溶剂。
(4)催化剂选择:催化剂对反应速度和产率有较大影响,本实验中未使用催化剂。
六、实验总结1. 通过本次实验,掌握了酰胺缩合反应的基本原理和实验操作。
2. 了解实验结果与理论计算结果的差异,提高了实验操作技能。
合成酰胺键的方法
在这里我们简单介绍一下多肽化学合成的方法以及常用的多肽缩合试剂。
1、酰卤法
最常用的是酰氯,一般的操作方法是将羧酸与SOCl2或者(COCl)2反应生成酰氯,然后与游离的氨基反应生成酰胺键。
催化量的DMF可以促进酰氯的生成,而DMAP可以促进酰氯和氨基的反应。
该方法的优点是活性高,可以与大位阻的氨基反应;缺点是在酸性条件下形成酰氯,很多对酸敏感的基团承受不了,还有就是产物比较容易消旋。
为了克服第一个缺点,人们发展了用氰脲酰氯(2, 4, 6-三氯-1, 3, 5-三嗪)/TEA或者PPh3/CCl4条件形成酰氯,第二个缺点可用酰氟代替酰氯加以克服。
2、混合酸酐法
氯甲酸乙酯或氯甲酸异丁酯是最常用的生成混酐的试剂。
它是利用羧酸羰基的亲电性高于碳酸羰基,从而使氨基选择性的进攻羧酸羰基形成酰胺键。
混酐法具有反应速度快,产物纯度较高等优点,但由于混酐的活性很高,极不稳定,要求反应在低温无水条件下进行,产品也容易出现消旋现象。
3、活化酯法
常见的活化酯有硝基苯酯,2, 4, 6-三氯苯酯,五氯苯酯,五氟苯酯(PfOH),N-羟基琥珀酰亚胺(HOSu)酯和N-羟基苯并三唑酯(HOBt)等。
一般的操作步骤是先制备并分离得到活化酯,再与氨基反应生成酰胺键。
由于活化酯活性较酰氯和酸酐低,可以极大地抑制消旋现象,并能在加热的条件下反应。
4、酰基迭氮法
一般是用酰肼与亚硝酸钠反应制成酰基迭氮,然后与氨基反应形成酰胺键。
优点是迭氮法引起的消旋程度较小,比活化酯法效率更高,但是,酰基迭氮中间体不稳定,产生的迭氮酸有毒,而且制备步骤繁琐。
Shioiri等人发展的DPPA可以与羧酸现场生成酰基迭氮,很好地解决了酰基迭氮制备的问题,得到广泛的运用。
5、缩合试剂法
该方法是目前应用最广的形成酰胺键的方法,同时也广泛地应用于酯键、大环内酰胺和内酯的构建。
这种方法通常是将羧基组份和氨基组份混合,在缩合试剂作
用下,中间体不经分离直接进行反应形成酰胺键。
这样就无需预先制备酰卤、酸酐和活化酯等羧基被活化的中间体,不仅简捷高效,而且可以有效地避免在活化中间体分离提纯以及存放过程中产生的一些副反应。
目前已报道的多肽缩合试剂非常繁多,从分子结构的角度上主要分为碳化二亚胺类型、磷正离子或磷酸酯类型和脲正离子类型。
发展最早和最常用的碳化二亚胺类缩合试剂是DCC。
但由于反应生成的二环已基脲(DCU)在大多数有机溶剂中溶解度很小,难以除去,人们对DCC的结构进行了改进,发展了副产物的脂溶性很好的DIPCDI和BDDC等和副产物水溶性很好的EDCI(Figure 1.7)。
由于这类缩合试剂活性很高,往往会导致产物有较大程度的消旋,为此通常要加入HOSu,HOBt,HOAt或HOOBt等添加剂一起使用来抑制产物消旋,同时也可有效地抑制N-酰基脲等副产物的生成。
目前常用的磷正离子或磷酸酯缩合试剂主要有BOP,PyBOP,BOP-Cl,FDP,FDPP,DEPBT,PyBrOP等(Figure 1.8)。
这类缩合试剂形成酰胺键的机理主要是在碱性条件下羧基负离子进攻缩合试剂生成相应的酰氧基磷正离子或者碳磷混酐,然后此活泼中间体受苯并三唑氧基,卤素或者五氟苯酚负离子的进攻生成活化酯或酰卤,再与氨基反应形成酰胺键。
BOP和PyBOP是HOBt衍生的试剂,BOP试剂因为实验操作简单以及它能够提高缩合反应速度,所以它广被泛应用于肽的合成当中,缺点是在反应过程中产生致癌的有毒物质六甲基磷酰亚胺(HMPA);而PyBOP就避免了这一缺点,因为它用吡咯啉代替了二甲胺。
BOP-Cl 和PyBrOP都是形成活泼的酰卤中间体,可以高效地促进有空间位阻的酰胺键的形成且消旋较小。
FDP和FDPP都是五氟苯酚衍生的试剂,在多肽合成中具有产物收率高,后处理简单等优点,但不适用于有空间位阻多肽的合成,FDPP特别
适用于环肽的合成。
DEPBT是HOOBt衍生的磷酸酯,其特点是产物的消旋较小。
脲正离子型缩合试剂种类繁多,自1978年Dourtoglou成功地将基于HOBt的脲正离子HBTU用于多肽合成中以来,这一类型缩合试剂得到迅速的发展,并先后开发出一系列基于HOBt,HOAt,HOOBt和PfOH等的脲正离子型试剂,常见的有TBTU,HBPyU,HATU,HAPyU,HDTU,HAPyTU等。
另外,α-卤代的脲正离子型缩合试剂也越来越在多肽合成中显示其重要的地位。
这类缩合试剂中应用较为广泛的有PyClU,TFFH,BTFFH,CIP和CTDP等(Figure 1.9)。
与磷正离子型缩合试剂类似,HOBt和HOAt衍生的脲正离子型缩合试剂参与多肽缩合反应的主要中间体分别是羧基组份的苯并三唑酯和7-氮杂苯并三唑酯。
当α-卤代的脲正离子型缩合试剂参与多肽合成时,反应的活泼中间体主要是羧基组份的酰卤和酸酐。