实验十五磺基水杨酸和铁(III)配合物的组成及稳定常数的测定
- 格式:pdf
- 大小:1.06 MB
- 文档页数:5


磺基水杨酸合铁报告:水杨酸报告磺基水杨酸测铁磺基水杨酸合铁结构磺基水杨酸有毒吗篇一:磺基水杨酸合铁磺基水杨酸合铁(Ⅲ)配合物的组成及稳定常数的测定【摘要】HOSO3H磺基水杨酸(简化为H3R),与Fe3+可以形成稳定的配合物,配合物的组成随溶液的pH值的不同而改变。
在pH=2~3时,pH=4~9时,pH=9~11.5时,磺基水杨酸与Fe3+能分别形成不同颜色且具有不同组成的配离子。
等摩尔连续变化法是配制一系列溶液,保持溶液中度、离子强度、温度和金属离子与配体的总物质的量不变改变金属离子cM和配体的摩尔分数使之连续化,在最大吸收波长处测定各溶液的吸光度,以吸光度A配体的摩尔分数xR作图,根据两边线性部分的延线相交之点所对应的配体摩尔分数值可求出配合的组成比,即可以认为相交之点Amax为配合物以n完全配位而不离解的吸光度,而实验测得值为A,两者之差就是由配合物离解所造成的.由此可求K稳,相应计算同摩尔比法.【关键字】分光广度法等摩尔连续变化法伯朗-比尔定律配合物配位数【实验目的】1、了解光度法测配合物配位数和稳定常数的一种原理和方法;2、测定pH2.5时,磺基水杨酸合铁(Ⅲ)配合物的组成及稳定常数;3、学习分光光度计的应用;4、巩固溶液配制及作图法处理数据的方法。
【实验原理】1、伯朗-比尔定律当具有一定波长的单色光通过有色溶液时,一部分光被溶液吸收,另一部分光透过溶液。
Io一定时,Ia越大,It就越小。
一般将透过光强度It与入射光强度I0之比叫透光度,以T表示:T越大,溶液透光程度越大,对光的吸收程度越小。
一般用A表示有色溶液对光的吸收程度,A越大,T 越大,对于同一溶液而言,其吸光度与浓度c和液层厚度d成正比,即伯朗-比尔定律,若入射光波长、比色皿(溶液)的厚度d一定时,吸光度只与溶液的浓度c成正比。
通常测定某一物的一系列已知浓度的吸光度,以A为纵标,c 为横标,绘出A-c标准曲线,则其斜率为k = εd,如果测定该物未知浓度ci溶液的吸光度为Ai,则由Ai/k或从标准曲线就可以求出ci来。

实验六 磺基水杨酸铁(Ⅲ)配离子的组成和稳定常数的测定一、实验目的1.采用浓度连续变更法测量配合物的组成和配位化合物的稳定常数。
2.学习分光光度计的使用及实验数据的处理方法。
二、实验原理磺基水杨酸与Fe 3+离子可形成稳定的配合物:起始浓度/mol·dm -3 c 0 0 平衡浓度/ mol·dm -3 c-c α c α c α()n eq Leq eqc c c K ⋅=MML (表观)不稳 或()eq neq Leqc c c K MLM⋅=(表观)稳97.21010⋅=(表观)稳稳K K当pH=2~3时,生成1:1型紫红色螯合物ML ,其表观稳定常数:2MLM 1ααc c c c K eq eqL eq -=⋅=稳 121-DDD =αα配合物的解离度:—朗伯比尔定律:有色溶液的吸光度D 与溶液的浓度成正比()1 c b D ⋅⋅=ε当温度、液层厚度及溶液性质一定时,()1式可写成:()2 kc D =以吸光度D 为纵坐标,以配体的物质的量分数为横坐标作图。
n n ML L M +LM ML n n +三、实验内容1.溶液的配制(1)配制3dm mol 0010.0-⋅ +3Fe溶液:准确吸取35.00cm 3dmmol 0100.0-⋅()()244SO Fe NH 溶液于350cm 容量瓶中,用3dmmol 0100.0-⋅4HClO 溶液稀释至刻度,摇匀备用。
(2)配制3dm mol 0010.0-⋅磺基水杨酸溶液:准确吸取35.00cm 3dm mol 0100.0-⋅磺基水杨酸溶液于350cm 容量瓶中,用3dm mol 0100.0-⋅4HClO 溶液稀释至刻度,摇匀备用。
2.浓度连续变更法配制配离子溶液及吸光度的测定(1)按下表配制溶液于310.00cm 比色管中,注意比色管编号,用3dm mol 0100.0-⋅4HClO 溶液稀释至310.00cm 刻度线,摇匀。

磺基水杨酸合铁配合物组成及其稳定常数测定实验七铁(III)离子与磺基水杨酸配合物的组成和稳定常数的测定一、实验目的1.了解采用分光光度法测定配合物组成和稳定常数的原理和方法。
2.学习用图解法处理实验数据的方法。
3.进一步学习分光光度计使用方法,了解其工作原理。
4. 进一步练习吸量管、容量瓶的使用二、实验原理磺基水杨酸(简式为H3R)可以与Fe3+ 形成稳定的配合物。
配合物的组成随溶液pH值的不同而改变。
在pH=2~3、4~9、9~11时,磺基水杨酸与Fe3+能分别形成三种不同颜色、不同组成的配离子。
本实验是测定pH=2~3时所形成的红褐色磺基水杨酸合铁(Ⅲ)配离子的组成及其稳定常数。
实验中通过加入一定量的HClO4溶液来控制溶液的pH值。
由于所测溶液中磺基水杨酸是无色的,Fe3+溶液的浓度很小,也可认为是无色的,只有磺基水杨酸合铁(Ⅲ)配离子(MRn)是有色的。
根据朗伯—比耳定律A=εbc可知,当波长λ、溶液的温度T及比色皿的厚度b均一定时,溶液的吸光度A只与有色配离子的浓度c成正比。
通过对溶液吸光度的测定,可以求出配离子的组成。
用光度法测定配离子组成,通常有摩尔比法、等摩尔连续变化法、斜率法和平衡移动法等,每种方法都有一定的适用范围,本实验采用等摩尔连续变化法,通过分光光度计测定配位化合物的组成。
具体操作时,取用摩尔浓度相等的金属离子溶液和配位体溶液,按照不同的体积比(即摩尔数之比)配成一系列溶液,测定其吸光度值。
以吸光度值A 为纵坐标,体积分数(,即摩尔分数。
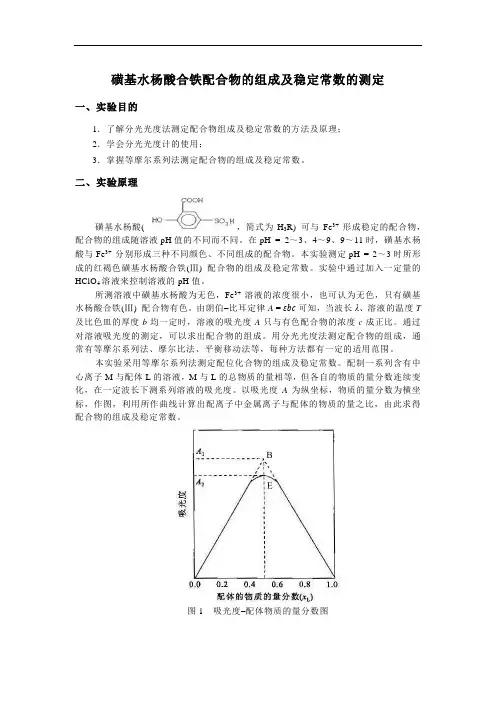
式中:V M为金属离子溶液的体积,V L为配位体溶液的体积)为横坐标作图得如图1所示的曲线,将曲线两边的直线部分延长相交于B点,B点对应的吸光度值A B 最大。
由B点对应的摩尔分数值,可计算配离子中金属离子与配位体的摩尔数之比,即可求得配离子MLn 中配位体的数目n 。
图 1 配位体摩尔分数-吸光度图在图1中,在B点最大吸收处对应的摩尔分数值为0.5,则:即:金属离子与配位体摩尔数之比为1︰1。

实验22 磺基水杨酸合铁(III )配 合物的组成及其稳定常数的测定一、实验目的1.掌握等摩尔连续变化法测定配合物组成及其稳定常数的原理和方法。
2.学习分光光度计的使用。
3. 进一步巩固溶液的配制、液体的移取等操作。
二、实验原理在溶液中,磺基水杨酸(,简写为H 3R )与Fe 3+可以形成稳定的配合物,因溶液pH 值的不同,形成配合物的组成也不同。
在pH10左右,可生成1׃3的配合物,呈黄色。
在pH 为4~10之间生成红色的1׃2配合物。
在pH <4时,它形成1׃1的配合物,呈紫红色(也有称红褐色),配位反应为:Fe 3+ ++ 2H +本实验通过加入一定量的HClO 4溶液来控制溶液的pH 值,测定pH <2.5时所形成的紫红色的磺基水杨酸合铁(III )配离子的组成及稳定常数。
目前测定配合物组成及稳定常数的方法很多,其中分光光度法是常用的方法之一。
其基本原理如下:当一束波长一定的单色光通过有色溶液时,光的一部分被溶液吸收,另一部分透过溶液。
对光的吸收和透过程度,通常有两种表示方法:一种是用透光率T 表示,即透过光的强度I t 与入射光强度I 0之比,即 0I I T t=另一种是用吸光度A (又称消光度,光密度)来表示,它是透光率的负对数,即tI I T A 0lglg =−= A 值越大,表示单色光被有色溶液吸收的程度越大,反之A 值小,光被有色溶液吸收的程度小。
朗伯-比尔定律指出:当一束单色光通过溶液时,溶液的吸光度与溶液的浓度c 和液层厚度l 的乘积成正比,即A = εcl式中:ε为摩尔吸光系数,在一定波长下,它是有色物质的一个特征常数。
在用分光光度法测定溶液中配合物的组成时,通常有摩尔比法、等摩尔连续变化法、斜率法和平衡移动法等,每种方法都有一定的适用范围,本实验采用等摩尔连续变化法。
由于所测溶液中,磺基水杨酸是无色的,Fe 3+溶液的浓度很稀,也可认为是无色的,只有磺基水杨酸合铁配离子(MR n )是有色的,因此溶液的吸光度只与配离子的浓度成正比。
磺基水杨酸合铁配合物的组成及稳定常数的测定一、实验目的1.了解分光光度法测定配合物组成及稳定常数的方法及原理;2.学会分光光度计的使用;3.掌握等摩尔系列法测定配合物的组成及稳定常数。
二、实验原理磺基水杨酸( ,简式为H3R) 可与Fe3+ 形成稳定的配合物,配合物的组成随溶液pH值的不同而不同。
在pH = 2~3、4~9、9~11时,磺基水杨酸与Fe3+ 分别形成三种不同颜色、不同组成的配合物。
本实验测定pH = 2~3时所形成的红褐色磺基水杨酸合铁(Ⅲ) 配合物的组成及稳定常数。
实验中通过加入一定量的HClO4溶液来控制溶液的pH值。
所测溶液中磺基水杨酸为无色,Fe3+ 溶液的浓度很小,也可认为无色,只有磺基水杨酸合铁(Ⅲ) 配合物有色。
由朗伯–比耳定律A = εbc可知,当波长λ、溶液的温度T 及比色皿的厚度b均一定时,溶液的吸光度A只与有色配合物的浓度c成正比。
通过对溶液吸光度的测定,可以求出配合物的组成。
用分光光度法测定配合物的组成,通常有等摩尔系列法、摩尔比法、平衡移动法等,每种方法都有一定的适用范围。
本实验采用等摩尔系列法测定配位化合物的组成及稳定常数。
配制一系列含有中心离子M与配体L的溶液,M与L的总物质的量相等,但各自的物质的量分数连续变化,在一定波长下测系列溶液的吸光度。
以吸光度A为纵坐标,物质的量分数为横坐标,作图,利用所作曲线计算出配离子中金属离子与配体的物质的量之比,由此求得配合物的组成及稳定常数。
图1吸光度–配体物质的量分数图具体操作时,取用物质的量浓度相同的金属离子溶液和配体溶液,按照不同的体积比(即物质的量之比) 配成一系列溶液,测定其吸光度值。
以吸光度值 A 为纵坐标,体积分数(,即物质的量分数。
式中:V M为金属离子溶液的体积,V L为配体溶液的体积) 为横坐标作图,得到吸光度–配体物质的量分数图(如图1所示),将曲线两边的直线部分延长相交于B点,B点对应的吸光度值A1 最大。

实验十五 磺基水酸和铁(III )配合物的组成及稳定常数的测定【实验目的】了解光度法测定配合物的组分及其稳定常数的原理和方法。
测定pH ﹤2.5时磺基水酸铁的组成及其稳定常数。
学习分光光度计的使用。
【实验原理】磺基水酸(,简式为R H 3)与+3Fe 可以形成稳定的配合物,因溶液pH 的不同,形成配合物的组成也不同。
本实验将测定pH ﹤2.5时形成红褐色的磺基水酸合铁(III )配离子的组成及其稳定常数。
测定配合物的组成常用光度法,其基本原理如下。
当一束波长一定的单色光通过有色溶液时一部分光被溶液吸收,一部分光透过溶液。
对光的被溶液吸收和投过程度,通常有两种表示方法:一种是同透光率T 表示。
即透过光的强度t I 与射入光的强度0I 之比:I I T t=另一种试用吸光度A (又称消光法,光密度)来表示。
它是取透光率的负对数:tI I T A 0lglg =-= A 值大表示光被有色溶液吸收的程度大,反之A 值小,光被溶液吸收的程度小。
实验结果证明:有色溶液对光的吸收程度与溶液的浓度c 和光穿过的液层厚度d 的乘积成正比。
这一规律称朗波—比耳定律:cd A ε=式中ε是消光系数(或吸光系数)。
当波长一定时,它是有色物质的一个特征常数。
由于所测溶液中磺基水酸是无色的,+3Fe 溶液的浓度很稀,也可认为是无色的,只是磺基水酸铁配合离子(n MR )是有色的,因此,溶液的吸光度只与配离子的浓度成正比。
通过对溶液吸光度的测定,可求出该配离子的组成。
下面介绍一种常用方法:等摩尔系列法:即用一定波长的单色光,测定一系列组分变化的溶液的吸光度(中心离子M 和配体R 的总物质的量保持不变,而M 和R 的摩尔分数连续[][][])RM/(R+图15—1 A—[][][])RM/(R+曲线变化)。
显然,在这一系列溶液中,有一些溶液的金属离子是过量的。
而另一些溶液配体也是过量的;在这两部分溶液中,配离子的浓度都不可达到最大值;只有当溶液中金属离子与配体的摩尔比与配离子的组成一致时配离子的浓度才能最大。

磺基水杨酸铁配合物稳定常数的测定一.实验目的1.了解比色法测定溶液中配合物的组成和稳定常数的原理。
2.学习分光光度计的使用方法。
二.基本原理磺基水杨酸(SO 3HHOCOOH简化为H 3R ),与Fe 3+可以形成稳定的配合物,配合物的组成随溶液的pH 值的不同而改变。
在pH=2~3时,pH=4~9时,pH=9~11.5时,磺基水杨酸与Fe 3+能分别形成不同颜色且具有不同组成的配离子。
本试验是测定pH=2~3时形成的紫红色的磺基水杨酸铁配离子的组成及其稳定常数。
实验中通过加入一定量的HClO 4溶液来控制溶液的pH 值。
测定配离子的组成时,分光光度法是一种有效的方法。
实验中,常用的方法有两种:一是摩尔比法,一是等摩尔数连续变化法(也叫浓比递变法)。
本实验采用后者,用上述方法时要求溶液中的配离子是有色的,并且在一定条件下只生成这一种配合物,本实验中所用的磺基水杨酸是无色的,Fe 3+溶液很稀,也可以认为是无色的,只有磺基水杨酸铁配离子显紫红色,并且能一定程度的吸收波长为500nm 的单色光。
光密度又称吸光度,是指光线通过溶液或某一物质前的入射光强度与该光线通过溶液或物质后的透射光强度比值的对数,可用分光光度计测定。
光密度与浓度的关系可用比尔定律表示:CL A ε=其中:A 代表光密度;ε代表某一有色物质的特征常数,称之为消光系数;L 为液层厚度;C 为溶液浓度,当液层厚度一定时,则溶液光密度就只与溶液的浓度成正比。
本实验过程中,保持溶液中金属离子的浓度(C M )与配位体的浓度(C R )之和不变(即总摩尔数不变)的前提下,改变C M 与C R 的相对量,配制一系列溶液,测其光密度,然后再以光密度A 为纵坐标,以溶液的组成(配位体的物质的量分数)为横坐标作图,得一曲线,如图1所示,显然,在这一系列溶液中,有一些是金属离子过量,而另一些溶液则是配位体过量,在这两部分溶液中,溶液离子的浓度都不可能到最大值,因此溶液的光密度也不可能达到最大值,只有当溶液中金属离子与配位体的摩尔比与配离子的组成一致时,配离子的浓度才最大,因而光密度才最大,所以光密度最大值所对应的溶液的组成,实际上就是配合物的组成。

磺基水杨酸合铁(ⅲ)配合物的稳定常数下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!本店铺为大家提供各种类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor. I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you! In addition, this shop provides you with various types of practical materials, such as educational essays, diary appreciation, sentence excerpts, ancient poems, classic articles, topic composition, work summary, word parsing, copy excerpts, other materials and so on, want to know different data formats and writing methods, please pay attention!磺基水杨酸合铁(Ⅲ)配合物的稳定常数摘要本文研究了磺基水杨酸合铁(Ⅲ)配合物的稳定常数。

磺基水杨酸合铁(Ⅲ)配合物的组成及稳定常数的测定【摘要】磺基水杨酸(SO3HHOCOOH简化为H3R),与Fe3+可以形成稳定的配合物,配合物的组成随溶液的pH值的不同而改变。
在pH=2~3时,pH=4~9时,pH=9~11.5时,磺基水杨酸与Fe3+能分别形成不同颜色且具有不同组成的配离子。
等摩尔连续变化法是配制一系列溶液,保持溶液中度、离子强度、温度和金属离子与配体的总物质的量不变改变金属离子cM和配体的摩尔分数使之连续化,在最大吸收波长处测定各溶液的吸光度,以吸光度A配体的摩尔分数xR作图,根据两边线性部分的延线相交之点所对应的配体摩尔分数值,即可求出配合的组成比可以认为相交之点Amax为配合物以n完全配位而不离解的吸光度,而实验测得值为A,两者之差就是由配合物离解所造成的.由此可求K稳,相应计算同摩尔比法.【关键字】分光广度法等摩尔连续变化法伯朗-比尔定律配合物配位数【实验目的】1、了解光度法测配合物配位数和稳定常数的一种原理和方法;2、测定pH<2.5时,磺基水杨酸合铁(Ⅲ)配合物的组成及稳定常数;3、学习分光光度计的应用;4、巩固溶液配制及作图法处理数据的方法。
【实验原理】1、伯朗-比尔定律当具有一定波长的单色光通过有色溶液时,一部分光被溶液吸收,另一部分光透过溶液。
I o一定时,I a越大,I t就越小。
一般将透过光强度I t与入射光强度I0之比叫透光度,以T表示:T越大,溶液透光程度越大,对光的吸收程度越小。
一般用A表示有色溶液对光的吸收程度,A越大,T越大,对于同一溶液而言,其吸光度与浓度c和液层厚度d成正比,即伯朗-比尔定律,若入射光波长、比色皿(溶液)的厚度d一定时,吸光度只与溶液的浓度c成正比。
通常测定某一物的一系列已知浓度的吸光度,以A为纵标,c为横标,绘出A-c标准曲线,则其斜率为k = εd,如果测定该物未知浓度c i溶液的吸光度为A i,则由A i/k或从标准曲线就可以求出c i来。

实验七铁(III)离子与磺基水杨酸配合物的组成和稳定常数的测定一、实验目的1.了解采用分光光度法测定配合物组成和稳定常数的原理和方法。
2.学习用图解法处理实验数据的方法。
3.进一步学习分光光度计使用方法,了解其工作原理。
4. 进一步练习吸量管、容量瓶的使用二、实验原理磺基水杨酸(简式为H3R)可以与Fe3+ 形成稳定的配合物。
配合物的组成随溶液pH值的不同而改变。
在pH=2~3、4~9、9~11时,磺基水杨酸与Fe3+能分别形成三种不同颜色、不同组成的配离子。
本实验是测定pH=2~3时所形成的红褐色磺基水杨酸合铁(Ⅲ)配离子的组成及其稳定常数。
实验中通过加入一定量的HClO4溶液来控制溶液的pH值。
由于所测溶液中磺基水杨酸是无色的,Fe3+溶液的浓度很小,也可认为是无色的,只有磺基水杨酸合铁(Ⅲ)配离子(MRn)是有色的。
根据朗伯—比耳定律A=εbc可知,当波长λ、溶液的温度T及比色皿的厚度b均一定时,溶液的吸光度A只与有色配离子的浓度c成正比。
通过对溶液吸光度的测定,可以求出配离子的组成。
用光度法测定配离子组成,通常有摩尔比法、等摩尔连续变化法、斜率法和平衡移动法等,每种方法都有一定的适用范围,本实验采用等摩尔连续变化法,通过分光光度计测定配位化合物的组成。
具体操作时,取用摩尔浓度相等的金属离子溶液和配位体溶液,按照不同的体积比(即摩尔数之比)配成一系列溶液,测定其吸光度值。
以吸光度值A 为纵坐标,体积分数(,即摩尔分数。
式中:V M为金属离子溶液的体积,V L为配位体溶液的体积)为横坐标作图得如图1所示的曲线,将曲线两边的直线部分延长相交于B点,B点对应的吸光度值A B 最大。
由B点对应的摩尔分数值,可计算配离子中金属离子与配位体的摩尔数之比,即可求得配离子MLn 中配位体的数目n 。
图 1 配位体摩尔分数-吸光度图在图1中,在B点最大吸收处对应的摩尔分数值为0.5,则:即:金属离子与配位体摩尔数之比为1︰1。
实验十五磺基水杨酸和铁(III)配合物的组成及稳定常数的测定【实验目的】了解光度法测定配合物的组分及其稳定常数的原理和方法。
测定pH﹤2.5时磺基水杨酸铁的组成及其稳定常数。
学习分光光度计的使用。
【实验原理】磺基水杨酸(,简式为)与可以形成稳定的配合物,因溶液pH 的不同,形成配合物的组成也不同。
本实验将测定pH﹤2.5时形成红褐色的磺基水杨酸合铁(III)配离子的组成及其稳定常数。
测定配合物的组成常用光度法,其基本原理如下。
当一束波长一定的单色光通过有色溶液时一部分光被溶液吸收,一部分光透过溶液。
对光的被溶液吸收和投过程度,通常有两种表示方法:一种是同透光率表示。
即透过光的强度与射入光的强度之比:另一种试用吸光度(又称消光法,光密度)来表示。
它是取透光率的负对数:值大表示光被有色溶液吸收的程度大,反之值小,光被溶液吸收的程度小。
实验结果证明:有色溶液对光的吸收程度与溶液的浓度和光穿过的液层厚度的乘积成正比。
这一规律称朗波—比耳定律:式中是消光系数(或吸光系数)。
当波长一定时,它是有色物质的一个特征常数。
由于所测溶液中磺基水杨酸是无色的,溶液的浓度很稀,也可认为是无色的,只是磺基水杨酸铁配合离子()是有色的,因此,溶液的吸光度只与配离子的浓度成正比。
通过对溶液吸光度的测定,可求出该配离子的组成。
下面介绍一种常用方法:等摩尔系列法:即用一定波长的单色光,测定一系列组分变化的溶液的吸光度(中心离子M和配体R的总物质的量保持不变,而M和R的摩尔分数连续变化)。
显然,在这一系列溶液中,有一些溶液的金属离子是过量的。
而另一些溶液配体也是过量的;在这两部分溶液中,配离子的浓度都不可达到最大值;只有当溶液中金属离子与配体的摩尔比与配离子的组成一致时配离子的浓度才能最大。
由于中心离子和配体对光几乎不吸收,所以配离子的浓度越大,溶液的吸光度也越大,总的来说就是在特定波长下,测定一系列的组成溶液的吸光度,作—的曲线图,则曲线必然存在着极大值,而极大值所对应的溶液组成就是配合物的组成。
光度法对磺基水杨酸铁配合物的组成及稳定常数的实验研究光度法是一种实验方法,通常用于研究溶液中某种物质的浓度和光吸收的关系。
在化学实验中,光度法被广泛应用于研究配位化合物的组成和稳定常数等性质。
这篇文章将着重介绍光度法在磺基水杨酸铁配合物的研究中的应用。
首先,我们需要明确一些概念。
所谓磺基水杨酸铁配合物,就是由铁离子和磺基水杨酸离子组成的一种化合物。
在溶液中,这种化合物会通过配位作用形成复合物,并且形成不同的比例,这些比例可以通过一定的实验方法来确定。
稳定常数是一种用来描述化学反应系统在平衡状态下强度的指标,通常用来衡量配位反应中复合物的稳定程度。
在实验过程中,首先我们需要制备磺基水杨酸铁配合物的溶液,然后通过光度法来研究它的组成和稳定常数。
为了确定配合物的组成,我们可以利用分光光度计来测量溶液的吸收度,并根据比例原理来计算不同组分的浓度。
通常情况下,我们使用一定的数学方法来处理实验数据,从而确定溶液中每种组分的浓度。
例如,可以使用计算机程序来拟合研究结果,得到精确的配合物组成。
测定配合物的稳定常数,则需要通过测定不同配比下的吸收度来实现。
在实验中,我们可以通过改变配合物中每种组分的浓度来确定其稳定常数。
通常来说,我们需要测定几个不同比例下的吸收度,然后将实验数据带入计算公式中,以得出配合物的稳定常数。
总之,光度法是一种非常重要的实验手段,可以被广泛应用于化学反应、药物研发等领域中。
特别是在磺基水杨酸铁配合物的研究中,光度法能够有效地研究其组成和稳定常数等性质,为我们深入了解化学反应提供了重要的实验手段。
磺基水杨酸合铁(Ⅲ)的组成和K 稳的测定(分光光度法)一、实验目的1.初步了解分光光度法测定溶液中配合物的组成和稳定常数的原理和方法。
2.学习有关实验数据的处理方法。
3.练习使用分光光度计。
二、实验原理当一束具有一定波长的单色光通过一定宽度的有色溶液时,有色物质对光的吸收程度(用吸光度A 表示)与有色物质的浓度、液层宽度成正比:A =Kbc这就是朗伯-比耳定律。
式中c 为有色物质浓度;b 为液层宽度;K 为比例常数,其数值与入射光的波长、有色物质的性质和温度有关。
当有色物质成分明确,其相对分子质量已知的情况下,可用ε代替K ,ε称摩尔吸光系数,在数值上等于单位摩尔浓度在单位光程中所测得的溶液的吸光度:A =εbc磺基水杨酸与Fe 3+形成的配合物的组成和颜色因pH 不同而异。
当溶液的pH <4时,形成紫红色的配合物;pH 在4~10 间生成红色的配合物;pH 在10左右时,生成黄色配合物。
本实验用等物质的量系列法测定pH=2时磺基水杨酸与Fe 3+形成的配合物的组成和稳定常数。
等物质的量系列法就是在保持每份溶液中金属离子的浓度(c M )与配体的浓度(c R )之和不变(即总的物质的量不变)的前提下,改变这两种溶液的相对量,配制一系列溶液并测定每份溶液的吸光度。
若以不同的物质的量比RM M n n n 与对应的吸光度A 作图得物质的量比-吸光度曲线,曲线上与吸光度极大值相对应的物质的量比就是该有色配合物中金属离子与配体的组成之比。
图1表示一个典型的低稳定性的配合物MR 的物质的量比与吸光度曲线,将两边直线部分延长相交于B ,B 点位于50%处,即金属离子与配体的物质的量比为1:1。
从图可见,当物质完全以MR 形式存在时,在B 点MR 的浓度最大,对应的吸光度为A 1,但由于配合物一部分离解,实验测得的最大吸光度对应于E 点的A 2。
若配合物的解离度为α,则图1物质的量比—吸光度曲线α =121A A A - l:l 型配合物的标准稳定常数K 可由下列平衡关系导出:M + MR起始浓度 0 0 c平衡浓度 cα cα c (1-α)21ααc c c c K R M MR -=⋅=式中,c MR 、、c M 、c R 为离解平衡时的各物质浓度,c 是溶液内MR 的起始浓度,即当RM M n n n +=50%时,其值相当于溶液中金属离子或配位体的起始浓度的一半。