第八章不对称合成
- 格式:ppt
- 大小:6.65 MB
- 文档页数:2



有机化学中的不对称合成在有机化学领域中,不对称合成是一项重要的研究领域,它可以有效地合成具有手性的有机分子。
手性分子在药物合成、天然产物合成以及材料科学等领域中具有重要的应用价值。
本文将探讨不对称合成的基本概念、方法和应用,并介绍一些常见的不对称合成反应。
一、不对称合成的基本概念不对称合成是指通过使用手性起始原料或手性催化剂,合成出具有手性的有机分子的化学合成方法。
在不对称合成中,合成的产物具有不对称的结构或旋光性。
与对称合成相比,不对称合成可以得到具有更高的立体选择性和手性纯度的产物。
不对称合成的基本原理是利用手性诱导或手性催化剂来选择性地激活反应物中的一个面或一个手性中心,从而控制反应的立体选择性。
手性诱导合成方法包括拆分法、不对称催化、酶催化和手性助剂等。
其中,不对称催化是最为常见的方法,它通过使用手性催化剂,使化学反应以特定的立体选择性进行。
二、不对称合成的方法1. 手性诱导合成手性诱导合成是通过使用手性起始原料或手性诱导剂来进行的合成方法。
手性诱导合成包括手性拆分法和手性诱导剂法。
手性拆分法是通过将手性分子与反应物进行化学或物理上的拆分,使得反应物在反应过程中保持立体选择性。
手性拆分法包括光学拆分法、金属配合物拆分法和手性分子的稳定性拆分法等。
手性诱导剂法是通过使用手性诱导剂来引发反应中的手性识别过程,从而控制反应的立体选择性。
手性诱导剂法包括非手性基团诱导和手性感受性诱导。
2. 不对称催化合成不对称催化合成是通过使用手性催化剂来实现的合成方法。
手性催化剂能够选择性地提供一个特定的反应路径,从而控制反应的立体选择性。
不对称催化合成通常包括氢化、氧化、醇缩合、酯化、醚化等反应。
不对称催化合成中最有代表性的方法是手性配体催化法。
手性配体催化法通过使用手性配体配位于金属催化剂上,使催化剂具有手性识别能力,从而实现对反应物的选择性激活。
3. 酶催化合成酶催化合成是通过使用天然酶或人工改造酶来进行的合成方法。
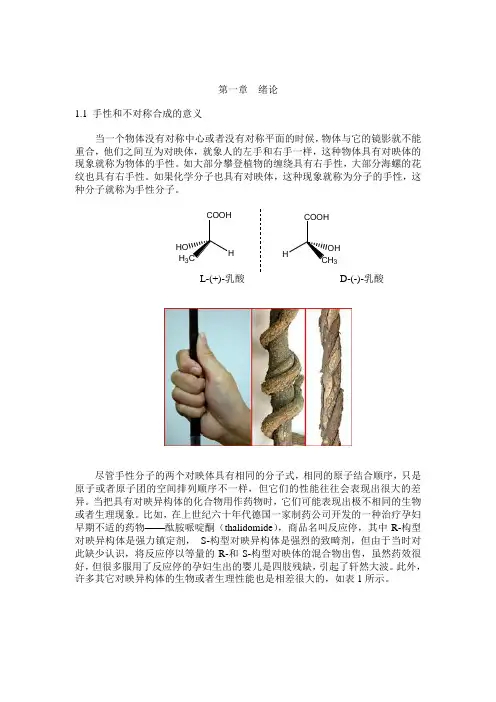
第一章 绪论1.1 手性和不对称合成的意义当一个物体没有对称中心或者没有对称平面的时候,物体与它的镜影就不能重合,他们之间互为对映体,就象人的左手和右手一样,这种物体具有对映体的现象就称为物体的手性。
如大部分攀登植物的缠绕具有右手性,大部分海螺的花纹也具有右手性。
如果化学分子也具有对映体,这种现象就称为分子的手性,这种分子就称为手性分子。
3HL-(+)-乳酸D-(-)-乳酸尽管手性分子的两个对映体具有相同的分子式,相同的原子结合顺序,只是原子或者原子团的空间排列顺序不一样,但它们的性能往往会表现出很大的差异。
当把具有对映异构体的化合物用作药物时,它们可能表现出极不相同的生物或者生理现象。
比如,在上世纪六十年代德国一家制药公司开发的一种治疗孕妇早期不适的药物——酞胺哌啶酮(thalidomide ),商品名叫反应停,其中R-构型对映异构体是强力镇定剂, S-构型对映异构体是强烈的致畸剂,但由于当时对此缺少认识,将反应停以等量的R-和S-构型对映体的混合物出售,虽然药效很好,但很多服用了反应停的孕妇生出的婴儿是四肢残缺,引起了轩然大波。
此外,许多其它对映异构体的生物或者生理性能也是相差很大的,如表1所示。
HN N O OOONHNOOOOS-thalidomider反应停, 致畸R-thalidomider反应停, 镇定表1 手性分子不同异构体不同的生理或者生物性能当我们认识到手性是生命的一个本质属性后,这种仅由于分子的立体结构不同而引起在生物体内极不相同的生理性能现象就容易得到解释。
在生命的产生和演变过程中,自然界往往只对一种手性有偏爱,构成生命的糖为D-构型,氨基酸为L-构型,蛋白质和DNA的螺旋结构又都是右旋的,因此整个生命体处在高度不对称的环境中。
当具有不同对称性的两个对映体进入生命体后,只有与生命体某种不对称受体在空间构型上相匹配的对映体才能表现出活性。
所以不同的构型会产生不同的生理活性和药理作用。

不对称合成方法
不对称合成方法是一种利用立体选择性反应,使两个对映体中的一个占优势的合成方法。
这种方法又被称为手性合成。
在不对称合成中,至少要有一个化合物是手性化合物,才能使反应中生成的两种过渡态互为非对映关系,它们的活化能差决定了产物产生不等量的对映体。
不对称合成可以通过使用手性试剂、催化剂或者物理方法(如圆偏振光)来进行。
成功的标准通常包括高的对映体过量百分数、手性试剂易得且可循环使用、可以分别制得R与S异构体,以及最好是催化性的合成。
此外,根据手性的来源,不对称合成可以分为普通不对称合成和绝对不对称合成。
普通不对称合成是指依靠直接或间接由天然获得的手性化合物衍生的基团诱导产生手性化合物的合成。
而绝对不对称合成是指绝对脱离天然产物来源,通过物理方法(如通过圆偏光的照射)诱导产生手性的合成。
不对称合成在合成某些药物、香料、氨基酸及具有生物活性的化合物等方面具有很重要的意义。

有机化学基础知识点有机合成中的不对称合成方法有机化学基础知识点:不对称合成方法不对称合成是有机化学中一种重要的合成策略,用于制备具有高立体选择性的有机分子。
本文将介绍不对称合成的基本原理和常用方法。
1. 不对称合成的原理不对称合成是在化学反应中控制立体选择性的方法。
通常情况下,有机分子具有手性,即它们可以存在两种依据空间构型的镜像异构体。
对于手性化合物的合成,通常需要选择性地生成一种手性异构体而不生成另一种。
不对称合成通过引入手性诱导剂或催化剂,以及具有手性中心的原料分子,来实现选择性合成手性分子的目的。
2. 常用的不对称合成方法2.1 催化不对称合成催化不对称合成是一种利用手性催化剂来控制反应立体选择性的方法,常用的手性催化剂包括金属配合物、有机小分子等。
例如,铑催化的酮还原反应、钯催化的Suzuki偶联反应等都是常见的不对称催化合成方法。
2.2 手性试剂参与的不对称合成手性试剂通常是指具有手性中心的化合物,它们可以作为手性源与底物反应,从而导致产物的手性选择性。
典型的手性试剂包括手性醇、手性酸等。
例如,进行不对称亲核取代反应时,可以使用手性的亲核试剂与底物反应来实现不对称合成。
2.3 手性配体参与的不对称合成手性配体在金属催化反应中起到了关键作用。
配体的选择可以导致反应的选择性以及对映选择性。
通常,配位基团与金属离子形成配合物,在反应过程中通过改变立体构型来控制手性产物的生成。
常用的手性配体包括膦配体、氨配体等。
2.4 手性溶剂参与的不对称合成手性溶剂是一种可以通过溶解性质改变反应体系手性选择性的方法。
在不对称合成过程中,手性溶剂可以与底物或催化剂形成氢键或其他作用力,从而促使产物的手性选择性。
手性溶剂的选择需要考虑溶解性、选择性和化学稳定性等因素。
3. 应用案例不对称合成方法在有机化学领域有着广泛的应用。
例如,药物合成中常使用不对称合成方法来合成药物的对映异构体,从而提高药物的效果和减少副作用。




不对称合成(Asymmetric Synthesis)在有机合成,特别是手性药物等合成中具有相当重要的意义。
定义按照IUPAC金皮书的定义,不对称合成(Asymmetric synthesis),也称手性合成、立体选择性合成、对映选择性合成,是研究向反应物引入一个或多个具手性元素的化学反应的有机合成分支。
按照Morrison和Mosher的定义,不对称合成是“一个有机反应,其中底物分子整体中的非手性单元由反应剂以不等量地生成立体异构产物的途径转化为手性单元”。
这里,反应剂可以是化学试剂、催化剂、溶剂或物理因素。
不对称合成目前在药物合成和天然产物全合成中都有十分重要的地位。
但无疑,现在最完善的不对称合成技术,要数存在于生物体内的酶。
能否实现像酶一样高效的催化体系,是对人类智慧的挑战。
不对称合成介绍首先说,什么是手性?在有机化合物中,化合物分子主要是以彼此相互连接的碳碳键构成骨架。
碳原子在成键时,采取了sp3的杂化方式,使得碳原子的四个价键彼此成109度28分,为一正四面体形。
正是因为这样的成键特性,导致了他们当中的有些碳原子,虽然其结合的四个基团的种类相同,但却始终无法重合,两者互为镜像,就像我们的左手和右手一样。
这样的性质就称之为手性。
我们称两种互为镜像的分子为对映异构体。
其次,什么是不对称合成?为了得到同一物质中的其中一种手性分子,我们就需要采取特定的合成方法,这种方法就是不对称合成。
然后,我们再来讨论,经过不对称合成得到的具有某一手性的分子有什么样的特性?手性分子最大的特点在于它的光学活性,它可以使通过它的偏振光发生一定角度的偏转,就是我们通常意义上的旋光性。
若光的旋转方向是顺时针,称为右旋;反之,称为左旋。
不对称合成的意义那么了解了一些基本常识以后,不对称合成有什么样的意义?举几个简单的例子,大家就知道了。
青霉素我们再熟悉不过了,作为一种药力强,副作用小的抗生素药物,长期以来一直被人们广泛的使用。
13,4-二氢嘧啶酮类化合物的合成1893年,意大利化学家Pietro.Biginelli首次报道了用苯甲醛、乙酰乙酸乙酯和尿素在浓盐酸催化条件下于乙醇中加热回流18h缩合得到了3,4-二氢嘧啶-2(1H)-酮(DHPM ),合成路线如图所示,后来人们将这一经典的化学反应称为Biginelli反应。
该反应的最大优点是操作简便,“一锅法”即可得到产物,但缺点是收率很低(20%-50%)。
此后,该反应一直被忽视,直到20 世纪80年代,人们通过大量研究发现该类化合物具有与1.4-二氢吡啶衍生物相似的药理活性,可以用作钙拮抗剂、降压剂、抗癌剂,除此之外还可作为研制抗癌药物的先导物及海洋生物碱的中间体。
因此,在近十几年里对Biginelli反应的研究是一个热点。
除了对其反应机理的探讨外,研究者们还将重点放在了对该反应条件的探索、改进以及产物多样性的选择上,各种各样的催化剂和促进剂被不断地应用于该反应中。
Biginelli反应的机理在Biginelli反应中,酸性催化剂是关键。
如果没有酸性催化剂,第一步芳香醛与脲素的缩合反应几乎不能进行。
这是因为脲素中-NH2的亲核性(碱性)很弱(与羰基共轭),而芳香醛中羰基碳的亲电性(酸性)也不强,所以二者的反应性很弱。
但是酸性催化剂可激活芳醛中的羰基,使羰基碳的亲电性增强,从而使醛可以与脲素反应。
因此选择高活性的酸性催化剂是提高该反应收率的重要手段。
彭家建等发现芳醛中环上取代基的电子效应对反应收率有很大影响,供电基团(如一0CH3)使反应易于进行,收率增加;而吸电基团(如-N02)则使产物收率降低。
这可能是由于芳环上的供电基使中间体(c)和(c)中的正电荷分散而稳定,使(c)易于生成而有利于反应进行。
人们更多地将研究重点放在对该反应条件的探索、改进以及合成范围的扩展之上。
各种各样的催化剂不断地应用于此反应,扩大了芳香醛、尿素和β-酮酸酯这三种代表性反应原料的范围,得到大量多官能化的嘧啶酮衍生物.许多Lewis 酸催化剂或促进剂被应用于Biginelli 反应中,同时固相合成法、微波促进法以及使用离子液体等多种合成方法也被应用于该反应中,并合成了大量的多功能的3, 4-二氢嘧啶-2-酮类衍生物。